Дифференциальная диагностика очаговых остеопластических образований в легких у шахтеров
ИГХИ — иммуногистохимическое исследование
ОП — остеопластическая пульмопатия
ЭМТ — эпителиально-мезенхимальная трансформация
В настоящее время известно более 20 этиологических групп заболеваний, которые проявляются синдромом очаговой легочной диссеминации. Среди них насчитывается более 150 различных нозологических групп и единиц. Развитие в легких костной ткани с очагами костномозгового кроветворения — остеопластическая пульмопатия (ОП) крайне редкая форма гетеропической оссификации с легочной локализацией. Число описанных случаев ОП в мировой литературе составляет всего 200 [1]. Клинические публикации посвящены обычно единичным случаям; патоморфологические сводки, охватывающие десятилетия, — нескольким наблюдениям. В отечественной литературе ОП обнаружены в 110 публикациях за период 1960—2014 гг.; однако ссылки на литературу в статьях минувших 10—20 лет относятся к началу того же столетия, поэтому можно предполагать большую частоту этого заболевания.
В структуре очаговых заболеваний легких наиболее часто встречаются саркоидоз (25,7%), туберкулез (19,8%), пневмокониоз (12,9%), карциноматоз (12,9%), идиопатические пневмонии (9,9%), ОП (менее 0,1%). Доля всех заболеваний составляет 81,2% от всей патологии легких. Остальные заболевания легких встречаются реже и составляют 18,8% в структуре всех диссеминаций. Дифференциальная диагностика очаговых патологических изменений в легких представляет значительные трудности для врачей различных специальностей: фтизиатров, пульмонологов, онкологов, терапевтов, торакальных хирургов. Срок от обращения за медицинской помощью до установления диагноза при очаговых поражениях легких колеблется от нескольких месяцев и может затягиваться до нескольких лет, а частота диагностических ошибок достигает 50—85%.
Патологические образования малого размера (диаметр менее 2 см), локализующиеся в легких, чаще выявляются лишь при компьютерной томографии грудной клетки, выполняемой по различным причинам. Обнаруженные при таком исследовании очаговые образования в легочной ткани нередко остаются без внимания специалистов, что порой приводит к неутешительным результатам лечения больных данной категории [2—5]. Трудности точной диагностики очаговых образований легких хорошо известны, так как дифференциальную диагностику чаще приходится проводить между периферическим раком, доброкачественной опухолью, туберкуломой, саркоидозом, метастатическим поражением легкого [3].
Для уточнения характера внутрилегочных очаговых образований малого диаметра в лечебной практике используется несколько диагностических и лечебных операций, цель которых удаление патологического образования легкого с окружающей тканью и последующим срочным или плановым гистологическим исследованием удаленной опухоли [6, 7].
Малые размеры образований и нередко небольшое их число обусловливают появление неопределенной рентгенологической картины, поэтому многие рентгенологи при описании и трактовке патологических процессов в легких пользуются термином «очаговоподобные затемнения». Обычно считается, что очаговые изменения характерны лишь для туберкулеза, а очаговоподобные — для большинства других патологических процессов, отличающихся от туберкулеза большей динамичностью и разнообразием как клинических, так и гистологических изменений. Это неверно, так как очаговая или очаговоподобная тень на рентгенограмме может быть отображением совершенно полиморфного морфологического субстрата, причем он может быть различным (воспалительный, опухолевый, рубцовый и т. д.). В связи с этим очаговоподобные тени весьма разнообразны по величине, локализации, интенсивности, характеру контуров очагов, изменению легочного рисунка и легочной ткани. Очаговые изменения в легких могут быть одиночными, множественными и рассеянными или диссеминированными [8].
Точная верификация таких очагов и адекватное лечение в большинстве случаев способствуют их рассасыванию частично или полностью. Однако чаще процесс рассасывания сочетается с частичным замещением патологических участков соединительной тканью или оссификацией. Со временем на месте очага образуется рубцовая, хрящевая или костная ткань, а вокруг очагов формируется фиброзная или гиалиновая капсула, что стимулирует развитие очагов типа метастатических или творожисто-некротических, фокусных наподобие зон Ашоффа—Пуля.
Своевременная и точная диагностика очаговых образований в легких включает широкий спектр исследований. Исходя из клинического статуса пациента, результатов фибробронхоскопии проводится визуальная оценка состояния трахеи и бронхиального дерева, при необходимости с целью наиболее точной дифференциальной диагностики поражений легких берется биопсия (фрагмент слизистой оболочки) для гистологического анализа и поиска атипичных клеток, прежде всего при цитологическом анализе бронхоальвеолярной лаважной жидкости.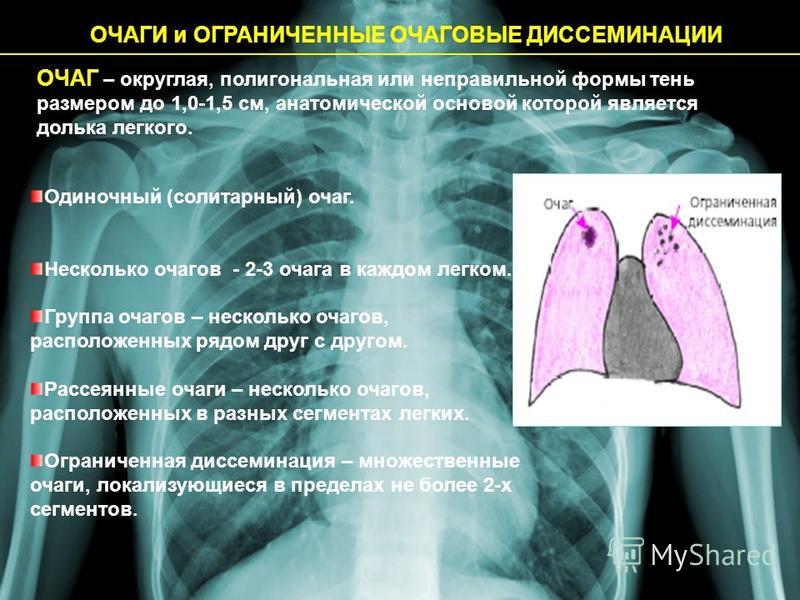 В диагностике большое значение имеет современная компьютерная томография легких, которая благодаря высокой разрешающей способности позволяет избежать врачебных ошибок и длительного так называемого пробного лечения.
В диагностике большое значение имеет современная компьютерная томография легких, которая благодаря высокой разрешающей способности позволяет избежать врачебных ошибок и длительного так называемого пробного лечения.
Однако, несмотря на все современные методы исследования, включая гистологические, морфологический диагноз почти всегда содержит некоторую долю сомнения, так как саркоидная гранулема, особенно отдельно взятая, может быть тождественна туберкулезному бугорку; дифференциальная диагностика туберкулеза, и саркоидоза примерно в 10% случаев невозможна [9], очаговые патологические образования остаются сложными и спорными в медицинском диагнозе. В условиях коммерциализации медицинской деятельности они являются еще и основой для дальнейших судебных разбирательств в спорных случаях.
Нами исследован редкий случай операционно-биопсийного материала с ОП у шахтера. Редкое исключение нашего случая заключается в сочетании ОП с профессиональным фактором запыленности. Мы использовали его для изучения роли эпителиально-мезенхимальной трансформации (ЭМТ) в развитии фиброза легочной ткани и О. П. Мужчина, 1959 года рождения, в 1971—2005 гг. работал шахтером в Кемеровской области в разных профессиях (горнорабочий очистного забоя, подземным электрослесарем, горным мастером). Периодически проходил профосмотры, был годен к работе. С осени 2011 г. госпитализирован в терапевтическое отделение в связи с болями в голеностопных и коленных суставах, связанными с остеоартрозом. Тогда рентгенологически случайно выявлено снижение пневмотизации легочной ткани, деформация легочного рисунка, малоструктурность корней. По данным мультиспиральной компьютерной томографии органов грудной клетки с болюсным контрастированием, в легких диффузно, практически симметрично, выявлялись участки уплотнения легочной ткани по типу матового стекла, чередующимися с небольшими участками альвеолярной консолидации. Выявленные изменения в легких протекали бессимптомно. Характер заболевания до весны 2014 г. не оставался полностью ясным. Предполагался ревматоидный артрит с развитием синдрома Каплана, недифференцированное заболевание соединительной ткани с поражением суставов и легких.
П. Мужчина, 1959 года рождения, в 1971—2005 гг. работал шахтером в Кемеровской области в разных профессиях (горнорабочий очистного забоя, подземным электрослесарем, горным мастером). Периодически проходил профосмотры, был годен к работе. С осени 2011 г. госпитализирован в терапевтическое отделение в связи с болями в голеностопных и коленных суставах, связанными с остеоартрозом. Тогда рентгенологически случайно выявлено снижение пневмотизации легочной ткани, деформация легочного рисунка, малоструктурность корней. По данным мультиспиральной компьютерной томографии органов грудной клетки с болюсным контрастированием, в легких диффузно, практически симметрично, выявлялись участки уплотнения легочной ткани по типу матового стекла, чередующимися с небольшими участками альвеолярной консолидации. Выявленные изменения в легких протекали бессимптомно. Характер заболевания до весны 2014 г. не оставался полностью ясным. Предполагался ревматоидный артрит с развитием синдрома Каплана, недифференцированное заболевание соединительной ткани с поражением суставов и легких.

До конца 90-х годов XX века представления о причинности развития ОП сводились к описанию имеющихся у больных сопутствующих нозологий или состояний, которые наблюдались не у всех пациентов. С конца 90-х годов на основе изучения биохимических и молекулярных звеньев патогенеза заболеваний, в том числе фиброзирующих и оссифицирующих, произошел значительный прорыв. Патогенетический каскад стал включать про-, противовоспалительные, ростовые факторы и рецепторы к ним, молекулы адгезии, молекулы сигнальной трансдукции, регуляторы трансляции (активирующие и ингибирующие).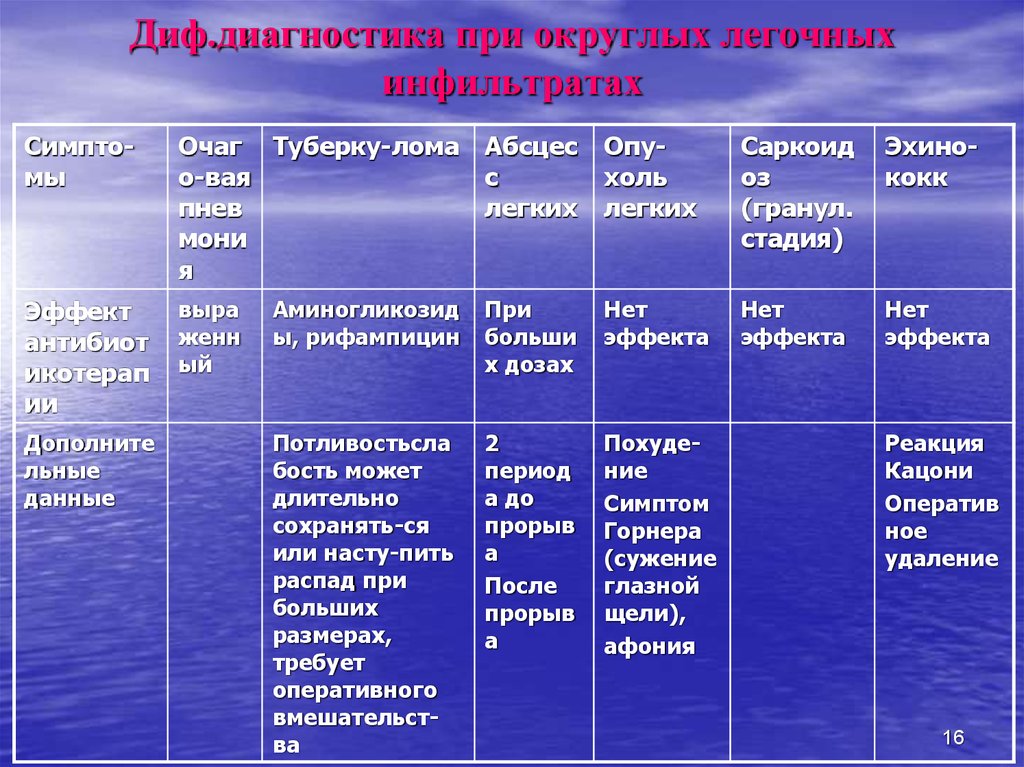
Частным случаем такой дедифференцировки клеток является ЭМТ, при которой эпителиальные или эндотелиальные клетки, оказавшись под воздействием механизмов патогенетического каскада, реверсируют в фенотип клеток своих гистогенетических предшественников, в фенотип мезенхимальных клеток, т. е. в миофибробласты и фиброласты. Гистогенетической потенцией мезенхимальных клеток является их способность образовывать различные виды соединительной ткани — от неоформленной рыхлой соединительной до костной, не говоря уже о возможности образования эндотелия, клеток крови, и мышц [10].
е. в миофибробласты и фиброласты. Гистогенетической потенцией мезенхимальных клеток является их способность образовывать различные виды соединительной ткани — от неоформленной рыхлой соединительной до костной, не говоря уже о возможности образования эндотелия, клеток крови, и мышц [10].
ЭМТ может быть отслежена при обычной световой микроскопии не только по исчезновению полярности клеток, изменению их внешнего вида, затрудняющих отличие их от фибробластов, но и по выявлению появившейся у них миграционной способности. Иммуногистохимически и иммуноферментативно у реверсируемых эпителиальных клеток обнаруживаются маркеры, свойственные мезенхимальным клеткам [11]. При ЭМТ исчезают многие специфичные для эпителиев белки кератиновой группы, из которых построены промежуточные филаменты, типичные для всех эпителиев. Эти кератины заменяются виментином — белком промежуточных филаментов, типичным для всех клеток мезенхимального происхождения. Аналогичо Е-кадхерин (белок эпителиальных межклеточных адгезионных контактов) заменяется N-кадхерином (белком контактов соединительнотканных клеток). При ЭМТ повышается экспрессии генов, кодирующих матриксные металлопротеиназы, которые участвуют в деградации внеклеточного матрикса и базальной мембраны. Меняется морфология межклеточных контактов и ряд эпителиальных контактов (плотные контакты, десмосомы), исчезают вместе с характерными для них специфичными белками (ZO-1, десмоплакины и др.). ЭМТ сопровождается изменениями актинового цитоскелета: характерные для индивидуальных дисковидных эпителиальных клеток кольцевые актинмиозиновые прикраевые пучки исчезают уже на ранних этапах ЭМТ; тонкие прямые актинмиозиновые пучки в небольшом количестве при ЭМТ сохраняются; исчезают и зрелые интегриновые фокальные контакты с матриксом, хотя Е-кадхериновые адгезионные структуры сохраняются вплоть до поздних стадий ЭМТ. Мезенхимальные и мезенхиподобные клетки начинают экспрессировать помимо виментина другие свои маркеры: немышечный актин, десмин, α-гладкомышечный актин, фибронектин, а также начинают синтезировать коллаген и гликозаминогликаны, указывающие на менее зрелый характер соединительной ткани.
При ЭМТ повышается экспрессии генов, кодирующих матриксные металлопротеиназы, которые участвуют в деградации внеклеточного матрикса и базальной мембраны. Меняется морфология межклеточных контактов и ряд эпителиальных контактов (плотные контакты, десмосомы), исчезают вместе с характерными для них специфичными белками (ZO-1, десмоплакины и др.). ЭМТ сопровождается изменениями актинового цитоскелета: характерные для индивидуальных дисковидных эпителиальных клеток кольцевые актинмиозиновые прикраевые пучки исчезают уже на ранних этапах ЭМТ; тонкие прямые актинмиозиновые пучки в небольшом количестве при ЭМТ сохраняются; исчезают и зрелые интегриновые фокальные контакты с матриксом, хотя Е-кадхериновые адгезионные структуры сохраняются вплоть до поздних стадий ЭМТ. Мезенхимальные и мезенхиподобные клетки начинают экспрессировать помимо виментина другие свои маркеры: немышечный актин, десмин, α-гладкомышечный актин, фибронектин, а также начинают синтезировать коллаген и гликозаминогликаны, указывающие на менее зрелый характер соединительной ткани. Наличие полной или неполной ЭМТ зависит скорее всего от глубины дерепрессии генома [11].
Наличие полной или неполной ЭМТ зависит скорее всего от глубины дерепрессии генома [11].
Таким образом, к продукции коллагена, развитию фиброза, мышц, хряща или костной ткани в очагах гетеротопической оссификации в любом месте, в том числе при ОП, могут оказаться причастными клетки трех линий — резидентные прогениторные клетки фибропластического фенотипа, пришлые из костного мозга стромальные клетки и образовавшиеся на месте при ЭМТ клетки фибропластической ориентации.
В представленном нами случае запыленность легких угольно-породной пылью, содержащей двуокись кремния, запускает макрофагальное воспаление, которое в свою очередь является триггером для мезенхимальных клеток, локализация угольной пыли в зонах оссификации также позволяет говорить о причастности к развитию ЭМТ, и костеобразующей ответной реакции фибробласта.
Впервые выявленные очаговые образования легких малого размера (до 2 см в диаметре). Динамическое наблюдение или операция?
Одиночный очаг в легких (ООЛ) определяют как локальный участок уплотнения легочной ткани округлой или близкой к ней формы диаметром до 3 см [15].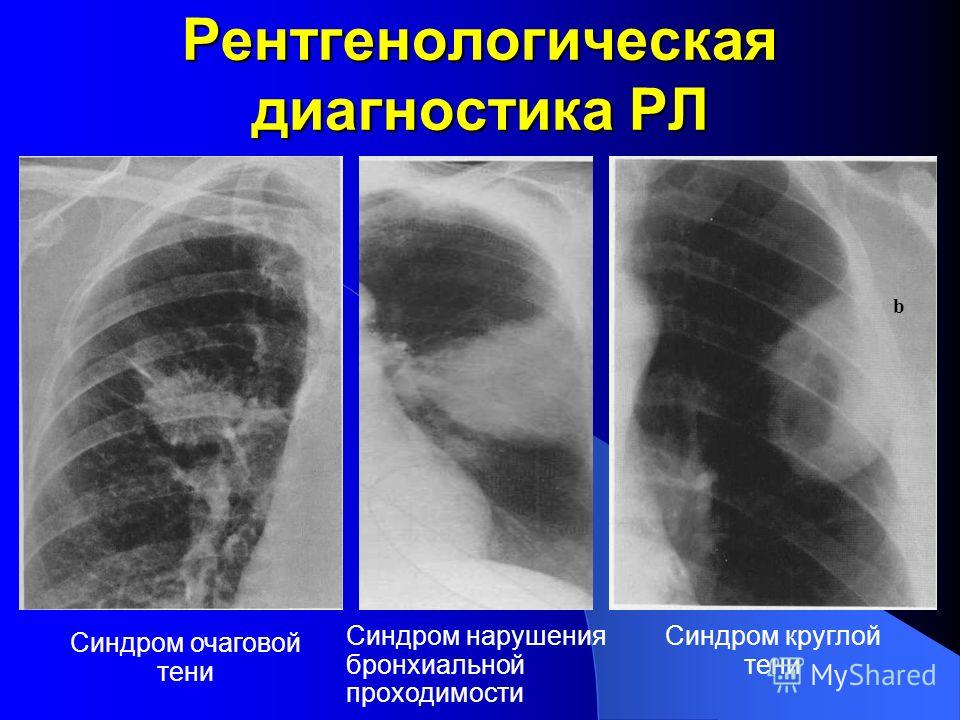 Это международное определение отличается от традиционного отечественного представления о легочных очагах, источником которого является фтизиатрическая практика (в классификации туберкулеза легких размер очагов не превышает 1 см, а уплотнения большего размера определяются как инфильтраты, туберкуломы и другие виды изменений) [14, 15].
Это международное определение отличается от традиционного отечественного представления о легочных очагах, источником которого является фтизиатрическая практика (в классификации туберкулеза легких размер очагов не превышает 1 см, а уплотнения большего размера определяются как инфильтраты, туберкуломы и другие виды изменений) [14, 15].
Патологические образования легких малого размера (до 2 см) в большинстве случаев выявляются при проведении компьютерной томографии грудной клетки, выполняемой по различным причинам [10, 11, 14, 16-18].
Некоторые характеристики объемных образований при КТ позволяют судить об их характере — доброкачественное или злокачественное, однако они не являются определяющими при постановке диагноза [19]. Также о характере образования можно судить по скорости его роста [20].
Между тем по результатам одного КТ-исследования часто трудно провести дифференциальную диагностику, требуются повторные исследования в динамике. При воспалительном процессе очаги исчезают через 1-2 мес. В случае атипичной железистой гиперплазии очаги не изменяются в течение нескольких лет. При аденокарциноме можно заметить увеличение размера и/или усиление плотности, а также сосудистую конвергенцию [11, 12].
В случае атипичной железистой гиперплазии очаги не изменяются в течение нескольких лет. При аденокарциноме можно заметить увеличение размера и/или усиление плотности, а также сосудистую конвергенцию [11, 12].
Обнаруженные при таком обследовании очаговые образования в легочной ткани нередко остаются без внимания специалистов, что порой влечет за собой неутешительные результаты лечения этой категории больных.
Трудности точной диагностики очаговых образований легких хорошо известны — дифференциальную диагностику чаще всего приходится проводить между периферическим раком, доброкачественной опухолью (гамартохондрома и др.), туберкуломой, саркоидозом, метастатическими поражениями легкого [1-4, 6, 7, 10, 12].
По мнению С.В. Миллер и соавт. [8], диагностическая торакотомия является завершающим методом комплексного обследования больных с округлыми образованиями легких небольшого размера и обеспечивает действительно раннюю диагностику и своевременное хирургическое лечение. Следовательно, радикальное хирургическое вмешательство, предпринятое при округлом образовании в легком, генез которого неясен, является методом, позволяющим провести морфологическую верификацию ранней стадии злокачественной опухоли и выполнить органосохраняющую операцию.
Следовательно, радикальное хирургическое вмешательство, предпринятое при округлом образовании в легком, генез которого неясен, является методом, позволяющим провести морфологическую верификацию ранней стадии злокачественной опухоли и выполнить органосохраняющую операцию.
Другие авторы считают, что в настоящее время не существует единого подхода к определению характера очаговых образований легких. Очевидно, что при высоком риске злокачественной опухоли оптимальный подход заключается в возможно более ранней морфологической верификации диагноза. В случае низкого риска злокачественного процесса более рационально проводить динамическое наблюдение [11].
Результатом этих действий может быть выделение группы пациентов с очевидно доброкачественным процессом, о чем свидетельствуют отсутствие динамики роста очага на протяжении 2 и более лет, наличие «доброкачественных» обызвествлений, включений жира (гамартома) или жидкости (киста) в очаге по данным КТ. В такой ситуации необходимо только наблюдение. Сюда же относятся случаи артериовенозных мальформаций и других сосудистых изменений, а также воспалительные процессы в легких (округлый туберкулезный инфильтрат, туберкулома, мицетома и др.), требующие специфического лечения [5, 9, 13].
Сюда же относятся случаи артериовенозных мальформаций и других сосудистых изменений, а также воспалительные процессы в легких (округлый туберкулезный инфильтрат, туберкулома, мицетома и др.), требующие специфического лечения [5, 9, 13].
Второй возможный результат — обнаружение признаков злокачественного процесса (очаг диаметром более 1 см с лучистыми неровными контурами, очаги по типу матового стекла и смешанного солидного типа, которые должны расцениваться как потенциально злокачественные), при которых необходима морфологическая верификация в условиях специализированного лечебного учреждения [12].
Ежегодно в России раком легкого заболевают свыше 63 тыс. человек, в том числе свыше 53 тыс. мужчин. У более 20 тыс. пациентов (34,2%) рак легкого выявляется в IV стадии, поэтому задача обнаружения злокачественных опухолей легких на ранних стадиях их развития чрезвычайно актуальна [2, 7, 8].
Угрожающим фактором при диагностике опухолей легких малого диаметра является их бессимптомность. Отсутствие жалоб, скудная клиническая картина заболевания, сложности с профилактикой и первичным выявлением очагов делают проблему образований легких до 2 см в диаметре актуальной для научных изысканий и практически значимой для сохранения здоровья и нередко жизни пациентов.
Отсутствие жалоб, скудная клиническая картина заболевания, сложности с профилактикой и первичным выявлением очагов делают проблему образований легких до 2 см в диаметре актуальной для научных изысканий и практически значимой для сохранения здоровья и нередко жизни пациентов.
Материал и методы
Работа основана на результатах обследования и лечения 110 больных с патологическими образованиями легких малого диаметра, находившихся в Клинике факультетской хирургии им. Н.Н. Бурденко с 1997 по 2013 г. Мужчин было 63, женщин — 47. Возраст больных находился в пределах 19-74 лет.
У всех больных при рентгенологическом исследовании, включая компьютерную томографию, были впервые выявлены очаговые образования в легких размером от 0,5 до 2 см. Всем пациентам были выполнены операции удаления участков легочной ткани с опухолью из различных доступов: 44 видеоторакоскопические резекции легкого, 43 миниторакотомии с видеосопровождением, 23 миниторакотомии. Окончательный диагноз формулировали после планового гистологического исследования удаленного патологического образования легкого. Летальных исходов не было.
Летальных исходов не было.
Все больные были разделены на группы в зависимости от размера очагового образования: 1-ю группу (диаметр ООЛ 0,5-1; рис. 1) составили 9 мужчин и 14 женщин, 2-ю группу (диаметр ООЛ 1-2 см; рис. 2) — 30 мужчин и 13 женщин, 3-ю группу (множественные ООЛ; рис. 3) — 27 мужчин и 17 женщин.
Рис. 1. Компьютерная томограмма груди пациента 1-й группы
Рис. 2. Компьютерная томограмма груди пациента 2-й группы.
Рис. 3. Компьютерная томограмма груди пациента 3-й группы.
Результаты и обсуждение
Больные 1-й группыбыли оперированы из миниторакотомного доступа, 2-й — из миниторакотомного доступа с видеоподдержкой, 3-й — из видеоторакоскопического доступа. Результаты гистологического исследования удаленных патологических образований представлены в таблице.
Данные гистологического исследования удаленных патологических образований
Очевидно, что в настоящее время остается нерешенным вопрос о показаниях и противопоказаниях к оперативному удалению одиночных образований легких размером от 0,5 до 1 см, диагностические алгоритмы у подобных пациентов также сформулированы нечетко. По нашим данным, злокачественное поражение легких и плевры в этой группе было диагностировано у 3 (13%) пациентов, доброкачественные опухоли — у 5 (21,7%).
По нашим данным, злокачественное поражение легких и плевры в этой группе было диагностировано у 3 (13%) пациентов, доброкачественные опухоли — у 5 (21,7%).
Во 2-й группе у 13 пациентов был выявлен рак легкого. Доброкачественные опухоли (гамартомы) легкого имелись у 18 больных, у 7 пациентов была диагностирована туберкулома. Таким образом, в этой группе частота злокачественных и доброкачественных опухолей вместе с туберкуломами составила 88,4%.
У 9 (20,4%) пациентов 3-й группы были выявлены злокачественные поражения легких, у 10 (22,7%) — диссеминированный туберкулез, у 20 (45,5%) — саркоидоз, что потребовало незамедлительного лечения в специализированных стационарах.
Таким образом, диагностический алгоритм исследований у больных с впервые выявленными периферическими образованиями легких определяют данные мультиспиральной компьютерной томографии. При малом размере образований (от 0,5 до 2 см) показано их удаление без морфологического подтверждения диагноза до операции. Оптимальный оперативный доступ для хирургического лечения пациентов с опухолями легких малого размера следует выбирать в зависимости от диаметра и количества патологических образований. При единичной опухоли легкого размером менее 0,5 см, впервые выявленной при компьютерной томографии, наиболее целесообразной тактикой будет динамическое наблюдение больного и проведение контрольной компьютерной томографии через 3, 6, 12 мес.
Оптимальный оперативный доступ для хирургического лечения пациентов с опухолями легких малого размера следует выбирать в зависимости от диаметра и количества патологических образований. При единичной опухоли легкого размером менее 0,5 см, впервые выявленной при компьютерной томографии, наиболее целесообразной тактикой будет динамическое наблюдение больного и проведение контрольной компьютерной томографии через 3, 6, 12 мес.
*e-mail: с[email protected]
Легочные узлы и поражения легких | Состояние
Одиночный легочный узел или «пятно на легком» определяется как дискретное, четко очерченное, округлое затемнение диаметром менее или равное 3 см (1,5 дюйма), полностью окруженное легочной тканью, не соприкасающееся с легочной тканью. корня легкого или средостения и не сопровождается увеличением лимфатических узлов, коллапсом легкого или плевральным выпотом.
Легочный узел может быть доброкачественным или раковым. Поражения размером более 3 см считаются новообразованиями и рассматриваются как злокачественные, пока не доказано обратное.
Узелки в легких встречаются довольно часто и обнаруживаются на одном из 500 рентгенограмм грудной клетки и одном на 100 КТ грудной клетки. Узелки в легких распознаются чаще благодаря более широкому применению КТ-скрининга рака легких. Примерно у половины курящих людей старше 50 лет на компьютерной томографии грудной клетки обнаруживаются узлы.
Торакальные хирурги и интервенционные пульмонологи в Юго-западном медицинском центре UT проводят передовые процедуры для оценки и лечения легочных узлов и различных поражений легких, включая бронхоскопические процедуры, взятие проб под визуальным контролем, традиционные хирургические процедуры и более современные минимально инвазивные и роботизированные методы. .
Мы предлагаем новейшие методы визуализации и лечения в нашем передовом центре визуализации, включая эндобронхиальное ультразвуковое исследование (EBUS), электромагнитную навигационную бронхоскопию (ENB) и многие другие методы.
Наши хирурги тесно сотрудничают с группой специалистов по интервенционным легочным заболеваниям UTSouthwestern, врачами-онкологами, рентгенологами и патологоанатомами для оказания комплексной помощи — и все это в одном месте и обычно в один и тот же день. Клиника легочных узлов в UTSouthwestern оптимизирует оценку и лечение пациентов с легочными узлами и аномальными результатами визуализации, включая скрининг КТ.
Клиника легочных узлов в UTSouthwestern оптимизирует оценку и лечение пациентов с легочными узлами и аномальными результатами визуализации, включая скрининг КТ.
Причины узелков в легких
Узлы в легких могут быть доброкачественными (нераковыми) или злокачественными (рак). Наиболее распространенными причинами доброкачественных узлов являются гранулемы (скопления воспаленной ткани) и гамартомы (доброкачественные опухоли легких).
Наиболее частая причина раковых или злокачественных узлов в легких включает рак легких или рак из других областей тела, который распространился на легкие (метастатический рак).
Узлы в легких можно разделить на несколько основных категорий:
- Доброкачественные опухоли, такие как гамартомы
- Инфекции, включая бактериальные инфекции, такие как туберкулез, и грибковые инфекции, такие как гистоплазмоз и кокцидиомикоз
- Воспаления, такие как ревматоидный артрит, саркоидоз и гранулематоз Вегенера, включая опухоли легких
- 4 90 и рак, который распространился на легкие из других частей тела.

В целом вероятность того, что узелок в легком является раком, составляет примерно 40 процентов, но риск того, что узелок в легком станет злокачественным, значительно варьируется в зависимости от нескольких факторов, в том числе:
- Возраст : Редко у людей моложе 35 лет. Половина легочных узлов у людей старше 50 лет являются злокачественными
- Кальцификация : Кальцинированные легочные узлы с большей вероятностью являются доброкачественными
- Кавитация на рентгеновских снимках кажется, что узелок содержит воздух, с большей вероятностью являются доброкачественными
- Рост : раковые узелки в легких имеют тенденцию расти довольно быстро со средним временем удвоения около четырех месяцев, в то время как доброкачественные узелки, как правило, остаются прежнего размера со временем
- Медицинский анамнез : Наличие рака в анамнезе увеличивает вероятность того, что он может быть злокачественным Текущие и бывшие у курильщиков вероятность развития раковых узлов в легких выше, чем у никогда не куривших0023 Форма : Гладкие, круглые узлы с большей вероятностью являются доброкачественными, в то время как узлы неправильной формы или с шипами, скорее всего, являются раковыми
Диагностика
физикальное обследование и назначение анализов для подтверждения диагноза.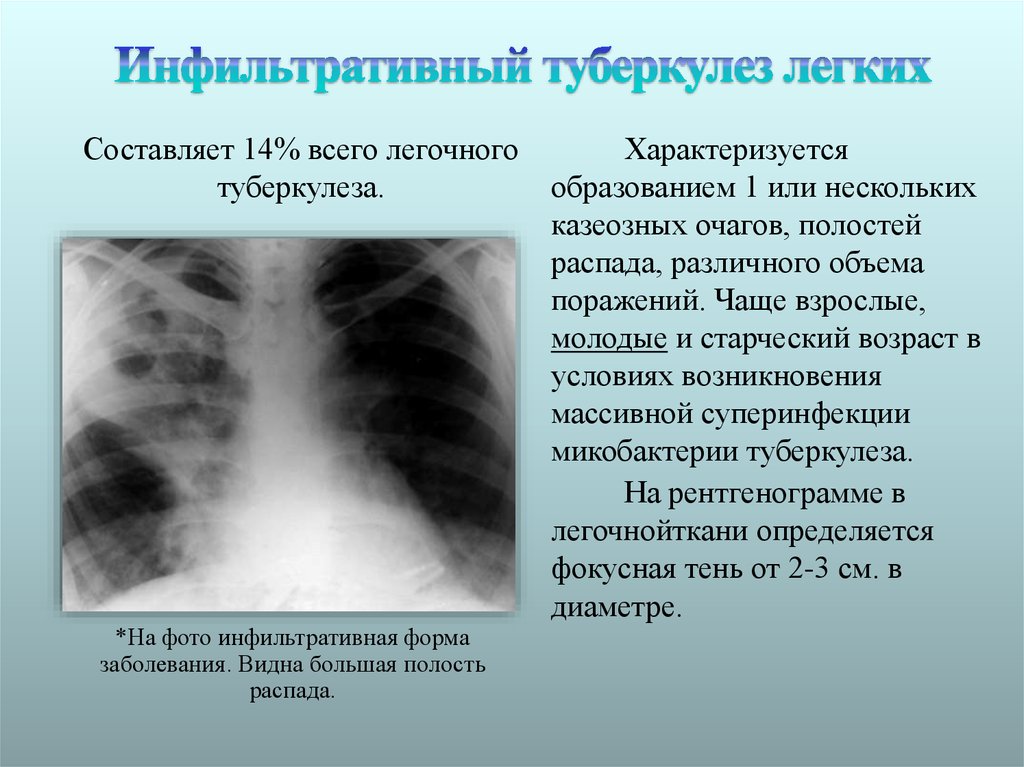 Исследования для оценки и диагностики легочных узлов могут включать:
Исследования для оценки и диагностики легочных узлов могут включать:
- Бронхоскопию, в том числе передовые управляемые методы, такие как эндобронхиальное ультразвуковое исследование (EBUS), электромагнитную навигационную бронхоскопию (ENB) и другие процедуры
- Рентген грудной клетки (рентгенограммы)
- Компьютерная томография (КТ), включая скрининговую компьютерную томографию
- Флюороскопия: рентгенография в режиме реального времени тонкоигольная аспирационная биопсия или FNA)
- Магнитно-резонансная томография (МРТ)
- Минимально инвазивная биопсия легкого (торакоскопическая или роботизированная)
- Позитронно-эмиссионная томография (ПЭТ)
- Исследования функции легких (PFT)
На основании характеристик и размера легочного узла на КТ мы можем рекомендовать:
- Наблюдение и повторные рентгенологические исследования, если узел, вероятно, доброкачественный грудной клетки или ПЭТ-сканирование
- Биопсия узла с помощью бронхоскопии (если узел находится рядом с одним из ваших дыхательных путей), пункционной биопсии (если узел расположен снаружи легких) или хирургии легких (видеоассистированная торакоскопическая хирургия), если мы думаем, что это может быть злокачественным
- Лечение
Когда операция является наиболее подходящей терапией, наши торакальные хирурги лечат легочные узлы и поражения легких с помощью процедур, которые включают:
Минимально инвазивная хирургия
По сравнению с операцией, выполняемой через открытый разрез грудной клетки, минимально инвазивная хирургия дает пациентам несколько важных преимуществ, в том числе:
- Быстрее восстановление и возвращение к нормальной деятельности
- Более короткое пребывание в больнице
- Меньшая боль
- Незначительные рубцы
- Минимальная кровопотеря
- Отсутствие рассечения ребер или грудины
Если операция у пациента с раковым или злокачественным узлом невозможна, наша многопрофильная команда хирургов, онкологов и онкологов-радиологов предоставит рекомендации по наилучшему варианту лечения. Эти варианты могут включать передовые методы лучевой терапии, системную терапию с традиционной химиотерапией и/или таргетную или персонализированную терапию.
Эти варианты могут включать передовые методы лучевой терапии, системную терапию с традиционной химиотерапией и/или таргетную или персонализированную терапию.
Клинические испытания
UTSouthwestern проводит клинические испытания, направленные на улучшение лечения легочных узлов. Поговорите со своим врачом, чтобы узнать, подходит ли вам клиническое испытание.
Очаговые аномалии | Учебник ESC по сердечно-сосудистой медицине | Публикации ESC
Фильтр поиска панели навигации Публикации ESCУчебник ESC по сердечно-сосудистой медицине (3-е изд.)Oxford Medicine OnlineBooksJournalsOxford Academic Мобильный телефон Введите поисковый запрос
Закрыть
Фильтр поиска панели навигации Публикации ESCУчебник ESC по сердечно-сосудистой медицине (3-е изд.)Oxford Medicine OnlineBooksJournalsOxford Academic Введите поисковый запрос
Расширенный поиск
Иконка Цитировать Цитировать
Разрешения
- Делиться
- Твиттер
- Подробнее
Укажите
Герольд, Кристиан и др. (ред.), «Очаговые аномалии», в книге А. Джона Кэмма и др. (ред.), Учебник ESC по сердечно-сосудистой медицине , 3 изд., Серия Европейского общества кардиологов (
(ред.), «Очаговые аномалии», в книге А. Джона Кэмма и др. (ред.), Учебник ESC по сердечно-сосудистой медицине , 3 изд., Серия Европейского общества кардиологов (
, 2018 г. ; онлайн-издание, ESC Publications, 1 июля 2018 г.), https://doi.org/10.1093/med/9780198784906.003.0081, по состоянию на 19 апреля 2023 г.
Выберите формат Выберите format.ris (Mendeley, Papers, Zotero).enw (EndNote).bibtex (BibTex).txt (Medlars, RefWorks)
Закрыть
Фильтр поиска панели навигации Публикации ESCУчебник ESC по сердечно-сосудистой медицине (3-е изд.)Oxford Medicine OnlineBooksJournalsOxford Academic Мобильный телефон Введите поисковый запрос
Закрыть
Фильтр поиска панели навигации
Публикации ESCУчебник ESC по сердечно-сосудистой медицине (3-е изд. )Oxford Medicine OnlineBooksJournalsOxford Academic
Введите поисковый запрос
)Oxford Medicine OnlineBooksJournalsOxford Academic
Введите поисковый запрос
Advanced Search
Abstract
Обнаружение и интерпретация очаговых аномалий на рентгенограмме грудной клетки (CXR) представляют собой сложные задачи. Точность CXR зависит от вида (например, вид в положении лежа имеет ограниченную чувствительность) и технологического оборудования. Обнаружение небольших очаговых аномалий (например, узелков в легких) варьируется в зависимости от анатомических областей в зависимости от наличия плотных анатомических структур, таких как кости и ворота. Интерпретация очаговых аномалий на рентгенограмме имеет первостепенное значение во всей клинической оценке, потому что результаты рентгенографии могут служить ориентиром для лечения пациента или требовать дальнейших исследований, таких как компьютерная томография. Очаговые аномалии легких на рентгенограмме до сих пор являются краеугольным камнем диагностических алгоритмов; однако за последнее десятилетие радиологический подход постепенно изменился из-за прогрессивного развития как аппаратных, так и программных приложений, которые обеспечивают чувствительное обнаружение и точную характеристику.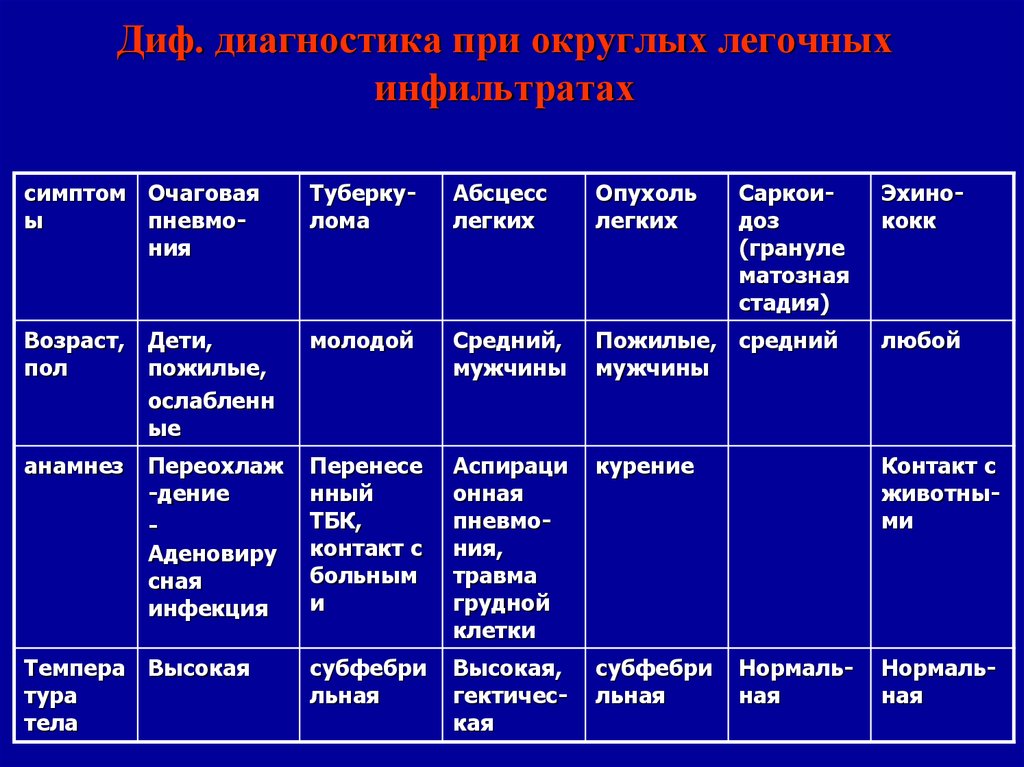
Ключевые слова: рентгенограмма грудной клетки, затемнение очага, пневмония, обнаружение, узелок, рак
Коллекция: Оксфорд Медицина Онлайн
Отказ от ответственности
Издательство Оксфордского университета не делает заявлений, явных или подразумеваемых, о том, что дозировки лекарств, указанные в этой книге, верны.
Поэтому читатели должны всегда…
Более
Издательство Оксфордского университета не делает заявлений, явных или подразумеваемых, о том, что дозировки лекарств, указанные в этой книге, верны.
Поэтому читатели должны всегда проверять информацию о продукте и клинических процедурах с самой последней опубликованной информацией о продукте и таблицами данных.
предоставленных производителями, а также самые последние кодексы поведения и правила техники безопасности.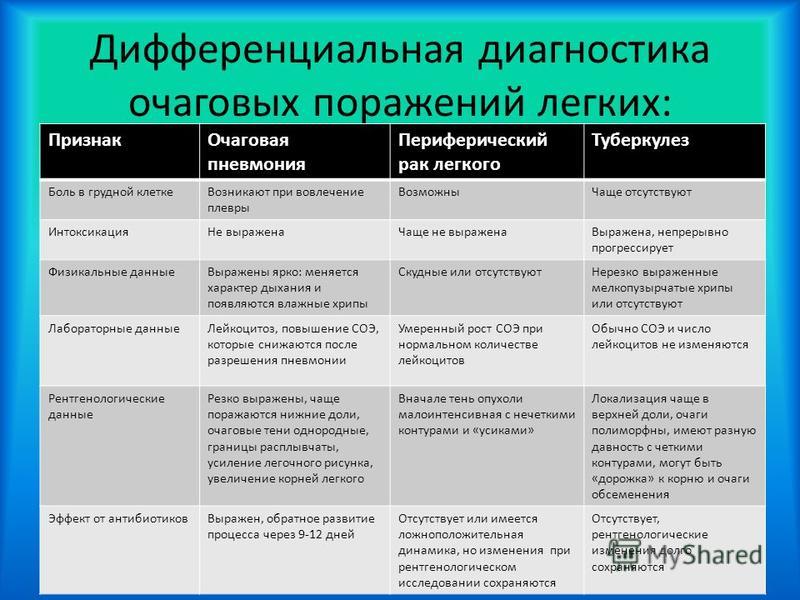 Авторы и издатели не несут ответственности и
юридическую ответственность за любые ошибки в тексте или за неправильное использование или неправильное применение материала в этой работе. Если не указано иное, дозы препаратов
и рекомендации для небеременных взрослых, которые не кормят грудью.
Авторы и издатели не несут ответственности и
юридическую ответственность за любые ошибки в тексте или за неправильное использование или неправильное применение материала в этой работе. Если не указано иное, дозы препаратов
и рекомендации для небеременных взрослых, которые не кормят грудью.
В настоящее время у вас нет доступа к этой главе.
Войти
Получить помощь с доступом
Получить помощь с доступом
Доступ для учреждений
Доступ к контенту в Oxford Academic часто предоставляется посредством институциональных подписок и покупок. Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов:
Доступ на основе IP
Как правило, доступ предоставляется через институциональную сеть к диапазону IP-адресов.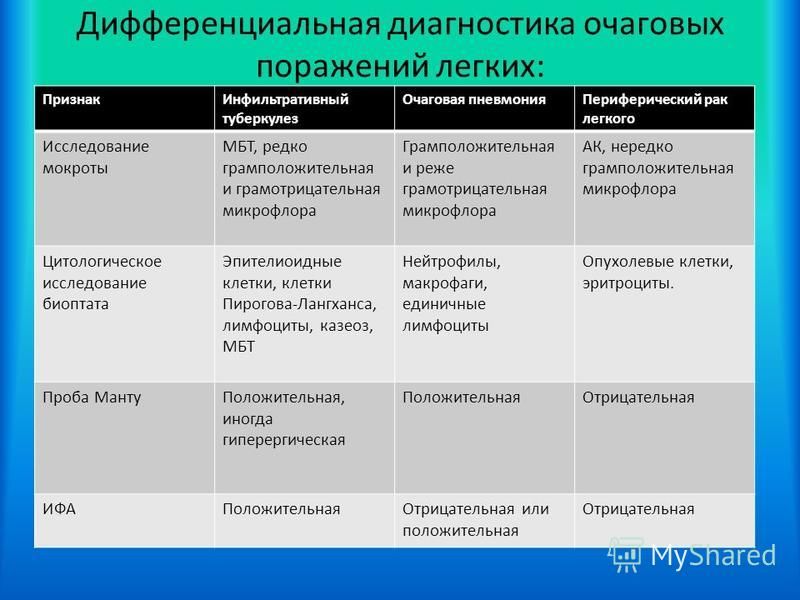 Эта аутентификация происходит автоматически, и невозможно выйти из учетной записи с IP-аутентификацией.
Эта аутентификация происходит автоматически, и невозможно выйти из учетной записи с IP-аутентификацией.
Войдите через свое учреждение
Выберите этот вариант, чтобы получить удаленный доступ за пределами вашего учреждения. Технология Shibboleth/Open Athens используется для обеспечения единого входа между веб-сайтом вашего учебного заведения и Oxford Academic.
- Щелкните Войти через свое учреждение.
- Выберите свое учреждение из предоставленного списка, после чего вы перейдете на веб-сайт вашего учреждения для входа.
- Находясь на сайте учреждения, используйте учетные данные, предоставленные вашим учреждением. Не используйте личную учетную запись Oxford Academic.
- После успешного входа вы вернетесь в Oxford Academic.
Если вашего учреждения нет в списке или вы не можете войти на веб-сайт своего учреждения, обратитесь к своему библиотекарю или администратору.
Вход с помощью читательского билета
Введите номер своего читательского билета, чтобы войти в систему. Если вы не можете войти в систему, обратитесь к своему библиотекарю.
Члены общества
Доступ члена общества к журналу достигается одним из следующих способов:
Войти через сайт сообщества
Многие общества предлагают единый вход между веб-сайтом общества и Oxford Academic. Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
- Щелкните Войти через сайт сообщества.
- При посещении сайта общества используйте учетные данные, предоставленные этим обществом. Не используйте личную учетную запись Oxford Academic.
- После успешного входа вы вернетесь в Oxford Academic.
Если у вас нет учетной записи сообщества или вы забыли свое имя пользователя или пароль, обратитесь в свое общество.
Вход через личный кабинет
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам. См. ниже.
Личный кабинет
Личную учетную запись можно использовать для получения оповещений по электронной почте, сохранения результатов поиска, покупки контента и активации подписок.
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам.
Просмотр ваших зарегистрированных учетных записей
Щелкните значок учетной записи в правом верхнем углу, чтобы:
- Просмотр вашей личной учетной записи и доступ к функциям управления учетной записью.
- Просмотр институциональных учетных записей, предоставляющих доступ.
Выполнен вход, но нет доступа к содержимому
Oxford Academic предлагает широкий ассортимент продукции.


