reproducibility of the ZAP classification among endoscopists
Аннотация:
Отделение хирургических наук, Упсальская университетская больница, Упсала, Швеция.
Фон : гистологическое присутствие кишечной метаплазии в пищеводе является необходимым условием для диагностики пищевода Барретта. Таким образом, использование термина пищевода Барретта для описания определенных эндоскопических особенностей дистального отдела пищевода нецелесообразно. Не существует общепринятой системы классификации для эндоскопического описания плоскоклеточного слизистого перехода, так называемой «Z-линии». Кроме того, не существует четкого определения нормальной Z-линии. Предложена классификация внешнего вида Z-линии: классификация ZAP. Целью данного исследования было оценить воспроизводимость этой классификации.
Методы: Десять врачей с различным опытом эндоскопии получили 15 эндоскопических фотографий Z-линии, и им было предложено классифицировать их в соответствии с классификацией ZAP. Вторая оценка была проведена между 7 и 15 неделями после первой.
Вторая оценка была проведена между 7 и 15 неделями после первой.
Результаты: Медианные значения каппа находились в диапазоне от 0,72 до 0,90 в отношении внутриобозревательной, а также воспроизводимости между наблюдателями, независимо от опыта с верхней эндоскопией.
Выводы: внутриобозревательная и межобозревательная воспроизводимость классификации ZAP является существенной, и, таким образом, целесообразно использовать эту классификацию для характеристики появления Z-линии при эндоскопии.
Abstract
Background: The histologic presence of intestinal metaplasia in the esophagus is a prerequisite for the diagnosis of Barrett’s esophagus. Thus, use of the term Barrett’s esophagus to describe certain endoscopic features in the distal esophagus is inappropriate. There is no accepted classification system for the endoscopic description of the squamocolumnar mucosal junction, the so-called “Z-line.” Furthermore, no clear definition of the normal Z-line exists. A classification of the Z-line appearance has been proposed: the ZAP classification.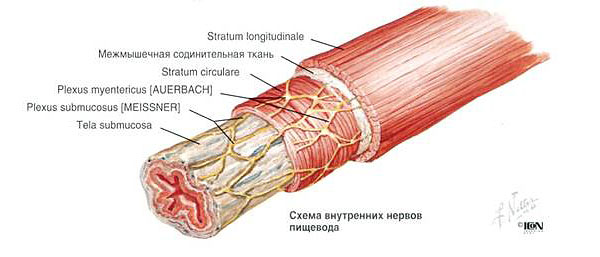 The aim of this study was to assess the reproducibility of this classification.
The aim of this study was to assess the reproducibility of this classification.
Methods: Ten physicians with varying endoscopy experience were presented with 15 endoscopic photographs of the Z-line and were asked to classify them according to the ZAP classification. A second assessment was conducted between 7 and 15 weeks after the first. Results: The median κ values were in the range of 0.72 to 0.90 with regard to intraobserver as well as interobserver reproducibility, irrespective of experience with upper endoscopy.
Conclusions: The intraobserver and interobserver reproducibility of the ZAP classification is substantial and thus it is feasible to use this classification to characterize the appearance of the Z-line at endoscopy. ( GASTROINTESTINAL ENDOSCOPY 2002;55:65-9.)
Классификация ZAP, вероятно, будет интересна для практического и повсеместного применения в России, однако до принятия ее Эндоскопическим сообществом может пройти очень много времени.
Список литературы:
1. Armstrong D, Bennett JR, Blum AL, Dent J, De Dombal FT, Galmiche JP,et al. The endoscopic assessment of esophagitis: a progress report on observer agreement. Gastroenterology 1996;111:85-92.
Armstrong D, Bennett JR, Blum AL, Dent J, De Dombal FT, Galmiche JP,et al. The endoscopic assessment of esophagitis: a progress report on observer agreement. Gastroenterology 1996;111:85-92.
2. Spechler SJ, Goyal RK. Barrett’s esophagus. N Engl J Med 1986;315:362-71.
3. Sampliner RE. Practice guidelines on the diagnosis, surveil¬lance, and therapy of Barrett’s esophagus. The Practice Parameters Committee of the American College of Gastro¬enterology. Am J Gastroenterol 1998;93:1028-32.
4. Spechler SJ, Zeroogian JM, Antonioli DA, Wang HH, Goyal RK. Prevalence of metaplasia at the gastro-oesophageal junc¬tion. Lancet 1994;344:1533-6.
5. Johnston MH, Hammond AS, Laskin W, Jones DM. The preva¬lence and clinical characteristics of short segments of special¬ized intestinal metaplasia in the distal esophagus on routine endoscopy. Am J Gastroenterol 1996;91:1507-11.
 Short segment Barrett’s esophagus: clin¬ical and histological features, associated endoscopic findings, and association with gastric intestinal metaplasia. Am J Gastroenterol 1996;91:981-6.
Short segment Barrett’s esophagus: clin¬ical and histological features, associated endoscopic findings, and association with gastric intestinal metaplasia. Am J Gastroenterol 1996;91:981-6.
7. Nandurkar S, Talley NJ, Martin CJ, Ng TH, Adams S. Short segment Barrett’s oesophagus: prevalence, diagnosis and associations. Gut 1997;40:710-5.
8. Trudgill NJ, Suvarna SK, Kapur KC, Riley SA. Intestinal
metaplasia at the squamocolumnar junction in patients attending for diagnostic gastroscopy [see comments]. Gut 1997;41:585-9.
9. Clark GWB, Ireland AP, Peters JH, Chandrasoma P, DeMeester TR, Bremner CG. Short-segment Barrett’s esophagus: a preva¬lent complication of gastroesophageal reflux disease with malig¬nant potential. J Gastrointest Surg 1997;1:113-22.
10. Csendes A, Smok G, Sagastume H, Rojas J. Endoscopic assessment of the prevalence of gastro esophageal junction intestinal metaplasia in gastroesophageal reflux [in Spanish with English abstract].
 Rev Med Chil 1998;126:155-61.
Rev Med Chil 1998;126:155-61.
11. Pereira AD, Suspiro A, Chaves P, Saraiva A, Gloria L,de Almeida JC, et al. Short segments of Barrett’s epithelium and intestinal metaplasia in normal appearing oesophagogastric junctions: the same or two different entities? Gut 1998;42:659-62.
12. Hackelsberger A, Gunther T, Schultze V, Manes G, Dominguez- Munoz JE, Roessner A, et al. Intestinal metaplasia at the gastro-oesophageal junction: Helicobacter pylori gastritis or gastro-oesophageal reflux disease? Gut 1998;43:17-21.
13. Voutilainen M, Farkkila M, Juhola M, Nuorva K, Mauranen K, Mantynen T, et al. Specialized columnar epithelium of the esophagogastric junction: prevalence and associations. The Central Finland Endoscopy Study Group. Am J Gastroenterol 1999;94:913-8.
15.
 Carton E, Caldwell MT, McDonald G, Rama D, Tanner WA, Reynolds JV. Specialized intestinal metaplasia in patients with gastro-oesophageal reflux disease. Br J Surg 2000;87:116-21.
Carton E, Caldwell MT, McDonald G, Rama D, Tanner WA, Reynolds JV. Specialized intestinal metaplasia in patients with gastro-oesophageal reflux disease. Br J Surg 2000;87:116-21.
16. Voutilainen M, Farkkila M, Mecklin JP, Juhola M, Sipponen P. Classical Barrett esophagus contrasted with Barrett-type epithelium at normal-appearing esophagogastric junction. Central Finland Endoscopy Study Group. Scand J Gastro¬enterol 2000;35:2-9.
17. Wallner B, Sylvan A, Stenling R, Janunger KG. The esophageal Z-line appearance correlates to the prevalence of intestinal metaplasia. Scand J Gastroenterol 2000;35:17-22.
18. Wallner B, Sylvan A, Janunger KG, Bozoky B, Stenling R. Immunohistochemical markers for Barrett’s esophagus and associations to esophageal Z-line appearance. Scand J Gastroenterol. 2001;36:910-5.
19. Wallner B, Sylvan A, Stenling R, Janunger KG.A postfundo- plication study on Z-line appearance and intestinal metapla¬sia in the gastroesophageal junction.
 Surg Laparosc Endosc 2001;11:235-41.
Surg Laparosc Endosc 2001;11:235-41.
20. Wallner B, Sylvan A, Stenling R, Janunger KG. The Z-line appearance and prevalence of intestinal metaplasia among patients without symptoms or endoscopical signs indicating gastroesophageal reflux. Surg Endosc. 2001;5:886-9.
22. Savary M, Miller G. The esophagus: handbook and atlas of endoscopy. Solothurn, Switzerland: Gassmann; 1978.
23. DeNardi FG, Riddell RH. The normal esophagus. Am S Surg Pathol 1991;15:296-309.
24. Landis JR, Koch GG. The measurement of observer agree¬ment for categorical data. Biometrics 1977;33:159-74.
25. Svanholm H, Starklint H, Gundersen HJ, Fabricius J, Barlebo H, Olsen S. Reproducibility of histomorphologic diagnoses with special reference to the kappa statistic. Apmis 1989;97: 689-98.
26. Lundell LR, Dent J, Bennett JR, Blum AL, Armstrong D, Galmiche JP, et al.
 Endoscopic assessment of oesophagitis: clinical and functional correlates and further validation of the Los Angeles classification. Gut 1999;45:172-80.
Endoscopic assessment of oesophagitis: clinical and functional correlates and further validation of the Los Angeles classification. Gut 1999;45:172-80.
VOLUME 55, NO. 1, 2002
GASTROINTESTINAL ENDOSCOPY 69
Пищевод Барретта: рекомендации ACG » Медвестник
Американская коллегия гастроэнтерологов (ACG) обновила рекомендации по диагностике, скринингу, наблюдению, эндоскопическому лечению и терапии пациентов с пищеводом Барретта.
ACG обновила клинические рекомендации по ведению пациентов с пищеводом Барретта. Полный текст опубликован в журнале AJG.
Пищевод Барретта — метаплазия дистальной части пищевода, вследствие которой плоский эпителий пищевода замещается цилиндрическим эпителием с бокаловидными клетками, сходным с кишечным. Заболевание связано с хронической гастроэзофагеальной рефлюксной болезнью (ГЭРБ), развивается у 5—12% пациентов. Это единственное известное предраковое заболевание для аденокарциномы пищевода. Цилиндрический эпителий при пищеводе Барретта содержит три типа клеток: эпителий фундального типа, переходный эпителий кардиального типа и специализированный столбчатый эпителий кишечного типа с бокаловидными клетками. Цилиндрический эпителий при пищеводе Барретта содержит три типа клеток: эпителий фундального типа, переходный эпителий кардиального типа и специализированный столбчатый эпителий кишечного типа с бокаловидными клетками. |
Диагностика
Для постановки диагноза необходимо выявление кишечной метаплазии пищевода во время эндоскопического исследования. Длина участка цилиндрического эпителия должна составлять хотя бы 1 см.
Пациентам с нормальной линией пищеводно-желудочного перехода (Z-линией), выявленной во время эндоскопического исследования, не показана рутинная биопсия. При отсутствии видимых очагов и смещении Z-линии менее чем на 1 см от верхней границы желудка проведение плановой эндоскопической биопсии не показано.
При выявлении во время эндоскопического исследования признаков, характерных для пищевода Барретта, показано проведение восьми эндоскопических биопсий. Если участок поражения больше 4 см длиной, показана биопсия в соответствии с Сиэтлским протоколом.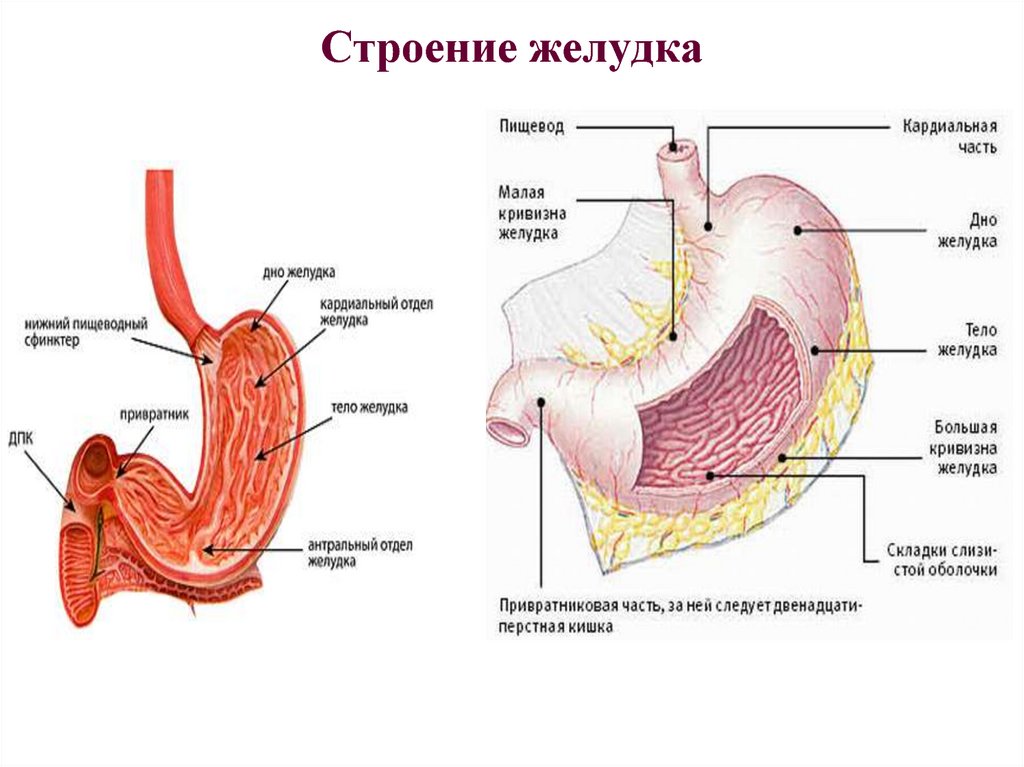 Согласно ему эндоскопистам следует внимательно осмотреть сегмент пищевода Барретта и взять биопсию из всех видимых очагов, а затем из четырех точек по окружности с интервалом 2 см и меньше от нижнего пищеводного сфинктера до Z-линии.
Согласно ему эндоскопистам следует внимательно осмотреть сегмент пищевода Барретта и взять биопсию из всех видимых очагов, а затем из четырех точек по окружности с интервалом 2 см и меньше от нижнего пищеводного сфинктера до Z-линии.
При выявлении дисплазии любой степени результаты биопсии пищевода Барретта следует подтвердить при участии другого гистолога с опытом работы в гастроэнтерологии.
Скрининг
Пациентам с симптомами хронической ГЭРБ при наличии трех факторов риска и более показано проведение однократного эндоскопического скринингового обследования для выявления пищевода Барретта.
К факторам риска относят мужской пол, возраст старше 50 лет, курение, ожирение, отягощенный семейный анамнез. Золотым стандартом скрининга является традиционное пероральное эндоскопическое исследование под седацией. Альтернативой эндоскопическому скринингу может служить проведение капсульной эндоскопии в сочетании с исследованием биомаркеров.
Если результат первичного обследования отрицательный, повторный скрининг не показан.
Динамическое наблюдение
При проведении контрольного обследования показано эндоскопическое исследование в белом свете и хромоэндоскопия.
При проведении биопсии рекомендовано придерживаться структурированного Сиэтлского протокола, чтобы уменьшить число ошибок при выявлении заболевания.
Частота проведения контрольных обследований при пищеводе Барретта должна определяться степенью ранее выявленной дисплазии. Кроме того, необходимо учитывать протяженность ранее выявленных изменений. Если пораженный сегмент меньше 3 см, интервалы между обследованиями можно увеличить.
Терапия
Пациентам с пищеводом Барретта показан прием ингибиторов протонной помпы хотя бы один раз в день при отсутствии противопоказаний и аллергических реакций. Ингибиторы протонной помпы уменьшают выраженность симптомов ГЭРБ и улучшают качество жизни.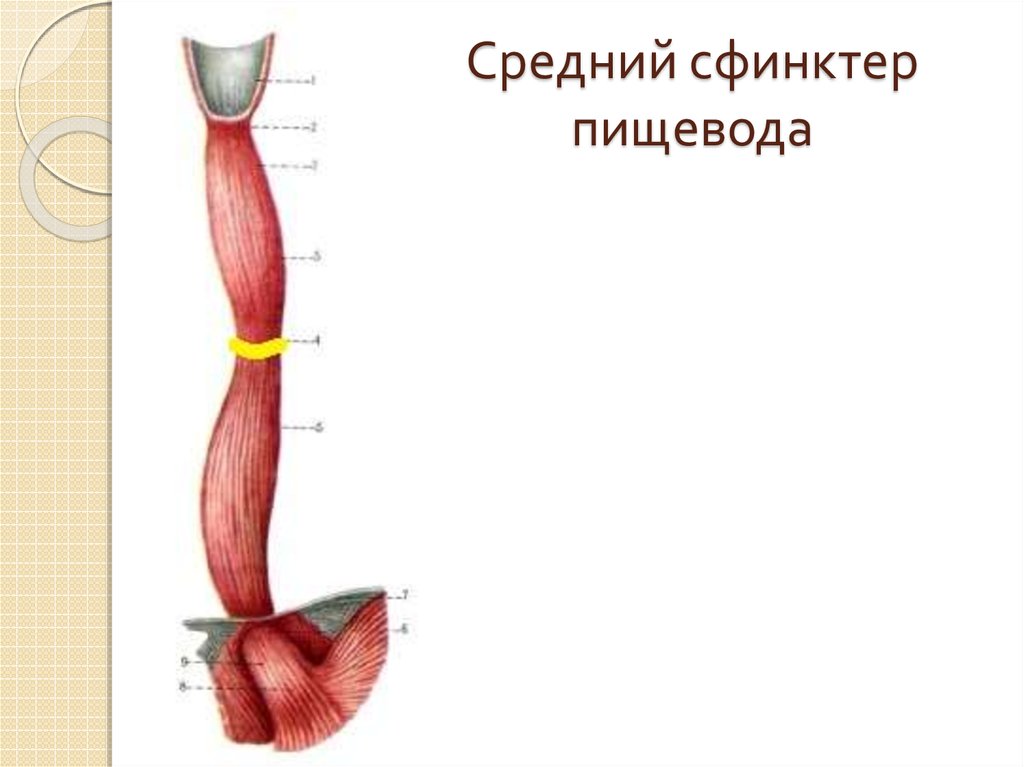 К тому же исследования показали, что их применение может предотвратить неопластическое прогрессирование.
К тому же исследования показали, что их применение может предотвратить неопластическое прогрессирование.
ACG не может дать рекомендаций по использованию сочетания ингибиторов протонной помпы и аспирина.
Проведение антирефлюксного оперативного лечения для предотвращения развития аденокарциномы пищевода не показано.
Эндоскопическое лечение
Пациентам с пищеводом Барретта, тяжелой дисплазией или раком в пределах слизистой оболочки рекомендуется проведение эндоскопической эрадикационной терапии. Обычно такое лечение включает эндоскопическую резекцию любых видимых очагов с последующим использованием радиочастотной абляции или криотерапии для полной эрадикации дисплазии и внутрислизистого рака.
Пациентам с легкой дисплазией показано проведение эндоскопической эрадикационной терапии, чтобы снизить риск прогрессирования в тяжелую дисплазию и аденокарциному пищевода. В качестве альтернативы возможно эндоскопическое наблюдение с контролем каждые шесть месяцев в течение первого года, а затем один раз в год.
Перед проведением абляции рекомендуется эндоскопическая резекция всех видимых очагов. Эндоскопическую эрадикационную терапию рекомендуется проводить в крупных медицинских центрах.
Пациентам, прошедшим эндоскопическую эрадикационную терапию, рекомендуется дальнейшее динамическое наблюдение. Частота рецидива кишечной метаплазии после полной эрадикации составляет 8,6—10,5%, по данным исследований. Частота рецидива тяжелой дисплазии/аденокарциномы пищевода — 1,2%. Чаще всего рецидивы происходят в течение первого года после лечения. Пациентам с легкой дисплазией рекомендуется эндоскопическое наблюдение через один и три года после эрадикации, а затем каждые два года. Пациентам с тяжелой дисплазией и внутрислизистым раком показано эндоскопическое исследование через 3, 6 и 12 месяцев после эрадикационной терапии, а затем ежегодно.
Важность неправильной линии Z: Барретт в глазах смотрящего?
Важность неправильной Z-линии: Барретт в глазах смотрящего?
Скачать PDF
Скачать PDF
- Редакция
- Опубликовано:
- Свати Элури 1 и
- Николас Дж. Шахин 1
Пищеварительные заболевания и науки том 63 , страницы 1378–1380 (2018)Цитировать эту статью
158 тыс. Доступов
2 Цитаты
2 Альтметрика
Сведения о показателях
Картина живет только в глазах смотрящего .
-Пабло Пикассо
Линия Z разграничивает плоскоклеточный переход (SCJ), переход плоскоклеточной слизистой оболочки пищевода в столбчатую слизистую оболочку, выстилающую желудок, или, в случае пищевода Барретта, между плоскоклеточным и интестинальным столбчатым эпителием метапластического сегмента. Неправильная Z-линия характеризуется столбчатыми языками < 1 см, которые простираются проксимальнее желудочно-пищеводного перехода, что было зарегистрировано примерно у 10–15% населения, подвергающегося эндоскопии верхних отделов [1, 2]. У пациентов с неправильной линией Z частота кишечной метаплазии (КМ) достигает 44% [3]. Тем не менее, клиническая значимость этого вывода в отношении риска прогрессирования неоплазии у пациентов с неправильной линией Z и ИМ неясна [4].
В то время как предшествующие руководства противоречат стратегиям лечения предполагаемых сегментов пищевода Барретта (ПБ) < 1 см, самые последние рекомендации Американского колледжа гастроэнтерологов (ACG) [5] не рекомендуют проводить биопсию из неправильной Z-линии, рекомендация, сделанная из-за плохой эндоскопической стандартизации этого вывода (нормальная линия Z одного эндоскописта является неправильной линией Z другого), дополнительных затрат, связанных с этой практикой, потенциального беспокойства пациента, а также низких показателей распространенной и эпизодической дисплазии и пищевода. В этих поражениях обнаружена аденокарцинома (EAC). Кроме того, пациенты с неправильной линией Z, у которых имеется ИМ, могут быть включены в протоколы эндоскопического наблюдения, что требует затрат и неудобств повторной эндоскопии наблюдения, а также стигмы ярлыка заболевания для потенциально неопластического состояния.
В этих поражениях обнаружена аденокарцинома (EAC). Кроме того, пациенты с неправильной линией Z, у которых имеется ИМ, могут быть включены в протоколы эндоскопического наблюдения, что требует затрат и неудобств повторной эндоскопии наблюдения, а также стигмы ярлыка заболевания для потенциально неопластического состояния.
Проспективное одноцентровое исследование, проведенное Ицковизом и соавт. опубликованный в текущем выпуске Digestive Diseases and Sciences [6], описывает риск развития BE, дисплазии и EAC у пациентов с нерегулярной Z-линией и IM по сравнению с теми, у кого неправильная Z-линия без IM. У 166 пациентов эндоскопически была диагностирована неправильная линия Z, определяемая здесь как вариабельность плоскостолбчатого соединения ≤ 5 мм при индексной эндоскопии. Из 166 пациентов, перенесших эндоскопию верхних отделов по поводу таких показаний, как изжога, дисфагия и боль в груди, 39% ( n = 64) имели ИМ, подтвержденный биопсией. Из 50 пациентов с ИМ, которые наблюдались в среднем в течение 70 месяцев, у 16% развилась недиспластическая ПБ (НДБЭ) ( n = 8), а у 4% ( n = 2) развилась дисплазия низкой степени (LGD ). Из случаев без ИМ только в 1/52 развилась ПБ, и ни в одном случае дисплазия не прогрессировала. В этой выборке 22% пациентов с ИМ и 49% без ИМ выбыли из-под наблюдения.
Из случаев без ИМ только в 1/52 развилась ПБ, и ни в одном случае дисплазия не прогрессировала. В этой выборке 22% пациентов с ИМ и 49% без ИМ выбыли из-под наблюдения.
В целом среди пациентов с неправильной линией Z в этом исследовании у 8,8% развился NDBE и у 1,9%% развился LGD в течение среднего времени 70 месяцев. Авторы отмечают в своем заключении, что у пациентов с неправильной линией Z «не развивается серьезное осложнение ПБ в течение более чем 5 лет наблюдения». Тем не менее, они также предполагают в своем обсуждении, что из-за 16% случаев ПБ в IM-положительной группе и у двух пациентов, у которых развилась LGD, «длительные последующие исследования могут выявить более злонамеренную природу неправильной Z-линии с кишечной инфекцией». метаплазия.»
Это исследование имеет несколько похвальных достоинств: оно является проспективным, со стандартизированным протоколом биопсии с последующим наблюдением, в среднем 70 месяцев, что является достаточной продолжительностью, чтобы можно было наблюдать клинически значимые тенденции, и были рассмотрены соответствующие ковариаты, включая тщательную оценку линии Z. Очевидны и некоторые недостатки: выбывание из наблюдения было значительным, особенно в группе без ИМ, где почти половина пациентов не проходили повторное обследование; Кроме того, учитывая, что неправильная Z-линия не является показанием для повторной ЭГДС, неясно, проводились ли эти последующие обследования как часть протокола исследования или для клинической помощи. Если верно последнее, результаты следует рассматривать в несколько ином свете из-за предвзятости, присущей мотивам, влияющим на пациентов, влияющих на повторные процедуры: можно ожидать, что пациенты, которые возвращаются с продолжающимися симптомами ГЭРБ, будут иметь иную распространенность ПБ, чем пациенты. тех, у кого нет симптомов.
Очевидны и некоторые недостатки: выбывание из наблюдения было значительным, особенно в группе без ИМ, где почти половина пациентов не проходили повторное обследование; Кроме того, учитывая, что неправильная Z-линия не является показанием для повторной ЭГДС, неясно, проводились ли эти последующие обследования как часть протокола исследования или для клинической помощи. Если верно последнее, результаты следует рассматривать в несколько ином свете из-за предвзятости, присущей мотивам, влияющим на пациентов, влияющих на повторные процедуры: можно ожидать, что пациенты, которые возвращаются с продолжающимися симптомами ГЭРБ, будут иметь иную распространенность ПБ, чем пациенты. тех, у кого нет симптомов.
Как и в большинстве исследований этого типа, количество полных данных несколько меньше, чтобы с уверенностью делать выводы, которые мы хотели бы сделать. Хотя авторы отмечают, что серьезных осложнений не развилось у 50 пациентов с ИМ с неправильной линией Z, которые наблюдались до конца исследования, будут ли они чувствовать себя комфортно, делая такой вывод, если у 51-го пациента разовьется ЭАК? Наконец, неясно, какой именно эндоскопист проводил исследования, и были ли предприняты какие-либо усилия для обеспечения того, чтобы оба исследования выполнял один и тот же эндоскопист. Учитывая существенную вариабельность диагноза неправильной Z-линии у разных наблюдателей [7], вполне вероятно, что разные эндоскописты могут прийти к разным выводам относительно прогрессирования или регресса этого поражения. Такая вариабельность почти наверняка объясняет, по крайней мере, некоторую долю из девяти пациентов с развившейся БЭ (все, что характерно, с БЭ короткого сегмента), а также удивительно высокие 32% пациентов с исходно патологическими изменениями, у которых было отмечено «нормальное» Z. очередь на повторную эндоскопию. Было бы полезно, если бы отдельный наблюдатель рассмотрел эндоскопические фотографии этих «нормализованных» случаев до и после, чтобы увидеть, какая часть изменений действительно относится к линии Z, а какая часть изменений связана с восприятием эндоскопист.
Учитывая существенную вариабельность диагноза неправильной Z-линии у разных наблюдателей [7], вполне вероятно, что разные эндоскописты могут прийти к разным выводам относительно прогрессирования или регресса этого поражения. Такая вариабельность почти наверняка объясняет, по крайней мере, некоторую долю из девяти пациентов с развившейся БЭ (все, что характерно, с БЭ короткого сегмента), а также удивительно высокие 32% пациентов с исходно патологическими изменениями, у которых было отмечено «нормальное» Z. очередь на повторную эндоскопию. Было бы полезно, если бы отдельный наблюдатель рассмотрел эндоскопические фотографии этих «нормализованных» случаев до и после, чтобы увидеть, какая часть изменений действительно относится к линии Z, а какая часть изменений связана с восприятием эндоскопист.
Результаты настоящего исследования дополняют немногочисленную, запутанную и неубедительную литературу о естественном развитии неправильной линии Z (таблица 1). Тота и др. провели недавнее проспективное многоцентровое исследование 167 пациентов с неправильной линией Z и ИМ. При среднем периоде наблюдения 71 месяц ни у одного из пациентов не развился ПБ, дисплазия или ЭАК [1]. В другом популяционном исследовании Jung et al. из 86 пациентов с неправильной линией Z и ИМ у 2% развилась LGD, и ни у одного из них не развилась BE, дисплазия высокой степени (HGD) или EAC в течение 8-летнего периода наблюдения [8]. Точно так же прогрессирование в неоплазию также оценивалось как низкое — 0,01% в другом исследовании 204 пациентов с длиной сегмента BE < 1 см, в котором использовались популяционные оценки для моделирования ежегодных показателей перехода рака у пациентов с различной длиной сегмента BE [9].].
При среднем периоде наблюдения 71 месяц ни у одного из пациентов не развился ПБ, дисплазия или ЭАК [1]. В другом популяционном исследовании Jung et al. из 86 пациентов с неправильной линией Z и ИМ у 2% развилась LGD, и ни у одного из них не развилась BE, дисплазия высокой степени (HGD) или EAC в течение 8-летнего периода наблюдения [8]. Точно так же прогрессирование в неоплазию также оценивалось как низкое — 0,01% в другом исследовании 204 пациентов с длиной сегмента BE < 1 см, в котором использовались популяционные оценки для моделирования ежегодных показателей перехода рака у пациентов с различной длиной сегмента BE [9].].
Полноразмерная таблица
Наличие грыжи пищеводного отверстия диафрагмы может не только затруднить точное определение дифференцировать неравномерную Z-линию и ПЭ с коротким сегментом при индексном эндоскопическом исследовании, но также может ложно увеличить сообщаемую распространенность ИМ, если биопсия была получена из кардии из-за ошибки взятия образца. Авторы попытались решить проблему ошибки отбора проб, включив только биопсии, полученные из чешуйчато-столбчатого перехода, которые имели признаки как плоскоклеточной, так и столбчатой ткани. Тем не менее, можно взять биопсию из совершенно регулярной Z-линии, включая как плоскоклеточную ткань, так и столбчатую ткань, и в результате не предотвратить забор кардиального отдела желудка. Кроме того, второй патологоанатом рассмотрел все гистологические образцы с дисплазией. Несмотря на это, в исходно положительной группе ИМ 63% были отрицательными при последующем обследовании с биопсией. Эти результаты аналогичны результатам предыдущего исследования, в котором сообщалось, что более чем у половины пациентов с неправильной линией Z и ИМ при индексной биопсии не было ИМ при последующем обследовании [1], что подчеркивает проблему ошибки выборки, которая усугубляется в наличие очень коротких сегментов цилиндрической слизистой оболочки. Наличие грыжи пищеводного отверстия диафрагмы также может усложнить интерпретацию наличия ПБ, поскольку чрезмерная инсуффляция пищевода может сбить с толку эндоскопистов, придав грыжевому мешку вид сегмента ПБ (рис.
Авторы попытались решить проблему ошибки отбора проб, включив только биопсии, полученные из чешуйчато-столбчатого перехода, которые имели признаки как плоскоклеточной, так и столбчатой ткани. Тем не менее, можно взять биопсию из совершенно регулярной Z-линии, включая как плоскоклеточную ткань, так и столбчатую ткань, и в результате не предотвратить забор кардиального отдела желудка. Кроме того, второй патологоанатом рассмотрел все гистологические образцы с дисплазией. Несмотря на это, в исходно положительной группе ИМ 63% были отрицательными при последующем обследовании с биопсией. Эти результаты аналогичны результатам предыдущего исследования, в котором сообщалось, что более чем у половины пациентов с неправильной линией Z и ИМ при индексной биопсии не было ИМ при последующем обследовании [1], что подчеркивает проблему ошибки выборки, которая усугубляется в наличие очень коротких сегментов цилиндрической слизистой оболочки. Наличие грыжи пищеводного отверстия диафрагмы также может усложнить интерпретацию наличия ПБ, поскольку чрезмерная инсуффляция пищевода может сбить с толку эндоскопистов, придав грыжевому мешку вид сегмента ПБ (рис.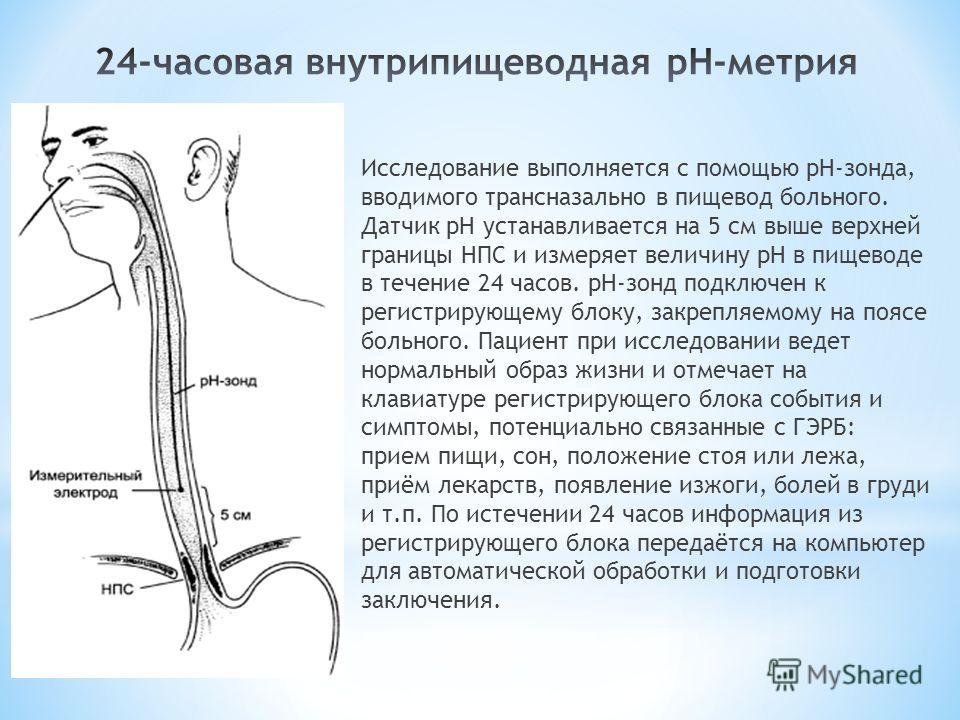 1).
1).
Чрезмерная инсуффляция пищевода ( a ) может привести к тому, что грыжевой мешок будет иметь вид пищевода Барретта по сравнению с тем же пищеводом без избыточной инсуффляции ( b ), в котором линия Z кажется правильной ( Изображение предоставлено доктором Пратиком Шармой )
Полноразмерное изображение
поражение низкого риска. Текущие данные не поддерживают рутинную биопсию из неправильной линии Z с экскурсией < 1 см, поскольку, как указано выше, такие биопсии могут привести к пожизненному наблюдению за пациентами в случае обнаружения ИМ. Мы, как гастроэнтерологи, вероятно, будем продолжать бороться, чтобы понять эту проблему, потому что у нас нет точных или надежных руководств по оценке, измерению и отчету о цилиндрической слизистой оболочке размером < 1 см. Хотя ранее была предложена четырехуровневая система классификации для оценки Z-линии, которая коррелировала с распространенностью ИМ [2], она не была принята и применена в клинических условиях. До тех пор, пока не станут возможными превосходные измерения мельчайших изменений вокруг линии Z или не будут проверены новые биомаркеры, эндоскописты должны признать, что небольшое количество Барретта, как и красота, находится в глазах смотрящего. В настоящее время ограниченные данные о риске неопластического прогрессирования у пациентов с неправильной линией Z таковы, что при неправильной линии Z не следует проводить рутинную биопсию.
До тех пор, пока не станут возможными превосходные измерения мельчайших изменений вокруг линии Z или не будут проверены новые биомаркеры, эндоскописты должны признать, что небольшое количество Барретта, как и красота, находится в глазах смотрящего. В настоящее время ограниченные данные о риске неопластического прогрессирования у пациентов с неправильной линией Z таковы, что при неправильной линии Z не следует проводить рутинную биопсию.
Ссылки
Thota PN, Vennalaganti P, Vennelaganti S, et al. Низкий риск дисплазии высокой степени или аденокарциномы пищевода среди пациентов с пищеводом Барретта менее 1 см (неправильная линия Z) в течение 5 лет после индексной эндоскопии. Гастроэнтерология . 2017; 152:987–992.
Артикул пабмед Google Scholar
Валлнер Б., Сильван А., Стенлинг Р., Янунгер К.Г. Появление Z-линии пищевода коррелирует с распространенностью кишечной метаплазии.
 Scand J Гастроэнтерол . 2000; 35:17–22.
Scand J Гастроэнтерол . 2000; 35:17–22.Артикул пабмед КАС Google Scholar
Дикман Р., Леви З., Вилкин А., Звиди И., Нив Ю. Предикторы специализированной кишечной метаплазии у пациентов со случайной неправильной линией Z. Eur J Гастроэнтерол Гепатол . 2010;22:135–138.
Артикул пабмед Google Scholar
Чаласани Н., Во Дж. М., Хантер Дж. Г., Уоринг Дж. П. Значение кишечной метаплазии в различных отделах пищевода, включая пищеводно-желудочный переход. Научные раскопки . 1997; 42: 603–607.
Артикул пабмед КАС Google Scholar
Шахин Н.Дж., Фальк Г.В., Айер П.Г., Герсон Л.Б. Клинические рекомендации ACG: диагностика и лечение пищевода Барретта. Am J Гастроэнтерол . 2016;111:30–50.
Артикул пабмед КАС Google Scholar
«>Гуда Н.М., Партингтон С., Вакил Н. Различия между и внутри наблюдателя в измерении длины при эндоскопии: значение для измерения пищевода Барретта. Гастроинтест Эндоск . 2004; 59: 655–658.
Артикул пабмед Google Scholar
Jung KW, Talley NJ, Romero Y, et al. Эпидемиология и естественное течение кишечной метаплазии желудочно-пищеводного перехода и пищевода Барретта: популяционное исследование. Am J Гастроэнтерол . 2011;106:1447–1455. (викторина 1456) .
Артикул пабмед ПабМед Центральный Google Scholar
Пол Х., Печ О.
 , Араш Х. и др. Длина пищевода Барретта и риск рака: последствия для большой выборки пациентов с ранней аденокарциномой пищевода. Гут . 2016;65:196–201.
, Араш Х. и др. Длина пищевода Барретта и риск рака: последствия для большой выборки пациентов с ранней аденокарциномой пищевода. Гут . 2016;65:196–201.Артикул пабмед Google Scholar
Ицковиц Д., Леви З., Болтин Д. и др. Риск неопластического прогрессирования у пациентов с неправильной линией Z при длительном наблюдении. Dig Dissci. (Epub перед печатью). https://doi.org/10.1007/s10620-018-4910-1.
Скачать ссылки
Финансирование
Финансирование этого анализа было частично поддержано NIH Award T32 DK07634 (SE), K24DK100548 (NJS).
Информация об авторе
Авторы и организации
Центр заболеваний пищевода и глотания, отделение гастроэнтерологии и гепатологии, Университет Северной Каролины, 4119B Bioinformatics Building, 130 Mason Farm Rd, Chapel Hill, NC, 2759 9-7080, США
Свати Элури и Николас Дж. Шахин
Авторы
- Свати Элури
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Николас Дж. Шахин
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Автор, ответственный за корреспонденцию
Свати Элури.
Права и разрешения
Перепечатка и разрешения
Об этой статье
Внешний вид Z-линии пищевода коррелирует с распространенностью кишечной метаплазии
. 2000 янв; 35(1):17-22.
дои: 10.1080/003655200750024470.
Б Вальнер 1 , A Sylvan, R Stenling, K G Janunger
принадлежность
- 1 Отделение хирургии и периоперационных наук, университетская больница Умео, Швеция.
- PMID: 10672829
- DOI: 10.1080/003655200750024470
B Wallner et al. Scand J Гастроэнтерол.
2000 9 января0003
Scand J Гастроэнтерол.
2000 9 января0003
. 2000 янв; 35(1):17-22.
дои: 10.1080/003655200750024470.
Авторы
Б Вальнер 1 , А. Сильван, Р. Стенлинг, К. Г. Янунгер
принадлежность
- 1 Кафедра хирургии и периоперационных наук, Университетская больница Умео, Швеция.
- PMID: 10672829
- DOI: 10.1080/003655200750024470
Абстрактный
Фон: Кишечная метаплазия в пищеводно-желудочном переходе связана с пищеводом Барретта, раком желудка и гастритом. Целью этого исследования было определить распространенность кишечной метаплазии среди пациентов с симптомами, указывающими на гастроэзофагеальную рефлюксную болезнь (ГЭРБ), и изучить клинические, эндоскопические и гистологические ассоциации с кишечной метаплазией в области плоскостолбчатого перехода.
Целью этого исследования было определить распространенность кишечной метаплазии среди пациентов с симптомами, указывающими на гастроэзофагеальную рефлюксную болезнь (ГЭРБ), и изучить клинические, эндоскопические и гистологические ассоциации с кишечной метаплазией в области плоскостолбчатого перехода.
Методы: В исследование были включены 186 пациентов с симптомами, указывающими на гастроэзофагеальный рефлюкс. Была использована новая классификация внешнего вида Z-линии.
Полученные результаты: Было обнаружено, что появление Z-линии коррелирует с распространенностью кишечной метаплазии в плоскостолбчатом переходе (P = 0,0001). Кишечная метаплазия в области плоскостолбчатого перехода обнаружена у 15,0% больных. Выявлена статистически значимая связь между кишечной метаплазией в области плоскостолбчатого перехода и языками столбчатого эпителия на Z-линии (P = 0,020), кишечной метаплазией в кардии (P = 0,020), положительным CLO-тестом (P = 0,026), курением. (P = 0,041) и возраст (P = 0,050). Не было выявлено связи с эндоскопическими или гистологическими признаками эзофагита или с тяжестью или продолжительностью симптомов ГЭРБ.
(P = 0,041) и возраст (P = 0,050). Не было выявлено связи с эндоскопическими или гистологическими признаками эзофагита или с тяжестью или продолжительностью симптомов ГЭРБ.
Заключение: Кишечная метаплазия в области плоскостолбчатого перехода коррелирует с появлением Z-линии, что оправдывает новую классификацию.
Похожие статьи
Отличается ли распространенность кишечной метаплазии в плоскостолбчатом переходе у пациентов с прогрессирующим системным склерозом?
Вардар Р, Вардар Э, Бор С. Вардар Р. и соавт. Терк Дж. Гастроэнтерол. 2010 сен; 21 (3): 251-6. doi: 10.4318/tjg.2010.0096. Терк Дж. Гастроэнтерол. 2010. PMID: 20931428
Воспаление и специализированная кишечная метаплазия слизистой оболочки сердца являются проявлением гастроэзофагеальной рефлюксной болезни.

Оберг С., Питерс Дж. Х., ДеМеестер Т. Р., Чандрасома П., Хаген Дж. А., Ирландия А. П., Риттер М. П., Мейсон Р. Дж., Крукс П., Бремнер К. Г. Оберг С. и соавт. Энн Сург. 1997 октября; 226(4):522-30; обсуждение 530-2. doi: 10.1097/00000658-199710000-00013. Энн Сург. 1997. PMID: 9351720 Бесплатная статья ЧВК.
Гистопатология столбчатого пищевода у пациентов с гастроэзофагеальной рефлюксной болезнью.
Ленглингер Дж., Рингхофер С., Эйслер М., Седиви Р., Врба Ф., Захерл Дж., Косентини Э.П., Прагер Г., Хефнер М., Риглер М. Ленглингер Дж. и соавт. Вена Клин Wochenschr. 2007;119(13-14):405-11. doi: 10.1007/s00508-007-0825-0. Вена Клин Wochenschr. 2007. PMID: 17671821
Патология желудочно-пищеводного перехода.

Одзе РД. Одзе РД. Семин Диагн Патол. 2005 ноябрь; 22 (4): 256-65. doi: 10.1053/j.semdp.2006.04.007. Семин Диагн Патол. 2005. PMID: 16939053 Обзор.
Короткий сегмент пищевода Барретта и специализированная столбчатая слизистая оболочка в области желудочно-пищеводного перехода.
Шарма П. Шарма П. Мэйо Клин Proc. 2001 март; 76(3):331-4. дои: 10.4065/76.3.331. Мэйо Клин Proc. 2001. PMID: 11243283 Обзор.
Посмотреть все похожие статьи
Цитируется
Важность неправильной линии Z: Барретт в глазах смотрящего?
Элури С., Шахин, штат Нью-Джерси. Элури С.
 и др.
Dig Dis Sci. 2018 июнь;63(6):1378-1380. doi: 10.1007/s10620-018-4998-3.
Dig Dis Sci. 2018.
PMID: 29492745
Аннотация недоступна.
и др.
Dig Dis Sci. 2018 июнь;63(6):1378-1380. doi: 10.1007/s10620-018-4998-3.
Dig Dis Sci. 2018.
PMID: 29492745
Аннотация недоступна.Классификация Hill превосходит осевую длину грыжи пищеводного отверстия диафрагмы для оценки механического антирефлюксного барьера в желудочно-пищеводном соединении.
Хансдоттер И., Бьор О., Андреассон А., Агреус Л., Хеллстрем П., Форсберг А., Тэлли Н.Дж., Вит М., Валлнер Б. Хансдоттер I и др. Endosc Int Open. 2016 март; 4(3):E311-7. doi: 10.1055/s-0042-101021. Epub 2016 10 февраля. Endosc Int Open. 2016. PMID: 27004249 Бесплатная статья ЧВК.
Частота гастроэзофагеальных и экстрагастроэзофагеальных симптомов у пациентов с легким эрозивным эзофагитом, тяжелым эрозивным эзофагитом и пищеводом Барретта на Тайване.

Као С.С., Чен В.К., Сюй П.И., Чуах С.К., Лу С.Л., Лай К.Х., Цай Ф.В., Чанг К.С., Тай В.К. Као С.С. и др. Гастроэнтерол Рез Практ. 2013;2013:480325. дои: 10.1155/2013/480325. Epub 2013 12 августа. Гастроэнтерол Рез Практ. 2013. PMID: 23997765 Бесплатная статья ЧВК.
Пищевод Барретта: обзор биологии и терапевтических подходов.
Кунтуракис П., Аджани Дж. А., Давила М., Ли Дж. Х., Бутани М. С., Иззо Дж. Г. Контуракис П. и соавт. Гастроинтест Рак Рез. 2012 март;5(2):49-57. Гастроинтест Рак Рез. 2012. PMID: 226
Бесплатная статья ЧВК.
Эндоскопические наблюдения вокруг желудочно-пищеводного перехода у пациентов с симптоматической гастроэзофагеальной рефлюксной болезнью в Южной Азии.



 Scand J Гастроэнтерол . 2000; 35:17–22.
Scand J Гастроэнтерол . 2000; 35:17–22. , Араш Х. и др. Длина пищевода Барретта и риск рака: последствия для большой выборки пациентов с ранней аденокарциномой пищевода. Гут . 2016;65:196–201.
, Араш Х. и др. Длина пищевода Барретта и риск рака: последствия для большой выборки пациентов с ранней аденокарциномой пищевода. Гут . 2016;65:196–201.
 и др.
Dig Dis Sci. 2018 июнь;63(6):1378-1380. doi: 10.1007/s10620-018-4998-3.
Dig Dis Sci. 2018.
PMID: 29492745
Аннотация недоступна.
и др.
Dig Dis Sci. 2018 июнь;63(6):1378-1380. doi: 10.1007/s10620-018-4998-3.
Dig Dis Sci. 2018.
PMID: 29492745
Аннотация недоступна.

