Трансплантация костного мозга. Booking Health
В настоящее время, в связи со сложностями, связанными с организацией лечения в Турции, Швейцарии, Южной Корее и Индии, мы приостановили обработку заявок по этим направлениям.
Если вас интересует организация лечения в Германии, оставьте, пожалуйста, заявку, и наши специалисты свяжутся с вами в ближайшее время.
Трансплантация костного мозга — что это?
Трансплантация костного мозга (ТКМ) — процедура имплантации здоровых гемопоэтических клеток в организм больного с целью возобновления процесса кроветворения.
Показания к трансплантации:
- Анемиях
- Всех видах лейкозов
- Миеломе
- Некоторых онкологических заболеваниях (например, при раке яичек)
- Болезни Ходжкина
- Неходжкинских лимфомах
Противопоказания к пересадке:
- Тяжелые патологии печени и почек
- Инфекционные болезни
- Беременность
- Физическая слабость организма (пожилой возраст, сопутствующие заболевания)
Пересадка костного мозга детям проводится по тем же показаниям и противопоказаниям, что и взрослым пациентам.
Какие бывают виды пересадок?
Принято различать такие виды пересадки костного мозга:
- Аутологичная пересадка — операция, при которой больному имплантируют его же клетки
- Аллогенная трансплантация от родственника
- Аллогенная пересадка от донора, не являющегося родственником
- Гаплоидентичная трансплантация — вид пересадки, при которой используют костный мозг родственника, частично совместимого. Приживаемость трансплантата после такой процедуры происходит только у 25% пациентов
Как происходит подготовка к трансплантации?
Подготовка пациента к пересадке
Важнейший этап подготовки к пересадке — кондиционирование. Это терапия, которая проводится при онкологических заболеваниях. Она заключается в приеме химиотерапевтических препаратов и иммуносупрессоров. Это угнетает иммунитет больного для того, чтобы не произошло отторжение пересаженного материала. Также метод помогает уничтожить раковые клетки и освобождает место для трансплантата.
В случае трансплантации собственных клеток, сперва делается забор, а после материал замораживается до окончания курса химиотерапии.
Диагностические процедуры перед операцией по пересадке костного мозга:
- Консультации специалистов, в т.ч. стоматолога
- МРТ и КТ, ПЭТ-КТ (если речь идет об онкологическом заболевании)А
- нализ крови (в т.ч. на ВИЧ, гепатиты и т.д.)
- Биохимический анализ крови проводят для того, чтобы убедиться в исправности работы печени и почек. В противном случае пересадка может быть противопоказана
- Трепан-биопсия и аспирация костного мозга. Это пункция костной ткани и костного мозга с последующим цитогенетическим анализом
При необходимости больной проходит лечение у дантиста. Это необходимо чтобы полностью исключить инфекции, поскольку после пересадки их наличие смертельно опасно.
Подготовка к донорству
Донор проходит рутинную диагностику чтобы исключить какие-либо заболевания, которые могут передаться реципиенту.
Если забор будет производиться из периферической крови, донору назначаются специальные препараты, которые необходимо принимать в течение 5 дней. Они способствуют активному выходу клеток в кровоток.
Возможны побочные эффекты приема этих препаратов. Обычно это непродолжительные боли в костях.
Как проводится трансплантация?
1 этап. Забор
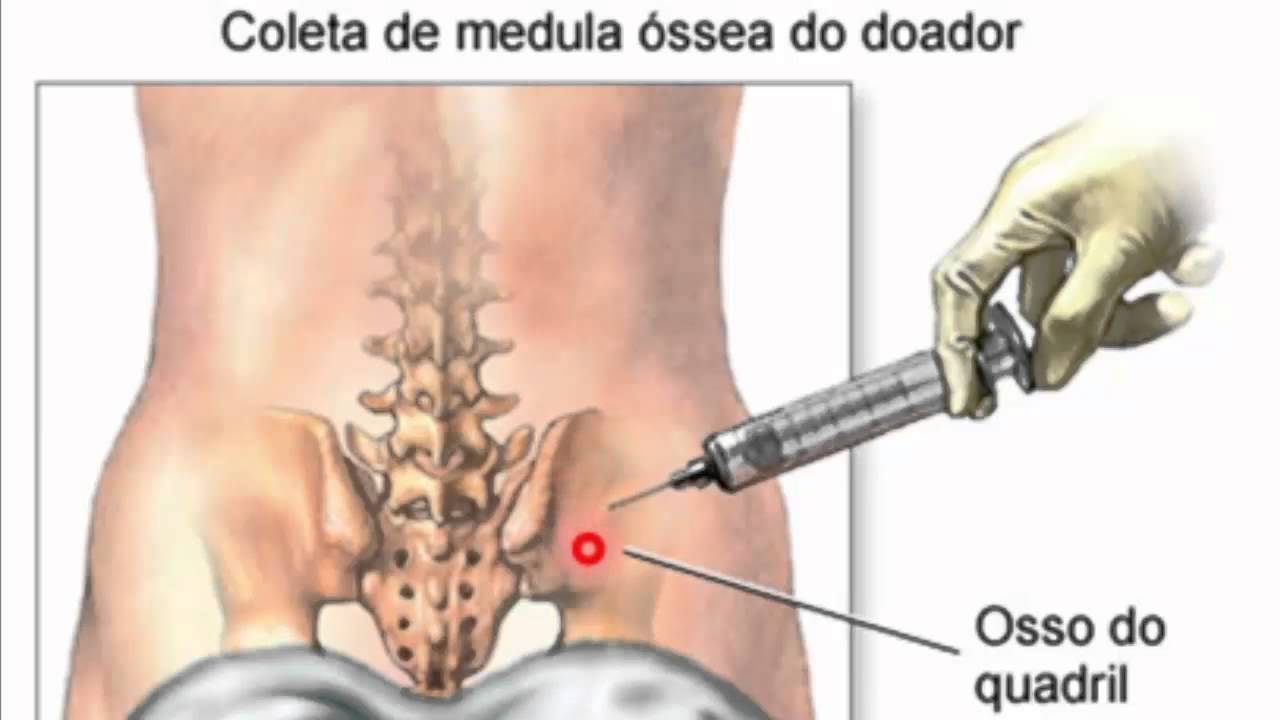
Костный мозг берут под общей анестезией. Сперва доктор делает небольшой разрез, а затем с помощью широкой иглы делает пункцию материала из бедренной кости.
Также донор может выбрать вариант забора клеток из периферической крови. Для этого донора на несколько часов подключают к аппарату, который качает кровь. Через специальный сепаратор клетки костного мозга отделяются от крови и собираются в отдельный резервуар.
2 этап. Пересадка
Костный мозг пересаживают путем внутривенной инъекции. Процедура длится до 2 часов.
3 этап. Период приживления
Введенные клетки со временем приживаются и начинают вырабатывать новые здоровые клетки крови.
Госпитализация длится около 3 месяцев.
Подобрать профильную клинику и лечение
Кто может стать донором для пересадки костного мозга?
Родственным донором может быть родной брат или сестра пациента. Однако, даже такой донор совместим не всегда. В редких случаях проводят гаплоидентичную пересадку. Донором для нее может выступать отец или мать пациента.
Для неродственной пересадки подбор кандидата происходит через базу данных банка доноров костного мозга. Поиск обычно занимает около 2 недель. Крупнейшими являются Банк доноров костного мозга США, Европейский и Немецкий банки. Обычно подбирают 2-3 человек, поскольку потенциальный кандидат может иметь временные противопоказания, отказаться от процедуры или его может не быть в стране.
Стоит отметить, что бывают случаи, когда найти подходящего кандидата не удается.
Противопоказаниями к донорству являются:
- Инфекционные болезни
- Аутоиммунные заболевания
- Психические расстройства
- Возраст младше 18 и старше 55 лет
Какие могут быть осложнения после процедуры?
Наиболее серьезные осложнения после трансплантации костного мозга — это отторжение трансплантата организмом и атака пересаженных клеток на организм пациента (реакция “трансплантат против хозяина”).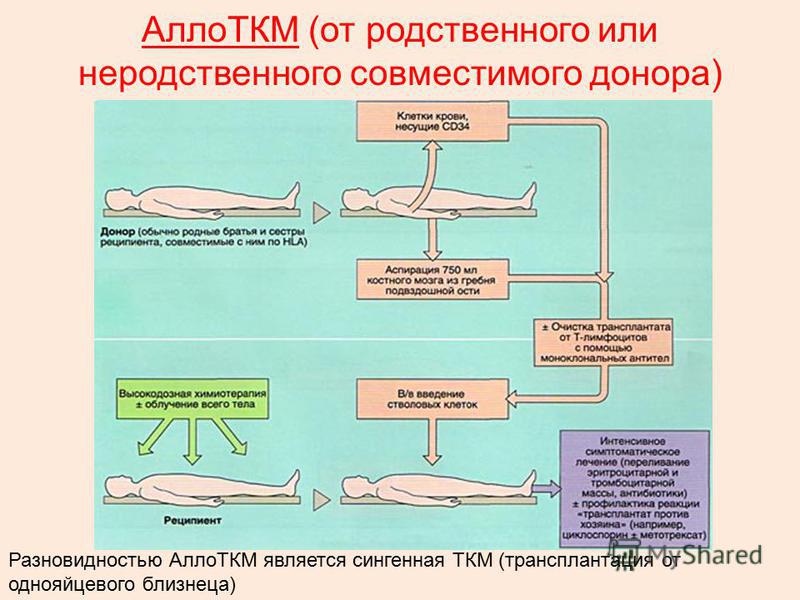 Чтобы предотвратить обе эти реакции, больному назначают иммуносупрессоры — препараты, подавляющие иммунитет.
Чтобы предотвратить обе эти реакции, больному назначают иммуносупрессоры — препараты, подавляющие иммунитет.
Такая терапия, в свою очередь, подвергает организм больного риску заражения инфекцией. Для того, чтобы максимально снизить этот риск, пациента помещают в стерильный бокс. Это изолированная стерильная палата, оснащенная противобактериальными фильтрами.
Для донора никакого риска осложнения при пересадке костного мозга не существует. Однако есть незначительные побочные эффекты. Возможны ощущения слабости, тошноты Госпитализация донора длится один день. Болевые ощущения в месте пункции проходят спустя несколько дней. Объем клеток костного мозга донора возобновляется после 2 недель.
Последствия трансплантации для пациента зависят от ряда факторов:
- Первоначального диагноза
- Степени совместимости донора
- Относительного физического здоровья
- Соблюдения режима изоляции в период приживления
- Грамотного протокола лечения
Если все необходимые меры предосторожности были соблюдены, а лечение проводилось в хорошо оснащенном центре под руководством опытного доктора, шансы на выздоровление высоки. Это касается в том числе и пациентов со злокачественными заболеваниями.
Это касается в том числе и пациентов со злокачественными заболеваниями.
Как проходит реабилитация после трансплантации кровеобразующих клеток?
Выводы об успешности пересадки можно делать только по прошествии нескольких недель после операции. За это время трансплантат приживается в организме пациента. На период приживления трансплантата больному назначается поддерживающая терапия в виде противовирусных и противогрибковых препаратов, а также антибиотики.
Пересадка костного мозга требует восстановления не только физического, но и психологического. Больной на протяжении длительного времени испытывает сильную слабость. Это состояние сказывается на его психическом самочувствии, поэтому крайне важно получать в этот период профессиональную помощь психолога. Также необходимо, чтобы родные пациента поддерживали его в это время.
Жизнь после пересадки костного мозга
Жизнь пациентов, которые перенесли пересадку мало чем отличается от повседневной жизни обычного человека. Какое-то время необходимо соблюдать предписания врача, но это существенно не влияет на качество жизни.
Какое-то время необходимо соблюдать предписания врача, но это существенно не влияет на качество жизни.
Какой прогноз жизни после трансплантации?
Выживаемость после пересадки костного мозга зависит, прежде всего, от первоначального диагноза. Также, имеет значение опыт онкогематолога, который пересаживает клетки. Так, в немецких и турецких клиниках средний показатель выживаемость больных после пересадки составляет более 90%.
Продолжительность жизни после пересадки костного мозга определить невозможно, поскольку этот показатель зависит от многих факторов. Человек считается полностью излечившимся, пережив рубеж 5 лет после процедуры.
Рецидив после пересадки костного мозга
Вероятность рецидива после пересадки костного мозга существует. Этот показатель значительно колеблется в зависимости от клиники, в которой проводят процедуру. Так, в зарубежных центрах пересадки костного мозга статистика возникновения рецидива намного меньше, чем такой же показатель в клиниках СНГ.
Чем больше времени прошло после пересадки — тем ниже вероятность возникновения рецидива. Если болезнь возвращается, трансплантация проводится повторно. Риск безрецидивной выживаемости после повторной пересадки зависит от промежутка времени между первой пересадкой и первым рецидивом. Если этот период длился более года, шансы на выздоровление высоки.
Где делают операцию по пересадке костного мозга?
Booking Health выделил для вас 2 лучших по нашему мнению клиники для пересадки костного мозга в лидирующих странах.
Германия
Ведущей немецкой клиникой в области пересадки кроветворных клеток является Университетская клиника Ульма. Отделение гематологии, онкологии, паллиативной медицины, ревматологии и инфектологии является частью Центра комплексного лечения рака Ульм и сертифицировано Немецким онкологическим обществом и Немецкой организацией по борьбе с раком.
Турция
Одна из ведущих турецких клиник в области онкогематологии — Клиника Мемориал Шишли, Стамбул.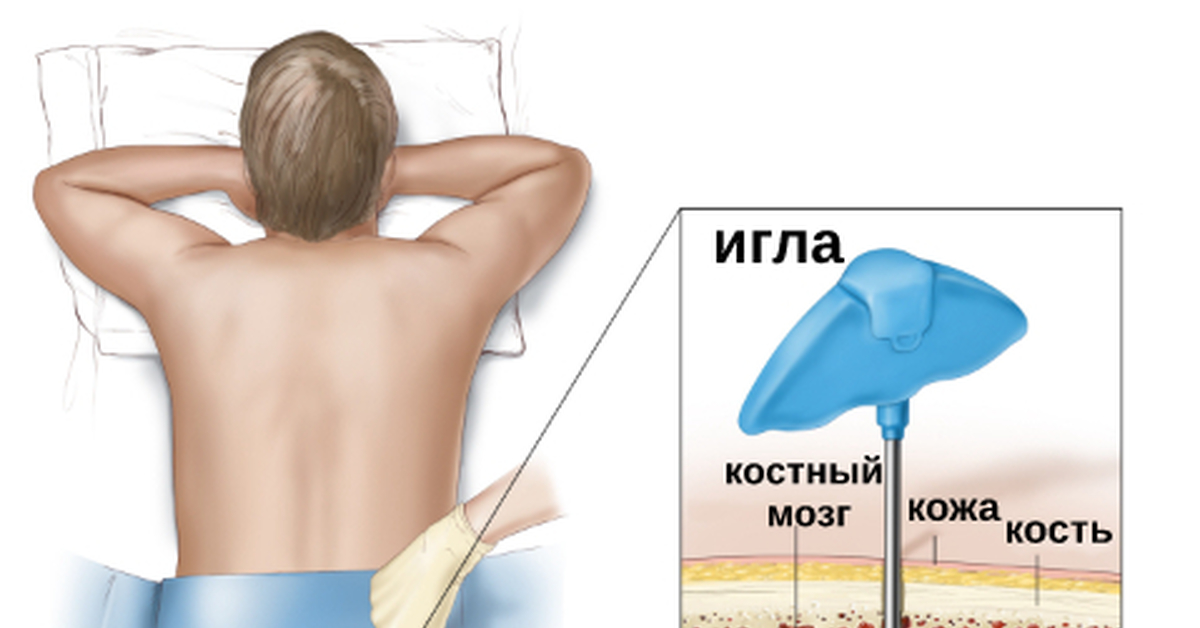 В Отделении детской гематологии и пересадки костного мозга Клиники Мемориал Шишли проводятся все виды пересадки костного мозга у детей. Главный врач отделения, профессор Атилла Танели, состоит в Европейском обществе по трансплантации костного мозга и организации JACIE по аккредитации медицинских учреждений, занимающихся пересадкой костного мозга.
В Отделении детской гематологии и пересадки костного мозга Клиники Мемориал Шишли проводятся все виды пересадки костного мозга у детей. Главный врач отделения, профессор Атилла Танели, состоит в Европейском обществе по трансплантации костного мозга и организации JACIE по аккредитации медицинских учреждений, занимающихся пересадкой костного мозга.
Сколько стоит трансплантация костного мозга?
Средняя цена пересадки в немецких клиниках – €345,800. При этом пересадка от неродственного донора будет стоить дороже, поскольку отдельно оплачивается поиск донора.
Средняя цена пересадки в Турции – €356,250. Цена зависит от типа пересадки, диагноза и общего состояния пациента.
Цена на пересадку костного мозга детям в любой из стран может несколько отличаться. Кроме того, некоторые зарубежные центры проводят пересадку детям только после полной предоплаты медицинской программы.
Подобрать профильную клинику и лечение
Донорство костного мозга — цена
Существует заблуждение, будто услуги доноров оплачиваются. На самом деле донор не получает никакого материального вознаграждения. Донорство основано на альтруистических побуждениях. Попытка покупки/продажи каких-либо органов, в том числе и костного мозга, расценивается как уголовное преступление в любой стране.
На самом деле донор не получает никакого материального вознаграждения. Донорство основано на альтруистических побуждениях. Попытка покупки/продажи каких-либо органов, в том числе и костного мозга, расценивается как уголовное преступление в любой стране.
Между тем отдельной оплаты требует поиск донора через один из регистров. Обычно подбор кандидата стоит порядка €12 000.
Организация пересадки костного мозга за границей
При необходимости проведения пересадки костного мозга возникает целый ряд вопросов. В какой стране сделать пересадку? Нужна ли виза? Нужна ли предоплата? Возможно ли срочно выехать на лечение? Где найти донора? Как попасть к лучшему специалисту?
Для того чтобы решить все эти вопросы, свяжитесь с менеджером Booking Health. Наши специалисты подберут для вас лучшее решение.
Наши преимущества:
- Индивидуальный подбор клиники
- Возможность выбора лучшего врача
- Сервисные услуги: предоставление трансфера и переводчика, оформление медицинской документации
- Страховка, которая обеспечит сохранение заявленной цены.
 Все непредвиденные расходы покроем мы
Все непредвиденные расходы покроем мы
Обратиться в Booking Health
Выбирайте лечение за рубежом и Вы, несомненно, получите отличный результат!
Trustpilot
Авторы:
Статья составлена под редакцией экспертов в области медицины, врачей-специалистов Доктор Валерия Кружилина, Александра Соловей. Для лечения состояний, о которых идет речь в статье, необходимо обратиться к врачу; информация в статье не предназначена для самолечения!
Источники:
National Center for Biotechnology
Cancer Support Community
National Cancer Institute
Читайте:
Почему Booking Health – Вопросы и ответы
Как не ошибиться в выборе клиники и специалиста
7 причин доверять рейтингу клиник на сайте Booking Health
Booking Health – Стандарты качества
Отправить запрос на лечение
Booking Health GmbH | Диагностика и лечение |
Что такое трансплантация костного мозга?
Далее
следует подобие репортажа, который описывает мой личный опыт в
процессе трансплантации костного мозга. У меня была
трансплантация в марте 2009 года в процессе моей борьбы с острой
промиелоцитарной лейкемией. Я находился в стерильной комнате в
течение примерно двух месяцев и испытал самые типичные эффекты,
которые чувствует пациент в подобной ситуации. Я надеюсь, что
мои описания достаточно ясны, чтобы вы смогли лучше разобратся в
той процедуре, в информированности о которой до сих пор еще
много путаницы. Я надеюсь, что моя личная точка зрения сможет
сделать нижеизложенное более легким и в то же время более
интересным для чтения, чем большинство из технической
информации, которое можно найти на других сайтах.
У меня была
трансплантация в марте 2009 года в процессе моей борьбы с острой
промиелоцитарной лейкемией. Я находился в стерильной комнате в
течение примерно двух месяцев и испытал самые типичные эффекты,
которые чувствует пациент в подобной ситуации. Я надеюсь, что
мои описания достаточно ясны, чтобы вы смогли лучше разобратся в
той процедуре, в информированности о которой до сих пор еще
много путаницы. Я надеюсь, что моя личная точка зрения сможет
сделать нижеизложенное более легким и в то же время более
интересным для чтения, чем большинство из технической
информации, которое можно найти на других сайтах.
Момент трансплантации был, как я
и ожидал, волшебным. Позвольте мне пояснить, что
пересадка костного мозга не является операцией, и
костный мозг — это не спинной мозг! Намного проще
использовать вместо этого термин «костная кровь»,
чтобы указать, что кровь течет в кости, каждой
кости, у каждого из нас.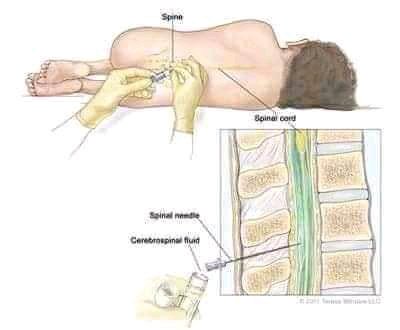
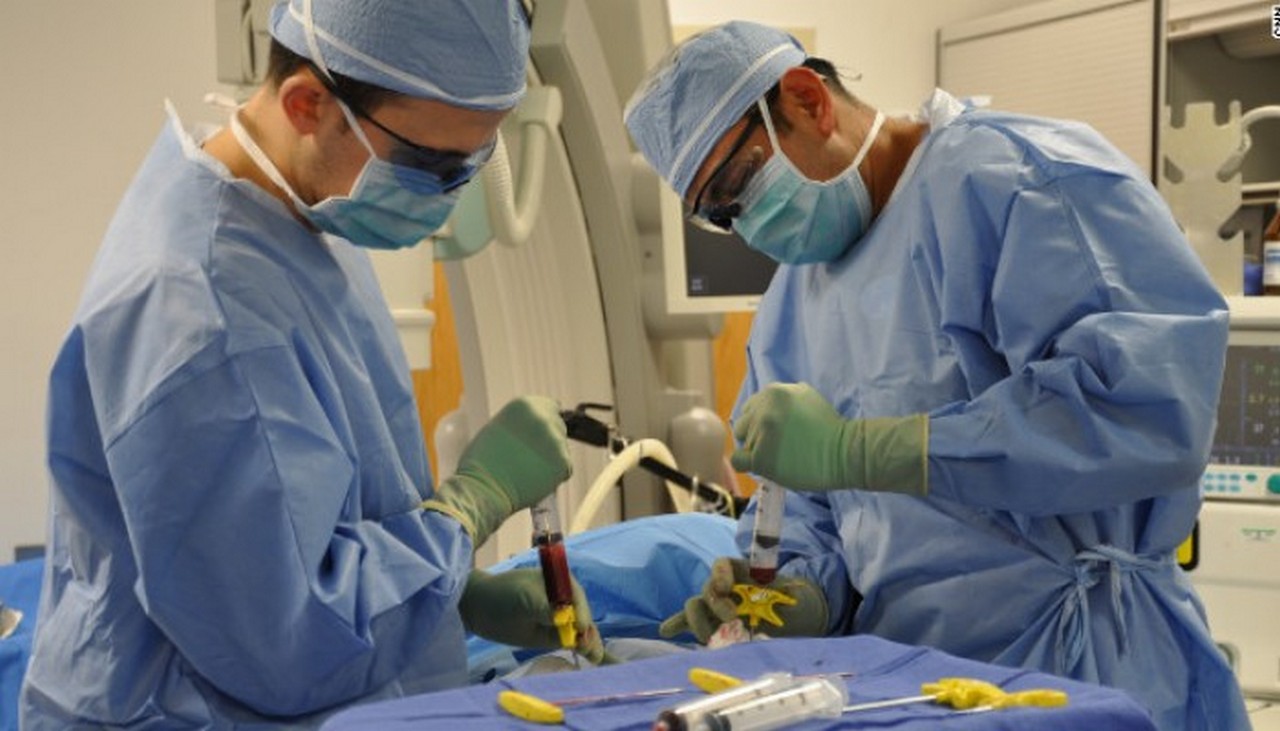 Т.е. костый мозг
совсем не белый, а это всего лишь кровь, которая
течет во всех наших костях, богатая стволовыми
клетками.
Т.е. костый мозг
совсем не белый, а это всего лишь кровь, которая
течет во всех наших костях, богатая стволовыми
клетками.Вы могли узнать больше о донорском переливании из сообщения моего брата Майкла несколько недель назад. У него эту кровь брали с помощью хирургической операции под общим наркозом, вставив иглы непосредственно в тазовую кость для переливания крови. Существует также менее сложные процедуры для сбора этой крови, а именно непосредственно из периферической крови, как если бы при нормальным донорстве крови. Есть преимущества и недостатки обоих процессов, как для донора, так для получателя, но не буду рассматривать их здесь.
Донорскую кровь моего брата ввели
в меня через капельницу. Вскоре вы увидите фото в
альбоме «Beat Leukemia» на Facebook и увидите , что
это очень похоже на нормальное переливание крови.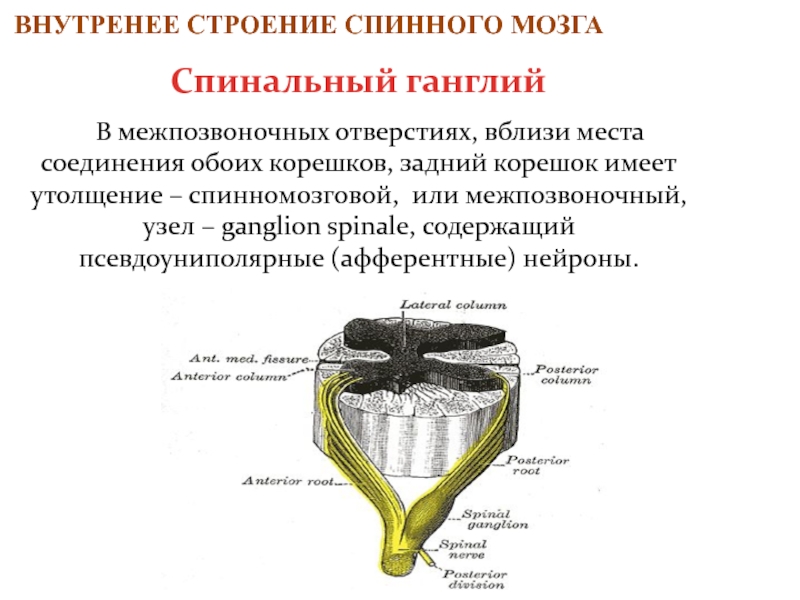 Для меня это был очень эмоциональный момент, я с
широко раскрытыми глазами и открытым ртом смотрел за
каждой каплей, что капала вниз и входила в меня.
После двух лет борьбы, это был особенно волнующий
момент. Однако, как я уже сказал, переливание – это
только один из этапов трансплантации костного мозга.
Для меня это был очень эмоциональный момент, я с
широко раскрытыми глазами и открытым ртом смотрел за
каждой каплей, что капала вниз и входила в меня.
После двух лет борьбы, это был особенно волнующий
момент. Однако, как я уже сказал, переливание – это
только один из этапов трансплантации костного мозга.
Трансплантация выглядит, как обычное переливание крови.
Чтобы лучше объяснить, что такое пересадка костного
мозга, я буду использовать метафору. Представьте
себе атолл, окруженный коралловым рифом. Это живая
подводная растительность, которая производит
кислород и пищу для морских рыб вокруг этого острова.
Теперь представьте, что барьер заболел и прекратил
производство питательных веществ в нужных
количествах. Рыбы начинают медленно умирать. На
данный момент единственное решение — это убить
данную растительность, искоренить ее полностью и
посадить новые и здоровые кораллы, с другого атолла.
Затем берутся новые «семена» из здорового атолла. Это стволовые клетки донора, которые выкладываются на умирающий коралловый риф, с целью восстановить и начать создание новой растительности. Однако, для того, чтобы это произошло, требуется время, от двух до трех недель, в течение которых рыбе остается мало, что поесть и они должны держаться из последних сил, чтобы выжить. В трансплантации костного мозга, это означает, что пациент должен постоянно делать переливание крови и тромбоцитов, и подвергатся высокому риску заражения, так как нет возможности переливание белых кровяных клеток.
 По этой причине,
пациент при пересадке костного мозга находится в
стерильной комнате все время, т.е. в целом около
полутора месяца.
По этой причине,
пациент при пересадке костного мозга находится в
стерильной комнате все время, т.е. в целом около
полутора месяца.К сожалению,
химиотерапия и облучение осуществляются в форме, так
называемых «ковровых бомбардировок», оказывая
воздействие на все «клетки быстрой репликации»,
например, таких как кожа. В здоровом теле,
поверхностные клетки кожи каждый день умирают для
того, чтобы их заменили на новые клетки, которые
производятся в нижележащих слоях.
 Как будто пчела
жалила меня каждый раз, когда я пытался проглотить.
Боль была и во рту, и скоро я потерял голос.
Как будто пчела
жалила меня каждый раз, когда я пытался проглотить.
Боль была и во рту, и скоро я потерял голос. Не существует способа противостоять этому феномену, вы можете только уменьшить боль. Фентанил и морфин помогли в моем случае или, вернее, давали такой эффект, который позволял мне спать и не думать слишком много. Я вынужден был прекратить есть и пить из-за расстройства воспаленного желудка. Волосы тела тоже относятся к «клеткам быстрой репликации», вот почему теряют волосы те, кто подвергается химиотерапии: они не будут заменены в течение некоторого времени.
После нескольких недель происходит приживление донорских стволовых клетках, т.е. когда они попадают внутрь костей получателя и закрепляются там, начиная производить новые клетки крови. Так же, как если бы они были семенами, в это время мы можем только ждать и быть терпеливыми, по возможности уменьшая все побочные эффекты, пытаясь снизить жар, температуру, которая повышается практически во всех случаях, чуть выше или ниже.

Этот этап для меня был особенно трудным, как с физической, так и психологической точки зрения. В течение этих двух лет я думал, что уже попробовал все, и действительно не думал, что будет так трудно.
Высокая температура поднялась неожиданно в воскресенье утром и вместе с ней усилились боли в местах повреждения кожи в результате лучевой терапии, особенно на груди, шее, спине и руках, до такой степени, что стало действительно трудно это терпеть. Ситуация с руками была особенно проблематична, поскольку именно они используются, чтобы делать все необходимое и когда руки повреждены, касание любого предмета превращается в пытку (представьте себе, как приходится мыться или чистить зубы!).
Повреждения-ожоги на руке, вызванные облучением всего тела (TBI).
С психологической
точки зрения, ситуация по меньшей мере довольно
пугающая, когда температура тела под 40 и не думает
снижатся, в то время как количество лейкоцитов
практически нулевое. Как представители человеческого
рода, мы так привыкли быть на вершине пищевой цепи,
что не чувствуем себя под угрозой чего-либо или
кого-либо, вплоть до того, что даже ищем сильные
эмоции, поднимаясь в горы или прыгая с парашютом.
Будучи в состоянии отсутствия защитного иммунитета,
ты беззащитен для невидимых хищников, вирусов и
бактерий, которые могут на самом деле повлечь
смертельный исход.
Как представители человеческого
рода, мы так привыкли быть на вершине пищевой цепи,
что не чувствуем себя под угрозой чего-либо или
кого-либо, вплоть до того, что даже ищем сильные
эмоции, поднимаясь в горы или прыгая с парашютом.
Будучи в состоянии отсутствия защитного иммунитета,
ты беззащитен для невидимых хищников, вирусов и
бактерий, которые могут на самом деле повлечь
смертельный исход.
Воспаление кожи, вызванное трансплантацией больному (GVHD)
Постепенно
результаты моих анализов улучшались и я начал
чувствовать себя лучше с каждым днем. Пришлось также
иметь дело с болезнью «трансплантанта против
получателя» (graft versus host disease или GVHD).
Это происходит, когда донорский костный мозг считает
некоторые ткани получателя врагами и нападает на них.
В моем случае это проявилось в виде сыпи на коже и
было назначено лечение с помощью высоких доз
кортизона, которые затем постепенно снижались.
Костный мозг прижился хорошо и состояние крови
улучшается (спасибо Микки, этот костный мозг просто
«бомба»!). Через несколько дней будут контролировать
мой костный мозг, чтобы посмотреть, как все прошло.
Может быть меня выпишут из больницы в ближайшее
время (хотя я предпочитаю не говорить об этом
заранее) и кажется, что ближайшие шесть месяцев
будут решающими.
Пришлось также
иметь дело с болезнью «трансплантанта против
получателя» (graft versus host disease или GVHD).
Это происходит, когда донорский костный мозг считает
некоторые ткани получателя врагами и нападает на них.
В моем случае это проявилось в виде сыпи на коже и
было назначено лечение с помощью высоких доз
кортизона, которые затем постепенно снижались.
Костный мозг прижился хорошо и состояние крови
улучшается (спасибо Микки, этот костный мозг просто
«бомба»!). Через несколько дней будут контролировать
мой костный мозг, чтобы посмотреть, как все прошло.
Может быть меня выпишут из больницы в ближайшее
время (хотя я предпочитаю не говорить об этом
заранее) и кажется, что ближайшие шесть месяцев
будут решающими.
Методы лечения,
которыми меня лечили — это был максимум, что мы
могли бы сделать и всему моему телу, а не только
иммунной системе, потребуется много времени, чтобы
восстановиться полностью.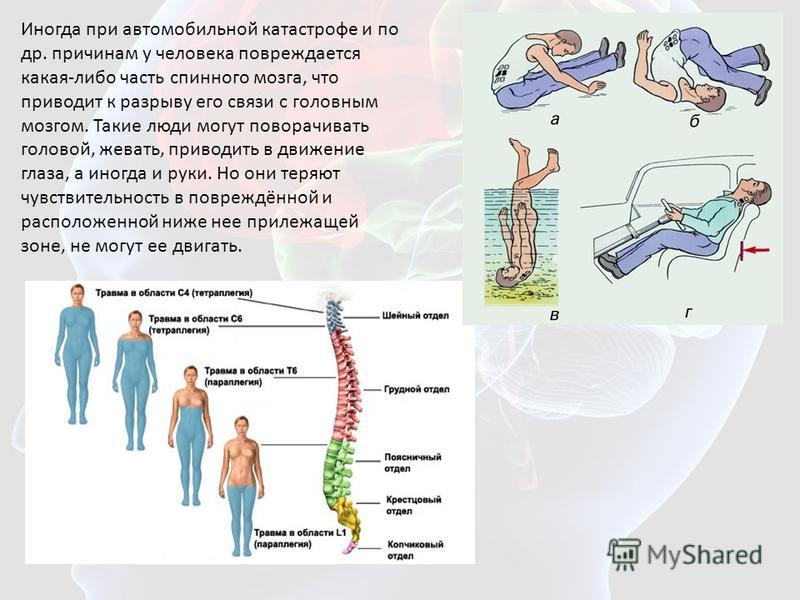 Кроме того, по статистике,
первые шесть месяцев – это тот период, когда
происходит то, что неизбежно должно случиться. Если
пережить его без проблем, то я действительно смогу
наконец немного расслабиться. Еще немного терпения,
но это определенно стоит того!
Кроме того, по статистике,
первые шесть месяцев – это тот период, когда
происходит то, что неизбежно должно случиться. Если
пережить его без проблем, то я действительно смогу
наконец немного расслабиться. Еще немного терпения,
но это определенно стоит того!
Я хочу быть
предельно честным с вами и рассказать правду об этой
болезни и трансплантации. Причиной этого нятья
конечно же не является желание привлечь ободрение и
поощрение, но чтобы объяснить вам то, что возможно
никто другой не осмеливается или же не желает
объяснять. Жизнь тяжела для любого больного раком и
если один из них скажет вам, что его лечение было
легким, знаете, что он говорит это только затем,
чтобы не перекладывать на вас свои проблемы или
потому, что думает, что вы не сможете его понять и
поэтому незачем тратить время. Конечно же, ничто не
идет в сравнение с тем, чтоб испробовать это на
своей шкуре, но было бы несправедливо оставлять в
неведении того, кого это не касается, в то время,
как тот, кто болен остается в одиночестве.
Конечно же, ничто не
идет в сравнение с тем, чтоб испробовать это на
своей шкуре, но было бы несправедливо оставлять в
неведении того, кого это не касается, в то время,
как тот, кто болен остается в одиночестве.
Надеюсь, что вы
мне поверите, если скажу, что эта трансплантация,
сделанная на полную мощность, была очень тяжелой.
После двух лет, в течение которых я испробовал всего
по немногу, а именно: две реанимации в отделении
интенсивной терапии, экстренную хирургию, а затем и
трансплантацию, я думаю, что могу почти объективно
сказать, насколько плохо это «плохо». Причина того,
что может быть ошибочно принято за жалобы, это то,
что я действительно не могу даже подумать, что
кто-то должен пройти через все, что прошел я.
Заболеваемость раком растет, все больше и больше
людей заболевают и среди них все больше молодых. Я
сам в этом убедился в больнице, где и познакомился
со многими из них. В этой ситуацией, мы больше не
можем играть в игру со стульями, просто надеясь не
оказаться теми несчастными, что остаются стоять,
когда музыка останавливается. Вероятность этого
слишком высока и мы не можем продолжать прятать
голову в песок и делать вид, что проблема не
существует только потому, что мы боимся даже
говорить об этом. Пора взглянуть в лицо
действительности.
Я
сам в этом убедился в больнице, где и познакомился
со многими из них. В этой ситуацией, мы больше не
можем играть в игру со стульями, просто надеясь не
оказаться теми несчастными, что остаются стоять,
когда музыка останавливается. Вероятность этого
слишком высока и мы не можем продолжать прятать
голову в песок и делать вид, что проблема не
существует только потому, что мы боимся даже
говорить об этом. Пора взглянуть в лицо
действительности.
Глядя на мой
диагноз, я задавался вопросом, почему я не сделал
что-то раньше, когда было в моих силах как-то
изменить положение вещей. Я не хочу, чтобы кто-то
когда-либо почувствует то, что я чувствовал тогда.
Хорошая новость — это то, что вместе мы можем
изменить наше будущее. Поэтому я призываю вас
действовать сейчас, найти на странице «Помощь BL» список организаций, борющихся с
лейкемией в вашей стране и выбрать, как вы хотите
внести свой вклад в эту борьбу: через пожертвования,
волонтерство или став донором крови и / или кости. Если вашей страны нет в списке, но вы знаете
надежные местные организации, пожалуйста,
свяжитесь со мной
для того, чтобы я мог их добавить. Если вашей страны
нет в списке и вы не знаете других местных
организаций, знайте, что исследовательские сети
являются глобальными и результаты сообщаются в
режиме реального времени, так что не имеет значения,
где и как вы намереваетесь помогать, ваша помощь
будет в любом случае ценной.
Если вашей страны нет в списке, но вы знаете
надежные местные организации, пожалуйста,
свяжитесь со мной
для того, чтобы я мог их добавить. Если вашей страны
нет в списке и вы не знаете других местных
организаций, знайте, что исследовательские сети
являются глобальными и результаты сообщаются в
режиме реального времени, так что не имеет значения,
где и как вы намереваетесь помогать, ваша помощь
будет в любом случае ценной.
Отфутболим этот шар в лицо тех, кто его послал. Мы
не искали и не заслуживаем этого.
Трансплантация спинного мозга и периферических нервов | Лаборатория нейротравмы Смита
- Домашний
- ИССЛЕДОВАНИЯ
- Пересадка спинного мозга и пересадка периферических нервов
ПЕРЕСАДКА СПИННОГО МОЗГА. По оценкам, ежегодно в США около 10 000 пациентов страдают травмой спинного мозга (ТСМ) и примерно 250 000 пациентов с хронической травмой спинного мозга. Соответственно, предпринимаются обширные исследовательские усилия по разработке методов, которые усиливают рост аксонов в поврежденном спинном мозге. Основная цель этих усилий состоит в том, чтобы стимулировать рост аксонов по всему поражению, чтобы интегрироваться с жизнеспособной тканью с обеих сторон и создать функциональные реле.
Соответственно, предпринимаются обширные исследовательские усилия по разработке методов, которые усиливают рост аксонов в поврежденном спинном мозге. Основная цель этих усилий состоит в том, чтобы стимулировать рост аксонов по всему поражению, чтобы интегрироваться с жизнеспособной тканью с обеих сторон и создать функциональные реле.
Были предприняты многочисленные заметные попытки продвижения аксонных мостиков через поражения спинного мозга. Некоторые из предыдущих методов были успешными в стимулировании прорастания аксонов в или вокруг поражений спинного мозга на животных моделях. Хотя это многообещающее разрастание обычно включает лишь небольшое количество спинальных аксонов, растущих на ограниченное расстояние. Было высказано предположение, что улучшение функционального восстановления, часто обнаруживаемое после ТСМ у этих трансплантированных животных, в первую очередь связано с физической и биохимической поддержкой ткани хозяина, окружающей поражение, а не с образованием новых интраспинальных цепей через поражение. Учитывая, что поражения ТСМ у человека обычно простираются на несколько сантиметров, соединение этих поражений с аксонами достаточного количества и длины для формирования функциональных реле остается огромной проблемой.
Учитывая, что поражения ТСМ у человека обычно простираются на несколько сантиметров, соединение этих поражений с аксонами достаточного количества и длины для формирования функциональных реле остается огромной проблемой.
В отличие от стимуляции роста аксонов путем стимуляции прорастания аксонов, исследователи недавно разработали технологию, которая вызывает быстрый рост аксонов за счет непрерывного механического удлинения интегрированных аксонных путей in vitro (Smith et al., 2001; Pfister et al., 2004). ). Эта технология роста растяжения аксонов была недавно адаптирована для создания нервных конструкций, состоящих из живых и функциональных аксонных трактов, которые способны перекрывать даже обширные поражения ТСМ (рис.: Иллюстрация трансплантата ТСМ). Совсем недавно было обнаружено, что трансплантированные удлиненные культуры трансгенных крыс GFP выживали в течение четырех недель в поврежденном спинном мозге (рис.: Выживание трансплантированных тканей). Эти результаты демонстрируют перспективность нервных конструкций лаборатории, состоящих из выращенных аксонов, для преодоления даже обширных поражений спинного мозга.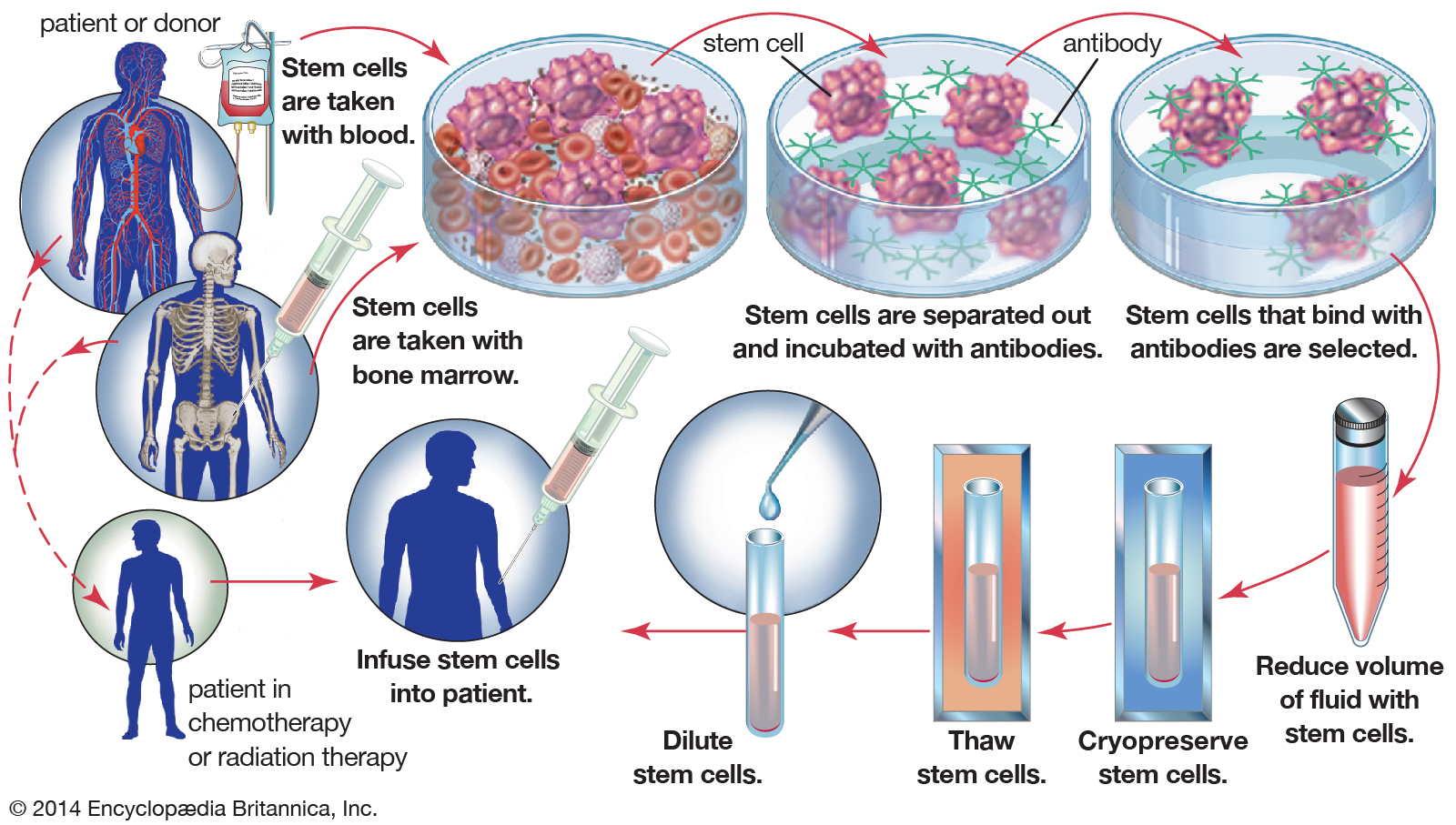 В настоящее время исследовательская группа изучает функциональное восстановление после ТСМ у трансплантированных животных.
В настоящее время исследовательская группа изучает функциональное восстановление после ТСМ у трансплантированных животных.
ПЕРЕСАДКА ПЕРИФЕРИЧЕСКИХ НЕРВОВ. Традиционные методы восстановления дефицита периферических нервов включают перекрытие нервного промежутка аутологичным трансплантатом или биорассасывающейся трубкой. Аутологичный трансплантат считается золотым стандартом для восстановления значительных поражений ПНС, но его проблемы включают ограниченный запас донорских нервов и заболеваемость донорского участка. Исследователи стремились проверить новую концепцию, согласно которой живые нейроны ганглия задних корешков и механически выращенные аксоны трансплантируются в щель седалищного нерва крысы диаметром 12 мм.
Трансплантация клеток для восстановления спинного мозга: кто, что, когда, где и почему?
1.
Cai J, Wu Y, Mirua T, Pierce JL, Lucero MT, Albertine KH, Spangrude GJ, Rao MS.
Свойства эмбриональной мультипотентной нервной стволовой клетки (клетки NEP). Дев биол. 2002;251(2):221–240. [PubMed] [Google Scholar]
Дев биол. 2002;251(2):221–240. [PubMed] [Google Scholar]
2. Кальяни А., Хобсон К., Рао М.С. Нейроэпителиальные стволовые клетки эмбрионального спинного мозга: выделение, характеристика и клональный анализ. Дев биол. 1997;186(2):202–223. [PubMed] [Академия Google]
3. Муджтаба Т., Пайпер Д.Р., Кальяни А., Гроувс А.К., Лусеро М.Т., Рао М.С. Нервные предшественники, ограниченные по клону, могут быть выделены как из нервной трубки мыши, так и из культивируемых ЭС клеток. Дев биол. 1999;214(1):113–127. [PubMed] [Google Scholar]
4. Лепор AC, Фишер И. Линейно-ограниченные нейральные предшественники выживают, мигрируют и дифференцируются после трансплантации в поврежденный спинной мозг взрослого человека. Опыт Нейрол. 2005;194(1):230–242. [PubMed] [Google Scholar]
5. Рейер П.Дж., Перлоу М.Дж., Гут Л. Разработка эмбриональных трансплантатов спинного мозга у крыс. Мозг Res. 1983;312(2):201–219. [PubMed] [Google Scholar]
6.
Уайт Т.Е., Лейн М.А., Сандху М. С., О’Стин Б.Е., Фуллер Д.Д., Рейер П.Дж.
Трансплантация нейронов-предшественников и респираторные исходы после повреждения верхнего шейного отдела спинного мозга у взрослых крыс. Опыт Нейрол. 2010;225(1):231–236. [Бесплатная статья PMC] [PubMed] [Google Scholar]
С., О’Стин Б.Е., Фуллер Д.Д., Рейер П.Дж.
Трансплантация нейронов-предшественников и респираторные исходы после повреждения верхнего шейного отдела спинного мозга у взрослых крыс. Опыт Нейрол. 2010;225(1):231–236. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Джованини М.А., Рейер П.Дж., Эскин Т.А., Вирт Э., Андерсон Д.К. Характеристики трансплантатов спинного мозга плода человека в спинном мозге взрослой крысы: влияние повреждений и условий трансплантации. Опыт Нейрол. 1997;148(2):523–543. [PubMed] [Google Scholar]
8. Спруанс В.М., Жолудева Л.В., Хормиго К.М., Рандельман М.Л., Бездудная Т., Марченко В., Лейн М.А. Интеграция трансплантированных нейронных предшественников с поврежденным шейным отделом спинного мозга. J Нейротравма. 2018;35(15):1781–1799. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9.
Лу П., Ван Ю, Грэм Л, Макхейл К, Гао М, Ву Д, Брок Дж, Блеш А, Розенцвейг Э.С., Хавтон Л.А., Чжэн Б., Коннер Дж.М., Марсала М., Тушински М.Х.
Рост на большие расстояния и связность нервных стволовых клеток после тяжелой травмы спинного мозга. Клетка. 2012;150(6):1264–1273. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Клетка. 2012;150(6):1264–1273. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Рейер П.Дж., Брегман Б.С., Вуек Дж.Р. Интраспинальные трансплантаты эмбриональной ткани спинного мозга у взрослых и новорожденных крыс: доказательства топографической дифференциации и аксональных взаимодействий с ЦНС хозяина В: Бьорклунд А., Стеневи У., редакторы. Пересадка нервов в ЦНС млекопитающих. Нью-Йорк, (Нью-Йорк), США: Публикации Elsevier Science; 1985. с. 257–263. [Google Академия]
11. Джейкман Л.Б., Рейер П.Дж., Брегман Б.С., Уэйд Э.Б., Дэйли М., Кастнер Р.Дж., Хаймс Б.Т., Тесслер А. Дифференциация желатинозоподобных участков субстанции в интраспинальных и внутримозговых трансплантатах эмбриональной ткани спинного мозга крысы. Опыт Нейрол. 1989;103(1):17–33. [PubMed] [Google Scholar]
12.
Хоул Дж. Д., Скиннер Р. Д., Гарсия-Рилл Э., Тернер К. Л.
Синаптические вызванные потенциалы от регенерирующих аксонов дорсальных корешков в трансплантатах ткани спинного мозга плода. Опыт Нейрол. 1996;139(2):278–290. [PubMed] [Google Scholar]
Опыт Нейрол. 1996;139(2):278–290. [PubMed] [Google Scholar]
13. Джейкман Л.Б., Рейер П.Дж. Проекции аксонов между трансплантатами спинного мозга плода и спинным мозгом взрослой крысы: нейроанатомическое отслеживание локальных взаимодействий. J Комп Нейрол. 1991;307(2):311–334. [PubMed] [Академия Google]
14. Lee KZ, Lane MA, Dougherty BJ, Mercier LM, Sandhu MS, Sanchez JC, Reier PJ, Fuller DD. Интраспинальная трансплантация и модуляция электрофизиологической активности донорских нейронов. Опыт Нейрол. 2014; 251:47–57. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15. Рейер П.Дж., Хоул Дж.Д. Глиальный рубец: его влияние на удлинение аксонов и трансплантационные подходы к восстановлению ЦНС. Ад Нейрол. 1988; 47: 87–138. [PubMed] [Google Scholar]
16.
Рейер П.Дж., Хоул Дж.Д., Тесслер А., Джейкман Л.
Астроглиоз и регенерация: новый взгляд на старую гипотезу В: Norenberg MD, Hertz L, Schousboe A, редактор. Биохимическая патология астроцитов. Нью-Йорк, (Нью-Йорк), США: Лисс;
1988. стр. 107–122. [Google Академия]
стр. 107–122. [Google Академия]
17. Хоул Дж. Структурная целостность глиальной рубцовой ткани, связанной с хроническим поражением спинного мозга, может быть изменена трансплантированной тканью спинного мозга плода. J Neurosci Res. 1992;31(1):120–130. [PubMed] [Google Scholar]
18. Лу Д.С., Ниу Т., Алейник В.А. Молекулярное и клеточное развитие двигательной схемы спинного мозга. Фронт Мол Невроски. 2015;8:25. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Жолудева Л.В., Цян Л., Марченко В., Догерти К.Дж., Сакияма-Элберт С.Е., Лейн М.А. Нейропластический и терапевтический потенциал спинальных интернейронов в поврежденном спинном мозге. Тренды Нейроси. 2018;41(9): 625–639. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20.
Врбова Г. Стимулирование регенерации нейронов хозяина: трансплантация нервных тканей в поврежденный спинной мозг трансплантатами эмбриональной нервной ткани В: Ногради А., изд. Трансплантация нервной ткани в спинной мозг. 2-е изд. Джорджтаун (Техас): Springer Science+Business Media, Inc.; 2006. стр. 89–109. [Google Академия]
Джорджтаун (Техас): Springer Science+Business Media, Inc.; 2006. стр. 89–109. [Google Академия]
21. Айер Н.Р., Вилемс Т.С., Сакияма-Элберт С.Е. Стволовые клетки при повреждении спинного мозга: стратегии информирования о дифференцировке и трансплантации. Биотехнология Биоинж. 2017;114(2):245–259. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Жолудева Л.В., Айер Н.Р., Цян Л., Спруанс В.М., Рандельман М.Л., Уайт Н.В., Бездудная Т., Фишер И., Сакияма-Элберт С.Е., Лейн М.А. Трансплантация нейральных предшественников и интернейронов V2a после повреждения спинного мозга. J Нейротравма. 2018;35(24):2883–2903. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Брок Дж. Х., Грэм Л., Штауфенберг Э., Им С., Тушински М. Х. Нервные клетки-предшественники грызунов поддерживают функциональное восстановление после ушиба шейного отдела спинного мозга. J Нейротравма. 2018;35(9): 1069–1078. [Бесплатная статья PMC] [PubMed] [Google Scholar]
24.
Баттс Дж. К., Маккриди Д. А., Мартинес-Варгас Дж. А., Мендоса-Камачо Ф. Н., Хукуэй Т. А., Гиффорд К. А., Танеджа П., Ноубл-Хеуслейн Л., Макдевитт Т. С.
Дифференциация интернейронов V2a из плюрипотентных стволовых клеток человека. Proc Natl Acad Sci U S A. 2017;114(19):4969–4974. [Бесплатная статья PMC] [PubMed] [Google Scholar]
А., Мартинес-Варгас Дж. А., Мендоса-Камачо Ф. Н., Хукуэй Т. А., Гиффорд К. А., Танеджа П., Ноубл-Хеуслейн Л., Макдевитт Т. С.
Дифференциация интернейронов V2a из плюрипотентных стволовых клеток человека. Proc Natl Acad Sci U S A. 2017;114(19):4969–4974. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Жолудева Л.В., Карлинер Дж.С., Догерти К.Дж., Лейн М.А. Анатомическое рекрутирование интернейронов спинного мозга V2a в схему диафрагмальной моторики после высокого шейного повреждения спинного мозга. J Нейротравма. 2017;34(21):3058–3065. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Romer SH, Seedle K, Turner SM, Li J, Baccei ML, Crone SA. Дополнительные дыхательные мышцы усиливают вентиляцию у мышей с моделью БАС и активируются возбуждающими нейронами V2a. Опыт Нейрол. 2017; 287 (часть 2): 192–204. [PubMed] [Google Scholar]
27.
Fandel TM, Trivedi A, Nicholas CR, Zhang H, Chen J, Martinez AF, Noble-Haeusslein LJ, Kriegstein AR.
Трансплантированные предшественники интернейронов, полученные из стволовых клеток человека, смягчают дисфункцию мочевого пузыря у мышей и центральную невропатическую боль после травмы спинного мозга. Клеточная стволовая клетка. 2016;19(4): 544–557. [PubMed] [Google Scholar]
Клеточная стволовая клетка. 2016;19(4): 544–557. [PubMed] [Google Scholar]
28. Браз Дж. М., Шариф-Наэйни Р., Фогт Д., Кригштейн А., Альварес-Буйлла А., Рубенштейн Дж. Л., Басбаум А. И. Предшественники ГАМКергических нейронов переднего мозга интегрируются в спинной мозг взрослого человека и уменьшают нейропатическую боль, вызванную травмой. Нейрон. 2012;74(4):663–675. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Браун К.Р., Баттс Дж.К., Маккриди Д.А., Сакияма-Элберт С.Е. Генерация интернейронов V2a из эмбриональных стволовых клеток мыши. Стволовые клетки Dev. 2014;23(15):1765–1776. [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Xu H, Iyer N, Huettner JE, Sakiyama-Elbert SE. Селектируемая пуромицином клеточная линия для обогащения интернейронов V3, полученных из эмбриональных стволовых клеток мыши. Стволовые клетки Res Ther. 2015;6:220. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31.
Сюй Х, Сакияма-Элберт С.Е.
Направленная дифференцировка интернейронов V3 из эмбриональных стволовых клеток мыши. Стволовые клетки Dev. 2015;24(22):2723–2732. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Стволовые клетки Dev. 2015;24(22):2723–2732. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Айер Н.Р., Хюттнер Дж.Э., Баттс Дж.К., Браун К.Р., Сакияма-Элберт С.Е. Генерация высокообогащенных интернейронов V2a из эмбриональных стволовых клеток мыши. Опыт Нейрол. 2016; 277:305–316. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Кальяни А.Дж., Пайпер Д., Муджтаба Т., Лусеро М.Т., Рао М.С. Предшественники нейронов спинного мозга генерируют множественные фенотипы нейронов в культуре. Дж. Нейроски. 1998;18(19):7856–7868. [Бесплатная статья PMC] [PubMed] [Google Scholar]
34. Майер-Прошель М., Кальяни А.Дж., Муджтаба Т., Рао М.С. Выделение предшественников нейронов с ограничением по происхождению из мультипотентных нейроэпителиальных стволовых клеток. Нейрон. 1997;19(4):773–785. [PubMed] [Google Scholar]
35.
Рао М.С., Майер-Прошел М.
Глиально-рестриктированные предшественники происходят из мультипотентных нейроэпителиальных стволовых клеток. Дев биол.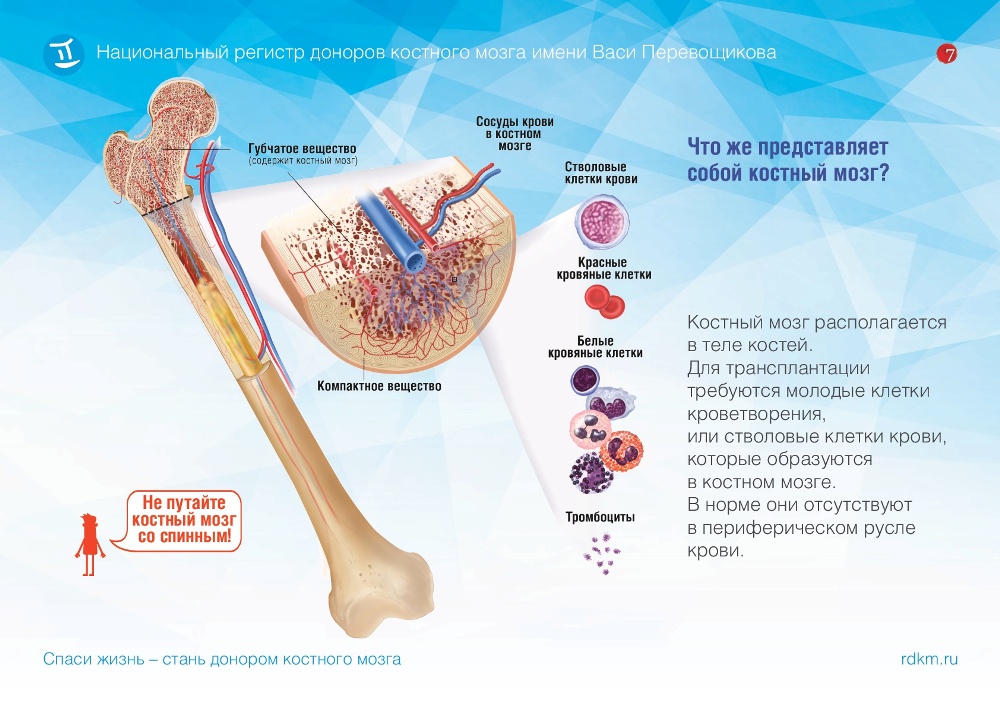 1997;188(1):48–63. [PubMed] [Google Scholar]
1997;188(1):48–63. [PubMed] [Google Scholar]
36. Боннер Дж. Ф., Хаас С. Дж., Фишер И. Подготовка нервных стволовых клеток и предшественников: производство нейронов и применение прививки. Методы Мол Биол. 2013; 1078: 65–88. [PubMed] [Google Scholar]
37. Хаас С., Нойхубер Б., Ямагами Т., Рао М., Фишер И. Фенотипический анализ астроцитов, полученных из глиальных ограниченных предшественников, и их влияние на регенерацию аксонов. Опыт Нейрол. 2012;233(2):717–732. [Бесплатная статья PMC] [PubMed] [Google Scholar]
38. Хан С.С., Канг Д.Ю., Муджтаба Т., Рао М.С., Фишер И. Привитые ограниченные по клону предшественники дифференцируются исключительно в нейроны во взрослом спинном мозге. Опыт Нейрол. 2002;177(2):360–375. [PubMed] [Google Scholar]
39.
Хань С.С., Лю Ю., Тайлер-Польш С., Рао М.С., Фишер И.
Трансплантация глиально-ограниченных клеток-предшественников во взрослый спинной мозг: выживание, глиально-специфическая дифференцировка и преимущественная миграция в белое вещество.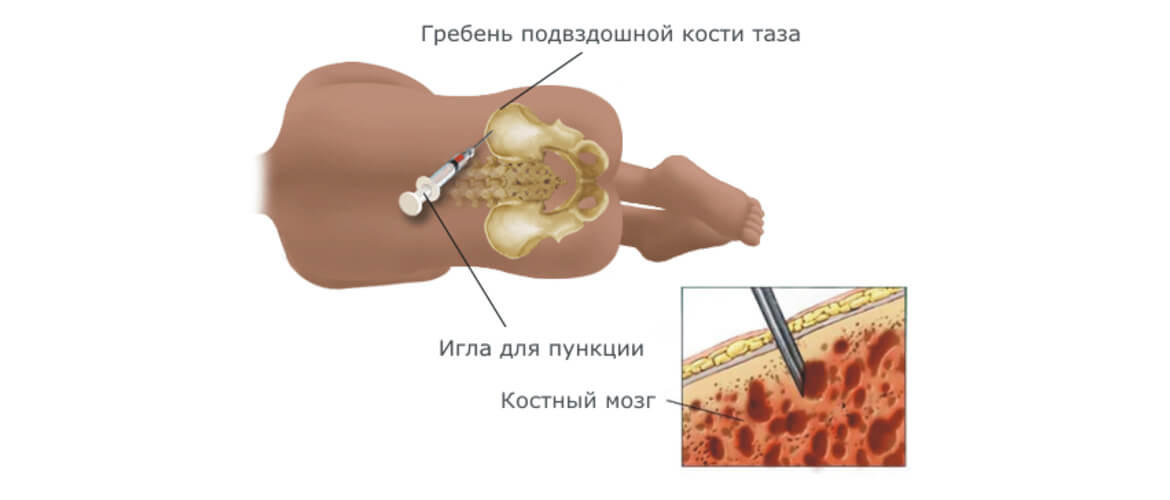 Глия. 2004;45(1):1–16. [PubMed] [Академия Google]
Глия. 2004;45(1):1–16. [PubMed] [Академия Google]
40. Кетчек А.Р., Хаас С., Галло Г., Фишер И. Роль нейрональных и глиальных предшественников в преодолении хондроитинсульфатного ингибирования протеогликана. Опыт Нейрол. 2012;235(2):627–637. [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Lepore AC, Neuhuber B, Connors TM, Han SS, Liu Y, Daniels MP, Rao MS, Fischer I. Долгосрочная судьба нервных клеток-предшественников после трансплантации в развивающуюся и взрослую ЦНС. Неврология. 2006;139(2):513–530. [PubMed] [Академия Google]
42. Medalha CC, Jin Y, Yamagami T, Haas C, Fischer I. Трансплантация нейронных предшественников в модель полного разреза повреждения спинного мозга. J Neurosci Res. 2014;92(5):607–618. [PubMed] [Google Scholar]
43.
Мицуи Т., Шумский Дж.С., Лепор А.С., Мюррей М., Фишер И.
Трансплантация нейрональных и глиальных ограниченных предшественников в ушибленный спинной мозг улучшает мочевой пузырь и моторные функции, снижает термическую гиперчувствительность и модифицирует интраспинальные схемы. Дж. Нейроски. 2005;25(42):9624–9636. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж. Нейроски. 2005;25(42):9624–9636. [Бесплатная статья PMC] [PubMed] [Google Scholar]
44. Хоу С., Том В.Дж., Грэм Л., Лу П., Блеш А. Частичное восстановление сердечно-сосудистой функции трансплантатами эмбриональных нейральных стволовых клеток после полной перерезки спинного мозга. Дж. Нейроски. 2013;33(43):17138–17149. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Приват А., Мансур Х., Пави А., Жеффард М., Сандиллон Ф. Трансплантация диссоциированных эмбриональных серотониновых нейронов в перерезанный спинной мозг взрослых крыс. Нейроски Летт. 1986;66(1):61–66. [PubMed] [Google Scholar]
46. Риботта М.Г., Провеншер Дж., Фераболи-Лонхерр Д., Россиньол С., Приват А., Орсал Д. Активация локомоции у взрослых крыс с хроническим позвоночником достигается путем трансплантации эмбриональных клеток шва, реиннервирующих определенный поясничный уровень. Дж. Нейроски. 2000;20(13):5144–5152. [Бесплатная статья PMC] [PubMed] [Google Scholar]
47.
Догерти Б. Дж., Гонсалес-Роти Э.Дж., Ли К.З., Росс Х.Х., Рейер П.Дж., Фуллер Д.Д.
Респираторные исходы после срединно-шейной трансплантации эмбриональных мозговых клеток у крыс с травмой шейного отдела спинного мозга. Опыт Нейрол. 2016; 278:22–26. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж., Гонсалес-Роти Э.Дж., Ли К.З., Росс Х.Х., Рейер П.Дж., Фуллер Д.Д.
Респираторные исходы после срединно-шейной трансплантации эмбриональных мозговых клеток у крыс с травмой шейного отдела спинного мозга. Опыт Нейрол. 2016; 278:22–26. [Бесплатная статья PMC] [PubMed] [Google Scholar]
48. Каммингс Б.Дж., Учида Н., Тамаки С.Дж., Салазар Д.Л., Хушманд М., Саммерс Р., Гейдж Ф.Х., Андерсон А.Дж. Нервные стволовые клетки человека дифференцируются и способствуют восстановлению двигательной активности у мышей с травмой спинного мозга. Proc Natl Acad Sci U S A. 2005;102(39):14069–14074. [Бесплатная статья PMC] [PubMed] [Google Scholar]
49. Каммингс Б.Дж., Учида Н., Тамаки С.Дж., Андерсон А.Дж. Дифференцировка нервных стволовых клеток человека после трансплантации мышам с травмами спинного мозга: связь с восстановлением двигательной функции. Нейрол Рез. 2006;28(5):474–481. [PubMed] [Академия Google]
50.
Хушманд М.Дж., Зонтаг С.Дж., Учида Н., Тамаки С., Андерсон А.Дж., Каммингс Б. Дж.
Анализ механизмов восстановления, опосредованных хозяином, после трансплантации стволовых клеток ЦНС человека при повреждении спинного мозга: корреляция приживления трансплантата с выздоровлением. ПЛОС Один. 2009;4(6):e5871. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж.
Анализ механизмов восстановления, опосредованных хозяином, после трансплантации стволовых клеток ЦНС человека при повреждении спинного мозга: корреляция приживления трансплантата с выздоровлением. ПЛОС Один. 2009;4(6):e5871. [Бесплатная статья PMC] [PubMed] [Google Scholar]
51. Салазар Д.Л., Учида Н., Хамерс Ф.П., Каммингс Б.Дж., Андерсон А.Дж. Нервные стволовые клетки человека дифференцируются и способствуют восстановлению двигательной активности на модели мышей NOD-scid с ранним хроническим повреждением спинного мозга. ПЛОС Один. 2010;5(8):e12272. [Бесплатная статья PMC] [PubMed] [Google Scholar]
52. Hooshmand MJ, Nguyen HX, Piltti KM, Benavente F, Hong S, Flanagan L, Uchida N, Cummings BJ, Anderson AJ. Нейтрофилы индуцируют астроглиальную дифференцировку и миграцию нервных стволовых клеток человека посредством синтеза C1q и C3a. Дж Иммунол. 2017;199(3):1069–1085. [Бесплатная статья PMC] [PubMed] [Google Scholar]
53.
О’Брайен М.К., Оппенгейм Р.В.
Развитие и выживание грудных мотонейронов и мускулатуры задних конечностей после трансплантации грудной нервной трубки в поясничную область куриного эмбриона: анатомические аспекты. Дж Нейробиол. 1990;21(2):313–340. [PubMed] [Google Scholar]
Дж Нейробиол. 1990;21(2):313–340. [PubMed] [Google Scholar]
54. Инь К.В., Джонсон Дж., Преветт Д., Оппенгейм Р.В. Гибель клеток спинномозговых мотонейронов у куриных эмбрионов после деафферентации: спасательные эффекты тканевых экстрактов, растворимых белков и нейротрофических агентов. Дж. Нейроски. 1994;14(12):7629–7640. [Бесплатная статья PMC] [PubMed] [Google Scholar]
55. Грамблз Р.М., Сесодиа С., Вуд П.М., Томас К.К. Нейротрофические факторы улучшают выживаемость мотонейронов и функцию мышц, реиннервируемых эмбриональными нейронами. J Neuropathol Exp Neurol. 2009 г.;68(7):736–746. [Бесплатная статья PMC] [PubMed] [Google Scholar]
56. Grumbles RM, Almeida VW, Casella GT, Wood PM, Hemstapat K, Thomas CK. Замена мотонейронов для реиннервации скелетных мышц у взрослых крыс. J Neuropathol Exp Neurol. 2012;71(10):921–930. [Бесплатная статья PMC] [PubMed] [Google Scholar]
57.
Грамблз Р.М., Лю Ю., Томас К.М., Вуд П.М., Томас К.К.
Острая стимуляция трансплантированных нейронов улучшает выживаемость мотонейронов, рост аксонов и реиннервацию мышц. J Нейротравма. 2013;30(12):1062–1069.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Нейротравма. 2013;30(12):1062–1069.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
58. Лейн М.А., Труттнер Дж.С., Бруншвиг Дж.П., Гомес А., Бунге М.Б., Дитрих В.Д., Дзигелевская К.М., Эк С.Дж., Вандеберг Дж.Л., Сондерс Н.Р. Возрастные различия локальных клеточных и молекулярных ответов на повреждение в развивающемся спинном мозге опоссума Monodelphis domestica. Евр Джей Нейроски. 2007;25(6):1725–1742. [PubMed] [Google Scholar]
59. Смит GM, Сильвер Дж. Трансплантация незрелых и зрелых астроцитов и их влияние на формирование рубца в пораженной центральной нервной системе. Прог Мозг Res. 1988;78:353–361. [PubMed] [Google Scholar]
60. Смит Г.М., Миллер Р.Х. Незрелые астроциты типа 1 подавляют образование глиальных рубцов, подвижны и взаимодействуют с кровеносными сосудами. Мозг Res. 1991;543(1):111–122. [PubMed] [Google Scholar]
61.
Хаас С, Фишер И.
Человеческие астроциты, полученные из глиальных ограниченных предшественников, поддерживают регенерацию поврежденного спинного мозга.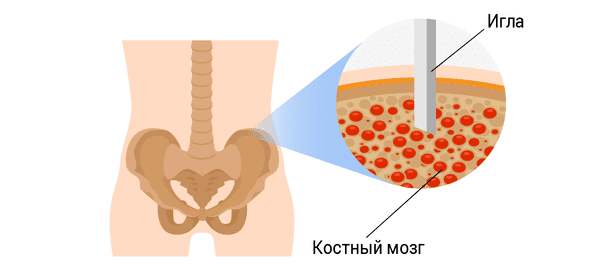 J Нейротравма. 2013;30(12):1035–1052. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Нейротравма. 2013;30(12):1035–1052. [Бесплатная статья PMC] [PubMed] [Google Scholar]
62. Джин Ю., Нойхубер Б., Сингх А., Буйер Дж., Лепор А., Боннер Дж., Хаймс Т., Кампанелли Дж. Т., Фишер И. Трансплантация человеческих глиальных ограниченных предшественников и производных астроцитов в модель контузии с повреждением спинного мозга. J Нейротравма. 2011;28(4):579–594. [Бесплатная статья PMC] [PubMed] [Google Scholar]
63. Hill CE, Proschel C, Noble M, Mayer-Proschel M, Gensel JC, Beattie MS, Bresnahan JC. Острая трансплантация клеток-предшественников, ограниченных глией, в контузионные повреждения спинного мозга: выживаемость, дифференцировка и влияние на среду поражения и регенерацию аксонов. Опыт Нейрол. 2004;190(2):289–310. [PubMed] [Google Scholar]
64. Лидделоу С.А., Баррес Б.А. Реактивные астроциты: производство, функция и терапевтический потенциал. Иммунитет. 2017;46(6):957–967. [PubMed] [Google Scholar]
65.
Ли К., Джавед Э., Скура Д., Хала Т.Дж. , Ситарам С., Фалникар А., Ричард Дж. П., Чорат А., Марагакис Н.Дж., Райт М.С., Лепор А.С.
Трансплантаты астроцитов, полученных из иПС-клеток человека, сохраняют дыхательную функцию после повреждения спинного мозга. Опыт Нейрол. 2015; 271:479–492. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Ситарам С., Фалникар А., Ричард Дж. П., Чорат А., Марагакис Н.Дж., Райт М.С., Лепор А.С.
Трансплантаты астроцитов, полученных из иПС-клеток человека, сохраняют дыхательную функцию после повреждения спинного мозга. Опыт Нейрол. 2015; 271:479–492. [Бесплатная статья PMC] [PubMed] [Google Scholar]
66. Фолкнер Дж., Кейрстед Х.С. Олигодендроциты-предшественники, полученные из эмбриональных стволовых клеток, для лечения травм спинного мозга. Транспл Иммунол. 2005;15(2):131–142. [PubMed] [Академия Google]
67. Кейрстед Х.С., Нистор Г., Бернал Г., Тотой М., Клотье Ф., Шарп К., Стюард О. Трансплантаты клеток-предшественников олигодендроцитов, полученных из эмбриональных стволовых клеток человека, вызывают ремиелинизацию и восстанавливают двигательную активность после повреждения спинного мозга. Дж. Нейроски. 2005;25(19):4694–4705. [Бесплатная статья PMC] [PubMed] [Google Scholar]
68.
Нистор Г.И., Тотойу М.О., Хак Н., Карпентер М.К., Кейрстед Х.С.
Эмбриональные стволовые клетки человека дифференцируются в олигодендроциты высокой чистоты и миелинизируются после трансплантации спинного мозга. Глия. 2005;49(3): 385–396. [PubMed] [Google Scholar]
Глия. 2005;49(3): 385–396. [PubMed] [Google Scholar]
69. Клотье Ф., Зигенталер М.М., Нистор Г., Кейрстед Х.С. Трансплантация предшественников олигодендроцитов, полученных из эмбриональных стволовых клеток, в области повреждений спинного мозга крыс не причиняет вреда. Реген Мед. 2006;1(4):469–479. [PubMed] [Google Scholar]
70. Шарп Дж., Кейрстед Х.С. Терапевтическое применение предшественников олигодендроцитов, полученных из эмбриональных стволовых клеток человека. Курр Опин Биотехнолог. 2007;18(5):434–440. [PubMed] [Академия Google]
71. Бамбакидис Н.К., Миллер Р.Х. Трансплантация предшественников олигодендроцитов и sonic hedgehog приводит к улучшению функции и сохранению белого вещества спинного мозга взрослых крыс после контузии. Спайн Дж. 2004;4(1):16–26. [PubMed] [Google Scholar]
72.
Розенблют Дж., Шифф Р., Лян В.Л., Менна Г., Янг В.
Ксенотрансплантация трансгенных клеток линии олигодендроцитов взрослым крысам с травмой спинного мозга. Опыт Нейрол. 1997;147(1):172–182. [PubMed] [Академия Google]
1997;147(1):172–182. [PubMed] [Академия Google]
73. Лю С., Ку Ю., Стюарт Т.Дж., Ховард М.Дж., Чакраборти С., Холекамп Т.Ф., Макдональд Дж.В. Эмбриональные стволовые клетки дифференцируются в олигодендроциты и миелинизируются в культуре и после трансплантации спинного мозга. Proc Natl Acad Sci U S A. 2000;97(11):6126–6131. [Бесплатная статья PMC] [PubMed] [Google Scholar]
74. Прист К.А., Мэнли Н.К., Денхэм Дж., Вирт Э.Д. III, Лебковски Д.С. Доклиническая безопасность олигодендроцитов-предшественников, полученных из эмбриональных стволовых клеток, в поддержку клинических испытаний при повреждении спинного мозга. Реген Мед. 2015;10(8):939–958. [PubMed] [Google Scholar]
75. Хорнер П.Дж., Рейер П.Дж., Стоукс Б.Т. Количественный анализ васкуляризации и цитохромоксидазы после трансплантации плода в контуженном спинном мозге крысы. J Комп Нейрол. 1996;364(4):690–703. [PubMed] [Google Scholar]
76.
Раух М.Ф., Хайнс С.Р., Бертрам Дж., Редмонд А., Робинсон Р., Уильямс С. , Сюй Х., Мадри Дж.А., Лавик Э.Б.
Инженерный ангиогенез после травмы спинного мозга: совместное культивирование нейронных клеток-предшественников и эндотелиальных клеток в разлагаемом полимерном имплантате приводит к увеличению плотности сосудов и образованию гемато-спинномозгового барьера. Евр Джей Нейроски. 2009 г.;29(1):132–145. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Сюй Х., Мадри Дж.А., Лавик Э.Б.
Инженерный ангиогенез после травмы спинного мозга: совместное культивирование нейронных клеток-предшественников и эндотелиальных клеток в разлагаемом полимерном имплантате приводит к увеличению плотности сосудов и образованию гемато-спинномозгового барьера. Евр Джей Нейроски. 2009 г.;29(1):132–145. [Бесплатная статья PMC] [PubMed] [Google Scholar]
77. Дулин Дж.Н., Адлер А.Ф., Кумамару Х., Поплавски Г.Х.Д., Ли-Кубли С., Стробл Х., Гиббс Д., Кадоя К., Фосетт Дж.В., Лу П., Тушинский М.Х. Поврежденные моторные и сенсорные аксоны взрослых регенерируют в соответствующие органотипические домены трансплантатов нейральных предшественников. Нац коммун. 2018;9(1):84. [Бесплатная статья PMC] [PubMed] [Google Scholar]
78.
Кортин Г., Герасименко Ю., Ван ден Бранд Р., Ю А., Мусиенко П., Чжун Х., Сонг Б., Ао Ю., Итияма Р. М., Лавров И., Рой Р. Р., Софронев М. В., Эдгертон В. Р.
Преобразование нефункциональных спинальных цепей в функциональные состояния после потери мозгового входа. Нат Нейроски. 2009 г.;12(10):1333–1342. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Нат Нейроски. 2009 г.;12(10):1333–1342. [Бесплатная статья PMC] [PubMed] [Google Scholar]
79. Кортин Г., Сонг Б., Рой Р. Р., Чжун Х., Херрманн Дж. Э., Ао Ю., Ци Дж., Эдгертон В. Р., Софронев М. В. Восстановление супраспинального контроля шагания через непрямые проприоспинальные релейные связи после травмы спинного мозга. Нат Мед. 2008;14(1):69–74. [Бесплатная статья PMC] [PubMed] [Google Scholar]
80. Барейр Ф.М., Кершенштайнер М., Рейнето О., Меттенлейтер Т.С., Вайнманн О., Шваб М.Э. Поврежденный спинной мозг спонтанно образует новую интраспинальную цепь у взрослых крыс. Нат Нейроски. 2004;7(3):269–277. [PubMed] [Google Scholar]
81. Чен Б., Ли И., Ю. Б., Чжан З., Броммер Б., Уильямс П.Р., Лю И., Хегарти С.В., Чжоу С., Чжу Дж., Го Х., Лу И., Чжан И., Гу Х., Хе З. Реактивация бездействующих релейных путей в поврежденном спинном мозге с помощью манипуляций с KCC2. Клетка. 2018;174(3):521–535.e13. [Бесплатная статья PMC] [PubMed] [Google Scholar]
82.
Роппер А. Э., Такор Д.К., Хань И., Ю Д., Зенг С., Андерсон Дж. Э., Алжубури З., Ким С. В., Ван Х., Сидман Р. Л., Зафонте Р. Д., Тенг Ю. Д.
Определение нейробиологии восстановления поврежденного спинного мозга путем имплантации hMSC с синтетической матрицей. Proc Natl Acad Sci U S A. 2017;114(5):E820–E829.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Э., Такор Д.К., Хань И., Ю Д., Зенг С., Андерсон Дж. Э., Алжубури З., Ким С. В., Ван Х., Сидман Р. Л., Зафонте Р. Д., Тенг Ю. Д.
Определение нейробиологии восстановления поврежденного спинного мозга путем имплантации hMSC с синтетической матрицей. Proc Natl Acad Sci U S A. 2017;114(5):E820–E829.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
83. Рейер П.Дж., Хоул Дж.Д., Джейкман Л., Виниалски Д., Тесслер А. Трансплантация ткани спинного мозга плода при острых и хронических гемисекциях и контузионных поражениях спинного мозга взрослых крыс. Прог Мозг Res. 1988; 78: 173–179. [PubMed] [Google Scholar]
84. Рейер П.Дж., Брегман Б.С., Вуек Дж.Р. Интраспинальная трансплантация эмбриональной ткани спинного мозга у новорожденных и взрослых крыс. J Комп Нейрол. 1986;247(3):275–296. [PubMed] [Академия Google]
85.
Тиле Д.П., Шримшер Г.В., Рейер П.Дж.
Сравнение роста и судьбы фетальных спинальных изо- и аллотрансплантатов у взрослых крыс с поврежденным спинным мозгом. Опыт Нейрол. 1996;142(1):128–143. [PubMed] [Google Scholar]
1996;142(1):128–143. [PubMed] [Google Scholar]
86. Боннер Дж. Ф., Коннорс Т. М., Сильверман В. Ф., Ковальски Д. П., Лемей М. А., Фишер И. Привитые нейронные предшественники интегрируются и восстанавливают синаптические связи в поврежденном спинном мозге. Дж. Нейроски. 2011;31(12):4675–4686. [Бесплатная статья PMC] [PubMed] [Google Scholar]
87. Боннер Дж. Ф., Блеш А., Нойхубер Б., Фишер И. Стимулирование направленного роста аксонов из нервных предшественников, трансплантированных в поврежденный спинной мозг. J Neurosci Res. 2010;88(6):1182–1192. [Бесплатная статья PMC] [PubMed] [Google Scholar]
88. Coumans JV, Lin TT, Dai HN, MacArthur L, McAtee M, Nash C, Bregman BS. Регенерация аксонов и функциональное восстановление после полной перерезки спинного мозга у крыс при отсроченном лечении трансплантатами и нейротрофинами. Дж. Нейроски. 2001;21(23):9334–9344. [Бесплатная статья PMC] [PubMed] [Google Scholar]
89.
Линь К.С., Лай С.Р., Шао Ю.Х., Чен С.Л., Ли К. З.
Терапевтическая эффективность отсроченной трансплантации ткани спинного мозга плода на дыхательную функцию после средней шейной травмы спинного мозга. Нейротерапия. 2017;14(3):792–809. [Бесплатная статья PMC] [PubMed] [Google Scholar]
З.
Терапевтическая эффективность отсроченной трансплантации ткани спинного мозга плода на дыхательную функцию после средней шейной травмы спинного мозга. Нейротерапия. 2017;14(3):792–809. [Бесплатная статья PMC] [PubMed] [Google Scholar]
90. Хуле Дж. Д., Рейер П. Дж. Трансплантация ткани спинного мозга плода в хронически поврежденный спинной мозг взрослой крысы. J Комп Нейрол. 1988;269(4):535–547. [PubMed] [Google Scholar]
91. Таширо С., Нисимура С., Иваи Х., Сугай К., Чжан Л., Шинозаки М., Иванами А., Тояма Ю., Лю М., Окано Х., Накамура М. Функциональное восстановление после трансплантации нервных стволовых клеток/клеток-предшественников в сочетании с тренировками на беговой дорожке у мышей с хроническим повреждением спинного мозга. Научный доклад 2016; 6: 30898. [Бесплатная статья PMC] [PubMed] [Google Scholar]
92.
Пилтти К.М., Салазар Д.Л., Учида Н., Каммингс Б.Дж., Андерсон А.Дж.
Безопасность трансплантации нервных стволовых клеток человека при хронической травме спинного мозга. Стволовые клетки Transl Med. 2013;2(12):961–974. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Стволовые клетки Transl Med. 2013;2(12):961–974. [Бесплатная статья PMC] [PubMed] [Google Scholar]
93. Ассинк П., Дункан Дж. Дж., Хилтон Б. Дж., Племель Дж. Р., Тецлафф В. Терапия клеточной трансплантацией при повреждении спинного мозга. Нат Нейроски. 2017;20(5):637–647. [PubMed] [Google Scholar]
94. Битти М.С., Бреснахан Дж. К., Комон Дж., Товар К.А., Ван Метер М., Андерсон Д.К., Фаден А.И., Хсу С.И., Ноубл Л.Дж., Зальцман С., Янг В. Эндогенная репарация после контузионных повреждений спинного мозга у крыс. Опыт Нейрол. 1997;148(2):453–463. [PubMed] [Google Scholar]
95. Хоул Дж. Д., Тесслер А. Восстановление хронической травмы спинного мозга. Опыт Нейрол. 2003;182(2):247–260. [PubMed] [Google Scholar]
96.
Судзуки Х., Ахуджа К.С., Салевски Р.П., Ли Л., Саткунендрараджа К., Нагоши Н., Шибата С., Фелингс М.Г.
Восстановление, опосредованное нервными стволовыми клетками, усиливается предварительной обработкой хондроитиназой ABC при хроническом повреждении шейного отдела спинного мозга. ПЛОС Один. 2017;12(8):e0182339. [Бесплатная статья PMC] [PubMed] [Google Scholar]
ПЛОС Один. 2017;12(8):e0182339. [Бесплатная статья PMC] [PubMed] [Google Scholar]
97. Уоррен П.М., Стайгер С.К., Дик Т.Э., Макфарлейн П.М., Алилайн В.Дж., Сильвер Дж. Быстрое и надежное восстановление дыхания в течение длительного времени после травмы спинного мозга. Нац коммун. 2018;9(1):4843. [Бесплатная статья PMC] [PubMed] [Google Scholar]
98. Иваи Х., Нори С., Нисимура С., Ясуда А., Такано М., Цудзи О., Фудзиёси К., Тояма Й., Окано Х., Накамура М. Трансплантация нервных стволовых клеток/клеток-предшественников в разных местах мышам с травмой спинного мозга. Трансплантация клеток. 2014;23(11):1451–1464. [PubMed] [Академия Google]
99. Вилемс Т.С., Пардик Дж., Айер Н., Сакияма-Элберт С.Е. Комбинированная терапия нейральными предшественниками, полученными из стволовых клеток, и лекарственная доставка антиингибиторных молекул при повреждении спинного мозга. Акта Биоматер. 2015;28:23–32. [Бесплатная статья PMC] [PubMed] [Google Scholar]
100.
Томпсон Р. Э., Пардик Дж., Смит Л., Кенни П., Кроуфорд Л., Шойхет М., Сакияма-Элберт С.
Влияние гидрогелей гиалуроновой кислоты, содержащих внеклеточный матрикс, полученный из астроцитов, и/или интернейроны V2a, на гистологические результаты после повреждения спинного мозга. Биоматериалы. 2018; 162: 208–223. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Э., Пардик Дж., Смит Л., Кенни П., Кроуфорд Л., Шойхет М., Сакияма-Элберт С.
Влияние гидрогелей гиалуроновой кислоты, содержащих внеклеточный матрикс, полученный из астроцитов, и/или интернейроны V2a, на гистологические результаты после повреждения спинного мозга. Биоматериалы. 2018; 162: 208–223. [Бесплатная статья PMC] [PubMed] [Google Scholar]
101. Томпсон Р., Сакияма-Элберт С. Использование биоматериалов для стимулирования прорегенеративных глиальных фенотипов после повреждений нервной системы. Биомед Матер. 2018;13(2):024104. [Бесплатная статья PMC] [PubMed] [Google Scholar]
102. Фераболи-Лонхерр Д., Орсал Д., Яковлефф А., Хименес-и-Риботта М., Приват А. Восстановление локомоторной активности у взрослых хронических спинальных крыс после подтравматической трансплантации эмбриональных нервных клеток: специфическая роль серотонинергических нейронов. Опыт Мозг Res. 1997;113(3):443–454. [PubMed] [Академия Google]
103.
Лепор А.С., Бакши А., Свэнгер С.А., Рао М. С., Фишер И.
Нервные клетки-предшественники могут быть доставлены в поврежденный шейный отдел спинного мозга путем интратекальной инъекции в поясничный отдел. Мозг Res. 2005;1045(1–2):206–216. [PubMed] [Google Scholar]
С., Фишер И.
Нервные клетки-предшественники могут быть доставлены в поврежденный шейный отдел спинного мозга путем интратекальной инъекции в поясничный отдел. Мозг Res. 2005;1045(1–2):206–216. [PubMed] [Google Scholar]
104. Бай Х, Сузуки Ю, Нода Т, Ву С, Катаока К, Китада М, Охта М, Чоу Х, Идэ С. Диссеминация и пролиферация нейральных стволовых клеток на спинном мозге путем инъекции в четвертый желудочек крысы: метод трансплантации клеток. J Neurosci Методы. 2003;124(2):181–187. [PubMed] [Академия Google]
105. Охта М., Судзуки Ю., Нода Т., Эдзири Ю., Дезава М., Катаока К., Чоу Х., Исикава Н., Мацумото Н., Ивасита Ю., Мизута Э., Куно С., Идэ К. Стромальные клетки костного мозга, введенные в спинномозговую жидкость, способствуют функциональному восстановлению поврежденного спинного мозга крыс с уменьшением образования полостей. Опыт Нейрол. 2004;187(2):266–278. [PubMed] [Google Scholar]
106.
Охта М., Сузуки Ю., Нода Т., Катаока К., Чоу Х., Исикава Н., Китада М., Мацумото Н.

 Все непредвиденные расходы покроем мы
Все непредвиденные расходы покроем мы