Эмболия околоплодными водами — причины, симптомы, диагностика и лечение
Эмболия околоплодными водами (ЭОВ) – это патология, развитие которой связано с попаданием амниотической жидкости в систему кровообращения матери с последующей анафилактоидной реакцией на компоненты этой жидкости. Клинические проявления преимущественно обусловлены кардиопульмональным шоком и нарушением системы коагуляции. Диагностика при эмболии околоплодными водами осуществляется путем комплексной оценки физикальных, лабораторных и инструментальных данных. Лечение ЭОВ заключается в устранении анафилактоидной реакции, нормализации работы сердечно-сосудистой и дыхательной систем, восстановлении ОЦК и системы гемостаза.
Общие сведения
Эмболия околоплодными водами, или анафилактоидный синдром беременности – это патологическое состояние в акушерстве, которое характеризуется попаданием амниотической жидкости в системный кровоток матери. Впервые клиническая картина ЭОВ была описана в 1926 году бразильским врачом Дж. Мейером. В 1941 году совокупность признаков данного состояния была объединена американцами П. Штейнером и К. Лашбоу в специальный акушерский синдром.
Впервые клиническая картина ЭОВ была описана в 1926 году бразильским врачом Дж. Мейером. В 1941 году совокупность признаков данного состояния была объединена американцами П. Штейнером и К. Лашбоу в специальный акушерский синдром.
Общая распространенность эмболии околоплодными водами составляет от 1 до 8 случаев на 10 000 родов. При этом показатель материнской и перинатальной смертности при данном осложнении колеблется в пределах 84-87%. В общей структуре материнской летальности эмболия околоплодными водами составляет порядка 15-17% всех случаев.
Эмболия околоплодными водами
Причины
Выделяют несколько механизмов развития эмболии околоплодными водами: повышение внутриматочного давления, падение кровяного давления в венах матки, непосредственный контакт между амниотическим мешком и поврежденными кровеносными сосудами. В первую группу включают все факторы, способные чрезмерно повышать давление в амниотическом мешке, которое в процессе родовой деятельности в норме составляет до 20 мм вод.
- многоплодная беременность
- масса тела ребенка свыше 4500 г («крупный плод»)
- многоводие
- тазовое предлежание
- потеря эластичности шейки матки
- неправильное проведение стимуляции сократительной деятельности матки
- слишком быстрое рождение ребенка
- наличие мекониальных масс в амниотической жидкости
- анатомо-физиологические особенности плода и/или родовых путей матери.
Развитие эмболии околоплодными водами на фоне падения венозного давления, как правило, обусловлено абсолютной или относительной гиповолемией и снижением давления в венах матки при родах ниже 40 мм вод. ст. Такое состояние может возникать на фоне:
- преэклампсии
- сахарного диабета
- различных пороков сердца
- потери тонуса сосудов у многорожавших женщин
- приема мочегонных препаратов
- нерационального использования антигипертензивных или сосудорасширяющих средств.

Высокий риск эмболии околоплодными водами всегда связан с непосредственной травмой амниотического мешка и нарушением целостности кровеносных сосудов матки. В большинстве случаев данный механизм развития ЭОВ обусловлен:
Патогенез
Патогенез клинических симптомов при эмболии околоплодными водами основывается на попадании в систему кровообращения матери вместе с амниотической жидкостью простагландинов, цитокинов, гистамина и других эйкозаноидов. Они вызывают анафилактоидную реакцию с развитием спазма легочных сосудов, нарушением системы свертываемости крови и механическим блоком в микроциркуляторном русле легких.
Классификация
В зависимости от превалирования тех или иных симптомов эмболии околоплодными водами выделяют следующие формы патологии:
- Коллаптоидная

- Судорожная. Основное проявление данной формы эмболии околоплодными водами – генерализованный судорожный синдром.
- Геморрагическая. Обусловлена смещением системы гемостаза в сторону гипокоагуляции. Основные признаки: профузные кровотечения из носа, рта, влагалища, мест пункции и постановки катетеров.
- Отечная. Клинический вариант эмболии околоплодными водами, проявляющийся отеком легочной ткани, который, в свою очередь, вызывает острую дыхательную недостаточность.
- Молниеносная. Наиболее опасная форма эмболии околоплодными водами, характеризующаяся стремительным развитием и полиорганной недостаточностью.
Симптомы эмболии околоплодными водами
Сценарий развития анафилактоидного синдрома беременных определяется тяжестью эмболии и ведущим синдромом (коллапсом, судорогами, кровотечениями, отеком легких). Возможно как относительно легкое течение, так и молниеносные формы, быстро заканчивающиеся остановкой сердца.
Данные реакции при эмболии околоплодными водами проявляются внезапным возникновением общего возбуждения и страха, озноба и повышения температуры тела, выраженной одышки инспираторного или смешанного характера, кашля, «обвала» АД, повышения ЧСС и ЧД. Также наблюдаются боли в области сердца, тошнота, рвота, тонико-клонические судороги, набухание и пульсация шейных вен, генерализованный цианоз и побледнение («мраморность кожи»), профузные кровотечения различной локализации. В зависимости от клинической формы эмболии околоплодными водами могут превалировать те или иные ее проявления.
Диагностика
Диагностика при эмболии околоплодными водами включает в себя сбор анамнестических данных и жалоб во время родов, физикальный осмотр, лабораторные и инструментальные исследования. Более высокий риск развития ЭОВ наблюдается у женщин, имеющих в анамнезе операции на половых органах, частые гинекологические патологии, большое количество родов, в особенности – с осложнениями.
- Оценка объективного статуса. Жалобы, которые предъявляет беременная, во многом зависят от клинической формы эмболии околоплодными водами. Физикальное обследование включает в себя оценку ЧСС, ЧД и АД, а также выявление симптомов ЭОВ, после которого при необходимости может проводиться осмотр шейки матки и ее пальпация.
- Анализы. Программа лабораторных тестов у женщин с признаками эмболии околоплодными водами включает в себя ОАК (уровень тромбоцитов, эритроцитов, показатели гемоглобина и гематокрита), коагулограмма (Д-димер, уровень фибриногена, свертываемость крови и АЧТВ), биохимическое исследование (рН крови, электролиты).
- Инструментальная диагностика. Из инструментальных методов исследования при эмболии околоплодными водами используется ЭКГ, на которой выявляются признаки ишемии миокарда и синусовая тахикардия, а также рентгенография ОГК, позволяющая определить наличие интерстициального отека легких сливного характера в виде «бабочки» и увеличение правых отделов сердца.
 При наличии центрального венозного доступа проводится мониторинг ЦВД.
При наличии центрального венозного доступа проводится мониторинг ЦВД.
Лечение эмболии околоплодными водами
Терапевтические меры при эмболии околоплодными водами направлены на купирование анафилактоидной реакции, кардиопульмонального шока и предотвращение развития критических нарушений системы гемостаза.
- Оксигенация. В первую очередь женщина обеспечивается подачей увлажненного кислорода или переводится на ИВЛ.
- Фармакологическая коррекция. Далее вводятся высокие дозы глюкокортикостероидов (преднизолон или гидрокортизон), восполняется ОЦК при помощи большого объема кровозамещающих жидкостей (сбалансированные коллоиды и кристаллоиды). Для коррекции ацидоза используется бикарбонат натрия. При выраженной гипотензии на фоне эмболии околоплодными водами препаратами выбора являются симпатомиметики (эфедрин), при необходимости могут применяться допамин или добутамин. Для устранения геморрагического синдрома вводятся ингибиторы фибринолиза (транексамовая кислота), концентраты антитромбина, протромбина и препараты крови.

- Родоразрешение. Тактика родовспоможения при эмболии околоплодными водами зависит от результатов лечения. Если терапевтические меры были эффективными, и состояние женщины удалось стабилизировать, родоразрешение осуществляется через родовые пути. При развитии осложнений эмболии околоплодными водами или отсутствии эффекта от консервативного лечения показано немедленное проведение кесарева сечения. При массивных маточных кровотечениях, которые не удается остановить, выполняется экстирпация матки.
Прогноз и профилактика
Исход при эмболии околоплодными водами зависит от общей тяжести состояния женщины, скорости развития симптомов и эффективности проводимых терапевтических мероприятий. В большинстве случаев прогноз неблагоприятный как для матери, так и для ребенка. Профилактика эмболии околоплодными водами подразумевает раннюю диагностику и лечение состояний, которые потенциально могут привести к ЭОВ: преэклампсии и эклампсии, фетоплацентарной недостаточности.
Необходимо купирование гипертонуса матки по время беременности, соблюдение доз назначенных лечащим акушером-гинекологом препаратов, рациональный выбор метода родоразрешения. Также к превентивным мерам относятся планирование беременности, своевременная постановка на учет в женской консультации и ее регулярное посещение с прохождением всех диагностических исследований, выполнение специальной ЛФК для беременных, исключение интенсивных психоэмоциональных нагрузок.
Реферат — Эмболия околоплодными водами: причины, клиника, диагностика,терапия.
Эмболия околоплодными водами легочной артерии и ее ветвей является крайне тяжелой акушерской патологией, которая может стать причиной внезапной смерти рожениц, родильниц, реже беременных.
Пути проникновения околоплодных вод в кровоток матери различны. При разрыве плодных оболочек околоплодные воды могут проникать в сосудистое русло матери через венозные сосуды тела и шейки матки.
Проникновение амниотических вод во вскрывшиеся венозные сосуды матери происходит за счет повышения гидростатического давления в матке или за счет снижения давления в венозной сети матки.
Повышение амниотического давления отмечается при многоплодии, многоводии, дискоординированной или чрезмерной родовой деятельности, быстрых и стремительных родах, при запоздалом вскрытии плодного пузыря, чрезмерном использовании родостимулирующих лекарственных средств.
Во время нормальных или затяжных родов возможна эмболия околоплодными водами через разрывы или трещины шейки матки при нормальном или несколько сниженном внутриматочном давлении.
Это происходит по причине того, что во время беременности шейка матки трансформируется, при этом изменяется местная гемодинамика (понижается сосудистое давление).
Возможно проникновение околоплодных вод через дефекты плаценты, через межворсинчатое пространство при преждевременной отслойке нормально расположенной плаценты.
К предрасполагающим факторам относят бурную родовую деятельность, чрезмерную стимуляцию сократительной деятельности матки окситоцином, наличие мекония в околоплодных водах.
Клиническая картина эмболии околоплодными водами начинается остро. Состояние женщины резко ухудшается, появляются удушье, кашель, боль за грудиной, слабость, чувство страха. Внезапно повышается температура тела до 39° и выше, появляется сильный озноб. Возможны тонические или клонические судороги, рвота.
Симптомы развиваются очень быстро. Лицо цианотично, быстро снижается артериальное давление, пульс частый, слабого наполнения и напряжения, наступает коллапс, потеря сознания.
При более медленном поступлении амниотической жидкости в кровь на первый план выступают симптомы, связанные с развитием ДВС-синдрома.
Для диагностики особенно сложны нерезко выраженные случаи эмболии в виде кашля, внезапных болей за грудиной по типу острой коронарной недостаточности, кратковременной одышки, судорог без изменения артериального давления, рвоты.
Различные варианты клинической картины требуют дифференциальной диагностики с эклампсией, тромбоэмболией легочной артерии, разрывом матки, септическим шоком, приступом бронхиальной астмы.
Для постановки правильного диагноза используют дополнительные методы исследования — ЭКГ, рентгеноскопию грудной клетки, анализ коагулограммы, газового состава крови.
Экстренная терапия начинается с внутривенного введения 1 мл 2 % раствора промедола, 2 мл 1 % раствора димедрола и 2 мл реланиума. Одновременно необходимо начать подачу кислорода.
Параллельно проводят инфузионную терапию, вводят глюкокортикостероиды, сердечные гликозиды, воздействуют на свертывающую систему крови в соответствии с фазой ДВС-синдрома.
После проведения неотложных мероприятий необходимо быстро и бережно родоразрешить женщину. При развитии ДВС-синдрома и при маточном кровотечении показана экстирпация матки.
Лекция — Эмболия околоплодными водами: причины, клиника, диагностика,терапия.
Эмболия околоплодными водами легочной артерии и ее ветвей является крайне тяжелой акушерской патологией, которая может стать причиной внезапной смерти рожениц, родильниц, реже беременных.
Пути проникновения околоплодных вод в кровоток матери различны. При разрыве плодных оболочек околоплодные воды могут проникать в сосудистое русло матери через венозные сосуды тела и шейки матки. Это происходит при разрывах матки, во время операций кесарева сечения или ручного отделения плотно прикрепленной плаценты, при разрывах шейки матки, предлежании и преждевременной отслойке нормально расположенной плаценты.
Проникновение амниотических вод во вскрывшиеся венозные сосуды матери происходит за счет повышения гидростатического давления в матке или за счет снижения давления в венозной сети матки.
Повышение амниотического давления отмечается при многоплодии, многоводии, дискоординированной или чрезмерной родовой деятельности, быстрых и стремительных родах, при запоздалом вскрытии плодного пузыря, чрезмерном использовании родостимулирующих лекарственных средств.
Во время нормальных или затяжных родов возможна эмболия околоплодными водами через разрывы или трещины шейки матки при нормальном или несколько сниженном внутриматочном давлении.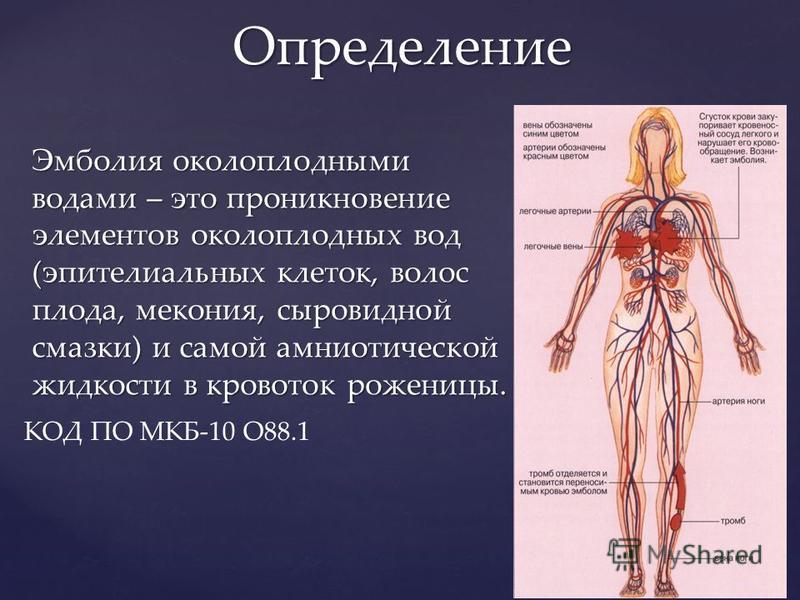
Это происходит по причине того, что во время беременности шейка матки трансформируется, при этом изменяется местная гемодинамика (понижается сосудистое давление).
Возможно проникновение околоплодных вод через дефекты плаценты, через межворсинчатое пространство при преждевременной отслойке нормально расположенной плаценты.
К предрасполагающим факторам относят бурную родовую деятельность, чрезмерную стимуляцию сократительной деятельности матки окситоцином, наличие мекония в околоплодных водах.
Клиническая картина эмболии околоплодными водами начинается остро. Состояние женщины резко ухудшается, появляются удушье, кашель, боль за грудиной, слабость, чувство страха. Внезапно повышается температура тела до 39° и выше, появляется сильный озноб. Возможны тонические или клонические судороги, рвота.
Симптомы развиваются очень быстро. Лицо цианотично, быстро снижается артериальное давление, пульс частый, слабого наполнения и напряжения, наступает коллапс, потеря сознания.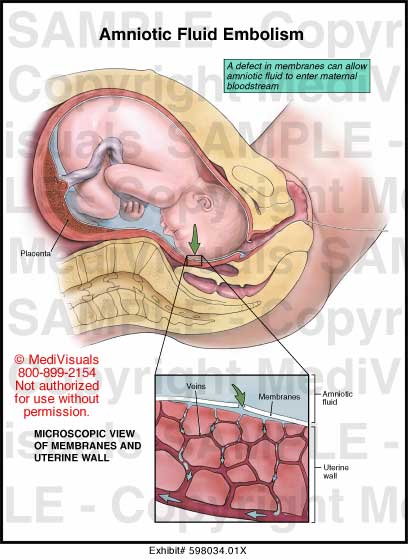
При более медленном поступлении амниотической жидкости в кровь на первый план выступают симптомы, связанные с развитием ДВС-синдрома.
Для диагностики особенно сложны нерезко выраженные случаи эмболии в виде кашля, внезапных болей за грудиной по типу острой коронарной недостаточности, кратковременной одышки, судорог без изменения артериального давления, рвоты.
Различные варианты клинической картины требуют дифференциальной диагностики с эклампсией, тромбоэмболией легочной артерии, разрывом матки, септическим шоком, приступом бронхиальной астмы.
Для постановки правильного диагноза используют дополнительные методы исследования — ЭКГ, рентгеноскопию грудной клетки, анализ коагулограммы, газового состава крови.
Экстренная терапия начинается с внутривенного введения 1 мл 2 % раствора промедола, 2 мл 1 % раствора димедрола и 2 мл реланиума. Одновременно необходимо начать подачу кислорода.
Параллельно проводят инфузионную терапию, вводят глюкокортикостероиды, сердечные гликозиды, воздействуют на свертывающую систему крови в соответствии с фазой ДВС-синдрома.
После проведения неотложных мероприятий необходимо быстро и бережно родоразрешить женщину. При развитии ДВС-синдрома и при маточном кровотечении показана экстирпация матки.
Эмболия околоплодными водами > Клинические протоколы МЗ РК
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных диагностических мероприятий:
1. R-графия легких
2. Эритроциты, гемоглобин, гематокрит
3. Тромбоциты
4. Фибриноген
5. Время свертывания
6. Паракоагуляционные тесты
7. ЭКГ
8. КОС и газы крови
9. ЦВД
Диагностические критерии:
Необходимые условия для попадания околоплодных вод в кровоток:
— превышение амниотического давления над венозным;
— зияние сосудов матки.
Факторы, повышающие риск ЭОВ:
— Многорожавшая
— Околоплодные воды, загрязненные меконием
— Разрывы шейки матки
— Внутриутробная гибель плода
— Очень сильные тетанические схватки
— Стремительные или затяжные роды
— Амниоцентез
— Приращение плаценты
— Преждевременная отслойка нормально расположенной плаценты
— Многоводие
— Разрыв матки
— Хориоамнионит
— Макросомия
— Плод мужского пола
— Операция кесарева сечения
Причины амниотической эмболии при кесаревом сечении:
— избыточное давление на матку извне;
— попытки извлечь плод через разрез несоответствующий размерам головки плода;
— выраженная гиповолемия.
Возможные пути проникновения околоплодных вод в кровоток матери:
1. Трансплацентарный путь (через дефект плаценты).
2. Через сосуды шейки матки.
3. Через межворсинчатое пространство – при преждевременной отслойке нормально расположенной плаценты.
4. Через сосуды любого участка матки – при кесаревом сечении, нарушении, нарушении целостности плодных оболочек, разрывах матки.
Клиника ЭОВ представлена двумя основными синдромами:
— кардиопульмональным шоком
— и коагулопатией (синдромом ДВС).
Клиническая картина амниотической эмболии во время родов и после родов:
внезапное начало— бледность кожных покровов
— беспокойство и страх, иногда боли в грудной клетке
— нарушение дыхания
— возникает потрясающий озноб
— гипертермия до 39 градусов и более
— нарастает цианоз кожи лица и конечностей
— резко затруднено дыхание, может развиться возбуждение с тонико – клоническими судорогами, и затем, почти сразу, может наступить кома.
— после вышеуказанной клинической симптоматики, возможно, ожидать профузное кровотечение из половых путей.
Клинические проявления амниотической эмболии при кесаревом сечении в условиях общей анестезии:
— внезапное трудно объяснимое снижение насыщения крови кислородом (SpO2) до 85%, а в тяжелых случаях до 70%, во время или сразу после извлечения плода;
— при ИВЛ повышение давления в дыхательном контуре до 35 – 40 и более см вод.ст.;
— при аускультации возможны хрипы в легких;
— развивается развернутый ДВС синдром.
Клинические проявления амниотической эмболии при кесаревом сечении в условиях регионарной анестезии:
— внезапное возбуждение пациентки во время или сразу после извлечения плода;
— снижение насыщения крови кислородом (SpO2) до 85%, а в тяжелых случаях до 70%, во время или сразу после извлечения плода;
— затрудненное дыхание;
— при аускультации возможны хрипы в легких;
— развивается развернутый ДВС синдром.
Эмболия околоплодными водами | Компетентно о здоровье на iLive
Как развивается эмболия околоплодными водами?
В норме у беременной женщины в матке содержится 0,5-1,5 л околоплодных вод — суспензии, содержащей как продукты жизнедеятельности плода, так и продукты секреции плацентарных оболочек. Из частиц, составляющих суспензию, наиболее значимы лануго, родовая смазка плода, чешуйки эпителия, меконий с желчными пигментами, кишечный муцин и трофобласты. В жидкой части околоплодные воды содержат огромное количество биологически активных веществ арахидоновую кислоту, тромбопластин, тканевой фактор III, лейкотриены С4 и D4, интерлейкин-1, ФНО, тромбоксан А2, фосфолипазу А2, простагладины, профибринолизин, эндотелии, коллаген и сурфактант. Помимо этого в околоплодных водах содержатся белки, жиры, липиды, углеводы, калий, кальций, натрий, микроэлементы, мочевина, гормоны (фолликулин, гонадотропный гормон и др ), лизоцим, молочная и другие кислоты, ферменты, вещества, способствующие сокращению матки (окситоцин), групповые антитела, соответствующие группе крови плода.
Эмболия околоплодными водами может проявить себя даже в раннем послеродовом периоде — сообщалось о развитии клинической картины ЭОВ через 10-20 и даже 32 ч после родов и операции кесарева сечения. Кроме того, тяжесть клинических проявлений часто не соответствует степени поражения легочных сосудов. В связи с этим в настоящее время принято связывать клинические проявления ЭОВ с развитием тяжёлой системной анафилактоидной реакции в ответ на поступление в материнский кровоток биологически активных веществ амниотической жидкости. При внутриутробной инфекции плода околоплодные воды могут быть инфицированы, и их попадание в материнский кровоток вызывает еще более тяжёлую анафилактоидную реакцию. Попадание в материнский кровоток с околоплодными водами значительного количества биологически активных веществ, перечисленных выше, вызывает дегрануляцию тучных клеток, высвобождение гистамина и эндотелина, лейкотриенов и ФИО. Столь мощный медиаторный взрыв может привести к развитию бронхоспазма, спазма лёгочных сосудов, правожелудочковой, а затем и левожелудочковой недостаточности с развитием ОЛ и шока смешанного генеза. В особо тяжелых случаях описана остановка сердца.
Через 1-1,5 ч после эпизода ЭОВ возникает острая коагулопатия с массивным кровотечением, что связано с поступлением тканевого тромбопластина и действием медиаторов. Клиническая картина протекает по сценарию молниеносного ДВС-синдрома с плохо купируемым массивным кровотечением, сопровождаемым критической кровопотерей с исходом в синдром ПОН.
Как сказано выше, эмболию околоплодными водами характеризуют массивные профузные кровотечения, обусловленные тяжёлым ДВС-синдромом с гипофибриногенемией, тромбоцитопенией, резко активированным фибринолизом и истощением всех факторов свертывания крови. В развитии тромбогеморрагических осложнений, связанных с ЭОВ, основную роль играют количество околоплодных вод, попавшее в материнский кровоток, а также степень иммунной реактивности женщины.
ДВС-синдром при эмболии околоплодными водами протекает в две стадии — весьма кратковременной стадии гиперкоагуляции и стадии гипокоагуляции и дефицита факторов свёртывания. Фаза гиперкоагуляции обусловлена попаданием в материнский кровоток вместе с околоплодными водами тканевого тромбопластина, который запускает внешний механизм коагуляции. Эта фаза носит стремительный характер и лабораторно выявляется крайне редко.
Наряду с тромбопластином околоплодные воды содержат фактор, ускоряющий ретракцию сгустка крови. В результате потребления наступает истощение факторов свёртывания и тромбоцитопения. Возникает активация фибринолиза и процесс переходит в стадию гипокоагуляции, характеризуемую массивными кровотечениями. По разным данным, гибель плода при выраженной клинической картине ЭОВ в родах составляет от 50 до 80% Из них большая часть (90%) погибает интранатально. Основная причина гибели — внутриутробная асфиксия.
Нередко ДВС-синдром может оказаться единственным проявлением ЭОВ. Необходимо заметить, что в основе большинства необъяснимых кровотечений в акушерстве, по-видимому, лежит этиологический фактор ЭОВ.
что это, чем опасно, как лечить
Эмболия околоплодными водами (ЭОВ) – патологическое состояние в период беременности, которое сопровождается с попаданием амниотической жидкости в системный кровоток женщины. Потребуется неотложное лечение, поскольку патология опасна для жизни малыша и матери. Подробно узнать состоянии можно в данной статье.
Что это за патология
В акушерстве ЭОВ связана с проникновением околоплодных вод в кровоток женщины. Опасность состоит в негативной реакции организма на компоненты данной жидкости.
Амниотическая жидкость состоит клеток эпидермиса, первородной смазки плода, мекония. Они провоцируют проявление анафилактоидного синдрома.
Клиническая картина имеет сходство с анафилактическим шоком и связана с нарушением коагуляции крови. При диагностике используют различные методики.
Причины
У пациентки наблюдается разная этиология нарушения. Основные причины развития опасного синдрома:
- повышение внутриматочного давления;
- снижение кровяного давления в сосудах матки;
- повреждение сосудов амниотического мешка.
В процессе родовой деятельности может возникать при:
Причины эмболии околоплодными водами при снижении венозного давления провоцирует:
Этиология опасного синдрома определяет врач после полноценной диагностики. Симптомы острой фазы ярко выражены, поэтому установить диагноз не сложно.
Виды
Патология имеет несколько видов. Понять, что это такое эмболия околоплодными водами поможет краткое описание каждого:
- Коллаптоидная. Сопровождается сильным кардиальным шоком.
- Судорожная. Характерным признаком является генерализованный судорожный симптом.
- Геморрагическая. Развивается гипокоагуляция (снижается способность крови сворачиваться). Характерными являются кровотечения из носа, рта, влагалища.
- Отечная. Возникает отек легких, на фоне которого появляется острая дыхательная недостаточность.
- Молниеносная. Самый сложный вид, при котором наблюдается стремительное развитие, полиорганная недостаточность. Часто приводит к внутриутробной гибели плода.
Любая форма патологии является угрожающей для жизни плода и матери. При отсутствии вовремя оказанной врачебной помощи, развивается стремительно в течение короткого времени.
Симптомы
Амниотическая эмболия сопровождается разными симптомами, скоростью и тяжестью их развития. Клиническая картина зависит от реакции организм на чужеродные компоненты. Характерные признаки:
При таких проявлениях женщине понадобится неотложная врачебная помощь.
Чем оно опасно
Если околоплодные воды попали в кровь, опасность проявляется в следующем:
- гибель плода;
- острая почечная недостаточность;
- нарушение кровообращения в головном мозге;
- возникновение процессов гноения.
Развитие осложнений в основном связно с отсутствием своевременного лечения.
Диагностика
В первую очередь врач проводит физикальный осмотр, изучает анамнез, выслушивает и фиксирует жалобы пациентки. После этого назначает лабораторные, инструментальные исследования:
- Анализы. Учитывают уровень тромбоцитов, гемоглобина, эритроцитов при получении анализа крови. Коагулограмма нужна для определения показателей свертываемости крови.
- Инструментальные методы. ЭКГ – определяет наличие ишемии, синусовой тахикардии. ОКГ для определения отека легких, увеличения размеров сердца.
Результаты обследования показывают вид эмболии. По показателям назначают подходящий протокол терапии.
Как лечить
Лечение необходимо для устранения анафилактоидной реакции, кардиального шока и предотвращения опасных осложнений. Терапия состоит из:
- оксигенации – подачи увлажненного воздуха в организм женщины;
- медикаментозного лечения – ведение глюкокортикостероидов в высоких дозах, кровозамещающих жидкостей.
При выраженной гипотензии используют симпатомиметики. Ингибиторы фибринолиза понадобятся для купирования геморрагического синдрома.
При эмболии амниотической жидкостью родоразрешение зависит от эффективности лечения. Если оно было проведено вовремя, а опасное состояние удалось устранить и нормализировать, роды могут проходить естественным путем.
При развитии патологического состояния и отсутствия терапии, проводится экстренное кесарево сечение. От своевременного и правильного лечения зависит жизнь малыша и матери.
Прогнозы и профилактика
Прогноз зависит от вида заболевания, состояния беременной, тяжести и стремительности развития течения патологии. На это влияет своевременная врачебная помощь.
Резкое развитие острого патологического состояния имеет неблагоприятный прогноз. Это связано со стремительным ухудшением самочувствия женщины.
Основная профилактика – своевременная диагностика и правильная терапия. Это поможет снизить риск появления преэклампсии, фетоплацентарной недостаточности. В период гестации важно контролировать гипертонус матки и вовремя его купировать.
Залог успешной беременности начинается с контроля на ранних сроках. Будущим мамам рекомендовано вовремя стать на учет в женскую консультацию, регулярно проходить плановые осмотры, своевременно сдавать анализы и обследования. Важно следить за физическим и психоэмоциональным состоянием.
Часто женщины интересуются, как околоплодные воды могут попасть в кровь. Развитие нарушения может быть связано с воздействием разных факторов. Поэтому при ухудшении самочувствия необходимо немедленно обратиться к врачу.
Своевременная терапия повышает шансы благоприятного исхода. Патологическое состояние опасно для жизни плода и беременной. Поэтому следует постоянно контролировать течение беременности, чтобы избежать тяжелых последствий.
Современные концепции иммунологии и диагностики эмболии околоплодными водами
Эмболия околоплодными водами (AFE) является одной из основных причин материнской смертности и заболеваемости в развитых странах. Современные представления о патофизиологии сместились от эмболии к материнскому иммунному ответу на плод. На сегодняшний день изучены два иммунологических механизма. Анафилаксия кажется сомнительной, в то время как имеющиеся данные подтверждают роль активации комплемента. Поскольку механизм еще предстоит выяснить, AFE остается клиническим диагнозом.Диагноз ставится на основании одного или нескольких из четырех ключевых признаков / симптомов: сердечно-сосудистый коллапс, респираторный дистресс, коагулопатия и / или кома / судороги. Единственный лабораторный тест, который надежно подтверждает диагноз, — это обнаружение материала плода в малом круге кровообращения матери при вскрытии. Возможно, самая неотразимая загадка, связанная с AFE, заключается не в том, почему страдает одна из 20 000 рожениц, а в том, как подавляющее большинство женщин могут переносить чужеродное антигенное присутствие своего плода как в матке, так и в кровообращении?
1.Введение
При первом описании в первой половине 20-го века эмболия околоплодными водами считалась результатом физического обструкции легочного кровотока матери плодным материалом, содержащимся в околоплодных водах [1, 2]. В первоначальных случаях, описанных при вскрытии, в легочных сосудах был обнаружен обильный материал плода. Заболевание встречается редко, с частотой от одного на 600 до одного на 80 000, возможно, потому, что не существует установленных лабораторных маркеров диагностики, подходящих как для выживших, так и для погибших [3, 4].AFE является одной из основных причин материнской смертности в США и вызывает примерно 10% всех случаев материнской смертности в развитых странах [5–7]. Возможно, не меньшее беспокойство вызывает значительная материнская заболеваемость, которая приводит к выживанию. Из 48 выживших британцев у четырех были неврологические травмы, у двух — тромботические осложнения, у одного — почечная недостаточность, а у другого — сепсис [8]. 94% поступили в отделение интенсивной терапии. В австралийском исследовании трое из тринадцати выживших перенесли инфаркт головного мозга [9]. Заболеваемость и смертность плода также значительны.В британском реестре среди пятнадцати женщин, умерших от AFE, одиннадцать их детей также умерли, а одна из выживших страдала гипоксической ишемической энцефалопатией [7]. Среди 31 выжившей женщины с известными исходами новорожденных девять новорожденных умерли или получили серьезные травмы. Несмотря на то, что это редкое осложнение беременности, высокий уровень травм как для матери, так и для новорожденного является убедительным аргументом в пользу лучшего понимания механизма заболевания.
В то время как «эмболия» содержится в названии болезни как в его оригинальном испанском, так и в английском описаниях, существует ряд противоречивых клинических наблюдений относительно AFE, которые ставят под сомнение этот механизм заболевания [1, 2].Во-первых, механическая обструкция легочного кровотока достоверно не выявляется при AFE [10]. Во-вторых, клинические проявления, характерные для AFE, коагулопатии, респираторного дистресс-синдрома взрослых и неврологических симптомов, не типичны для легочной эмболии. Возможно, в результате наблюдатели начали размышлять о возможной роли иммунного механизма еще в 1950 году [11]. Тем не менее, поскольку болезнь появляется редко, внезапно и непредсказуемо, получение соответствующих доказательств у людей оказалось необычно трудным.К сожалению, исследования на животных не дали ничего нового, кроме предположения, что на моделях на животных мало что можно узнать. Заболевание было вызвано у животных (кроликов и собак) при внутрисосудистой инъекции гетерологичных (человеческих) околоплодных вод, загрязненных меконием [2]. В частности, аутологичные околоплодные воды, введенные в материнский кровоток у обезьян, кажутся полностью безвредными [12, 13].
2. Анафилаксия
Первое конкретное предположение об анафилаксии как механизме AFE было сделано Attwood в 1956 году [14].Бенсон и Линдбург предположили, что эту гипотезу можно проверить на людях путем тестирования женщин, остро больных с AFE, на триптазу сыворотки [15]. Триптаза, сериновая протеаза с периодом полужизни в несколько часов, высвобождается тучными клетками вместе с гистамином, когда они дегранулируют в ответ на сшивание IgE на поверхности клетки в присутствии антигена. Хотя конкретная функция триптазы при анафилаксии неизвестна, с периодом полураспада гистамина в часах, а не в минутах, этот белок оказался полезным при диагностике анафилаксии.Гистамин в моче также используется для диагностики анафилаксии, поскольку небольшой процент гистамина выводится с мочой в неметаболизированном виде [16].
При рассмотрении роли дегрануляции тучных клеток в механизме эмболии околоплодными водами серологические данные следует рассматривать отдельно от гистологических данных, поскольку в обоих случаях доказательства несколько неоднозначны. Тестирование триптазы сыворотки в AFE указывает на роль AFE, в то время как окрашивание триптазой в легочной гистологии при вскрытии дает более детальную картину.
В 2001 году было опубликовано исследование девяти женщин с эмболией околоплодными водами, в котором искали конкретные доказательства анафилаксии [17]. У семи из девяти пациентов сыворотка хранилась в рамках японского национального проекта по надзору за материнской смертностью, в то время как два пациента были выжившими американцами, включенными в протокол, специально разработанный для сбора образцов острой фазы у пациентов с ОЯ. Пять пациентов дали отрицательный результат на триптазу сыворотки, один — на гистамин в моче и один — на оба.Ни у одного из пациентов не было положительных результатов ни на триптазу сыворотки, ни на гистамин в моче.
Со времени этого исследования сообщалось о повышенных уровнях триптазы в сыворотке крови в случаях летального исхода эмболии околоплодными водами. В трех таких отчетах уровни триптазы в сыворотке были повышены лишь незначительно, что вызывает серьезные вопросы относительно предположения, что анафилаксия отражает лежащий в основе механизм [18–20]. В четвертом случае AFE авторы также изучили посмертные уровни триптазы в сыворотке крови у небеременных, не связанных с AFE, таких как тромбоэмболия легочной артерии и дорожно-транспортные происшествия [21].В то время как уровень триптазы в сыворотке в случае AFE был в шесть раз выше верхнего уровня нормы через 17 часов после смерти, в одном подтвержденном случае анафилаксии уровень триптазы был более чем в 60 раз выше нормы, через 24 часа после смерти. Наконец, уровни триптазы в пятом выжившем случае AFE были нормальными [22]. Незначительное повышение сывороточного уровня при фатальных случаях AFE ниже, чем обычно наблюдается для посмертных значений, наблюдаемых при анафилаксии, и не поддерживает гипотезу о том, что дегрануляция тучных клеток играет центральную роль в патофизиологии эмболии околоплодными водами.
Учитывая, что 100% из 6 пациентов с AFE дали отрицательный результат на триптазу в наибольшей на сегодняшний день серии исследований, лучшее, что можно сказать о триптазе сыворотки при AFE, — это то, что она имеет очень низкую чувствительность [17]. Однако есть возражения и против специфики теста. Если триптаза не будет измерена как у нормальных рожениц, так и у смертельно больных акушерских пациентов с другими заболеваниями, кроме AFE, специфичность триптазы останется неизвестной. Возможно, что уровень триптазы повышен в определенных акушерских популяциях без AFE.В настоящее время сывороточная триптаза при AFE может рассматриваться только как инструмент исследования с нормальным и повышенным уровнями, не подтверждающими и не исключающими диагноз.
Данные по легочной гистологии матери более сложны в отношении роли анафилаксии в AFE. Два исследования итальянских патологов действительно обнаружили доказательства дегрануляции тучных клеток в легочной сосудистой сети матери. В первом исследовании проводился подсчет тучных клеток на фиксированную площадь с использованием иммуногистохимического окрашивания на триптазу [23].Исследователи сравнили шесть смертельных случаев AFE с шестью смертельными случаями от анафилактики, пятью случаями смерти в результате травматической беременности и шестью смертельными случаями от травм у небеременных женщин. Примечательно, что у группы AFE была более высокая плотность тучных клеток, чем у анафилактической группы, и намного выше, чем у двух других контрольных групп. Во втором исследовании, использующем аналогичный подход, исследователи смогли показать значительное увеличение внеклеточной триптазы, соответствующее дегрануляции тучных клеток, у восьми женщин в группе AFE по сравнению с шестью беременными женщинами, скончавшимися от травмы [20].В одном отчете о случае AFE не было обнаружено иммуногистохимических доказательств дегрануляции тучных клеток при вскрытии, но пациент, о котором идет речь, умер через несколько минут после удара головой в автомобильной аварии и явно не имел AFE [24].
Таким образом, имеющиеся данные свидетельствуют о том, что дегрануляция тучных клеток действительно происходит в легких в случаях летального исхода AFE и не происходит в других случаях смертельной беременности. Это трудно совместить с общим отсутствием значительного повышения уровня циркулирующей триптазы при AFE.Эти наблюдения вместе предполагают, что вовлечение легочных тучных клеток в летальных случаях может быть вторичным процессом, а не обязательно первичным механизмом AFE. Эта возможность тем более интригующая, что дегрануляция тучных клеток может происходить в результате активации комплемента [25]. При рассмотрении механизма заболевания свидетельство высвобождения триптазы не может рассматриваться как доказательство основной роли анафилаксии без одновременного измерения комплемента и подтверждения того, что активации не произошло.
Наконец, прежде чем оставить тему анафилаксии и эмболии околоплодными водами, следует рассмотреть предложение переименовать заболевание в «анафилактоидный синдром беременности» [26, 27]. Хотя термин «анафилаксия» может в общих чертах относиться к клиническим симптомам, возникающим в результате любого процесса, приводящего к дегрануляции тучных клеток, он чаще используется для обозначения процесса, опосредованного связыванием IgE с антигеном [28]. Напротив, обычное использование термина «анафилактоид» используется специально для обозначения неиммунно-опосредованной дегрануляции тучных клеток, не связанной с IgE [29].Наиболее известным примером «анафилактоидной» реакции у людей является высвобождение гистамина, которое иногда наблюдается у людей, впервые подвергшихся внутривенному рентгеновскому контрастированию [30]. Предположение, лежащее в основе анафилактоидных реакций, потенциально столь же фатальных, как IgE-опосредованная анафилаксия, состоит в том, что они не являются результатом запомненной антигенной реакции, поскольку ранее не было воздействия. Помимо того факта, что дегрануляция тучных клеток ни в коем случае не является доказанным механизмом AFE, является идея о том, что все предположения относительно механизма заболевания основаны на каком-то типе материнского иммунного ответа на фетальный антиген [31].Не было предложено никакого механизма для AFE, при котором тучные клетки дегранулируют в отсутствие взаимодействия антитело-антиген. Хотя «анафилактоидный синдром беременности» не получил широкого признания, имеющиеся данные не поддерживают изменение названия AFE, и от этого термина следует отказаться.
3. Активация комплемента в AFE
Частота респираторного дистресс-синдрома взрослых как следствие AFE была предложена Jacob и Hammershmidt в 1982 г. [32], а также Hammershmidt et al.[33], что активация комплемента может играть роль в патофизиологии заболевания. Первая серия, в которой уровни комплемента в сыворотке оценивались у пациентов с AFE, показала, что и C3, и C4 были значительно снижены у всех восьми пациентов с AFE, у которых можно было провести измерения [17]. Контрольная группа из двадцати трех нормальных рожениц имела уровни комплемента в нормальном диапазоне. Кроме того, в отчете о возможном «легком» AFE, при котором у пациента была преходящая одышка, сердцебиение и лабораторные доказательства коагулопатии, уровни комплемента также были понижены [34].Однако в отдельной серии пациентов с AFE в Японии средний уровень C3 был низким нормальным (71 мг / дл), тогда как средний уровень C4 был пониженным (13,9 мг / дл) [7]. Не было различий в средствах между теми, кто выжил, и теми, кто умер. Итальянская группа, проводившая гистологические исследования триптазы, также рассматривала активацию комплемента в своей последней статье [20]. Они обнаружили пониженное количество C3a в малом круге кровообращения у восьми пациентов с AFE по сравнению с шестью беременными женщинами, умершими от травмы.Исследователи предположили, что уменьшение легочного C3a согласуется с активацией комплемента. Как отмечалось ранее, были доказательства высвобождения триптазы в тех же гистологических образцах. Возможно, если маловероятно, что активация комплемента могла быть первоначальным иммунным ответом, который затем привел к вторичной дегрануляции тучных клеток.
При серологических и гистологических доказательствах путь комплемента представляется более многообещающим, чем анафилаксия, как возможный механизм заболевания.Однако как диагностический инструмент чувствительность и специфичность плохо охарактеризованы. Как и в случае с триптазой, уровни комплемента в AFE остаются инструментом исследования и не должны использоваться для подтверждения или опровержения клинического диагноза.
При исследовании активации комплемента в AFE следует упомянуть интересную сноску. Похоже, что некоторая степень активации комплемента во время нормальных родов является физиологической и достигает пика в момент рождения. Были проведены два отдельных исследования, в которых были получены серийные уровни комплемента у нормальных рожениц.Первое было проведено в рамках исследования 2001 г., посвященного изучению уровней комплемента и триптазы при AFE [17]. У здоровой контрольной группы из тринадцати американских женщин и девяти японок уровни комплемента были получены при поступлении в больницу во время родов и в первый послеродовой день. Был проведен внутрипарный анализ, и оба C3 и C4 продемонстрировали статистически значимые случаи эмболии околоплодными водами



 При наличии центрального венозного доступа проводится мониторинг ЦВД.
При наличии центрального венозного доступа проводится мониторинг ЦВД.
