Временная баллонная окклюзия общих подвздошных артерий у пациенток с рубцом на матке после кесарева сечения и placenta accreta. Преимущества и возможные осложнения
Цель исследования. Определить эффективность и возможность применения временной баллонной окклюзии общих подвздошных артерий при проведении органосохраняющих операций у пациенток с placenta accreta.
Материал и методы. В ходе ретроспективного исследования проанализированы данные 34 историй родов пациенток с врастанием плаценты в рубец на матке после кесарева сечения. У всех пациенток при родоразрешении проводилась временная баллонная окклюзия общих подвздошных артерий после извлечения плода.
Результаты. Применение современных технологий – временной баллонной окклюзии общих подвздошных артерий и аппаратной реинфузии аутоэритроцитов – позволило выполнить органосохраняющие операции у всех обследованных. Средняя интраоперационная кровопотеря составила 1656±1042 мл, у 20,6% родильниц зафиксирована минимальная кровопотеря 400–700 мл. Осложнения послеоперационного периода наблюдались у 8,8% и не были обусловлены ангиохирургическим вмешательством.
Заключение. Временная баллонная окклюзия общих подвздошных артерий является эффективной методикой снижения кровопотери при родоразрешении пациенток с placenta accretа и рубцом на матке после кесарева сечения, позволяя проводить органосохраняющие операции. Она может быть рекомендована к использованию в стационарах III уровня.
временная баллонная окклюзия общих подвздошных артерий
1. Chantraine F., Braun T., Gonser M., Henrich W., Tutschek B. Prenatal diagnosis of abnormally invasive placenta reduces maternal peripartum hemorrhage and morbidity. Acta Obstet. Gynecol. Scand. 2013; 92(4): 439-44.
2. Timor-Tritsch I.E., Monteagudo A., Cali G., Palacios-Jaraquemada J.M., Maymon R., Arslan A.A. et al. Cesarean scar pregnancy and early placenta accreta share common histology. Ultrasound Obstet. Gynecol. 2014; 43(4): 383-95.
3.
4. Wu S., Kocherginsky M., Hibbard J.U. Abnormal placentation: twenty-year analysis. Am. J. Obstet. Gynecol. 2005; 192(5): 1458-61.
5. Shrivastava V., Nageotte M., Major C., Haydon M., Wing D. Case-control comparison of cesarean hysterectomy with and without prophylactic placement of intravascular balloon catheters for placenta accreta. Am. J. Obstet. Gynecol. 2007; 197(4): 402. e1-5.
6. Wright J.D., Devine P., Shah M., Gaddipati S., Lewin S.N., Simpson L.L. et al. Morbidity and mortality of peripartum hysterectomy. Obstet. Gynecol. 2010; 115(6): 1187-93.
7. O’Brien J.M., Barton J.R., Donaldson E.S. The management of placenta percreta: conservative and operative strategies. Am. J. Obstet. Gynecol. 1996; 175(6): 1632-8.
8. Савельева Г.М., Курцер М.А., Бреслав И.Ю., Панина О.Б., Андреев А.И., Барыкина О.П., Латышкевич О.А. Врастание предлежащей плаценты (placenta accreta) у пациенток с рубцом на матке после кесарева сечения. Клинико-морфологическое сопоставление. Акушерство и гинекология. 2015; 11: 41-5.
9. Silver R.M., Barbour K.D. Placenta accreta spectrum: accreta, increta, and percreta. Obstet. Gynecol. Clin. North Am. 2015; 42(2): 381-402.
10. Латышкевич О.А., Курцер М.А., Савельева Г.М., Бреслав И.Ю., Евтеев В.Б., Платицын И.В., Щербакова Л.Н., Анисимова Н.Б., Аболиц М.А., Панина О.Б. Антенатальная диагностика врастания плаценты у женщин с кесаревым сечением в анамнезе. Вопросы гинекологии, акушерства и перинатологии. 2013; 12(6): 36-41.
11. Kotsuji F., Nishijima K., Kurokawa T. et al. Usefulness of the transverse uterine fundal incision for placenta previa. J. Matern. Fetal Neonatal Med. (Abstracts of the XXII European Congress of Perinatal Medicine. May 26-29, 2010. Granada, Spain) 2010; 23(Suppl. 1): 618.
12. Chandraharan E., Rao S., Belli A.M., Arulkumaran S. The Triple-P procedure as a conservative surgical alternative to peripartum hysterectomy for placenta percreta. Int. J. Gynaecol. Obstet. 2012; 117(2): 191-4.
Int. J. Gynaecol. Obstet. 2012; 117(2): 191-4.
13. Курцер М.А., Бреслав И.Ю., Григорьян А.М., Латышкевич О.А. Опыт использования временной баллонной окклюзии общих подвздошных артерий при органосохраняющих операциях у пациенток с врастанием плаценты. Акушерство и гинекология. 2013; 7: 80-4.
14. Курцер М.А., Бреслав И.Ю., Латышкевич О.А., Лукашина М.В., Штабницкий А.М. Опыт выполнения органосохраняющей операции при placenta accreta у пациентки с бихориальной двойней. Вопросы гинекологии, акушерства и перинатологии. 2015; 14(4): 75-8.
15. Латышкевич О.А. Врастание плаценты у пациенток с рубцом на матке после кесарева сечения. Органосохраняющие операции: дисс. … канд. мед. наук. М.; 2015.
16. ACOG Committee Opinion. Placenta accreta. Number 529, July 2012. American College of Obstetricians and Gynaecologists. Obstet. Gynecol. 2012; 120(1): 207-11.
17. Broekman E.A., Versteeg H., Vos L.D., Dijksterhuis M.G., Papatsonis D.N. Temporary balloon occlusion of the internal iliac arteries to prevent massive hemorrhage during cesarean delivery among patients with placenta previa. Int. J. Gynaecol. Obstet. 2015;128(2): 118-21.
18. Minas V., Gul N., Shaw E., Mwenenchanya S. Prophylactic balloon occlusion of the common iliac arteries for the management of suspected placenta accreta/percreta: conclusions from a short case series. Arch. Gynecol. Obstet. 2015; 291(2): 461-5.
19. Palacios Jaraquemada J.M., Pesaresi M., Nassif J.C., Hermosid S. Anterior placenta percreta: surgical approach, hemostasis and uterine repair. Acta Obstet. Gynecol. Scand. 2004; 83(8): 738-44.
20. D’Souza D.L., Kingdom J.C., Amsalem H., Beecroft J.R., Windrim R.C., Kachura J.R. Conservative management of invasive placenta using combined prophylactic internal iliac artery ballon occlusion and immediate postoperative uterine artery embolization. Can. Assoc. Radiol. J. 2015; 66(2): 179-84.
21. Duan X.H., Wang Y.L., Han X.W., Chen Z.M., Chu Q.J., Wang L.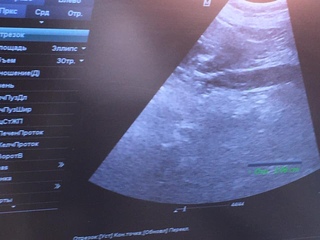 , Hai D.D. Caesarean section combined with temporary aortic balloon occlusion followed by uterine artery embolization for the management of placenta accrerta. Clin. Radiol. 2015; 70(9): 932-7.
, Hai D.D. Caesarean section combined with temporary aortic balloon occlusion followed by uterine artery embolization for the management of placenta accrerta. Clin. Radiol. 2015; 70(9): 932-7.
22. Dubois J., Garel L., Grignon A., Lemay M., Leduc L. Placenta percreta: balloon occlusion and embolization of the internal iliac arteries to reduce intraoperative blood losses. Am. J. Obstet. Gynecol. 1997; 176(3): 723-6.
23. Eller A.G., Bennett M.A., Sharshiner M., Masheter C., Soisson A.P., Dodson M., Silver R.M. Maternal morbidity in cases of placenta accreta by a multidisciplinary care team compared with standard obstetric care. Obstet. Gynecol. 2011; 117(2, Pt 1): 331-7.
24. Dilauro M.D., Dason S., Athreya S. Prophylactic ballon occlusion of internal iliac arteries in women with placenta accreta: literature review and analysis. Clin. Radiol. 2012; 67(6): 515-20.
25. Gagnon J., Boucher L., Kaufman I., Brown R., Moore A. Iliac artery rupture related to balloon insertion for placenta accrete causing maternal hemorrhage and neonatal compromise. Can. J. Anesth. 2013; 60(12): 1212-7.
26. Teixidor Viñas M., Chandraharan E., Moneta M.V., Belli A.M. The role of interventional radiology in reducing haemorrhage and hysterectomy following caesarean section for morbidly adherent placenta. Clin. Radiol. 2014; 69(8): e345-51.
27. Shih J.C., Liu K.L., Shyu M.K. Temporary balloon occlusion of the common iliac artery: new approach to bleeding control during cesarean hysterectomy for placenta percreta. Am. J. Obstet. Gynecol. 2005; 193(5): 1756-8.
28. Matsubara S., Nonaka H., Kobayashi M., Kuwata T., Fujii H. Intrauterine balloon occlusion during caesarean hysterectomy for placenta previa accreta: the internal or common iliac artery? Acta Obstet. Gynecol. Scand. 2014; 93(1): 122-3.
29. Hishikawa K., Koshiyama M., Ueda M., Yamaguchi A., Ukita S., Yagi H., Kakui K. Exchange of intraoperative balloon occlusion of the internal iliac artery for the common iliac artery during cesarean hysterectomy in a patient with placenta percreta. Am. J. Case Rep. 2013; 14: 409-11.
Am. J. Case Rep. 2013; 14: 409-11.
30. Chou M.M., Kung H.F., Hwang J.I., Chen W.C., Tseng J.J. Temporary prophylactic intravascular balloon occlusion of the common iliac arteries before cesarean hysterectomy for controlling operative blood loss in abnormal placentation. Taiwan. J. Obstet. Gynecol. 2015; 54(5): 493-8.
Поступила 20.06.2016
Принята в печать 02.09.2016
Курцер Марк Аркадьевич, член-корреспондент РАН, профессор кафедры акушерства и гинекологии педиатрического факультета РНИМУ им. Н.И. Пирогова Минздрава России. Адрес: 117997, Россия, Москва, ул. Островитянова, д. 1. Телефон: 8 (495) 718-34-72. E-mail:
Бреслав Ирина Юрьевна, к.м.н., докторант кафедры акушерства и гинекологии педиатрического факультета РНИМУ им. Н.И. Пирогова Минздрава России. Адрес: 117997, Россия, Москва, ул. Островитянова, д. 1. Телефон: 8 (495) 718-34-72. E-mail:
Латышкевич Олег Александрович, к.м.н., главный врач ГБУЗ ЦПСиР ДЗ г. Москвы. Адрес: 117209, Россия, Москва, Севастопольский проспект, д. 24а. Телефон: 8 (495) 718-20-70. E-mail:
Григорьян Ашот Михайлович, к.м.н., научный сотрудник отделения рентгенохирургических методов исследования и лечения сердца и сосудов ФГБУ НЦССХ им. А.Н. Бакулева Минздрава России. Адрес: 121552, Россия, Москва, Рублевское шоссе, д. 135. Телефон: 8 (495) 414-77-08. E-mail:
Для цитирования: Курцер М.А., Бреслав И.Ю., Латышкевич О.А., Григорьян А.М. Временная баллонная окклюзия общих подвздошных артерий у пациенток с рубцом на матке после кесарева сечения и placenta accreta. Преимущества и возможные осложнения. Акушерство и гинекология. 2016; 12: 70-5.
Операционный блок | ЦПСиР
Операционный блок Центра планирования семьи и репродукции является современным, высокотехнологичным комплексом по оказанию круглосуточной хирургической помощи пациентам акушерского и гинекологического профиля.
Первым заведующим операционным отделением ЦПСиР была Архипова Людмила Александровна, которая продолжает свою деятельность до настоящего времени, работая акушером-гинекологом в послеродовом отделении.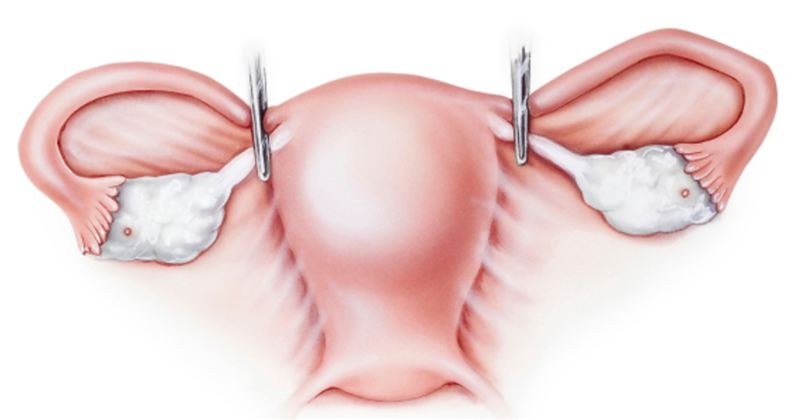
Архипова Людмила Александровна
Первая заведующая отделением
Сейчас возглавляет отделение Константин Олегович Веклич, врач акушер-гинеколог высшей категории, который за 20 лет в ЦПСиР прошел путь от ординатора до руководителя отделения. Старшая операционная сестра высшей категории Ирина Борисовна Чмелёва. В оперблоке работают 13 высококвалифицированных опытных операционных медицинских сестёр.
| Веклич Константин Олегович Заведующий отделением | Чмелева Ирина Борисовна Старшая медицинская сестра |
В состав операционного блока входят 8 операционных: 4 — для акушерских операций (в т.ч. оборудованная ангиографической аппаратурой), а также 4 для гинекологических операционных, позволяющих проводить лапароскопические, лапаротомические, влагалищные, реконструктиивно-пластические операции.
Впервые в России под руководством членкорра РАН, профессора Курцера М.А. на базе отделения разработаны и внедрены уникальные органосохраняющие операции при врастании плаценты, множественной миоме матки.
Профессором Курцером М.А. и зав. отделением патологии Лукашиной М.В. В 2009 г. получен патент № 2394509: “Способ лечения послеродовых кровотечений путем тампонирующих скобкообразных швов на матку” .
Кроме того в операционном блоке ЦПСиР проводятся эндоваскулярные методики профилактики/остановки акушерских кровотечений (эмболизация маточных артерий, временная баллонная окклюзия общих подвздошных артерий), ангиографические операции при миоме матки (ЭМА). Это современный, малоинвазивный, органосохраняющий метод лечения миомы матки. ЭМА выполняется при миомах практически любых размеров и локализации, приводит к прекращению кровотока в миоматозных узлах с их последующим «рассасыванием».
Особое значение имеет применение ЭМА у женщин, планирующих беременность. При наличии множественной миомы матки, миомы больших размеров, а также миомы с интерстициальным компонентом, эмболизация позволяет избежать формирования рубцов на матке, являющихся основной причиной такого грозного осложнения, как разрыв матки во время беременности и родов, а также развития спаечной болезни. Зачастую, эмболизация маточных артерий является единственным шансом сохранить матку и способность к деторождению.
При наличии множественной миомы матки, миомы больших размеров, а также миомы с интерстициальным компонентом, эмболизация позволяет избежать формирования рубцов на матке, являющихся основной причиной такого грозного осложнения, как разрыв матки во время беременности и родов, а также развития спаечной болезни. Зачастую, эмболизация маточных артерий является единственным шансом сохранить матку и способность к деторождению.
В операционном отделении ежедневно проводится до 10 плановых и 15 экстренных операций. В 2013 году было проведено более 2500 операций.
Врастание плаценты
Врастание плаценты остается одной из ведущих причин массивных кровотечений в акушерстве, что связано с возрастанием количества операций кесарева сечения. По мнению Курцера М.А. и соавторов для обозначения врастания плаценты целесообразно использовать термин placenta accreta, объединяющий применяемые ранее в нашей стране placenta accreta, placenta increta, placenta percreta, основанные на глубине повреждения миометрия. В настоящее время диагноз placenta accreta фигурирует с частотой 1 на 533 – 2500 родов.
По данным Курцера М.А. и соавторов (2016), placenta accreta формируется в результате полного «расползания» несостоятельного рубца, область которого не содержит мышечных волокон и представлена фиброзной тканью, покрытой брюшиной с прикрепляющейся к ней ворсинами хориона. Ворсины хориона не прорастают в мочевой пузырь, а невозможность отделения плаценты от его задней стенки объясняется выраженным спаечным процессом между мочевым пузырем и патологически измененной стенкой матки.
При подозрении на врастание плаценты беременным группы риска (наличие рубца на матке после операции кесарева сечения и предлежания плаценты, располагающейся по передней стенке матки в области рубца) должно быть выполнено 2D ультразвуковое исследование (УЗИ) с цветовым допплеровским картированием или магнитно – резонансная томография (МРТ).
Эхографическими критериями, позволяющими поставить диагноз placenta accreta, являются наличие плацентарных лакун, облитерация гипоэхогенной зоны между плацентой и миометрием, истончение миометрия менее 1 мм, отсутствие четкой границы между стенкой матки и мочевым пузырем.
К МР — признакам врастания плаценты относятся аневризма нижнего маточного сегмента, истончение прилежащего к плаценте миометрия, разнокалиберные сосудистые плацентарные лакуны, наличие патологических сосудов, выходящих за пределы органа.
По данным нашего главного врача – О.А. Латышкевича (2015) — методы обладают сопоставимой диагностической ценностью – при наличии высококвалифицированных специалистов предпочтение должно отдаваться экономически более приемлемому УЗИ.
В последние годы у беременных с диагнозом врастание плаценты при родоразрешении появилась возможность избежать неминуемой ранее гистерэктомии благодаря метропластике.
Современный хирургический подход заключается в проведении оперативного родоразрешения с одномоментной пластикой матки и мочевого пузыря. На первом этапе операции производится донное кесарево сечение, позволяющее минимизировать кровопотерю и обеспечить атравматичное извлечение плода. На втором этапе выполняется метропластика. Метропластика заключается в резекции измененного участка миометрия единым блоком с подлежащей плацентой с последующей реконструкцией стенки матки.
Такие операции начали разрабатываться в ЦПСиР с 2006 г: всего за период с 2006 по 2017 г были прооперированы 154 пациентки с диагнозом placenta accreta.
При диагностировании врастания плаценты беременную необходимо маршрутизировать в стационар III уровня, где должен соблюдаться мультидисциплинарный подход к родоразрешению, предусматривающий наличие высококвалифицированной акушерско – анестезиологической службы, препаратов крови и возможности использования аппаратов для аутологической реинфузии крови, урологической и хирургической помощи в круглосуточной доступности с применением современных эндоваскулярных методик. Стационар должен располагать современной рентгеноперационной или передвижной ангиографической установкой (RCOG,2011).
Стационар должен располагать современной рентгеноперационной или передвижной ангиографической установкой (RCOG,2011).
ЦПСиР предоставляет медицинскую помощь пациенткам с placenta accreta в рамках программы ОМС, у нас используются как современные диагностические, так и высокотехнологичные методики в области эндоваскулярной хирургии — эмболизация маточных артерий (ЭМА), временная баллонная окклюзия общих подвздошных артерий.
Временная баллонная окклюзия общих подвздошных артерий обладает высокой эффективностью и создает условия для выполнения метропластики с минимальной интраоперационной кровопотерей (Курцер М.А. и соавт., 2016). После достижения полной окклюзии артерий начинается этап акушерской операции — с 20 – минутным интервалом проводится попеременное сдувание баллонов продолжительностью 30 – 40 секунд — достигается восстановление кровотока по общим подвздошным артериям в органах малого таза и нижних конечностях.
В 2013 году команда врачей акушеров–гинекологов и сосудистых хирургов под руководством Марка Аркадьевича Курцера (ГБУЗ ЦПСиР ДЗМ, Перинатального медицинского центра г. Москвы, Клинического госпиталя Лапино) была удостоена премии «Призвание» в номинации «За создание нового метода лечения» — за создание новой технологии одномоментного проведения родоразрешения путем кесарева сечения с одномоментной пластикой матки и мочевого пузыря.
Врастание плаценты в рубец на матке после операции кесарево сечения: оперативное лечение
При наличии рубца на матке после операции кесарево сечение во время беременности может возникнуть осложнение – врастание плаценты в рубец на матке, которое часто сопровождается растяжением рубцовой ткани, условно называемой «аневризмой матки».
При наличии рубца на матке после операции кесарево сечение во время беременности может возникнуть осложнение – врастание плаценты в рубец на матке, которое часто сопровождается растяжением рубцовой ткани, условно называемой «аневризмой матки» (рис. 1).
1).
Рис.1. «Аневризма матки» при врастании плаценты в рубец после кесарева сечения в нижнем маточном сегменте.
Современные органосохраняющие методы родоразрешения пациенток с врастанием плаценты после кесарева сечения:
Кесарево сечение при врастании плаценты может сопровождаться быстрым, массивным кровотечением. В большинстве случаев такие операции раньше заканчивались экстирпацией матки. В настоящее время разработаны и применяются органосохраняющие методики при врастании плаценты с использованием ангиографических методов гемостаза во время кесарева сечения – эмболизации маточных артерий, баллонной окклюзии общих подвздошных артерий.
В акушерской практике метод баллонной окклюзии общих подвздошных артерий начал применяться с 1995 г. при гистерэктомии во время кесарева сечения с целью уменьшения объема кровопотери. Эндоваскулярная блокада кровотока (в маточных, общих подвздошных артериях) в настоящее время является современным методом лечения массивных послеродовых кровотечений. Впервые в России операция временной баллонной окклюзии подвздошных артерий во время КС при врастании плаценты была произведена профессором Курцером Марком Аркадьевичем в декабре 2012 года.
При отсутствии дополнительных осложнений беременные с врастанием плаценты госпитализируются в плановом порядке в сроке 36-37 недель. Проводится дополнительное обследование, подготовка препаратов крови, аутоплазмодонороство, определяется хирургическая тактика.
Всем пациентам, поступившим в плановом порядке, в предоперационном периоде выполняется дуплексное сканирование общих подвздошных артерий с обеих сторон. Производится оценка диаметра артерии для оптимального подбора баллона. Диаметр баллона для временной окклюзии должен соответствовать диаметру сосуда, что, в конечном счете, позволит выполнить эффективную окклюзию сосуда. Принимая во внимание склонность рожениц к гиперкоагуляции, в дооперационном периоде у всех пациентов определяется степень агрегации тромбоцитов, т. к. высокий показатель, является противопоказанием к проведению данного рода вмешательства, ввиду возможного тромбоза артерий нижних конечностей.
к. высокий показатель, является противопоказанием к проведению данного рода вмешательства, ввиду возможного тромбоза артерий нижних конечностей.
Предоперационная подготовка при врастании плаценты включает в себя:
- катетеризацию центральной вены;
- обеспечение донорской кровью и совмещение ее с кровью беременной;
- готовность к применению системы для аутогемотрансфузии.
Во время операции желательно присутствие ангиохирурга и трансфузиолога.
При врастании плаценты предпочтительна срединная лапаротомия, донное кесарево сечение. Извлечение плода осуществляют через разрез в дне матки, не затрагивая плаценту. После пересечения пуповины пуповинный остаток погружается в матку, производится ушивание разреза на матке. Преимуществом донного кесарева сечения является проведение метропластики в более комфортных условиях для хирурга – после извлечения ребенка легче отсепаровать при необходимости мочевой пузырь для визуализации нижнего края неизмененного миометрия.
С целью гемостаза сразу после извлечения плода возможно проводение эмболизации маточных артерий, используя большое количество эмболов. Но в настоящее время наиболее эффективным методом является временная баллонная окклюзия общих подвздошных артерий под рентгенологическим контролем (рис. 2).
Рис. 2. Баллонная окклюзия общих подвздошных артерий под рентгенологическим контролем.
Использование временной баллонной окклюзии подвздошных артерий имеет ряд преимуществ: минимальная кровопотеря, временное прекращение кровотока в данных сосудах, что позволяет проводить более тщательный гемостаз.
Противопоказаниями для ЭМА и временной баллонной окклюзии подвздошных артерий являются:
нестабильная гемодинамика;
геморрагический шок II-III ст.;
подозрение на внутрибрюшное кровотечение.
Завершающим этапом операции является иссечение аневризмы матки, удаление плаценты, выполнение метропластики нижнего маточного сегмента. Удаленные ткани (плацента и стенка матки) обязательно направляются на гистологическое исследование.
Удаленные ткани (плацента и стенка матки) обязательно направляются на гистологическое исследование.
В настоящее время данные операции проводятся в трех госпиталях Группы компаний «Мать и дитя»: в г. Москве в Перинатальном медицинском центре, в Московской области в Клиническом госпитале «Лапино», в г. Уфе в Клиническом госпитале «Мать и дитя Уфа» и в Клиническом госпитале «Мать и дитя Авиценна» в г. Новосибирске. С 1999 года всего было проведено 138 операции при врастании плаценты, из них у 56 пациентке применялась эмболизация маточных артерий, и у 24 – временная баллонная окклюзия общих подвздошных артерий.
В случае, когда врастание плаценты в рубец на матке диагностируется интраоперационно, при отсутствии кровотечения необходимо вызвать сосудистого хирурга, трансфузиолога, заказать компоненты крови, произвести катетеризацию центральной вены, подготовить аппарат для реинфузии аутологичной крови. Если лапаротомия выполнена поперечным разрезом, расширяют доступ (срединная лапаротомия). Методом выбора является донное кесарево сечение.
Если нет условий для осуществления гемостаза (эмболизация маточных артерий, временная баллонная окклюзия подвздошных артерий), возможно отсроченное удаление плаценты, однако обязательным условием для выбора такой тактики является отсутствие кровотечения и гипотонии матки.
размышления и комментарии – тема научной статьи по клинической медицине читайте бесплатно текст научно-исследовательской работы в электронной библиотеке КиберЛенинка
Рентгеноэндоваскулярная окклюзия маточных артерий у больных с миомой матки: размышления и комментарии
М.И. Билан1
АНО «МСЧ» администрации г. Магнитогорск и ОАО «ММК», отделение ангиографии и рентгенохирургии
Известно, что миома матки — самое частое доброкачественное опухолевидное образование, которое выявляется у 40% женщин старше 50 лет [1, 2] .
Несмотря на большое число исследований и определенные успехи в терапии у больных с миомой матки, до настоящего времени основным методом лечения этого заболевания остается хирургический. Причем у 8-9 из 10 женщин производится радикальная операция на матке [3]. В последние годы в мире в целом значительно повышается интерес к сохранению и увеличению длительности репродуктивной функции женщин с миомой матки. Вот поэтому ведутся поиски альтернативных способов лечения данного заболевания, эффективно устраняющих патологические симптомы и сохраняющих репродуктивную функцию.
С 1995 года, когда французский гинеколог J. Ravina опубликовал результаты успешного лечения миомы матки способом окклюзии ее артерий [4], в арсенале терапии этого заболевания появился еще один органосохраняющий метод.
Несомненными преимуществами способа рентгеноэндоваскулярной окклюзии маточных артерий (РЭО МА) являются малотравматичность, высокая эффективность, низкий процент осложнений, универсальность, отсутствие рецидивов [5-7].
До настоящего времени многие вопросы, связанные с применением способа РЭО МА, исследованы недостаточно.
Целью настоящей публикации является обсуждение научных исследований, посвященных некоторым аспектам способа РЭО МА.
Так, одним из ключевых вопросов является механизм избирательного воздействия РЭО МА на миому при двухсторонней окклюзии маточных артерий. Локальное повреждающее воздействие способа РЭО МА принято объяснять своеобразием кровоснабжения узла миомы. Обособленность кровообращения в узле миомы и его отличия заложены в особенностях развития сосудов при морфогенезе миомы. По данным Г.А. Савицкого и со-авт., узлы миомы начинают формироваться из зон
1 45500 г. Также особенностью сосудов миомы является пассивное изменение их диаметра за счет давления крови [3].
Также особенностью сосудов миомы является пассивное изменение их диаметра за счет давления крови [3].
Установлено, что узлы миомы в своей структуре содержат меньше сосудов, чем окружающий миометрий [8, 9].
Различия в кровоснабжении узла миомы и мио-метрия матки были обнаружены при лечении миомы у 45 пациенток способом РЭО МА с магнитнорезонансным томографическим (МРТ) наблюдением [10]. До лечения способом РЭО МА окружающий миометрий имел достоверно выше уровень перфузии, чем узлы миомы. Сразу после проведения двусторонней окклюзии маточных артерий отмечено падение уровня перфузии в узлах миомы до 0%, тогда как в окружающих тканях миометрия перфузия сохранялась на уровне 26%. Полное восстановление перфузии миометрия отмечено при следующем МРТ-исследовании через один месяц. Другое исследование показывает восстановление нормального кровоснабжения окружающего миометрия уже через одну неделю [11].
F. Burbank et al. так описывают процессы происходящие в миоматозной матке после острой закупорки маточных артерий [12]: «После окклюзии маточных артерий, кровоснабжающих ткани матки и узлы миомы, резко замедляется кровоток с образованием внутрисосудистого тромба. Наступает время ишемии тканей матки, которое клинически проявляется значительным болевым симптомом. Примерно через шесть часов во внутриматочных артериях начинается лизис тромба с восстановление кровообращения в матке через артерии яичника или другие коллатеральные сосуды. Клетки тканей матки в состоянии перенести период преходящей ишемии. Этот же период времени приводит к гибели миомы, в сосудах узла лизис тромба не происходит, не восстанавливается кровообращение.»
В более поздних публикациях эти же авторы [13] высказывают предположение о причинах устойчивости тканей матки к преходящей ишемии. Подобное состояние ишемии матка испытывает при родах.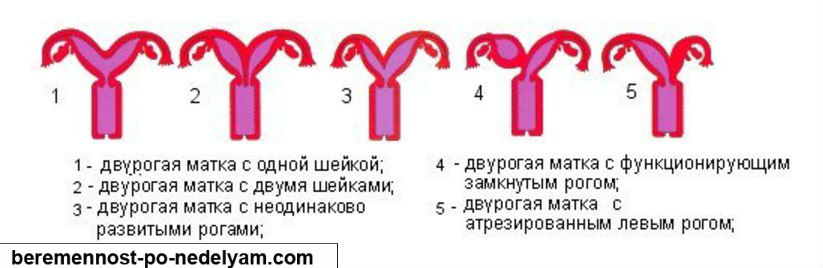 После отторжения плаценты происхо-
После отторжения плаценты происхо-
дит тромбоз сосудов миометрия, защищая женщину от профузного кровотечения и гибели. В течение ограниченного периода наступает ишемия тканей матки. Позднее, под воздействием фибринолити-ческих энзимов, происходит восстановление кровотока в сосудах миометрия, не связанных с кровоснабжением плаценты. Отличительная устойчивость матки к ишемии в сравнении с миомой, вероятно, обусловлена ее предназначением — детородной функцией.
Таким образом, можно предположить, что особенности кровоснабжения миомы (строение сосудистой стенки, отсутствие коллатерального кровоснабжения, объем сосудов) и генетическая устойчивость матки к ишемии являются причинами избирательных деструктивных изменений узла миомы при лечении больных способом РЭО МА.
С пониманием механизма лечебного воздействия связана другая проблема — степень окклюзии маточной артерии при выполнении РЭО МА.
С момента клинического применения способа РЭО МА [4] и последующие несколько лет основным эмболизирующим веществом были частицы поливинилалкоголя (ПВА). По физическим характеристикам ПВА — это частицы с выраженной неровной поверхностью. Данное свойство приводит к взаимному слипанию частиц и неконтролируемой фиксации к стенке сосуда и катетера. Как отметили Pelage et al, уровень окклюзии артерии, вызванный ПВА-частицами, не соответствует их размерам [5]. Использование в качестве эмболизирующего вещества частиц ПВА размером 350-700 микрон позволяет проводить полную окклюзию маточных артерий, при этом происходит деваскуляризация не только миомы, но и тканей матки. Оптимальная степень вмешательства при РЭО МА — избирательная окклюзия ветвей маточной артерии, которые кровоснабжают только миоматозный узел, оставляя проходимыми артерии идущие к миометрию. На тот период времени желание проводить эмбо-лизацию только артерий миомы не соответствовало техническим возможностям.
Появление на рынке медицинских препаратов калиброванных эмболизирующих веществ (первое из них микросферы «Embosphere»), казалось, открывало эти новые возможности. Гладкая поверхность частиц позволяла достигать эмболизации артерий необходимого размера, чаще использовать микрокатетеры. Использование калиброванных частиц позволило некоторым исследователям определить новые ангиографические критерии успешной окклюзии маточных артерий («pruned tree»): исчезновение зон гиперваскуляризации миомы, замедление кровотока в дистальных отделах маточной артерии с сохранением в проксимальных и шеечно-влагалищной ветви [14, 15]. Такая ограниченная окклюзия маточной артерии, по мнению авторов, должна приводить к преимущественной деваскуляризации миомы. Проведенные экспериментальные и первые клинические иссле-
дования показали преимущества калиброванных частиц перед некалиброванными [16-19]. Хотя последующие сравнительные исследования не выявили убедительных преимуществ этих частиц [20, 21].
На основании предполагаемого механизма лечебного воздействия для гибели миоматозных узлов необходима их ишемия на срок до шести часов. Важно отметить, что при проведении вмешательства РЭО МА нет необходимости создавать максимальную окклюзию частицами артерий миомы. Можно предположить, что «идеальным» видом РЭО МА у больных с миомой матки является двухсторонняя временная (до шести часов) проксимальная (дистальнее отхождения шеечно-влагалищной ветви) изолированная (с полным сохранением дистального русла и коллатералей) окклюзия маточных артерий. Хочется отметить, это относится к миомам, имеющим преимущественное кровоснабжение из бассейна маточных артерий.
В подтверждение этих выводов, можно отметить успешность лечения пациенток с миомой матки способом эндоскопического клипирования или коагуляции маточных артерий [22-24]. Данный вид вмешательств аналогичен эндоваскулярной постоянной проксимальной изолированной окклюзии маточных артерий.
Данный вид вмешательств аналогичен эндоваскулярной постоянной проксимальной изолированной окклюзии маточных артерий.
Вариант временной окклюзии успешно продемонстрирован в работе О. 1э1гб при лечении 43-летней пациентки с множественной миомой [25]. Авторы под трансвагинальным ультразвуковым контролем произвели клипирование маточных артерий. Через шесть часов произведено снятие клипсы с артерий с восстановлением кровотока. При контрольном осмотре через 3 месяца отмечено клиническое улучшение и уменьшение размеров матки на 48,9%, а наибольшего узла миомы — на 77,2%.
Предложенные выводы основаны на анализе научной литературы и личного опыта являются предварительными и требуют серьезного изучения.
Дальнейшие исследования помогут выбору оптимального эмболизирующего вещества и степени окклюзии при лечении способом РЭО МА, а возможно, и внедрению альтернативных способов лечения больных с миомой матки.
Прежде всего хотелось вызвать интерес читателей журнала к данным актуальным вопросам по лечению пациенток способом РЭО МА и желание высказать свое мнение по ним.
Литература
1. Тихомиров А.Л., Серов В.Н.. Современные принципы диагностики лечения и профилактики лейомиомы матки. Русский медицинский журнал. 2000, №11, 473-474.
2. Broer MS, Kanouse DE, Mittman BS. The appropriateness of recommendations for hysterectomy. Obstet.Ginecol., 2000, 95, 199-205.
3. Савицкий ГА., Савицкий А.Г. Миома матки (проблемы патогенеза и патогенетической терапии).( СПб: ЭЛБИ, 2000, стр. 45-46.
4. Ravina JH, Herbreteau D, Ciraru-Vigneron N, et al. Arterial embolization to treat uterine myomata. Lancet, 1995, 346(8976), 671-672.
5. Pelage JP, Laurent A, Wasser M, et al. Uterine artery embolization: choice of an embolic particle. J. Vasc. Interv. Radiol., 2000, 11, P.189.
6. Ravina JH, Aymard A, Ciraru-Vigneron N, et al. Arterial embolization of uterine myoma: results apropos of 286 cases. J. Gynecol. Obstet. Biol. Reprod., 2000, 29, 272(275.
7. Spies JB, Ascher SA, Roth AR, et al. Uterine artery embolization for leiomyomata. Obstet. Gynecol., 2001, 98(1), 29-34.
8. Farrer-Brown G, Beilby JO, Tarbit MH. Microvasculature of the uterus: an injection method of study. Obstet. Gynecol., 1970, 35, 21-30.
9. Casey R, Rogers PAW, Vollenhoven BJ. An immunohisto-chemical analysis of fibroid vasculature. Human reproduction, 2000, 15, 1469-1475.
10. deSouza NM, Williams AD. Uterine arterial embolization for leiomyomas: perfusion and volume changes at MR imaging and relation to clinical outcome. Radiology, 2002, 222(2), 367-374.
11. Katsumori T, Nakajima K, Tokuhiro M. Gadolinium-enhanced MR imaging in the evaluation of uterine fibroids treated with uterine artery embolization. Am. J. Roentgenol., 2001, 177(2), 303-307.
12. Burbank F, Hutchins FL. Uterine artery occlusion by embolization or surgery for the treatment of fibroids: A unifying hypothesis-transient uterine ischemia. J. Am. Assoc. Ginecol. Laparosc., 2000, 7, 145-149.
13. Burbank F. Childbirth and myoma treatment by uterine artery occlusion they share a common biology? J. Am. Assoc. Ginecol. Laparosc., 2004,11,138-152.
14. Worthington-Kirsch RL, Fueredi GA, Goodwin SC, et al. Polyvinyl alcohol particle size for uterine artery embolization. Radiology, 2001, 218, 605-606.
15. Pelage JP, Le Dref O, Beregi JP, et al. Limited uterine artery embolization with tris-acril gelatin micrispheres for uterine fibroids. J. Vasc. Interv. Radiol., 2003, 14(1), 15-20.
16. Derdeyn CP, Graves VB, Salamat MS, et al. Collagen-coated acrylic microspheres for embolotherapy: in vivo and in vitro characteristics. Am. J. Neuroradiol., 1997, 18, 647-653.
17. Pelage JP, Laurent A, Wassef M, et al. Uterine artery embolization in sheep: comparison of acute effects with polyvinil alkohol particles and calibrated microspheres. Radiology, 2002, 224(2), 436-445.
18. Bendszus M, Klein R, Burger R, et al. Efficacy of trisacryl gelatin microspheres versus polyvinyl alcohol particles in the preoperative embolization of meningiomas. Am. J. Neuroradiol.,
2000, 21,255-261.
19. Spies JB, Benenati JF, Worthington- Kirsch RL, et al. Initial experience with use of tris-acril gelatin microspheres uterine artery embalization for leiomyomata. J.Vasc. Interv. Radiol.,
2001, 12(9), 1059-1063.
20. Ryu RK, Omary RA, Sichlau MJ, et al. Comparison of pain after uterine artery embolization using tris-acryl gelatin microspheres versus polyvinyl alcohol particles. Cardiovasc. Intervent. Radiol., 2003, 26, 375-378.
21. Spies JB, Allison S, Flick P, et al. Polyvinyl alcohol particles and tris-acryl gelatin microspheres for uterine artery embolization for leiomyomas: results of a randomized comparative study. J. Vasc. Interv. Radiol., 2004, 15(8), 793-800.
22. Liu WM, Ng HT, Wu YC, et al. Laparoscopic bipolar coagulation of uterine vessels: a new method for treating simptomatic fibroids. Fertil. Steril. 2001, 75(2), 417-422.
23. Lichtinger M, Hallson L, Calvo P, et al. Laparoscopic uterine artery occlusion for symptomatic leiomyomas. J. Am. Assoc. Gynecol. Laparosc., 2002, 9(2), 191-198.
24. Hald K, Langebrekke A, Klow NE, et al. Laparoscopic occlusion of uterine vessels for the treatment of symptomatic fibroid: Initial experience and comparison to uterine artery embolization. Am. J. Obstet. Gynecol., 2004, 190(1). 37-43.
25. Istre O, Hald K, Qvigstad E. Multiple myomas treated with a temporary, noninvasive, Doppler-directed, transvaginal uterine artery clamp. J. Am. Assoc. Gynecol. Laparosc., 2004, 11(2), 273-276.
Случай благополучного завершения беременности при врастании плаценты
Врастание плаценты у пациенток с рубцом на матке после предыдущих операций кесарево сечение — это чрезвычайно важная проблема, которая активно обсуждается в современном акушерстве. Этот вид осложнений все чаще диагностируется у женщин с повторными беременностями после операций кесарево сечение, число которых продолжает быть высоким в связи с расширением показаний для оперативных родов. Во время родоразрешения неизбежно возникают массивные кровотечения, которые несут опасность для жизни матери.
Раньше при врастании плаценты хирурги принимали радикальное решение — удаляли матку, что, впрочем, не уменьшало кровопотерю и притом лишало пациентку в дальнейшем репродуктивной функции.
Сегодня появилась возможность проводить органосохраняющие операции, применяя методики временного снижения кровоснабжения матки (деваскуляризацию), такие как временная окклюзия общих подвздошных артерий баллонными катетерами, эмболизация маточных артерий, перевязка внутренних подвздошных артерий, создание тоннелей в широкой связке матки с временным наложением катетера Фоллея на область нижнего сегмента. Применяется инновационная органосохраняющая хирургическая техника — донное кесарево сечение с проведением метропластики (иссечения участка матки с врастанием плаценты). Кровопотеря восполняется путем реинфузии собственной крови с помощью аппарата Сell Saver.
Клинический случай: Беременная Д., 37 лет поступила в родильный дом по направлению врача женской консультации для родоразрешения. В анамнезе у пациентки — операция кесарево сечение, во время данной беременности при УЗИ исследовании было диагностировано предлежание плаценты и заподозрено врастание плаценты. Амбулаторно проведена дополнительная диагностика — МРТ, диагноз был подтвержден.
Принимая во внимание предлежание плаценты и подозрение на врастание плаценты, было принято решение в сроке беременности 37 −38 недель в плановом порядке провести родоразрешение путём операции кесарево сечение в условиях рентгеноперационной.
Родоразрешение проводили две бригады врачей: акушер-гинекологи — Иван Осокин и Василий Грабовский — и рентгенхирурги Александр Ванюков и Сергей Бондаренко. В ходе операции врастание плаценты подтвердилось на достаточно большом (размером в 6 сантиметров) участке передней стенки матки. Учитывая данную особенность, было проведено кесарево сечение в области дна матки, в результате чего родился живой доношенный малыш.
После рождения ребёнка врачам предстояло выполнить операцию по иссечению участка матки с вросшей плацентой. Чтобы избежать массивного кровотечения, рентгенхирурги выполнили временную окклюзию общих подвздошных артерий.
Комментирует заведующий отделением рентгенхирургических методов диагностики и лечения Ванюков Александр Евгеньевич:
— Обычно для этой процедуры выполняется пункция левой и правой общей бедренных артерий. Однако пункция бедренных артерий связана с выраженным дискомфортом для пациента, т.к. требует длительной иммобилизации конечности и тугой перевязки в области операционной раны при срединном доступе при кесаревом сечении. Также для пункции бедренной артерии свойственно большее количество послеоперационных гематом и
кровотечений. Исходя из этого, мы решили в качестве артериального доступа использовать левую и правую лучевые артерии. Это артерии руки. Наша часть работы начинается после рождения ребёнка, чтобы не подвергать новорожденного радиационной нагрузке. Под рентген-навигацией с помощью С-дуги была выполнена пункция левой и правой лучевых артерий. Баллонные катетеры проведены по аорте и установлены в левую и правую общие подвздошные артерии. С этого момента мы были готовы выполнить внутриартериальный гемостаз (т.е. остановку кровотечения) в любую секунду. На этот раз экстренного гемостаз не потребовалось, и перед тем как хирурги начали отделять вросшую часть плаценты от тела матки, мы раздули баллонные катетеры в общих подвздошных артериях, тем самым, перекрыв кровоток в питающих матку сосудах. Когда плацента была удалена и наложены швы на тело матки, баллоны были сдуты, что позволило убедиться в отсутствии кровотечения. Затем баллоны и направляющие катетеры были удалены, на место пункции наложены повязки. Такая методика позволила сохранить матку и избежать массивной кровопотери. К тому же лучевой доступ позволяет сохранить подвижность в конечностях и гораздо более безопасен, чем бедренный.
Эта история благополучно закончилась для мамы и новорожденного благодаря слаженной работе специалистов акушеров-гинекологов и врачей отделения эндоваскулярной хирургии.
Операционная бригада:
Врачи акушеры-гинекологи: Грабовский В. М., Осокин И. П.
Рентгенэндоваскулярные хирурги: Ванюков А. Е., Бондаренко С. А.
Врач-анестезиолог: Сизова И. Ю.
Операционная сестра: Рзянкина О.
Врачи акушеры-гинекологи: Богатырев Ю. А., Ефремов А. Н.
РЕМОДЕЛИРОВАНИЕ РУБЦА НА МАТКЕ ПОСЛЕ МИОМЭКТОМИИ И РОЛЬ ДОППЛЕРОМЕТРИИ В ЕГО ОЦЕНКЕ | Баширов
1. Беженарь В.Ф., Медведева Н. С., Айламазян Э. К. Современная стратегия и хирургическая техника при лапароскопической миомэктомии // Здоровье женщины. – 2008. – № 4 (36). – С. 22 – 26.
2. Приходько А.М., Баев О.Р., Луньков С.С. и др. Возможности методов оценки состояния матки после операции кесарева сечения // Акуш. и гин. – 2013. – № 10. – С. 12-16.
3. Dubuisson J., Ramyead L., Streuli I. The role of preventive uterine artery occlusion during laparoscopic myomectomy: a review of the literature // Arch Gynecol Obstet. – 2015. – V. 291 – N 4. – P. 737-43.
4. Kwon Y. S., Roh H. J., Ahn J.W. et. al. Transient occlusion of uterine arteries in laparoscopic uterine surgery // JSLS. – 2015. – V. 19 – N 1. – e2014.00189.
5. Wang P. H., Liu W. M., Fuh J. L. et. al. Symptomatic myoma treated with laparoscopic uterine vessel occlusion and subsequent immediate myomectomy: which is the optimal surgical approach? // Fertil Steril. – 2009. – V. 92 – N 2. – P. 762-9.
6. Alborzi S., Ghannadan E., Alborzi S. et al. A comparison of combined laparoscopic uterine artery ligation and myomectomy versus laparoscopic myomectomy in treatment of symptomatic myoma // Fertil Steril. – 2009. – V. 92 – N 2. – P. 742-7.
7. Blagovest B., Magunska N., Kovachev E. et al. Laparoscopic myomectomy with uterine artery clipping versus conventional laparoscopic myomectomy // Akush Ginekol. – 2015. – V. 54. – N 7. – P. 8-10.
8. El Behery M.M., Zaitoun M.M., Siam S. et al. Threedimensional power Doppler study of changes in uterine vascularity after absorbable cervical tourniguet during open myomectomy // Arch. Gyn. Obstetrics. – 2011. – V. 284. – P. 157-161.
Рак шейки матки — Медицинский центр «Мидекея МС»
Во многих странах рак шейки матки является одной их самых распространенных форм рака, составляя около 25% от всех злокачественных опухолей у женщин.
К сожалению, многие женщины обращаются к врачу на поздних стадиях заболевания, когда помочь сохранить здоровье и жизнь очень сложно, основная причина этой проблемы – отсутствие доступной информации о заболеваниях шейки матки и их проявлениях, а также методах раннего выявления рака шейки матки, из которых наиболее надежным на сегодняшний день является регулярное (не реже 1-го раза в год, а старше 40 лет – 2-х раз в год) посещение врача-гинеколога, Никто не будет заботиться о здоровье женщины так, как сам женщина.
От чего же возникает рак шейки матки?
Сегодня мы не знаем всех причин возникновения рака, но некоторые факторы риска известны.
Среди основных факторов развития шейки матки следует выделить вирусные инфекции (папилломовирус и герпес), которые провоцируют развитие фоновых или предраковых заболеваний шейки матки, при отсутствии лечения переходящих в рак.
В возникновении этой злокачественной опухоли большое значение придается фоновым заболеваниям, к которым относятся малые гинекологические заболевания – дискератозы (лейкоплакии, акантопапилломатоз, эритроплакии), железисто-мышечные гиперплазии (папиллярная или фолликулярная эрозия, фолликулярная гипертрофия). Предраковым заболеванием является дисплазия.
Наблюдается связь развития шейки матки с беспорядочными половыми связями и ранним началом половой жизни. Нормы морали и нравственности, предписывающие женщине любого вероисповедания скромное поведение – это не ханжество, а проявление вековой народной мудрости, охраняющей женщину от серьезного заболевания – рака шейки матки.
Это женское заболевание во многом зависит от мужчины – постоянного полового партнера. Если точнее, то того, насколько он озабочен здоровьем своих половых органов. Хронические заболевания половой сферы мужчин способствуют развитию рака шейки матки у их жен и подруг.
Появление злокачественной опухоли провоцируют также травмы шейки матки при абортах или в родах.
Курение разрушает весь организм женщины, но еще является и немаловажным фактором риска развития рака шейки матки.
Конечно, чем старше женщина, тем больше у нее шансов заболеть. Наиболее часто рак шейки матки регистрируется в старших возрастных группах (старше 40 лет), достигая максимума в 55-65 лет. Последнее обстоятельство связано с тем, что в период от 40 до 60 лет в организме женщины происходят существенные гормональные изменения, обусловленные началом развития климакса и наступлением менопаузы. Развитие климакса является нормальным физиологическим процессом, но в этот период происходит определенное снижение адаптационных возможностей и устойчивости эндокринной системы к воздействию различных факторов. Поэтому вероятность развития опухолей шейки матки в этот период возрастает.
Нельзя сбрасывать со счетов и наследственность. Предрасположенность к развитию рака шейки матки может передаваться по материнской линии у женщин первой степени родства – от мамы, бабушки, сестры, тетушки. Это не значит, что подобное суждение ждет и вас, но вероятность есть, и поэтому вы должны относиться к себе внимательнее, бережнее.
Немаловажная роль отводиться и длительному, затяжному стрессу или хронической усталости. Эти состояния снижают адаптационные возможности организма, подрывают его защитные силы, в результате чего обостряются все формы доброкачественных болезней шейки матки, и начинается рост онкологической патологии.
Учитывая то, что рак шейки матки обычно начинается с какого-либо предракового заболевания, единственным эффективным способом защитить себя является регулярное посещение врача-гинеколога. Молодые женщины должны проходить осмотр у гинеколога не реже 1-го ража в год, а женщины старше 40 лет – не реже 2-х раз в год. Это позволит Вам своевременно заметить гинекологическое заболевание и начать лечение еще на стадии предрака.
Ранние стадии рака шейки матки и предраковые гинекологические заболевания могут клинически не проявляться, однако достаточно легко выявляются при осмотре.
Следует знать, что рак шейки матки – это заболевание, хорошо поддающееся лечению на ранних стадиях. Рак шейки матки лечится только в онкологическом учреждении.
Необходимо срочно показаться врачу, если появились следующие симптомы:
— кровотечения или кровянистые выделения из наружных половых путей после полового акта, между менструациями, после установившейся менопаузы или при дефекации,
— бели (иногда с неприятным запахом),
— боли внизу живота или в пояснице.
При появлении любых симптомов со стороны женских половых органов следует немедленно обратиться к врачу.
Эффективность лечения зависит, в первую очередь, от Вашего раннего обращения.
PS. Разместить «для пациентов»
Окклюзия маточной артерии для лечения симптоматической миомы матки
JSLS. Июль-сентябрь 2010 г .; 14 (3): 386–390.
, MD, , MD и, MDAdel Helal
Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Абд Эль-Магид Машали
Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Талал Амер
Отделение радиологии, Университетские больницы Мансура, Медицинский факультет, Университет Мансура, Египет.
Адель Хелал, Отделение акушерства и гинекологии, Больницы Университета Мансуры, Медицинский факультет, Университет Мансуры, Египет.
Автор для переписки. Адрес для корреспонденции: Адель Саад Хелал Эль-Сайед, телефон: +20101655174, +20502117358, электронная почта: moc.oohay@lalehdaasleda Авторские права © 2010 JSLS, Журнал Общества лапароэндоскопических хирургов. Статья в открытом доступе, распространяемая в соответствии с условиями некоммерческой лицензии Creative Commons Attribution без производных (http: // creativecommons.org / licenses / by-nc-nd / 3.0 /), который разрешает некоммерческое использование, распространение и воспроизведение на любом носителе, при условии, что оригинальная работа должным образом процитирована и никоим образом не изменена. статьи в ЧВК.Abstract
Цель:
Сравнить эффективность и безопасность окклюзии маточной артерии лапароскопией и эмболизацией в качестве метода лечения симптоматической миомы матки.
Методы:
Обследовано 96 женщин в пременопаузе с симптоматической лейомиомой матки.Никто из них не желал дальнейшей беременности. Они были рандомизированы для лечения либо лапароскопической окклюзией (группа 1), либо радиологической эмболизацией маточных артерий (группа 2). Первичным критерием оценки была удовлетворенность пациентки менструальной кровопотерей по сравнению с потерей до лечения. Вторичные критерии оценки включали послеоперационную боль, осложнения, вторичные вмешательства и неудачи.
Результаты:
Девяносто женщин наблюдались в течение 1, 3, 6 и 12 месяцев после обеих процедур.Первичный результат был сопоставим между двумя группами (86,7% после лапароскопической окклюзии против 88,8% после эмболизации, без статистически значимой разницы). Через 12 месяцев наблюдения у большего числа пациентов возобновились тяжелые периоды в группе окклюзии маточной артерии [4/45 пациенток, 8,8% в группе окклюзии по сравнению с 3/45 (6,6%) в группе эмболизации, P = 0,044].
Заключение:
Как лапароскопическая окклюзия, так и суперселективная эмболизация маточных артерий улучшили клинические симптомы у большинства пациентов.При контрольном наблюдении через 12 месяцев эмболизация может быть более эффективной.
Ключевые слова: Миома матки, Окклюзия маточной артерии, Лапароскопия
ВВЕДЕНИЕ
Лейомиома матки, которая встречается у каждой 4-5 женщин в репродуктивной жизни, является наиболее распространенной солидной опухолью таза у женщин. 1 Нарушения менструального цикла, особенно меноррагия, которая часто приводит к железодефицитной анемии, являются наиболее частыми осложнениями лейомиомы матки. 1
Гистерэктомия — наиболее распространенное лечение симптоматической лейомиомы.Медикаментозное лечение, сочетающее прогестаген и гормональную терапию агонистами гонадотропин-рилизинг-гормона, часто дает обнадеживающие, но временные результаты в виде лейомиомы матки. 2 Хирургические процедуры, включая миомэктомию и гистерэктомию, часто необходимы позже в ходе событий. 3,4 Но помимо рисков, связанных с хирургическими вмешательствами, гистерэктомия может быть причиной эмоциональной травмы. 5,6
По этим причинам спрос на альтернативные методы лечения увеличился за последнее десятилетие как со стороны пациентов, так и со стороны врачей, ищущих менее инвазивные процедуры.Эмболизация лейомиомы матки стала одной из таких альтернативных процедур, а лапароскопическая окклюзия маточных сосудов предлагается в качестве другой.
В предварительном нерандомизированном исследовании 7 авторы сообщили об уменьшении менструального кровотечения и уменьшении объема лейомиомы как после эмболизации лейомиомы матки, так и после лапароскопической окклюзии маточных сосудов. В настоящем рандомизированном исследовании сравнивается клинический результат этих двух методов. Снижение кровотечений через 6 и 12 месяцев, по оценке самих пациентов, было основной переменной результата.Вторичные критерии оценки заключались в собственной оценке пациентами уменьшения симптомов давления, послеоперационной боли и регистрации тошноты по визуальным аналоговым шкалам, времени восстановления, осложнений, вторичных вмешательств и неудач.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводилось в отделении акушерства и гинекологии и отделении радиологии университетской больницы Мансура. Девяносто шесть женщин в пременопаузе, направленных в университетскую клинику по поводу лейомиомы матки и меноррагии или симптомов давления в период с августа 2006 г. по декабрь 2008 г., были включены в это рандомизированное неслепое исследование.Критериями включения были собственная интерпретация женщин в отношении увеличения количества кровотечений, симптомов давления и выраженного желания не делать гистерэктомию. Критериями исключения были подозрение на злокачественное новообразование, субсерозные лейомиомы, которые можно было легко удалить лапароскопической операцией, известный аденомиоз и размер матки, превышающий пупочный. Подслизистые лейомиомы диаметром <3,5 см, расположенные полностью внутриполостно или с интрамуральным расширением> 50%, считались более подходящими для гистероскопической резекции и поэтому были исключены.Кроме того, были исключены женщины, желающие иметь детей, а также те, у кого были противопоказания к операции. Все подходящие пациенты посетили консультацию гинеколога, которая включала гинекологическое обследование, ультразвуковое исследование (предоперационное обследование матки проводилось с помощью ультразвука, который является стандартным методом оценки миомы в нашей больнице). Пациенты были проинформированы о возможных рисках и преимуществах обоих методов лечения. Согласившись на участие, пациенты подписали письменную форму информированного согласия перед проведением рандомизации.Рандомизация 1: 1 проводилась в 10 блоках по 10 пациентов в каждой с использованием запечатанных конвертов. Пять конвертов в каждом блоке из 10 были назначены для лапароскопического лечения и 5 — для эмболизации лейомиомы матки. Конверты в каждом блоке были закрыты, перемешаны, а затем пронумерованы. Лечение было решено путем рисования следующего доступного конверта в порядке возрастания номеров.
Всасывающая эвакуация с использованием двухклапанного шприца IPAS с пластиковой канюлей Кармен № 6 была выполнена всем пациентам для исключения злокачественных новообразований и небольших внутриполостных поражений.
Операцию эмболизации выполнили интервенционные радиологи. Была пунктирована правая бедренная артерия, а маточные артерии интубированы катетером 4F Cobra или микрокатетером. Во всех случаях обе артерии были эмболизированы частицами поливинилового спирта размером от 355 до 500 микрон.
Лапароскопическая двусторонняя окклюзия маточных артерий производилась по стандартной методике, установленной Семме. 8 Маточные артерии и места анастомоза между маточными и яичниковыми артериями были закупорены с помощью зажимов или биполярной коагуляции.Передний лист широкой связки вскрывали ножницами, затем зажимом Мэриленда рассекали широкую связку по направлению к ее основанию. Рассечена крыша мочеточникового канала, проведено скелетирование маточной артерии от мочеточника. Основной ствол маточной артерии перекрыли с помощью 2 зажимов () или с помощью биполярной коагуляции. Затем было выполнено прижигание мест анастомоза между маточной и яичниковой артериями и процедура повторилась с другой стороны.
Боль и тошнота зафиксированы в первые 48 часов после лечения. SEM = стандартная ошибка среднего.
Участникам было рекомендовано использовать один и тот же тип гигиенических прокладок в течение периода исследования. Участники исследования были опрошены относительно имеющихся у них симптомов лейомиомы до лечения и через 1, 3, 6 и 12 месяцев соответственно.
На всех приемах использовалась стандартизированная анкета. Кровотечение оценивалось как «небольшое», «умеренное», «сильное» или «очень сильное».Симптомы давления, включая проблемы с мочеиспусканием, были записаны как «да» или «нет». Участников попросили оценить изменения количества симптомов кровотечения и давления как улучшение, ухудшение или неизменность. Полное облегчение симптомов через 12 месяцев наблюдения определялось как незначительное или умеренное кровотечение и отсутствие симптомов давления. Клиническая неудача определялась как сохраняющиеся симптомы, требующие вторичного лечения или отсутствие улучшения в течение 6-месячного периода наблюдения. Послеоперационная боль и тошнота во время пребывания в больнице регистрировались в послеоперационных картах.Постоянных врачей попросили указать уровень боли и тошноты, которые пациенты испытывали каждые 4 часа в течение первых 24 часов в больнице и каждые 6 часов в течение следующих 24 часов или до тех пор, пока пациент не выпадет из больницы. Режим обезболивания состоял из нестероидных противовоспалительных препаратов и комбинации парацетамол-кодеин в фиксированных дозах.
Нежелательные явления также регистрировались для каждого пациента во время пребывания в больнице и во время амбулаторных посещений через 1, 3, 6 и 12 месяцев.Все последующие хирургические и медицинские вмешательства, а также повторная госпитализация или длительная госпитализация регистрировались как нежелательные явления. Допплеровское исследование маточных артерий было выполнено через 48 часов после процедуры всем участникам.
Статистический анализ был выполнен с помощью SPSS 12.0 (Чикаго, Иллинойс), и данные представлены как средние значения для нормально распределенных данных и как медианные значения для искаженных данных. Двусторонний тест t использовался для сравнения непрерывной переменной в 2 группах пациентов, если рассматриваемая переменная не имела заметно искаженного распределения.Если распределение было заметно искажено, использовали двусторонний критерий Вилкоксона-Манна-Уитни. Для всех тестов использовался уровень значимости 0,05. Мощность исследования и размер выборки были получены с использованием PASS 2008 (анализ мощности и размер выборки, NCSS, Кейсвилл, Юта, США), нам потребовался размер выборки из 90 пациентов, по 45 в каждой группе, достигнув 98% мощности для обнаружения разницы. -1,0, между нулевой гипотезой о том, что средние значения для обеих групп были 0,0, и альтернативной гипотезой о том, что среднее значение для группы 2 было 1,0, с оцененными стандартными отклонениями группы, равными 1.0 и 1,0 и с уровнем значимости (альфа) 0,05000 с использованием двустороннего двухвыборочного теста t . 9,10
РЕЗУЛЬТАТЫ
Из 96 пациентов, рандомизированных и включенных в исследование, 90 пациентов получили лечение, 45 — с двусторонней лапароскопической окклюзией маточных артерий (группа 1) и 45 — с эмболизацией маточных артерий (группа 2). Все участники в каждой группе завершили 12-месячное испытание. Две группы были похожи по возрасту, индексу массы тела, паритету и исходным симптомам.
Число пациенток, сообщивших об уменьшении менструального кровотечения, уменьшении симптомов давления или полном облегчении всех симптомов после лечения, существенно не отличалось между двумя группами лечения () .
Таблица 1.
Клинический результат через 1 год наблюдения
| LOUA (n = 45) | ОАЭ (n = 45) | P | |
|---|---|---|---|
| Уменьшение кровотечения | 39 | 40 | 0.69 |
| Симптомы снижения давления | 35 | 36 | 0,88 |
| Полное снятие давления | 33 | 35 | 0,15 | Все симптомы полностью устранены | 0,18 |
| Удовлетворенность | 36 | 39 | 0,23 |
| Клиническая неудача | 6 | 5 | 0.13 |
Клиническая неудача наблюдалась у 5 (11,2%) пациентов после эмболизации лейомиомы матки и у 6 (13,3%) пациентов после лапароскопической окклюзии. Статистической разницы между двумя группами не было (P = 0,13). Тем не менее, 11 из 90 (12,2%) женщин по-прежнему сообщали о сильном или очень сильном кровотечении через 6 месяцев после лечения: 5 из 45 (11,1%) после эмболизации лейомиомы матки и 6 из 45 (13,3%) после лапароскопического лечения () . Разница в анализе намерения лечиться относительно количества пациентов, сообщивших об сильном кровотечении, была статистически незначимой (P = 0.044). Четыре из этих пациенток, 2 в группе эмболизации лейомиомы матки и 2 в группе лапароскопии, не соответствовали определению клинической неудачи. Все 4 участника сообщили об улучшении симптомов, а также об уменьшении кровотечений и не получали дополнительного лечения в течение периода исследования. Если бы эти 4 участника были добавлены к группе пациентов с клинической неудачей, было бы 5 (11,2%) пациентов после эмболизации лейомиомы матки и 6 (13,3%) после лапароскопии с неблагоприятными результатами через 12 месяцев после лечения (P = 0.094).
Значительно более выраженная боль и тошнота наблюдались после эмболизации лейомиомы матки, чем после лапароскопии. Среднее количество анальгетика, используемого после процедуры эмболизации, было в 4 раза выше, чем после лапароскопической операции: 46 мг по сравнению с 12 мг (P <0,001). Не наблюдалось значительных различий в уменьшении кровотечений между группами лечения через 1 месяц после лечения (P = 0,96). При контрольном наблюдении через 1 месяц у субъектов, получавших эмболизацию маточной артерии, средняя оценка кровотечения снизилась на 88.8% по сравнению с 86,7% для тех, кто лечился лапароскопией. Кроме того, через 3 месяца наблюдения у субъектов, получавших эмболизацию маточной артерии, среднее снижение оценки кровотечения составило 88,9% по сравнению с 84,4% для пациентов, получавших лапароскопию () , в то время как через 6 месяцев после эмболизации лейомиомы матки , уменьшение по-прежнему составляло 88,9%, а соответствующее уменьшение при лапароскопическом лечении составило 86,7% () . Через 12 месяцев наблюдения результаты составили 91,9% против 93,3% в группе 1 и группе 2 соответственно () .
Таблица 2.
Побочные явления после лечения через 3, 6 и 12 месяцев наблюдения
| LUAO | UAE | P | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 6 м | 12 м | 3 м | 6 м | 12 м | ||||||||||
| Меноррагия | 4 | 3 | 2 | 3 | 3 | 3 | 2 | 2 | 3 | 2 | 1.00 | |||
| Рецидивирующие симптомы давления | 0 | 1 | 2 | 1 | 2 | 2 | 0,19 | |||||||
| Всего | 7 | 7 | 7 | 7 | 5 | 0,12 | ||||||||
Наблюдались только незначительные внутрибольничные побочные эффекты. Пациенты должны были оставаться в отделении до 48 часов после лечения.
Двадцать две пациентки отметили усиление выделений из влагалища в послеоперационный период, возможно, из-за пропуска подслизистых или внутриутробных опухолей у этих пациентов.Не наблюдалось значительных различий в доле женщин с выделениями из влагалища, продолжавшимися до 7 дней. Наиболее серьезное нежелательное явление, односторонний тромбоз глубоких вен, произошло у одного пациента, который был повторно госпитализирован через 1 неделю после лапароскопической двусторонней окклюзии.
ОБСУЖДЕНИЕ
Основная цель настоящего исследования заключалась в сравнении улучшения характера кровотечений при эмболизации маточной артерии и лапароскопической окклюзии. Не было обнаружено значительной разницы в уменьшении симптомов между двумя вариантами лечения через 12 месяцев после лечения.
В литературе в одном дополнительном исследовании 11 сообщается с использованием графической таблицы оценки кровотечения у 76 пациентов, получавших эмболизацию, и сообщается об улучшении на 55,6% через 3 месяца и 58,1% через 6 месяцев, что значительно меньше, чем в нашем исследовании.
Собственная оценка облегчения симптомов пациентом чаще используется в качестве параметра исхода, чем графическая таблица оценки кровотечения, даже несмотря на отсутствие единообразия в определении степени улучшения.Несмотря на эти ограничения, настоящие результаты, основанные на собственной оценке пациентов через 6 месяцев после эмболизации артерии лейомиомы матки, аналогичны результатам других исследований. 2,3,5,6,11 Уменьшение симптомов менструального кровотечения у 93,3% и 91,9% пациенток после эмболизации лейомиомы матки и лапароскопической окклюзии соответственно в этом исследовании соответствует краткосрочным результатам 2 крупнейших проспективных одноцентровых исследования по оценке эмболизации лейомиомы матки на сегодняшний день, которые сообщили об улучшении меноррагии у 89% пациентов через 6 месяцев и у 84% через 16 месяцев, соответственно. 6,11 Кроме того, уменьшение количества кровотечений у 91,9% пациентов после двусторонней лапароскопической окклюзии в этом исследовании аналогично таковому в других исследованиях, в которых сообщается об улучшении этих симптомов примерно у 90% участников.
В отличие от отсутствия разницы между двумя группами лечения в отношении процентного снижения собственной оценки кровотечения пациентами, значительно больше участников сообщили о сильном или очень сильном кровотечении через 6 месяцев после лапароскопического лечения.Одним из возможных объяснений этого несоответствия могут быть различия в оценке кровотечения.
Есть несколько возможных объяснений несколько менее благоприятных результатов после лапароскопического лечения. В литературе ангиографические и хирургические исследования показали многочисленные анатомические вариации маточных артерий. 12,13 Таким образом, можно перекрыть не ту артерию при лапароскопии или пропустить одну артерию в случаях, когда на одной стороне две артерии вместо одной.Причина неудачи — недостаточная окклюзия маточной артерии с одной стороны.
Коллатеральное артериальное кровоснабжение матки в целом может объяснить меньшую боль после хирургической окклюзии маточной артерии, несмотря на ишемию и инфаркт лейомиомы. Поскольку эмболизация представляет собой более дистальную окклюзию, уменьшающую коллатеральный кровоток, можно ожидать увеличения ишемии матки, что приводит к усилению боли и потенциально большей эффективности по сравнению с проксимальной хирургической окклюзией.Интервенционные радиологи выражают опасения, что лейомиомы, у которых не полностью инфаркт инфаркта, могут вырасти снова. 13 В 2 проспективных исследованиях было обнаружено 16% 14 и 20% 15 рецидивов от 5 до 7 лет после эмболизации. Если бы меньшее количество боли после лапароскопии было вызвано меньшей ишемией и, следовательно, неполным инфарктом лейомиомы, можно было бы ожидать еще большего количества рецидивов со временем после лапароскопической окклюзии.
Доля пациентов, которым потребовалось вторичное хирургическое вмешательство, составила 5 (11.2%) в группе ОАЭ и 6 (13,3%) в группе LOUA в нашем исследовании. Это соотношение соответствует другим зарегистрированным исходам после эмболизации лейомиомы матки или лапароскопической окклюзии. В 2 более крупных исследованиях последующие вмешательства или повторная госпитализация произошли в 10,5% через 21 месяц 6 и в 7,5% через 17 месяцев, 11 соответственно. В обоих этих исследованиях основные показания для вторичной хирургии были аналогичны показаниям в этом исследовании: продолжающаяся меноррагия или симптомы, связанные с изгнанием лейомиомы.Отбор пациентов, вероятно, наиболее важен для получения положительных результатов, и более тщательный отбор может снизить количество случаев вторичной хирургии, вызванной стойкой меноррагией или изгнанием лейомиомы.
На основании этого исследования, как лапароскопическая окклюзия маточного сосуда, так и эмболизация, по-видимому, улучшают симптомы, связанные с лейомиомой матки у большинства пациентов. Лапароскопическая процедура привела к уменьшению послеоперационной боли и тошноты и более короткому пребыванию в больнице, хотя значительно больше участников испытали сильное менструальное кровотечение через 6 месяцев после лапароскопической окклюзии, что указывает на более благоприятный эффект после эмболизации лейомиомы матки.В свете этих результатов и с учетом значительного риска хирургических осложнений и отсутствия долгосрочных результатов, учитывая тот факт, что лапароскопические методы применяются в области гинекологической хирургии, лапароскопическая окклюзия маточной артерии, вероятно, вызовет значительный интерес как метод лечения. эффективная альтернатива гистерэктомии при симптоматической лейомиоме матки.
ЗАКЛЮЧЕНИЕ
Для успешной лапароскопической окклюзии маточной артерии хирург должен иметь необходимые лапароскопические навыки и уметь точно определить местонахождение маточной артерии для правильной перевязки сосудов.Если эти предпосылки не соблюдены, массивное кровотечение может потребовать лапаротомии; Следовательно, лапароскопическая процедура лечения лейомиомы должна проводиться только в центрах, имеющих соответствующий опыт в лапароскопической хирургии.
Информация для авторов
Адель Хелал, Отделение акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Абд Эль-Магид Машали, Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Талал Амер, отделение радиологии, больницы университета Мансура, медицинский факультет, университет Мансура, Египет.
Каталожные номера:
1. Волленховен Б.Дж., Лоуренс А.С., Хили Д. Миома матки: клинический обзор. Br J Obstet Gynecol. 1990; 97: 285–298 [PubMed] [Google Scholar] 2. Уортингтон-Кирш Р.Л., Попки Г.Л., Хатчинс Флорида. Эмболизация маточной артерии для лечения лейомиом: оценка качества жизни и клинический ответ. Радиология. 1998; 208: 225–229 [PubMed] [Google Scholar] 3.Гудвин С.К., Маклукас Б., Ли М. и др. Эмболизация маточной артерии для лечения лейомиомы матки в среднесрочных результатах. J Vasc Interv Radiol. 1999; 10: 1159–1165 [PubMed] [Google Scholar] 4. Хили Д., Волленховен Б.Дж. Роль агонистов ГнРГ в лечении миомы матки. Br J Obstet Gynecol. 1992; 99: 23–26 [PubMed] [Google Scholar] 5. Пелаж Дж. П., Ле Дреф О, Сойер П. и др. Меноррагия, связанная с миомой: лечение с помощью суперселективной эмболизации маточных артерий и промежуточное наблюдение.Радиология. 2000; 215: 228–231 [PubMed] [Google Scholar] 6. Шпионы Дж. Б., Ашер С. А., Рот А. Р., Ким Дж., Леви Э. Б., Гомес-Хорхе Дж. Эмболизация маточной артерии при лейомиомах. Obstet Gynecol. 2001; 98: 29–34 [PubMed] [Google Scholar] 7. Hald K, Langebrekke A, Klow NE, Noreng HJ, Berge AB, Istre O. Лапароскопическая окклюзия маточных сосудов для лечения симптоматической миомы: первоначальный опыт и сравнение с эмболизацией маточной артерии. Am J Obstet Gynecol. 2004; 190: 37–43 [PubMed] [Google Scholar] 8. Семм К., Меттлер Л.Технический прогресс в хирургии органов малого таза с помощью оперативной лапароскопии. Am J Obstet Gynecol. 1980; 138: 121. [PubMed] [Google Scholar] 9. Машин Д., Кэмпбелл М., Файерс П., Пинол А. Таблицы размеров выборки для клинических исследований. 2-е изд Мальден, Массачусетс: наука Блэквелла; 1997 [Google Scholar] 10. Зар Джеррольд Х. Биостатистический анализ. 2-е изд Энглвуд Клиффс, Нью-Джерси; Прентис-Холл; 1984 [Google Scholar] 11. Спис Дж. Б., Купер Дж. М., Уортингтон-Кирш Р., Липман Дж. К., Миллс Б. Б., Бененати Дж. Ф. Исход эмболизации матки и гистерэктомии по поводу лейомиомы: результаты многоцентрового исследования.Am J Obstet Gynecol. 2004; 191: 22–31 [PubMed] [Google Scholar] 12. Уокер WJ, Pelage JP. Эмболизация маточной артерии при симптоматической миоме: клинические результаты у 400 женщин с последующей визуализацией. BJOG. 2002; 109: 1262–1272 [PubMed] [Google Scholar] 13. Голуб З., Лукач Дж., Климент Л., Урбанек С. Вариабельность происхождения маточной артерии: лапароскопическое хирургическое наблюдение. J Obstet Gynaecol Res. 2005; 31: 158–163 [PubMed] [Google Scholar] 14. Гомес-Хорхе Дж., Кейунг А., Леви Э. Б., Шпионы Дж. Б.. Анатомия маточной артерии, имеющая отношение к эмболизации лейомиомы матки.Cardiovasc Intervent Radiol. 2003; 26: 522–527 [PubMed] [Google Scholar] 15. Iverson RE, Chelmow D, Strohbehn K, Waldman L, Evantash EG. Относительная заболеваемость и смертность после абдоминальной гистерэктомии и миомэктомии для лечения лейомиомы матки. Obstet Gynecol. 1996; 88: 415–419 [PubMed] [Google Scholar]Окклюзия маточной артерии для лечения симптоматической миомы матки
JSLS. Июль-сентябрь 2010 г .; 14 (3): 386–390.
, MD, , MD и, MDAdel Helal
Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Абд Эль-Магид Машали
Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Талал Амер
Отделение радиологии, Университетские больницы Мансура, Медицинский факультет, Университет Мансура, Египет.
Адель Хелал, Отделение акушерства и гинекологии, Больницы Университета Мансуры, Медицинский факультет, Университет Мансуры, Египет.
Автор для переписки. Адрес для корреспонденции: Адель Саад Хелал Эль-Сайед, телефон: +20101655174, +20502117358, электронная почта: moc.oohay @ lalehdaasleda Авторские права © 2010, JSLS, Журнал Общества лапароэндоскопических хирургов. Это статья в открытом доступе, распространяемая в соответствии с некоммерческой лицензией Creative Commons Attribution без производных (http://creativecommons.org/licenses/by- nc-nd / 3.0 /), который разрешает некоммерческое использование, распространение и воспроизведение на любом носителе при условии, что оригинальная работа должным образом процитирована и никоим образом не изменена. Эта статья цитируется в других статьях в PMC.Abstract
Цель:
Сравнить эффективность и безопасность окклюзии маточной артерии лапароскопией и эмболизацией в качестве метода лечения симптоматической миомы матки.
Методы:
Обследовано 96 женщин в пременопаузе с симптоматической лейомиомой матки. Никто из них не желал дальнейшей беременности. Они были рандомизированы для лечения либо лапароскопической окклюзией (группа 1), либо радиологической эмболизацией маточных артерий (группа 2). Первичным критерием оценки была удовлетворенность пациентки менструальной кровопотерей по сравнению с потерей до лечения. Вторичные критерии оценки включали послеоперационную боль, осложнения, вторичные вмешательства и неудачи.
Результаты:
Девяносто женщин наблюдались в течение 1, 3, 6 и 12 месяцев после обеих процедур. Первичный результат был сопоставим между двумя группами (86,7% после лапароскопической окклюзии против 88,8% после эмболизации, без статистически значимой разницы). Через 12 месяцев наблюдения у большего числа пациентов возобновились тяжелые периоды в группе окклюзии маточной артерии [4/45 пациенток, 8,8% в группе окклюзии по сравнению с 3/45 (6,6%) в группе эмболизации, P = 0,044].
Заключение:
Как лапароскопическая окклюзия, так и суперселективная эмболизация маточных артерий улучшили клинические симптомы у большинства пациентов.При контрольном наблюдении через 12 месяцев эмболизация может быть более эффективной.
Ключевые слова: Миома матки, Окклюзия маточной артерии, Лапароскопия
ВВЕДЕНИЕ
Лейомиома матки, которая встречается у каждой 4-5 женщин в репродуктивной жизни, является наиболее распространенной солидной опухолью таза у женщин. 1 Нарушения менструального цикла, особенно меноррагия, которая часто приводит к железодефицитной анемии, являются наиболее частыми осложнениями лейомиомы матки. 1
Гистерэктомия — наиболее распространенное лечение симптоматической лейомиомы.Медикаментозное лечение, сочетающее прогестаген и гормональную терапию агонистами гонадотропин-рилизинг-гормона, часто дает обнадеживающие, но временные результаты в виде лейомиомы матки. 2 Хирургические процедуры, включая миомэктомию и гистерэктомию, часто необходимы позже в ходе событий. 3,4 Но помимо рисков, связанных с хирургическими вмешательствами, гистерэктомия может быть причиной эмоциональной травмы. 5,6
По этим причинам спрос на альтернативные методы лечения увеличился за последнее десятилетие как со стороны пациентов, так и со стороны врачей, ищущих менее инвазивные процедуры.Эмболизация лейомиомы матки стала одной из таких альтернативных процедур, а лапароскопическая окклюзия маточных сосудов предлагается в качестве другой.
В предварительном нерандомизированном исследовании 7 авторы сообщили об уменьшении менструального кровотечения и уменьшении объема лейомиомы как после эмболизации лейомиомы матки, так и после лапароскопической окклюзии маточных сосудов. В настоящем рандомизированном исследовании сравнивается клинический результат этих двух методов. Снижение кровотечений через 6 и 12 месяцев, по оценке самих пациентов, было основной переменной результата.Вторичные критерии оценки заключались в собственной оценке пациентами уменьшения симптомов давления, послеоперационной боли и регистрации тошноты по визуальным аналоговым шкалам, времени восстановления, осложнений, вторичных вмешательств и неудач.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводилось в отделении акушерства и гинекологии и отделении радиологии университетской больницы Мансура. Девяносто шесть женщин в пременопаузе, направленных в университетскую клинику по поводу лейомиомы матки и меноррагии или симптомов давления в период с августа 2006 г. по декабрь 2008 г., были включены в это рандомизированное неслепое исследование.Критериями включения были собственная интерпретация женщин в отношении увеличения количества кровотечений, симптомов давления и выраженного желания не делать гистерэктомию. Критериями исключения были подозрение на злокачественное новообразование, субсерозные лейомиомы, которые можно было легко удалить лапароскопической операцией, известный аденомиоз и размер матки, превышающий пупочный. Подслизистые лейомиомы диаметром <3,5 см, расположенные полностью внутриполостно или с интрамуральным расширением> 50%, считались более подходящими для гистероскопической резекции и поэтому были исключены.Кроме того, были исключены женщины, желающие иметь детей, а также те, у кого были противопоказания к операции. Все подходящие пациенты посетили консультацию гинеколога, которая включала гинекологическое обследование, ультразвуковое исследование (предоперационное обследование матки проводилось с помощью ультразвука, который является стандартным методом оценки миомы в нашей больнице). Пациенты были проинформированы о возможных рисках и преимуществах обоих методов лечения. Согласившись на участие, пациенты подписали письменную форму информированного согласия перед проведением рандомизации.Рандомизация 1: 1 проводилась в 10 блоках по 10 пациентов в каждой с использованием запечатанных конвертов. Пять конвертов в каждом блоке из 10 были назначены для лапароскопического лечения и 5 — для эмболизации лейомиомы матки. Конверты в каждом блоке были закрыты, перемешаны, а затем пронумерованы. Лечение было решено путем рисования следующего доступного конверта в порядке возрастания номеров.
Всасывающая эвакуация с использованием двухклапанного шприца IPAS с пластиковой канюлей Кармен № 6 была выполнена всем пациентам для исключения злокачественных новообразований и небольших внутриполостных поражений.
Операцию эмболизации выполнили интервенционные радиологи. Была пунктирована правая бедренная артерия, а маточные артерии интубированы катетером 4F Cobra или микрокатетером. Во всех случаях обе артерии были эмболизированы частицами поливинилового спирта размером от 355 до 500 микрон.
Лапароскопическая двусторонняя окклюзия маточных артерий производилась по стандартной методике, установленной Семме. 8 Маточные артерии и места анастомоза между маточными и яичниковыми артериями были закупорены с помощью зажимов или биполярной коагуляции.Передний лист широкой связки вскрывали ножницами, затем зажимом Мэриленда рассекали широкую связку по направлению к ее основанию. Рассечена крыша мочеточникового канала, проведено скелетирование маточной артерии от мочеточника. Основной ствол маточной артерии перекрыли с помощью 2 зажимов () или с помощью биполярной коагуляции. Затем было выполнено прижигание мест анастомоза между маточной и яичниковой артериями и процедура повторилась с другой стороны.
Боль и тошнота зафиксированы в первые 48 часов после лечения. SEM = стандартная ошибка среднего.
Участникам было рекомендовано использовать один и тот же тип гигиенических прокладок в течение периода исследования. Участники исследования были опрошены относительно имеющихся у них симптомов лейомиомы до лечения и через 1, 3, 6 и 12 месяцев соответственно.
На всех приемах использовалась стандартизированная анкета. Кровотечение оценивалось как «небольшое», «умеренное», «сильное» или «очень сильное».Симптомы давления, включая проблемы с мочеиспусканием, были записаны как «да» или «нет». Участников попросили оценить изменения количества симптомов кровотечения и давления как улучшение, ухудшение или неизменность. Полное облегчение симптомов через 12 месяцев наблюдения определялось как незначительное или умеренное кровотечение и отсутствие симптомов давления. Клиническая неудача определялась как сохраняющиеся симптомы, требующие вторичного лечения или отсутствие улучшения в течение 6-месячного периода наблюдения. Послеоперационная боль и тошнота во время пребывания в больнице регистрировались в послеоперационных картах.Постоянных врачей попросили указать уровень боли и тошноты, которые пациенты испытывали каждые 4 часа в течение первых 24 часов в больнице и каждые 6 часов в течение следующих 24 часов или до тех пор, пока пациент не выпадет из больницы. Режим обезболивания состоял из нестероидных противовоспалительных препаратов и комбинации парацетамол-кодеин в фиксированных дозах.
Нежелательные явления также регистрировались для каждого пациента во время пребывания в больнице и во время амбулаторных посещений через 1, 3, 6 и 12 месяцев.Все последующие хирургические и медицинские вмешательства, а также повторная госпитализация или длительная госпитализация регистрировались как нежелательные явления. Допплеровское исследование маточных артерий было выполнено через 48 часов после процедуры всем участникам.
Статистический анализ был выполнен с помощью SPSS 12.0 (Чикаго, Иллинойс), и данные представлены как средние значения для нормально распределенных данных и как медианные значения для искаженных данных. Двусторонний тест t использовался для сравнения непрерывной переменной в 2 группах пациентов, если рассматриваемая переменная не имела заметно искаженного распределения.Если распределение было заметно искажено, использовали двусторонний критерий Вилкоксона-Манна-Уитни. Для всех тестов использовался уровень значимости 0,05. Мощность исследования и размер выборки были получены с использованием PASS 2008 (анализ мощности и размер выборки, NCSS, Кейсвилл, Юта, США), нам потребовался размер выборки из 90 пациентов, по 45 в каждой группе, достигнув 98% мощности для обнаружения разницы. -1,0, между нулевой гипотезой о том, что средние значения для обеих групп были 0,0, и альтернативной гипотезой о том, что среднее значение для группы 2 было 1,0, с оцененными стандартными отклонениями группы, равными 1.0 и 1,0 и с уровнем значимости (альфа) 0,05000 с использованием двустороннего двухвыборочного теста t . 9,10
РЕЗУЛЬТАТЫ
Из 96 пациентов, рандомизированных и включенных в исследование, 90 пациентов получили лечение, 45 — с двусторонней лапароскопической окклюзией маточных артерий (группа 1) и 45 — с эмболизацией маточных артерий (группа 2). Все участники в каждой группе завершили 12-месячное испытание. Две группы были похожи по возрасту, индексу массы тела, паритету и исходным симптомам.
Число пациенток, сообщивших об уменьшении менструального кровотечения, уменьшении симптомов давления или полном облегчении всех симптомов после лечения, существенно не отличалось между двумя группами лечения () .
Таблица 1.
Клинический результат через 1 год наблюдения
| LOUA (n = 45) | ОАЭ (n = 45) | P | |
|---|---|---|---|
| Уменьшение кровотечения | 39 | 40 | 0.69 |
| Симптомы снижения давления | 35 | 36 | 0,88 |
| Полное снятие давления | 33 | 35 | 0,15 | Все симптомы полностью устранены | 0,18 |
| Удовлетворенность | 36 | 39 | 0,23 |
| Клиническая неудача | 6 | 5 | 0.13 |
Клиническая неудача наблюдалась у 5 (11,2%) пациентов после эмболизации лейомиомы матки и у 6 (13,3%) пациентов после лапароскопической окклюзии. Статистической разницы между двумя группами не было (P = 0,13). Тем не менее, 11 из 90 (12,2%) женщин по-прежнему сообщали о сильном или очень сильном кровотечении через 6 месяцев после лечения: 5 из 45 (11,1%) после эмболизации лейомиомы матки и 6 из 45 (13,3%) после лапароскопического лечения () . Разница в анализе намерения лечиться относительно количества пациентов, сообщивших об сильном кровотечении, была статистически незначимой (P = 0.044). Четыре из этих пациенток, 2 в группе эмболизации лейомиомы матки и 2 в группе лапароскопии, не соответствовали определению клинической неудачи. Все 4 участника сообщили об улучшении симптомов, а также об уменьшении кровотечений и не получали дополнительного лечения в течение периода исследования. Если бы эти 4 участника были добавлены к группе пациентов с клинической неудачей, было бы 5 (11,2%) пациентов после эмболизации лейомиомы матки и 6 (13,3%) после лапароскопии с неблагоприятными результатами через 12 месяцев после лечения (P = 0.094).
Значительно более выраженная боль и тошнота наблюдались после эмболизации лейомиомы матки, чем после лапароскопии. Среднее количество анальгетика, используемого после процедуры эмболизации, было в 4 раза выше, чем после лапароскопической операции: 46 мг по сравнению с 12 мг (P <0,001). Не наблюдалось значительных различий в уменьшении кровотечений между группами лечения через 1 месяц после лечения (P = 0,96). При контрольном наблюдении через 1 месяц у субъектов, получавших эмболизацию маточной артерии, средняя оценка кровотечения снизилась на 88.8% по сравнению с 86,7% для тех, кто лечился лапароскопией. Кроме того, через 3 месяца наблюдения у субъектов, получавших эмболизацию маточной артерии, среднее снижение оценки кровотечения составило 88,9% по сравнению с 84,4% для пациентов, получавших лапароскопию () , в то время как через 6 месяцев после эмболизации лейомиомы матки , уменьшение по-прежнему составляло 88,9%, а соответствующее уменьшение при лапароскопическом лечении составило 86,7% () . Через 12 месяцев наблюдения результаты составили 91,9% против 93,3% в группе 1 и группе 2 соответственно () .
Таблица 2.
Побочные явления после лечения через 3, 6 и 12 месяцев наблюдения
| LUAO | UAE | P | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 6 м | 12 м | 3 м | 6 м | 12 м | ||||||||||
| Меноррагия | 4 | 3 | 2 | 3 | 3 | 3 | 2 | 2 | 3 | 2 | 1.00 | |||
| Рецидивирующие симптомы давления | 0 | 1 | 2 | 1 | 2 | 2 | 0,19 | |||||||
| Всего | 7 | 7 | 7 | 7 | 5 | 0,12 | ||||||||
Наблюдались только незначительные внутрибольничные побочные эффекты. Пациенты должны были оставаться в отделении до 48 часов после лечения.
Двадцать две пациентки отметили усиление выделений из влагалища в послеоперационный период, возможно, из-за пропуска подслизистых или внутриутробных опухолей у этих пациентов.Не наблюдалось значительных различий в доле женщин с выделениями из влагалища, продолжавшимися до 7 дней. Наиболее серьезное нежелательное явление, односторонний тромбоз глубоких вен, произошло у одного пациента, который был повторно госпитализирован через 1 неделю после лапароскопической двусторонней окклюзии.
ОБСУЖДЕНИЕ
Основная цель настоящего исследования заключалась в сравнении улучшения характера кровотечений при эмболизации маточной артерии и лапароскопической окклюзии. Не было обнаружено значительной разницы в уменьшении симптомов между двумя вариантами лечения через 12 месяцев после лечения.
В литературе в одном дополнительном исследовании 11 сообщается с использованием графической таблицы оценки кровотечения у 76 пациентов, получавших эмболизацию, и сообщается об улучшении на 55,6% через 3 месяца и 58,1% через 6 месяцев, что значительно меньше, чем в нашем исследовании.
Собственная оценка облегчения симптомов пациентом чаще используется в качестве параметра исхода, чем графическая таблица оценки кровотечения, даже несмотря на отсутствие единообразия в определении степени улучшения.Несмотря на эти ограничения, настоящие результаты, основанные на собственной оценке пациентов через 6 месяцев после эмболизации артерии лейомиомы матки, аналогичны результатам других исследований. 2,3,5,6,11 Уменьшение симптомов менструального кровотечения у 93,3% и 91,9% пациенток после эмболизации лейомиомы матки и лапароскопической окклюзии соответственно в этом исследовании соответствует краткосрочным результатам 2 крупнейших проспективных одноцентровых исследования по оценке эмболизации лейомиомы матки на сегодняшний день, которые сообщили об улучшении меноррагии у 89% пациентов через 6 месяцев и у 84% через 16 месяцев, соответственно. 6,11 Кроме того, уменьшение количества кровотечений у 91,9% пациентов после двусторонней лапароскопической окклюзии в этом исследовании аналогично таковому в других исследованиях, в которых сообщается об улучшении этих симптомов примерно у 90% участников.
В отличие от отсутствия разницы между двумя группами лечения в отношении процентного снижения собственной оценки кровотечения пациентами, значительно больше участников сообщили о сильном или очень сильном кровотечении через 6 месяцев после лапароскопического лечения.Одним из возможных объяснений этого несоответствия могут быть различия в оценке кровотечения.
Есть несколько возможных объяснений несколько менее благоприятных результатов после лапароскопического лечения. В литературе ангиографические и хирургические исследования показали многочисленные анатомические вариации маточных артерий. 12,13 Таким образом, можно перекрыть не ту артерию при лапароскопии или пропустить одну артерию в случаях, когда на одной стороне две артерии вместо одной.Причина неудачи — недостаточная окклюзия маточной артерии с одной стороны.
Коллатеральное артериальное кровоснабжение матки в целом может объяснить меньшую боль после хирургической окклюзии маточной артерии, несмотря на ишемию и инфаркт лейомиомы. Поскольку эмболизация представляет собой более дистальную окклюзию, уменьшающую коллатеральный кровоток, можно ожидать увеличения ишемии матки, что приводит к усилению боли и потенциально большей эффективности по сравнению с проксимальной хирургической окклюзией.Интервенционные радиологи выражают опасения, что лейомиомы, у которых не полностью инфаркт инфаркта, могут вырасти снова. 13 В 2 проспективных исследованиях было обнаружено 16% 14 и 20% 15 рецидивов от 5 до 7 лет после эмболизации. Если бы меньшее количество боли после лапароскопии было вызвано меньшей ишемией и, следовательно, неполным инфарктом лейомиомы, можно было бы ожидать еще большего количества рецидивов со временем после лапароскопической окклюзии.
Доля пациентов, которым потребовалось вторичное хирургическое вмешательство, составила 5 (11.2%) в группе ОАЭ и 6 (13,3%) в группе LOUA в нашем исследовании. Это соотношение соответствует другим зарегистрированным исходам после эмболизации лейомиомы матки или лапароскопической окклюзии. В 2 более крупных исследованиях последующие вмешательства или повторная госпитализация произошли в 10,5% через 21 месяц 6 и в 7,5% через 17 месяцев, 11 соответственно. В обоих этих исследованиях основные показания для вторичной хирургии были аналогичны показаниям в этом исследовании: продолжающаяся меноррагия или симптомы, связанные с изгнанием лейомиомы.Отбор пациентов, вероятно, наиболее важен для получения положительных результатов, и более тщательный отбор может снизить количество случаев вторичной хирургии, вызванной стойкой меноррагией или изгнанием лейомиомы.
На основании этого исследования, как лапароскопическая окклюзия маточного сосуда, так и эмболизация, по-видимому, улучшают симптомы, связанные с лейомиомой матки у большинства пациентов. Лапароскопическая процедура привела к уменьшению послеоперационной боли и тошноты и более короткому пребыванию в больнице, хотя значительно больше участников испытали сильное менструальное кровотечение через 6 месяцев после лапароскопической окклюзии, что указывает на более благоприятный эффект после эмболизации лейомиомы матки.В свете этих результатов и с учетом значительного риска хирургических осложнений и отсутствия долгосрочных результатов, учитывая тот факт, что лапароскопические методы применяются в области гинекологической хирургии, лапароскопическая окклюзия маточной артерии, вероятно, вызовет значительный интерес как метод лечения. эффективная альтернатива гистерэктомии при симптоматической лейомиоме матки.
ЗАКЛЮЧЕНИЕ
Для успешной лапароскопической окклюзии маточной артерии хирург должен иметь необходимые лапароскопические навыки и уметь точно определить местонахождение маточной артерии для правильной перевязки сосудов.Если эти предпосылки не соблюдены, массивное кровотечение может потребовать лапаротомии; Следовательно, лапароскопическая процедура лечения лейомиомы должна проводиться только в центрах, имеющих соответствующий опыт в лапароскопической хирургии.
Информация для авторов
Адель Хелал, Отделение акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Абд Эль-Магид Машали, Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Талал Амер, отделение радиологии, больницы университета Мансура, медицинский факультет, университет Мансура, Египет.
Каталожные номера:
1. Волленховен Б.Дж., Лоуренс А.С., Хили Д. Миома матки: клинический обзор. Br J Obstet Gynecol. 1990; 97: 285–298 [PubMed] [Google Scholar] 2. Уортингтон-Кирш Р.Л., Попки Г.Л., Хатчинс Флорида. Эмболизация маточной артерии для лечения лейомиом: оценка качества жизни и клинический ответ. Радиология. 1998; 208: 225–229 [PubMed] [Google Scholar] 3.Гудвин С.К., Маклукас Б., Ли М. и др. Эмболизация маточной артерии для лечения лейомиомы матки в среднесрочных результатах. J Vasc Interv Radiol. 1999; 10: 1159–1165 [PubMed] [Google Scholar] 4. Хили Д., Волленховен Б.Дж. Роль агонистов ГнРГ в лечении миомы матки. Br J Obstet Gynecol. 1992; 99: 23–26 [PubMed] [Google Scholar] 5. Пелаж Дж. П., Ле Дреф О, Сойер П. и др. Меноррагия, связанная с миомой: лечение с помощью суперселективной эмболизации маточных артерий и промежуточное наблюдение.Радиология. 2000; 215: 228–231 [PubMed] [Google Scholar] 6. Шпионы Дж. Б., Ашер С. А., Рот А. Р., Ким Дж., Леви Э. Б., Гомес-Хорхе Дж. Эмболизация маточной артерии при лейомиомах. Obstet Gynecol. 2001; 98: 29–34 [PubMed] [Google Scholar] 7. Hald K, Langebrekke A, Klow NE, Noreng HJ, Berge AB, Istre O. Лапароскопическая окклюзия маточных сосудов для лечения симптоматической миомы: первоначальный опыт и сравнение с эмболизацией маточной артерии. Am J Obstet Gynecol. 2004; 190: 37–43 [PubMed] [Google Scholar] 8. Семм К., Меттлер Л.Технический прогресс в хирургии органов малого таза с помощью оперативной лапароскопии. Am J Obstet Gynecol. 1980; 138: 121. [PubMed] [Google Scholar] 9. Машин Д., Кэмпбелл М., Файерс П., Пинол А. Таблицы размеров выборки для клинических исследований. 2-е изд Мальден, Массачусетс: наука Блэквелла; 1997 [Google Scholar] 10. Зар Джеррольд Х. Биостатистический анализ. 2-е изд Энглвуд Клиффс, Нью-Джерси; Прентис-Холл; 1984 [Google Scholar] 11. Спис Дж. Б., Купер Дж. М., Уортингтон-Кирш Р., Липман Дж. К., Миллс Б. Б., Бененати Дж. Ф. Исход эмболизации матки и гистерэктомии по поводу лейомиомы: результаты многоцентрового исследования.Am J Obstet Gynecol. 2004; 191: 22–31 [PubMed] [Google Scholar] 12. Уокер WJ, Pelage JP. Эмболизация маточной артерии при симптоматической миоме: клинические результаты у 400 женщин с последующей визуализацией. BJOG. 2002; 109: 1262–1272 [PubMed] [Google Scholar] 13. Голуб З., Лукач Дж., Климент Л., Урбанек С. Вариабельность происхождения маточной артерии: лапароскопическое хирургическое наблюдение. J Obstet Gynaecol Res. 2005; 31: 158–163 [PubMed] [Google Scholar] 14. Гомес-Хорхе Дж., Кейунг А., Леви Э. Б., Шпионы Дж. Б.. Анатомия маточной артерии, имеющая отношение к эмболизации лейомиомы матки.Cardiovasc Intervent Radiol. 2003; 26: 522–527 [PubMed] [Google Scholar] 15. Iverson RE, Chelmow D, Strohbehn K, Waldman L, Evantash EG. Относительная заболеваемость и смертность после абдоминальной гистерэктомии и миомэктомии для лечения лейомиомы матки. Obstet Gynecol. 1996; 88: 415–419 [PubMed] [Google Scholar]Окклюзия маточной артерии для лечения симптоматической миомы матки
JSLS. Июль-сентябрь 2010 г .; 14 (3): 386–390.
, MD, , MD и, MDAdel Helal
Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Абд Эль-Магид Машали
Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Талал Амер
Отделение радиологии, Университетские больницы Мансура, Медицинский факультет, Университет Мансура, Египет.
Адель Хелал, Отделение акушерства и гинекологии, Больницы Университета Мансуры, Медицинский факультет, Университет Мансуры, Египет.
Автор для переписки. Адрес для корреспонденции: Адель Саад Хелал Эль-Сайед, телефон: +20101655174, +20502117358, электронная почта: moc.oohay @ lalehdaasleda Авторские права © 2010, JSLS, Журнал Общества лапароэндоскопических хирургов. Это статья в открытом доступе, распространяемая в соответствии с некоммерческой лицензией Creative Commons Attribution без производных (http://creativecommons.org/licenses/by- nc-nd / 3.0 /), который разрешает некоммерческое использование, распространение и воспроизведение на любом носителе при условии, что оригинальная работа должным образом процитирована и никоим образом не изменена. Эта статья цитируется в других статьях в PMC.Abstract
Цель:
Сравнить эффективность и безопасность окклюзии маточной артерии лапароскопией и эмболизацией в качестве метода лечения симптоматической миомы матки.
Методы:
Обследовано 96 женщин в пременопаузе с симптоматической лейомиомой матки. Никто из них не желал дальнейшей беременности. Они были рандомизированы для лечения либо лапароскопической окклюзией (группа 1), либо радиологической эмболизацией маточных артерий (группа 2). Первичным критерием оценки была удовлетворенность пациентки менструальной кровопотерей по сравнению с потерей до лечения. Вторичные критерии оценки включали послеоперационную боль, осложнения, вторичные вмешательства и неудачи.
Результаты:
Девяносто женщин наблюдались в течение 1, 3, 6 и 12 месяцев после обеих процедур. Первичный результат был сопоставим между двумя группами (86,7% после лапароскопической окклюзии против 88,8% после эмболизации, без статистически значимой разницы). Через 12 месяцев наблюдения у большего числа пациентов возобновились тяжелые периоды в группе окклюзии маточной артерии [4/45 пациенток, 8,8% в группе окклюзии по сравнению с 3/45 (6,6%) в группе эмболизации, P = 0,044].
Заключение:
Как лапароскопическая окклюзия, так и суперселективная эмболизация маточных артерий улучшили клинические симптомы у большинства пациентов.При контрольном наблюдении через 12 месяцев эмболизация может быть более эффективной.
Ключевые слова: Миома матки, Окклюзия маточной артерии, Лапароскопия
ВВЕДЕНИЕ
Лейомиома матки, которая встречается у каждой 4-5 женщин в репродуктивной жизни, является наиболее распространенной солидной опухолью таза у женщин. 1 Нарушения менструального цикла, особенно меноррагия, которая часто приводит к железодефицитной анемии, являются наиболее частыми осложнениями лейомиомы матки. 1
Гистерэктомия — наиболее распространенное лечение симптоматической лейомиомы.Медикаментозное лечение, сочетающее прогестаген и гормональную терапию агонистами гонадотропин-рилизинг-гормона, часто дает обнадеживающие, но временные результаты в виде лейомиомы матки. 2 Хирургические процедуры, включая миомэктомию и гистерэктомию, часто необходимы позже в ходе событий. 3,4 Но помимо рисков, связанных с хирургическими вмешательствами, гистерэктомия может быть причиной эмоциональной травмы. 5,6
По этим причинам спрос на альтернативные методы лечения увеличился за последнее десятилетие как со стороны пациентов, так и со стороны врачей, ищущих менее инвазивные процедуры.Эмболизация лейомиомы матки стала одной из таких альтернативных процедур, а лапароскопическая окклюзия маточных сосудов предлагается в качестве другой.
В предварительном нерандомизированном исследовании 7 авторы сообщили об уменьшении менструального кровотечения и уменьшении объема лейомиомы как после эмболизации лейомиомы матки, так и после лапароскопической окклюзии маточных сосудов. В настоящем рандомизированном исследовании сравнивается клинический результат этих двух методов. Снижение кровотечений через 6 и 12 месяцев, по оценке самих пациентов, было основной переменной результата.Вторичные критерии оценки заключались в собственной оценке пациентами уменьшения симптомов давления, послеоперационной боли и регистрации тошноты по визуальным аналоговым шкалам, времени восстановления, осложнений, вторичных вмешательств и неудач.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводилось в отделении акушерства и гинекологии и отделении радиологии университетской больницы Мансура. Девяносто шесть женщин в пременопаузе, направленных в университетскую клинику по поводу лейомиомы матки и меноррагии или симптомов давления в период с августа 2006 г. по декабрь 2008 г., были включены в это рандомизированное неслепое исследование.Критериями включения были собственная интерпретация женщин в отношении увеличения количества кровотечений, симптомов давления и выраженного желания не делать гистерэктомию. Критериями исключения были подозрение на злокачественное новообразование, субсерозные лейомиомы, которые можно было легко удалить лапароскопической операцией, известный аденомиоз и размер матки, превышающий пупочный. Подслизистые лейомиомы диаметром <3,5 см, расположенные полностью внутриполостно или с интрамуральным расширением> 50%, считались более подходящими для гистероскопической резекции и поэтому были исключены.Кроме того, были исключены женщины, желающие иметь детей, а также те, у кого были противопоказания к операции. Все подходящие пациенты посетили консультацию гинеколога, которая включала гинекологическое обследование, ультразвуковое исследование (предоперационное обследование матки проводилось с помощью ультразвука, который является стандартным методом оценки миомы в нашей больнице). Пациенты были проинформированы о возможных рисках и преимуществах обоих методов лечения. Согласившись на участие, пациенты подписали письменную форму информированного согласия перед проведением рандомизации.Рандомизация 1: 1 проводилась в 10 блоках по 10 пациентов в каждой с использованием запечатанных конвертов. Пять конвертов в каждом блоке из 10 были назначены для лапароскопического лечения и 5 — для эмболизации лейомиомы матки. Конверты в каждом блоке были закрыты, перемешаны, а затем пронумерованы. Лечение было решено путем рисования следующего доступного конверта в порядке возрастания номеров.
Всасывающая эвакуация с использованием двухклапанного шприца IPAS с пластиковой канюлей Кармен № 6 была выполнена всем пациентам для исключения злокачественных новообразований и небольших внутриполостных поражений.
Операцию эмболизации выполнили интервенционные радиологи. Была пунктирована правая бедренная артерия, а маточные артерии интубированы катетером 4F Cobra или микрокатетером. Во всех случаях обе артерии были эмболизированы частицами поливинилового спирта размером от 355 до 500 микрон.
Лапароскопическая двусторонняя окклюзия маточных артерий производилась по стандартной методике, установленной Семме. 8 Маточные артерии и места анастомоза между маточными и яичниковыми артериями были закупорены с помощью зажимов или биполярной коагуляции.Передний лист широкой связки вскрывали ножницами, затем зажимом Мэриленда рассекали широкую связку по направлению к ее основанию. Рассечена крыша мочеточникового канала, проведено скелетирование маточной артерии от мочеточника. Основной ствол маточной артерии перекрыли с помощью 2 зажимов () или с помощью биполярной коагуляции. Затем было выполнено прижигание мест анастомоза между маточной и яичниковой артериями и процедура повторилась с другой стороны.
Боль и тошнота зафиксированы в первые 48 часов после лечения. SEM = стандартная ошибка среднего.
Участникам было рекомендовано использовать один и тот же тип гигиенических прокладок в течение периода исследования. Участники исследования были опрошены относительно имеющихся у них симптомов лейомиомы до лечения и через 1, 3, 6 и 12 месяцев соответственно.
На всех приемах использовалась стандартизированная анкета. Кровотечение оценивалось как «небольшое», «умеренное», «сильное» или «очень сильное».Симптомы давления, включая проблемы с мочеиспусканием, были записаны как «да» или «нет». Участников попросили оценить изменения количества симптомов кровотечения и давления как улучшение, ухудшение или неизменность. Полное облегчение симптомов через 12 месяцев наблюдения определялось как незначительное или умеренное кровотечение и отсутствие симптомов давления. Клиническая неудача определялась как сохраняющиеся симптомы, требующие вторичного лечения или отсутствие улучшения в течение 6-месячного периода наблюдения. Послеоперационная боль и тошнота во время пребывания в больнице регистрировались в послеоперационных картах.Постоянных врачей попросили указать уровень боли и тошноты, которые пациенты испытывали каждые 4 часа в течение первых 24 часов в больнице и каждые 6 часов в течение следующих 24 часов или до тех пор, пока пациент не выпадет из больницы. Режим обезболивания состоял из нестероидных противовоспалительных препаратов и комбинации парацетамол-кодеин в фиксированных дозах.
Нежелательные явления также регистрировались для каждого пациента во время пребывания в больнице и во время амбулаторных посещений через 1, 3, 6 и 12 месяцев.Все последующие хирургические и медицинские вмешательства, а также повторная госпитализация или длительная госпитализация регистрировались как нежелательные явления. Допплеровское исследование маточных артерий было выполнено через 48 часов после процедуры всем участникам.
Статистический анализ был выполнен с помощью SPSS 12.0 (Чикаго, Иллинойс), и данные представлены как средние значения для нормально распределенных данных и как медианные значения для искаженных данных. Двусторонний тест t использовался для сравнения непрерывной переменной в 2 группах пациентов, если рассматриваемая переменная не имела заметно искаженного распределения.Если распределение было заметно искажено, использовали двусторонний критерий Вилкоксона-Манна-Уитни. Для всех тестов использовался уровень значимости 0,05. Мощность исследования и размер выборки были получены с использованием PASS 2008 (анализ мощности и размер выборки, NCSS, Кейсвилл, Юта, США), нам потребовался размер выборки из 90 пациентов, по 45 в каждой группе, достигнув 98% мощности для обнаружения разницы. -1,0, между нулевой гипотезой о том, что средние значения для обеих групп были 0,0, и альтернативной гипотезой о том, что среднее значение для группы 2 было 1,0, с оцененными стандартными отклонениями группы, равными 1.0 и 1,0 и с уровнем значимости (альфа) 0,05000 с использованием двустороннего двухвыборочного теста t . 9,10
РЕЗУЛЬТАТЫ
Из 96 пациентов, рандомизированных и включенных в исследование, 90 пациентов получили лечение, 45 — с двусторонней лапароскопической окклюзией маточных артерий (группа 1) и 45 — с эмболизацией маточных артерий (группа 2). Все участники в каждой группе завершили 12-месячное испытание. Две группы были похожи по возрасту, индексу массы тела, паритету и исходным симптомам.
Число пациенток, сообщивших об уменьшении менструального кровотечения, уменьшении симптомов давления или полном облегчении всех симптомов после лечения, существенно не отличалось между двумя группами лечения () .
Таблица 1.
Клинический результат через 1 год наблюдения
| LOUA (n = 45) | ОАЭ (n = 45) | P | |
|---|---|---|---|
| Уменьшение кровотечения | 39 | 40 | 0.69 |
| Симптомы снижения давления | 35 | 36 | 0,88 |
| Полное снятие давления | 33 | 35 | 0,15 | Все симптомы полностью устранены | 0,18 |
| Удовлетворенность | 36 | 39 | 0,23 |
| Клиническая неудача | 6 | 5 | 0.13 |
Клиническая неудача наблюдалась у 5 (11,2%) пациентов после эмболизации лейомиомы матки и у 6 (13,3%) пациентов после лапароскопической окклюзии. Статистической разницы между двумя группами не было (P = 0,13). Тем не менее, 11 из 90 (12,2%) женщин по-прежнему сообщали о сильном или очень сильном кровотечении через 6 месяцев после лечения: 5 из 45 (11,1%) после эмболизации лейомиомы матки и 6 из 45 (13,3%) после лапароскопического лечения () . Разница в анализе намерения лечиться относительно количества пациентов, сообщивших об сильном кровотечении, была статистически незначимой (P = 0.044). Четыре из этих пациенток, 2 в группе эмболизации лейомиомы матки и 2 в группе лапароскопии, не соответствовали определению клинической неудачи. Все 4 участника сообщили об улучшении симптомов, а также об уменьшении кровотечений и не получали дополнительного лечения в течение периода исследования. Если бы эти 4 участника были добавлены к группе пациентов с клинической неудачей, было бы 5 (11,2%) пациентов после эмболизации лейомиомы матки и 6 (13,3%) после лапароскопии с неблагоприятными результатами через 12 месяцев после лечения (P = 0.094).
Значительно более выраженная боль и тошнота наблюдались после эмболизации лейомиомы матки, чем после лапароскопии. Среднее количество анальгетика, используемого после процедуры эмболизации, было в 4 раза выше, чем после лапароскопической операции: 46 мг по сравнению с 12 мг (P <0,001). Не наблюдалось значительных различий в уменьшении кровотечений между группами лечения через 1 месяц после лечения (P = 0,96). При контрольном наблюдении через 1 месяц у субъектов, получавших эмболизацию маточной артерии, средняя оценка кровотечения снизилась на 88.8% по сравнению с 86,7% для тех, кто лечился лапароскопией. Кроме того, через 3 месяца наблюдения у субъектов, получавших эмболизацию маточной артерии, среднее снижение оценки кровотечения составило 88,9% по сравнению с 84,4% для пациентов, получавших лапароскопию () , в то время как через 6 месяцев после эмболизации лейомиомы матки , уменьшение по-прежнему составляло 88,9%, а соответствующее уменьшение при лапароскопическом лечении составило 86,7% () . Через 12 месяцев наблюдения результаты составили 91,9% против 93,3% в группе 1 и группе 2 соответственно () .
Таблица 2.
Побочные явления после лечения через 3, 6 и 12 месяцев наблюдения
| LUAO | UAE | P | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 6 м | 12 м | 3 м | 6 м | 12 м | ||||||||||
| Меноррагия | 4 | 3 | 2 | 3 | 3 | 3 | 2 | 2 | 3 | 2 | 1.00 | |||
| Рецидивирующие симптомы давления | 0 | 1 | 2 | 1 | 2 | 2 | 0,19 | |||||||
| Всего | 7 | 7 | 7 | 7 | 5 | 0,12 | ||||||||
Наблюдались только незначительные внутрибольничные побочные эффекты. Пациенты должны были оставаться в отделении до 48 часов после лечения.
Двадцать две пациентки отметили усиление выделений из влагалища в послеоперационный период, возможно, из-за пропуска подслизистых или внутриутробных опухолей у этих пациентов.Не наблюдалось значительных различий в доле женщин с выделениями из влагалища, продолжавшимися до 7 дней. Наиболее серьезное нежелательное явление, односторонний тромбоз глубоких вен, произошло у одного пациента, который был повторно госпитализирован через 1 неделю после лапароскопической двусторонней окклюзии.
ОБСУЖДЕНИЕ
Основная цель настоящего исследования заключалась в сравнении улучшения характера кровотечений при эмболизации маточной артерии и лапароскопической окклюзии. Не было обнаружено значительной разницы в уменьшении симптомов между двумя вариантами лечения через 12 месяцев после лечения.
В литературе в одном дополнительном исследовании 11 сообщается с использованием графической таблицы оценки кровотечения у 76 пациентов, получавших эмболизацию, и сообщается об улучшении на 55,6% через 3 месяца и 58,1% через 6 месяцев, что значительно меньше, чем в нашем исследовании.
Собственная оценка облегчения симптомов пациентом чаще используется в качестве параметра исхода, чем графическая таблица оценки кровотечения, даже несмотря на отсутствие единообразия в определении степени улучшения.Несмотря на эти ограничения, настоящие результаты, основанные на собственной оценке пациентов через 6 месяцев после эмболизации артерии лейомиомы матки, аналогичны результатам других исследований. 2,3,5,6,11 Уменьшение симптомов менструального кровотечения у 93,3% и 91,9% пациенток после эмболизации лейомиомы матки и лапароскопической окклюзии соответственно в этом исследовании соответствует краткосрочным результатам 2 крупнейших проспективных одноцентровых исследования по оценке эмболизации лейомиомы матки на сегодняшний день, которые сообщили об улучшении меноррагии у 89% пациентов через 6 месяцев и у 84% через 16 месяцев, соответственно. 6,11 Кроме того, уменьшение количества кровотечений у 91,9% пациентов после двусторонней лапароскопической окклюзии в этом исследовании аналогично таковому в других исследованиях, в которых сообщается об улучшении этих симптомов примерно у 90% участников.
В отличие от отсутствия разницы между двумя группами лечения в отношении процентного снижения собственной оценки кровотечения пациентами, значительно больше участников сообщили о сильном или очень сильном кровотечении через 6 месяцев после лапароскопического лечения.Одним из возможных объяснений этого несоответствия могут быть различия в оценке кровотечения.
Есть несколько возможных объяснений несколько менее благоприятных результатов после лапароскопического лечения. В литературе ангиографические и хирургические исследования показали многочисленные анатомические вариации маточных артерий. 12,13 Таким образом, можно перекрыть не ту артерию при лапароскопии или пропустить одну артерию в случаях, когда на одной стороне две артерии вместо одной.Причина неудачи — недостаточная окклюзия маточной артерии с одной стороны.
Коллатеральное артериальное кровоснабжение матки в целом может объяснить меньшую боль после хирургической окклюзии маточной артерии, несмотря на ишемию и инфаркт лейомиомы. Поскольку эмболизация представляет собой более дистальную окклюзию, уменьшающую коллатеральный кровоток, можно ожидать увеличения ишемии матки, что приводит к усилению боли и потенциально большей эффективности по сравнению с проксимальной хирургической окклюзией.Интервенционные радиологи выражают опасения, что лейомиомы, у которых не полностью инфаркт инфаркта, могут вырасти снова. 13 В 2 проспективных исследованиях было обнаружено 16% 14 и 20% 15 рецидивов от 5 до 7 лет после эмболизации. Если бы меньшее количество боли после лапароскопии было вызвано меньшей ишемией и, следовательно, неполным инфарктом лейомиомы, можно было бы ожидать еще большего количества рецидивов со временем после лапароскопической окклюзии.
Доля пациентов, которым потребовалось вторичное хирургическое вмешательство, составила 5 (11.2%) в группе ОАЭ и 6 (13,3%) в группе LOUA в нашем исследовании. Это соотношение соответствует другим зарегистрированным исходам после эмболизации лейомиомы матки или лапароскопической окклюзии. В 2 более крупных исследованиях последующие вмешательства или повторная госпитализация произошли в 10,5% через 21 месяц 6 и в 7,5% через 17 месяцев, 11 соответственно. В обоих этих исследованиях основные показания для вторичной хирургии были аналогичны показаниям в этом исследовании: продолжающаяся меноррагия или симптомы, связанные с изгнанием лейомиомы.Отбор пациентов, вероятно, наиболее важен для получения положительных результатов, и более тщательный отбор может снизить количество случаев вторичной хирургии, вызванной стойкой меноррагией или изгнанием лейомиомы.
На основании этого исследования, как лапароскопическая окклюзия маточного сосуда, так и эмболизация, по-видимому, улучшают симптомы, связанные с лейомиомой матки у большинства пациентов. Лапароскопическая процедура привела к уменьшению послеоперационной боли и тошноты и более короткому пребыванию в больнице, хотя значительно больше участников испытали сильное менструальное кровотечение через 6 месяцев после лапароскопической окклюзии, что указывает на более благоприятный эффект после эмболизации лейомиомы матки.В свете этих результатов и с учетом значительного риска хирургических осложнений и отсутствия долгосрочных результатов, учитывая тот факт, что лапароскопические методы применяются в области гинекологической хирургии, лапароскопическая окклюзия маточной артерии, вероятно, вызовет значительный интерес как метод лечения. эффективная альтернатива гистерэктомии при симптоматической лейомиоме матки.
ЗАКЛЮЧЕНИЕ
Для успешной лапароскопической окклюзии маточной артерии хирург должен иметь необходимые лапароскопические навыки и уметь точно определить местонахождение маточной артерии для правильной перевязки сосудов.Если эти предпосылки не соблюдены, массивное кровотечение может потребовать лапаротомии; Следовательно, лапароскопическая процедура лечения лейомиомы должна проводиться только в центрах, имеющих соответствующий опыт в лапароскопической хирургии.
Информация для авторов
Адель Хелал, Отделение акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Абд Эль-Магид Машали, Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Талал Амер, отделение радиологии, больницы университета Мансура, медицинский факультет, университет Мансура, Египет.
Каталожные номера:
1. Волленховен Б.Дж., Лоуренс А.С., Хили Д. Миома матки: клинический обзор. Br J Obstet Gynecol. 1990; 97: 285–298 [PubMed] [Google Scholar] 2. Уортингтон-Кирш Р.Л., Попки Г.Л., Хатчинс Флорида. Эмболизация маточной артерии для лечения лейомиом: оценка качества жизни и клинический ответ. Радиология. 1998; 208: 225–229 [PubMed] [Google Scholar] 3.Гудвин С.К., Маклукас Б., Ли М. и др. Эмболизация маточной артерии для лечения лейомиомы матки в среднесрочных результатах. J Vasc Interv Radiol. 1999; 10: 1159–1165 [PubMed] [Google Scholar] 4. Хили Д., Волленховен Б.Дж. Роль агонистов ГнРГ в лечении миомы матки. Br J Obstet Gynecol. 1992; 99: 23–26 [PubMed] [Google Scholar] 5. Пелаж Дж. П., Ле Дреф О, Сойер П. и др. Меноррагия, связанная с миомой: лечение с помощью суперселективной эмболизации маточных артерий и промежуточное наблюдение.Радиология. 2000; 215: 228–231 [PubMed] [Google Scholar] 6. Шпионы Дж. Б., Ашер С. А., Рот А. Р., Ким Дж., Леви Э. Б., Гомес-Хорхе Дж. Эмболизация маточной артерии при лейомиомах. Obstet Gynecol. 2001; 98: 29–34 [PubMed] [Google Scholar] 7. Hald K, Langebrekke A, Klow NE, Noreng HJ, Berge AB, Istre O. Лапароскопическая окклюзия маточных сосудов для лечения симптоматической миомы: первоначальный опыт и сравнение с эмболизацией маточной артерии. Am J Obstet Gynecol. 2004; 190: 37–43 [PubMed] [Google Scholar] 8. Семм К., Меттлер Л.Технический прогресс в хирургии органов малого таза с помощью оперативной лапароскопии. Am J Obstet Gynecol. 1980; 138: 121. [PubMed] [Google Scholar] 9. Машин Д., Кэмпбелл М., Файерс П., Пинол А. Таблицы размеров выборки для клинических исследований. 2-е изд Мальден, Массачусетс: наука Блэквелла; 1997 [Google Scholar] 10. Зар Джеррольд Х. Биостатистический анализ. 2-е изд Энглвуд Клиффс, Нью-Джерси; Прентис-Холл; 1984 [Google Scholar] 11. Спис Дж. Б., Купер Дж. М., Уортингтон-Кирш Р., Липман Дж. К., Миллс Б. Б., Бененати Дж. Ф. Исход эмболизации матки и гистерэктомии по поводу лейомиомы: результаты многоцентрового исследования.Am J Obstet Gynecol. 2004; 191: 22–31 [PubMed] [Google Scholar] 12. Уокер WJ, Pelage JP. Эмболизация маточной артерии при симптоматической миоме: клинические результаты у 400 женщин с последующей визуализацией. BJOG. 2002; 109: 1262–1272 [PubMed] [Google Scholar] 13. Голуб З., Лукач Дж., Климент Л., Урбанек С. Вариабельность происхождения маточной артерии: лапароскопическое хирургическое наблюдение. J Obstet Gynaecol Res. 2005; 31: 158–163 [PubMed] [Google Scholar] 14. Гомес-Хорхе Дж., Кейунг А., Леви Э. Б., Шпионы Дж. Б.. Анатомия маточной артерии, имеющая отношение к эмболизации лейомиомы матки.Cardiovasc Intervent Radiol. 2003; 26: 522–527 [PubMed] [Google Scholar] 15. Iverson RE, Chelmow D, Strohbehn K, Waldman L, Evantash EG. Относительная заболеваемость и смертность после абдоминальной гистерэктомии и миомэктомии для лечения лейомиомы матки. Obstet Gynecol. 1996; 88: 415–419 [PubMed] [Google Scholar]Окклюзия маточной артерии для лечения симптоматической миомы матки
JSLS. Июль-сентябрь 2010 г .; 14 (3): 386–390.
, MD, , MD и, MDAdel Helal
Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Абд Эль-Магид Машали
Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Талал Амер
Отделение радиологии, Университетские больницы Мансура, Медицинский факультет, Университет Мансура, Египет.
Адель Хелал, Отделение акушерства и гинекологии, Больницы Университета Мансуры, Медицинский факультет, Университет Мансуры, Египет.
Автор для переписки. Адрес для корреспонденции: Адель Саад Хелал Эль-Сайед, телефон: +20101655174, +20502117358, электронная почта: moc.oohay @ lalehdaasleda Авторские права © 2010, JSLS, Журнал Общества лапароэндоскопических хирургов. Это статья в открытом доступе, распространяемая в соответствии с некоммерческой лицензией Creative Commons Attribution без производных (http://creativecommons.org/licenses/by- nc-nd / 3.0 /), который разрешает некоммерческое использование, распространение и воспроизведение на любом носителе при условии, что оригинальная работа должным образом процитирована и никоим образом не изменена. Эта статья цитируется в других статьях в PMC.Abstract
Цель:
Сравнить эффективность и безопасность окклюзии маточной артерии лапароскопией и эмболизацией в качестве метода лечения симптоматической миомы матки.
Методы:
Обследовано 96 женщин в пременопаузе с симптоматической лейомиомой матки. Никто из них не желал дальнейшей беременности. Они были рандомизированы для лечения либо лапароскопической окклюзией (группа 1), либо радиологической эмболизацией маточных артерий (группа 2). Первичным критерием оценки была удовлетворенность пациентки менструальной кровопотерей по сравнению с потерей до лечения. Вторичные критерии оценки включали послеоперационную боль, осложнения, вторичные вмешательства и неудачи.
Результаты:
Девяносто женщин наблюдались в течение 1, 3, 6 и 12 месяцев после обеих процедур. Первичный результат был сопоставим между двумя группами (86,7% после лапароскопической окклюзии против 88,8% после эмболизации, без статистически значимой разницы). Через 12 месяцев наблюдения у большего числа пациентов возобновились тяжелые периоды в группе окклюзии маточной артерии [4/45 пациенток, 8,8% в группе окклюзии по сравнению с 3/45 (6,6%) в группе эмболизации, P = 0,044].
Заключение:
Как лапароскопическая окклюзия, так и суперселективная эмболизация маточных артерий улучшили клинические симптомы у большинства пациентов.При контрольном наблюдении через 12 месяцев эмболизация может быть более эффективной.
Ключевые слова: Миома матки, Окклюзия маточной артерии, Лапароскопия
ВВЕДЕНИЕ
Лейомиома матки, которая встречается у каждой 4-5 женщин в репродуктивной жизни, является наиболее распространенной солидной опухолью таза у женщин. 1 Нарушения менструального цикла, особенно меноррагия, которая часто приводит к железодефицитной анемии, являются наиболее частыми осложнениями лейомиомы матки. 1
Гистерэктомия — наиболее распространенное лечение симптоматической лейомиомы.Медикаментозное лечение, сочетающее прогестаген и гормональную терапию агонистами гонадотропин-рилизинг-гормона, часто дает обнадеживающие, но временные результаты в виде лейомиомы матки. 2 Хирургические процедуры, включая миомэктомию и гистерэктомию, часто необходимы позже в ходе событий. 3,4 Но помимо рисков, связанных с хирургическими вмешательствами, гистерэктомия может быть причиной эмоциональной травмы. 5,6
По этим причинам спрос на альтернативные методы лечения увеличился за последнее десятилетие как со стороны пациентов, так и со стороны врачей, ищущих менее инвазивные процедуры.Эмболизация лейомиомы матки стала одной из таких альтернативных процедур, а лапароскопическая окклюзия маточных сосудов предлагается в качестве другой.
В предварительном нерандомизированном исследовании 7 авторы сообщили об уменьшении менструального кровотечения и уменьшении объема лейомиомы как после эмболизации лейомиомы матки, так и после лапароскопической окклюзии маточных сосудов. В настоящем рандомизированном исследовании сравнивается клинический результат этих двух методов. Снижение кровотечений через 6 и 12 месяцев, по оценке самих пациентов, было основной переменной результата.Вторичные критерии оценки заключались в собственной оценке пациентами уменьшения симптомов давления, послеоперационной боли и регистрации тошноты по визуальным аналоговым шкалам, времени восстановления, осложнений, вторичных вмешательств и неудач.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводилось в отделении акушерства и гинекологии и отделении радиологии университетской больницы Мансура. Девяносто шесть женщин в пременопаузе, направленных в университетскую клинику по поводу лейомиомы матки и меноррагии или симптомов давления в период с августа 2006 г. по декабрь 2008 г., были включены в это рандомизированное неслепое исследование.Критериями включения были собственная интерпретация женщин в отношении увеличения количества кровотечений, симптомов давления и выраженного желания не делать гистерэктомию. Критериями исключения были подозрение на злокачественное новообразование, субсерозные лейомиомы, которые можно было легко удалить лапароскопической операцией, известный аденомиоз и размер матки, превышающий пупочный. Подслизистые лейомиомы диаметром <3,5 см, расположенные полностью внутриполостно или с интрамуральным расширением> 50%, считались более подходящими для гистероскопической резекции и поэтому были исключены.Кроме того, были исключены женщины, желающие иметь детей, а также те, у кого были противопоказания к операции. Все подходящие пациенты посетили консультацию гинеколога, которая включала гинекологическое обследование, ультразвуковое исследование (предоперационное обследование матки проводилось с помощью ультразвука, который является стандартным методом оценки миомы в нашей больнице). Пациенты были проинформированы о возможных рисках и преимуществах обоих методов лечения. Согласившись на участие, пациенты подписали письменную форму информированного согласия перед проведением рандомизации.Рандомизация 1: 1 проводилась в 10 блоках по 10 пациентов в каждой с использованием запечатанных конвертов. Пять конвертов в каждом блоке из 10 были назначены для лапароскопического лечения и 5 — для эмболизации лейомиомы матки. Конверты в каждом блоке были закрыты, перемешаны, а затем пронумерованы. Лечение было решено путем рисования следующего доступного конверта в порядке возрастания номеров.
Всасывающая эвакуация с использованием двухклапанного шприца IPAS с пластиковой канюлей Кармен № 6 была выполнена всем пациентам для исключения злокачественных новообразований и небольших внутриполостных поражений.
Операцию эмболизации выполнили интервенционные радиологи. Была пунктирована правая бедренная артерия, а маточные артерии интубированы катетером 4F Cobra или микрокатетером. Во всех случаях обе артерии были эмболизированы частицами поливинилового спирта размером от 355 до 500 микрон.
Лапароскопическая двусторонняя окклюзия маточных артерий производилась по стандартной методике, установленной Семме. 8 Маточные артерии и места анастомоза между маточными и яичниковыми артериями были закупорены с помощью зажимов или биполярной коагуляции.Передний лист широкой связки вскрывали ножницами, затем зажимом Мэриленда рассекали широкую связку по направлению к ее основанию. Рассечена крыша мочеточникового канала, проведено скелетирование маточной артерии от мочеточника. Основной ствол маточной артерии перекрыли с помощью 2 зажимов () или с помощью биполярной коагуляции. Затем было выполнено прижигание мест анастомоза между маточной и яичниковой артериями и процедура повторилась с другой стороны.
Боль и тошнота зафиксированы в первые 48 часов после лечения. SEM = стандартная ошибка среднего.
Участникам было рекомендовано использовать один и тот же тип гигиенических прокладок в течение периода исследования. Участники исследования были опрошены относительно имеющихся у них симптомов лейомиомы до лечения и через 1, 3, 6 и 12 месяцев соответственно.
На всех приемах использовалась стандартизированная анкета. Кровотечение оценивалось как «небольшое», «умеренное», «сильное» или «очень сильное».Симптомы давления, включая проблемы с мочеиспусканием, были записаны как «да» или «нет». Участников попросили оценить изменения количества симптомов кровотечения и давления как улучшение, ухудшение или неизменность. Полное облегчение симптомов через 12 месяцев наблюдения определялось как незначительное или умеренное кровотечение и отсутствие симптомов давления. Клиническая неудача определялась как сохраняющиеся симптомы, требующие вторичного лечения или отсутствие улучшения в течение 6-месячного периода наблюдения. Послеоперационная боль и тошнота во время пребывания в больнице регистрировались в послеоперационных картах.Постоянных врачей попросили указать уровень боли и тошноты, которые пациенты испытывали каждые 4 часа в течение первых 24 часов в больнице и каждые 6 часов в течение следующих 24 часов или до тех пор, пока пациент не выпадет из больницы. Режим обезболивания состоял из нестероидных противовоспалительных препаратов и комбинации парацетамол-кодеин в фиксированных дозах.
Нежелательные явления также регистрировались для каждого пациента во время пребывания в больнице и во время амбулаторных посещений через 1, 3, 6 и 12 месяцев.Все последующие хирургические и медицинские вмешательства, а также повторная госпитализация или длительная госпитализация регистрировались как нежелательные явления. Допплеровское исследование маточных артерий было выполнено через 48 часов после процедуры всем участникам.
Статистический анализ был выполнен с помощью SPSS 12.0 (Чикаго, Иллинойс), и данные представлены как средние значения для нормально распределенных данных и как медианные значения для искаженных данных. Двусторонний тест t использовался для сравнения непрерывной переменной в 2 группах пациентов, если рассматриваемая переменная не имела заметно искаженного распределения.Если распределение было заметно искажено, использовали двусторонний критерий Вилкоксона-Манна-Уитни. Для всех тестов использовался уровень значимости 0,05. Мощность исследования и размер выборки были получены с использованием PASS 2008 (анализ мощности и размер выборки, NCSS, Кейсвилл, Юта, США), нам потребовался размер выборки из 90 пациентов, по 45 в каждой группе, достигнув 98% мощности для обнаружения разницы. -1,0, между нулевой гипотезой о том, что средние значения для обеих групп были 0,0, и альтернативной гипотезой о том, что среднее значение для группы 2 было 1,0, с оцененными стандартными отклонениями группы, равными 1.0 и 1,0 и с уровнем значимости (альфа) 0,05000 с использованием двустороннего двухвыборочного теста t . 9,10
РЕЗУЛЬТАТЫ
Из 96 пациентов, рандомизированных и включенных в исследование, 90 пациентов получили лечение, 45 — с двусторонней лапароскопической окклюзией маточных артерий (группа 1) и 45 — с эмболизацией маточных артерий (группа 2). Все участники в каждой группе завершили 12-месячное испытание. Две группы были похожи по возрасту, индексу массы тела, паритету и исходным симптомам.
Число пациенток, сообщивших об уменьшении менструального кровотечения, уменьшении симптомов давления или полном облегчении всех симптомов после лечения, существенно не отличалось между двумя группами лечения () .
Таблица 1.
Клинический результат через 1 год наблюдения
| LOUA (n = 45) | ОАЭ (n = 45) | P | |
|---|---|---|---|
| Уменьшение кровотечения | 39 | 40 | 0.69 |
| Симптомы снижения давления | 35 | 36 | 0,88 |
| Полное снятие давления | 33 | 35 | 0,15 | Все симптомы полностью устранены | 0,18 |
| Удовлетворенность | 36 | 39 | 0,23 |
| Клиническая неудача | 6 | 5 | 0.13 |
Клиническая неудача наблюдалась у 5 (11,2%) пациентов после эмболизации лейомиомы матки и у 6 (13,3%) пациентов после лапароскопической окклюзии. Статистической разницы между двумя группами не было (P = 0,13). Тем не менее, 11 из 90 (12,2%) женщин по-прежнему сообщали о сильном или очень сильном кровотечении через 6 месяцев после лечения: 5 из 45 (11,1%) после эмболизации лейомиомы матки и 6 из 45 (13,3%) после лапароскопического лечения () . Разница в анализе намерения лечиться относительно количества пациентов, сообщивших об сильном кровотечении, была статистически незначимой (P = 0.044). Четыре из этих пациенток, 2 в группе эмболизации лейомиомы матки и 2 в группе лапароскопии, не соответствовали определению клинической неудачи. Все 4 участника сообщили об улучшении симптомов, а также об уменьшении кровотечений и не получали дополнительного лечения в течение периода исследования. Если бы эти 4 участника были добавлены к группе пациентов с клинической неудачей, было бы 5 (11,2%) пациентов после эмболизации лейомиомы матки и 6 (13,3%) после лапароскопии с неблагоприятными результатами через 12 месяцев после лечения (P = 0.094).
Значительно более выраженная боль и тошнота наблюдались после эмболизации лейомиомы матки, чем после лапароскопии. Среднее количество анальгетика, используемого после процедуры эмболизации, было в 4 раза выше, чем после лапароскопической операции: 46 мг по сравнению с 12 мг (P <0,001). Не наблюдалось значительных различий в уменьшении кровотечений между группами лечения через 1 месяц после лечения (P = 0,96). При контрольном наблюдении через 1 месяц у субъектов, получавших эмболизацию маточной артерии, средняя оценка кровотечения снизилась на 88.8% по сравнению с 86,7% для тех, кто лечился лапароскопией. Кроме того, через 3 месяца наблюдения у субъектов, получавших эмболизацию маточной артерии, среднее снижение оценки кровотечения составило 88,9% по сравнению с 84,4% для пациентов, получавших лапароскопию () , в то время как через 6 месяцев после эмболизации лейомиомы матки , уменьшение по-прежнему составляло 88,9%, а соответствующее уменьшение при лапароскопическом лечении составило 86,7% () . Через 12 месяцев наблюдения результаты составили 91,9% против 93,3% в группе 1 и группе 2 соответственно () .
Таблица 2.
Побочные явления после лечения через 3, 6 и 12 месяцев наблюдения
| LUAO | UAE | P | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 6 м | 12 м | 3 м | 6 м | 12 м | ||||||||||
| Меноррагия | 4 | 3 | 2 | 3 | 3 | 3 | 2 | 2 | 3 | 2 | 1.00 | |||
| Рецидивирующие симптомы давления | 0 | 1 | 2 | 1 | 2 | 2 | 0,19 | |||||||
| Всего | 7 | 7 | 7 | 7 | 5 | 0,12 | ||||||||
Наблюдались только незначительные внутрибольничные побочные эффекты. Пациенты должны были оставаться в отделении до 48 часов после лечения.
Двадцать две пациентки отметили усиление выделений из влагалища в послеоперационный период, возможно, из-за пропуска подслизистых или внутриутробных опухолей у этих пациентов.Не наблюдалось значительных различий в доле женщин с выделениями из влагалища, продолжавшимися до 7 дней. Наиболее серьезное нежелательное явление, односторонний тромбоз глубоких вен, произошло у одного пациента, который был повторно госпитализирован через 1 неделю после лапароскопической двусторонней окклюзии.
ОБСУЖДЕНИЕ
Основная цель настоящего исследования заключалась в сравнении улучшения характера кровотечений при эмболизации маточной артерии и лапароскопической окклюзии. Не было обнаружено значительной разницы в уменьшении симптомов между двумя вариантами лечения через 12 месяцев после лечения.
В литературе в одном дополнительном исследовании 11 сообщается с использованием графической таблицы оценки кровотечения у 76 пациентов, получавших эмболизацию, и сообщается об улучшении на 55,6% через 3 месяца и 58,1% через 6 месяцев, что значительно меньше, чем в нашем исследовании.
Собственная оценка облегчения симптомов пациентом чаще используется в качестве параметра исхода, чем графическая таблица оценки кровотечения, даже несмотря на отсутствие единообразия в определении степени улучшения.Несмотря на эти ограничения, настоящие результаты, основанные на собственной оценке пациентов через 6 месяцев после эмболизации артерии лейомиомы матки, аналогичны результатам других исследований. 2,3,5,6,11 Уменьшение симптомов менструального кровотечения у 93,3% и 91,9% пациенток после эмболизации лейомиомы матки и лапароскопической окклюзии соответственно в этом исследовании соответствует краткосрочным результатам 2 крупнейших проспективных одноцентровых исследования по оценке эмболизации лейомиомы матки на сегодняшний день, которые сообщили об улучшении меноррагии у 89% пациентов через 6 месяцев и у 84% через 16 месяцев, соответственно. 6,11 Кроме того, уменьшение количества кровотечений у 91,9% пациентов после двусторонней лапароскопической окклюзии в этом исследовании аналогично таковому в других исследованиях, в которых сообщается об улучшении этих симптомов примерно у 90% участников.
В отличие от отсутствия разницы между двумя группами лечения в отношении процентного снижения собственной оценки кровотечения пациентами, значительно больше участников сообщили о сильном или очень сильном кровотечении через 6 месяцев после лапароскопического лечения.Одним из возможных объяснений этого несоответствия могут быть различия в оценке кровотечения.
Есть несколько возможных объяснений несколько менее благоприятных результатов после лапароскопического лечения. В литературе ангиографические и хирургические исследования показали многочисленные анатомические вариации маточных артерий. 12,13 Таким образом, можно перекрыть не ту артерию при лапароскопии или пропустить одну артерию в случаях, когда на одной стороне две артерии вместо одной.Причина неудачи — недостаточная окклюзия маточной артерии с одной стороны.
Коллатеральное артериальное кровоснабжение матки в целом может объяснить меньшую боль после хирургической окклюзии маточной артерии, несмотря на ишемию и инфаркт лейомиомы. Поскольку эмболизация представляет собой более дистальную окклюзию, уменьшающую коллатеральный кровоток, можно ожидать увеличения ишемии матки, что приводит к усилению боли и потенциально большей эффективности по сравнению с проксимальной хирургической окклюзией.Интервенционные радиологи выражают опасения, что лейомиомы, у которых не полностью инфаркт инфаркта, могут вырасти снова. 13 В 2 проспективных исследованиях было обнаружено 16% 14 и 20% 15 рецидивов от 5 до 7 лет после эмболизации. Если бы меньшее количество боли после лапароскопии было вызвано меньшей ишемией и, следовательно, неполным инфарктом лейомиомы, можно было бы ожидать еще большего количества рецидивов со временем после лапароскопической окклюзии.
Доля пациентов, которым потребовалось вторичное хирургическое вмешательство, составила 5 (11.2%) в группе ОАЭ и 6 (13,3%) в группе LOUA в нашем исследовании. Это соотношение соответствует другим зарегистрированным исходам после эмболизации лейомиомы матки или лапароскопической окклюзии. В 2 более крупных исследованиях последующие вмешательства или повторная госпитализация произошли в 10,5% через 21 месяц 6 и в 7,5% через 17 месяцев, 11 соответственно. В обоих этих исследованиях основные показания для вторичной хирургии были аналогичны показаниям в этом исследовании: продолжающаяся меноррагия или симптомы, связанные с изгнанием лейомиомы.Отбор пациентов, вероятно, наиболее важен для получения положительных результатов, и более тщательный отбор может снизить количество случаев вторичной хирургии, вызванной стойкой меноррагией или изгнанием лейомиомы.
На основании этого исследования, как лапароскопическая окклюзия маточного сосуда, так и эмболизация, по-видимому, улучшают симптомы, связанные с лейомиомой матки у большинства пациентов. Лапароскопическая процедура привела к уменьшению послеоперационной боли и тошноты и более короткому пребыванию в больнице, хотя значительно больше участников испытали сильное менструальное кровотечение через 6 месяцев после лапароскопической окклюзии, что указывает на более благоприятный эффект после эмболизации лейомиомы матки.В свете этих результатов и с учетом значительного риска хирургических осложнений и отсутствия долгосрочных результатов, учитывая тот факт, что лапароскопические методы применяются в области гинекологической хирургии, лапароскопическая окклюзия маточной артерии, вероятно, вызовет значительный интерес как метод лечения. эффективная альтернатива гистерэктомии при симптоматической лейомиоме матки.
ЗАКЛЮЧЕНИЕ
Для успешной лапароскопической окклюзии маточной артерии хирург должен иметь необходимые лапароскопические навыки и уметь точно определить местонахождение маточной артерии для правильной перевязки сосудов.Если эти предпосылки не соблюдены, массивное кровотечение может потребовать лапаротомии; Следовательно, лапароскопическая процедура лечения лейомиомы должна проводиться только в центрах, имеющих соответствующий опыт в лапароскопической хирургии.
Информация для авторов
Адель Хелал, Отделение акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Абд Эль-Магид Машали, Кафедра акушерства и гинекологии, Больницы Университета Мансура, Медицинский факультет, Университет Мансура, Египет.
Талал Амер, отделение радиологии, больницы университета Мансура, медицинский факультет, университет Мансура, Египет.
Каталожные номера:
1. Волленховен Б.Дж., Лоуренс А.С., Хили Д. Миома матки: клинический обзор. Br J Obstet Gynecol. 1990; 97: 285–298 [PubMed] [Google Scholar] 2. Уортингтон-Кирш Р.Л., Попки Г.Л., Хатчинс Флорида. Эмболизация маточной артерии для лечения лейомиом: оценка качества жизни и клинический ответ. Радиология. 1998; 208: 225–229 [PubMed] [Google Scholar] 3.Гудвин С.К., Маклукас Б., Ли М. и др. Эмболизация маточной артерии для лечения лейомиомы матки в среднесрочных результатах. J Vasc Interv Radiol. 1999; 10: 1159–1165 [PubMed] [Google Scholar] 4. Хили Д., Волленховен Б.Дж. Роль агонистов ГнРГ в лечении миомы матки. Br J Obstet Gynecol. 1992; 99: 23–26 [PubMed] [Google Scholar] 5. Пелаж Дж. П., Ле Дреф О, Сойер П. и др. Меноррагия, связанная с миомой: лечение с помощью суперселективной эмболизации маточных артерий и промежуточное наблюдение.Радиология. 2000; 215: 228–231 [PubMed] [Google Scholar] 6. Шпионы Дж. Б., Ашер С. А., Рот А. Р., Ким Дж., Леви Э. Б., Гомес-Хорхе Дж. Эмболизация маточной артерии при лейомиомах. Obstet Gynecol. 2001; 98: 29–34 [PubMed] [Google Scholar] 7. Hald K, Langebrekke A, Klow NE, Noreng HJ, Berge AB, Istre O. Лапароскопическая окклюзия маточных сосудов для лечения симптоматической миомы: первоначальный опыт и сравнение с эмболизацией маточной артерии. Am J Obstet Gynecol. 2004; 190: 37–43 [PubMed] [Google Scholar] 8. Семм К., Меттлер Л.Технический прогресс в хирургии органов малого таза с помощью оперативной лапароскопии. Am J Obstet Gynecol. 1980; 138: 121. [PubMed] [Google Scholar] 9. Машин Д., Кэмпбелл М., Файерс П., Пинол А. Таблицы размеров выборки для клинических исследований. 2-е изд Мальден, Массачусетс: наука Блэквелла; 1997 [Google Scholar] 10. Зар Джеррольд Х. Биостатистический анализ. 2-е изд Энглвуд Клиффс, Нью-Джерси; Прентис-Холл; 1984 [Google Scholar] 11. Спис Дж. Б., Купер Дж. М., Уортингтон-Кирш Р., Липман Дж. К., Миллс Б. Б., Бененати Дж. Ф. Исход эмболизации матки и гистерэктомии по поводу лейомиомы: результаты многоцентрового исследования.Am J Obstet Gynecol. 2004; 191: 22–31 [PubMed] [Google Scholar] 12. Уокер WJ, Pelage JP. Эмболизация маточной артерии при симптоматической миоме: клинические результаты у 400 женщин с последующей визуализацией. BJOG. 2002; 109: 1262–1272 [PubMed] [Google Scholar] 13. Голуб З., Лукач Дж., Климент Л., Урбанек С. Вариабельность происхождения маточной артерии: лапароскопическое хирургическое наблюдение. J Obstet Gynaecol Res. 2005; 31: 158–163 [PubMed] [Google Scholar] 14. Гомес-Хорхе Дж., Кейунг А., Леви Э. Б., Шпионы Дж. Б.. Анатомия маточной артерии, имеющая отношение к эмболизации лейомиомы матки.Cardiovasc Intervent Radiol. 2003; 26: 522–527 [PubMed] [Google Scholar] 15. Iverson RE, Chelmow D, Strohbehn K, Waldman L, Evantash EG. Относительная заболеваемость и смертность после абдоминальной гистерэктомии и миомэктомии для лечения лейомиомы матки. Obstet Gynecol. 1996; 88: 415–419 [PubMed] [Google Scholar]Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookieЭтот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера на прием файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
| Дания | |
| Больница Выборгского округа | |
| Выборг, Дания, DK-8800 | |
| Франция | |
| Университетская больница | |
| Angers cedex, France, 49033 | |
| Service de Gynecologie Obsterique, Hopital Antoine Beclere | |
| Clamart Cedex, France, 92414 | |
| Maternite les Bazennes | |
| Dunkerque, France, 59430 | |
| CHRU de Lille, Hopital Jeanne de Flandre | |
| Lille Cedex, France, 59037 | |
| Германия | |
| Universitaeklinikum Erlangen | |
| Эрланген, Германия, | |
| Universitats-Frauenklinik Tubingen | |
| Тюбинген, Германия, 72076 | |
| Нидерланды | |
| Медицинский центр VU | |
| Амстердам, Нидерланды, 1081 HV | |
| Норвегия | |
| Ullevaal University | |
| Осло, Норвегия, N-0407 | |
| Швейцария | |
| Universitats-Frauenklinik | |
| Берн, Швейцария, 3012 | |
| Соединенное Королевство | |
| Материнство M1, Королевский лазарет Брэдфорда | |
| Брэдфорд, Соединенное Королевство, BD9 6RJ | |
| Госпиталь для женщин и детей Халла и Восточного Йоркшира | |
| Халл, Великобритания, HU3 2JZ | |
| Больница Элизабет Гаррет Андерсон | |
| Лондон, Великобритания, WC1E 6DH | |
| Больница королевы Елизаветы и королевы-матери | |
| Маргейт, Соединенное Королевство, CT9 4AN | |
Временная окклюзия маточной артерии для лечения меноррагии и миомы матки с использованием трансвагинального зажима без разреза под контролем Доплера: клинический случай | Репродукция человека
Аннотация
Мы сообщаем об успешном лечении 43-летней женщины с меноррагией и множественной миомой матки путем временной окклюзии маточной артерии.С помощью трансвагинального зажима с допплеровским контролем маточные артерии были идентифицированы неинвазивно и перекрыты механическим сдавливанием шейки матки в течение 6 часов. После снятия зажима кровоток в маточных артериях немедленно восстановился. Симптомы меноррагии отслеживались с помощью Шкалы тяжести меноррагии Рута. Объемы матки и миомы измеряли путем анализа магнитно-резонансных изображений. Симптомы меноррагии, о которых пациентка сообщила самостоятельно, значительно уменьшились через 6 месяцев (снижение на 70% по шкале Ruta), а объем матки и объем миомы уменьшился более чем на 44% через 6 месяцев.Этот клинический случай иллюстрирует потенциальную применимость простого в использовании нехирургического устройства для лечения меноррагии и миомы матки путем временной окклюзии маточной артерии.
Было продемонстрировано, что окклюзия маточной артерии является эффективным средством лечения симптоматической миомы матки, будь то перманентная лапароскопическая окклюзия или эмболизация маточной артерии (ЭМА) (Pron et al ., 2003; Hald et al ., 2004; Spies и др. ., 2004). Целью этого исследования было изучить безопасность и эффективность трансвагинальной системы при использовании для временной 6-часовой окклюзии маточных артерий при лечении симптоматической миомы матки.Эта система, система Flostat ™ (Vascular Control Systems, Сан-Хуан-Капистрано, Калифорния, США), в настоящее время одобрена Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для выявления и временной окклюзии маточных артерий в сочетании с консервативной гинекологической хирургией.
История болезниУ нерожавшей женщины 43 лет была меноррагия. После того, как плановое гинекологическое обследование выявило миому матки в сочетании с жалобой на меноррагию, пациентке было предложено принять участие в одобренном комитетом по этике пилотном исследовании системы Flostat, которое идентифицирует и временно перекрывает маточные артерии.
После получения информированного согласия и до лечения временной окклюзии пациент был обследован с помощью магнитно-резонансной томографии (МРТ) таза. Пациентка продемонстрировала умеренно увеличенную матку размером 310 куб. См с четырьмя миомами диаметром от 3 до 6 см. Для количественной оценки симптомов меноррагии у пациента перед процедурой и во время последующих посещений через 1, 3 и 6 месяцев вводили шкалу тяжести меноррагии Рута (Ruta et al ., 1995).
Система Flostat состоит из (а) направляющего шейного зажима, (б) трансвагинального сосудистого зажима со встроенными ультразвуковыми кристаллами Доплера, (в) соединителя, который продвигает зажим по тенакулуму, и (г) ультразвукового приемопередатчика с батарейным питанием который генерирует звуковой доплеровский сигнал (рисунки 1 и 2).
Рисунок 1.
Текущая система Flostat состоит из (a) направляющего шейного зажима, (b) трансвагинального сосудистого зажима со встроенными ультразвуковыми кристаллами Допплера, (c) соединителя, который продвигает зажим по тенакулуму, и ( г) ультразвуковой приемопередатчик с батарейным питанием, который генерирует звуковой доплеровский сигнал. 404 × 411 мм (72 × 72 d.p.i.).
Рисунок 1.
Текущая система Flostat состоит из (a) направляющего шейного зажима, (b) трансвагинального сосудистого зажима со встроенными ультразвуковыми кристаллами Допплера, (c) соединителя, который продвигает зажим над зажимом, и (d) ультразвуковой приемопередатчик с батарейным питанием, который генерирует звуковой доплеровский сигнал.404 × 411 мм (72 × 72 d.p.i.).
Рисунок 2.
Принципиальная схема системы Flostat. 127 × 100 мм (150 × 150 d.p.i.).
Рисунок 2.
Принципиальная схема системы Flostat. 127 × 100 мм (150 × 150 d.p.i.).
Во время лечения пациент был помещен в положение для литотомии в хирургическом кабинете. После рутинного гистероскопического исследования матки и диагностической дилатации и выскабливания направляющий зажим был помещен с фиксирующим крючком в положение шейки матки на 6 часов.Трансвагинальный зажим шарнирно соединяли с направляющим зажимом и продвигали по направляющей вместе с соединителем, чтобы поместить концы зажима в боковые своды влагалища в положениях на 9:00 и 3:00.
Когда ультразвуковые кристаллы на концах зажима касались боковой слизистой оболочки влагалища, они возвращали слышимые доплеровские сигналы от правой и левой маточных артерий. По мере того, как зажим продвигался дальше по направляющему выступу, зажим сгибал влагалищную ткань вокруг маточных артерий и смещал маточные артерии выше точек их введения в матку.В закрытом состоянии зажим перекрывал маточные артерии с двух сторон, сдавливая слизистую влагалища и маточные артерии по боковым границам нижней части матки. Окклюзия маточной артерии подтверждалась прекращением звукового допплеровского сигнала.
После непродолжительного пребывания в зоне послеоперационного восстановления пациентка была переведена в гинекологическое отделение, где оставалась до конца 6-часового периода окклюзии. Устройство было удалено у постели больного. В момент отпускания зажима доплеровский сигнал немедленно возвращался из каждой маточной артерии.Во время удаления направляющего зажима и зажима или при последующих контрольных обследованиях повреждений слизистой оболочки влагалища не наблюдалось.
К процедуре пациенту подготовили эпидуральную анестезию (бупивакаин 0,25%, 48 мл за период лечения) и морфин (50 мг за период лечения) внутривенно. для обезболивания. Ондансетрон (4 мг) и дименгидринат (50 мг) также вводили для контроля тошноты. Пока пациент находился в больнице, дополнительных обезболивающих не давали, и пациенту не требовались обезболивающие при выписке наутро после процедуры.Ультразвуковое исследование почек через 24 часа после окклюзии маточной артерии было нормальным. Это указывало на то, что зажим не повлиял на мочеточники.
Шкала тяжести меноррагии Рута — это самостоятельно вводимый инструмент для оценки качества жизни, включающий 13 вопросов для оценки менструального цикла пациентки за последние 3 месяца. Более высокий балл указывает на более низкое качество жизни. Этот тест на меноррагию был ранее проверен на внутреннюю надежность и надежность повторных тестов, а также подтвержден по Краткой форме-36 (Ruta et al ., 1995). До начала лечения пациентка сообщила о 20-балльной оценке по Ruta. При контрольном осмотре через 6 месяцев она сообщила о 6-балльной оценке, что означает снижение тяжести меноррагии на 70%.
МРТ, показывающая объемы матки и миомы до лечения и через 8 месяцев после лечения, представлена на рисунке 3. Объемы (в кубических сантиметрах) были рассчитаны по формуле для объема вытянутого эллипса [длина × ширина × передне-задний диаметр × (π / 6), каждая измеряется в см]. Матка уменьшилась на 44% в объеме к 8 месяцам, по четырем измерениям миомы уменьшились на 71, 84 и 99%.Одна из миом, как показано на рисунке 3, больше не может быть идентифицирована. Четвертая миома, за которой наблюдали и измеряли, не видна на этом изображении, поскольку она расположена латеральнее средней линии.
Рис. 3.
(A) Предварительная обработка Т2-взвешенная средняя линия, сагиттальное магнитно-резонансное изображение, показывающее матку и одну 4 см (F1) и две 3 см (F2, F3) миомы. (B) Восемь месяцев после временной окклюзии маточной артерии, демонстрирующее уменьшение объема матки (44%) и уменьшение миомы: F1 (71%), F2 (100%; больше не идентифицировано), F3 (84%).740 × 529 мм (72 × 72 d.p.i.).
Рис. 3.
(A) Предварительная обработка Т2-взвешенная средняя линия, сагиттальное магнитно-резонансное изображение, показывающее матку и одну 4 см (F1) и две 3 см (F2, F3) миомы. (B) Восемь месяцев после временной окклюзии маточной артерии, демонстрирующее уменьшение объема матки (44%) и уменьшение миомы: F1 (71%), F2 (100%; больше не идентифицировано), F3 (84%). 740 × 529 мм (72 × 72 d.p.i.).
ОбсуждениеЭти данные об уменьшении объема матки и миомы и облегчении симптомов меноррагии выгодно сравниваются с опубликованными данными о постоянной лапароскопической окклюзии маточной артерии и ЭМА.В сравнительном исследовании постоянной лапароскопической окклюзии и эмболизации Hald et al . (2004) сообщили о сокращении матки на 36,7% при постоянной окклюзии и 40,1% при эмболизации через 6 месяцев наблюдения. Аналогичным образом, доминирующее сокращение миомы было зарегистрировано как 36,2% для окклюзии и 45,1% для эмболизации с тем же интервалом. Авторы определили, что эти сокращения статистически не различались между этими двумя популяциями. Тем не менее, они наблюдали значительные различия в боли пациентов после процедуры между двумя популяциями, как измерено с помощью визуальной аналоговой шкалы и по потреблению обезболивающих.Группе лапароскопического лечения потребовалось значительно меньше обезболивающих после лечения, чем группе эмболизации.
Во второй исследовательской группе Прон и др. . (2004), сообщая от имени Испытания эмболизации миомы матки (UFE) в Онтарио, отметили, что 6% пациентов, получавших эмболизацию, необходимо было посетить отделение неотложной помощи для купирования продолжающейся постпроцедурной боли. Мы считаем, что временная окклюзия маточной артерии может привести к еще более низкому уровню послеоперационной боли, поскольку кровообращение в матке восстанавливается сразу после удаления устройства.
В другой недавней серии эмболизаций 102 пациентов, Spies et al . (2004) сообщили о среднем уменьшении объема матки и миомы на 33,1 и 54% соответственно через 6 месяцев. Эта серия также привела к снижению показателей меноррагии на 58,1% через 6 месяцев. Однако в этой серии также сообщалось об аменорее у семи пациентов (6,8%) и общей заболеваемости 15%.
Другие исследования эмболизации сообщили о подобных осложнениях. Прон и др. . (2004), сообщая от имени исследования UFE в Онтарио, сообщает о 8% случаев аменореи.Поскольку временная окклюзия маточной артерии не зависит от эмболизации частицами для лечения миомы, можно избежать эффектов нецелевой эмболизации яичников и, как следствие, дисфункции яичников.
Шесть часов окклюзии маточных артерий трансвагинальным зажимом с доплеровским контролем оказались эффективной терапией для лечения меноррагии и миомы у этой пациентки. Продолжительность 6 часов была получена из предыдущего исследования лапароскопической двусторонней постоянной окклюзии маточной артерии, которое показало, что миометрий реперфузировался в течение 6 часов примерно у 80% женщин (Lichtinger et al ., 2004).
Это простое в использовании нехирургическое устройство может быть установлено любым гинекологом и может обеспечить таким пациентам результаты лечения, сопоставимые с результатами более инвазивных глобальных методов лечения миомы. В настоящее время продолжаются дальнейшие исследования с большим количеством пациентов.
Список литературы, Langebrekke A, Klow NE, Noreng HJ, Berge AB и Istre O (
2004
) Лапароскопическая окклюзия маточных сосудов для лечения симптоматической миомы: первоначальный опыт и сравнение с эмболизацией маточной артерии.Am J Obstet Gynecol
190
,37
–43., Бербанк Ф., Холлсон Л., Герберт С., Уйено Дж. И Джонс М. (
2004
) Динамика ишемии и реперфузии миометрия после лапароскопической окклюзии маточной артерии. Теоретические выводы.J Am Assoc Gynecol Laparosc
10
,553
–556., Mocarski E, Bennett J, Vilos G, Common A, Zaidi M et al. (
2003
) Толерантность, пребывание в больнице и восстановление после эмболизации маточной артерии по поводу миомы: испытание эмболизации миомы матки в Онтарио.J Vasc Interv Radiol
14
,1243
–1250., Bennett J, Common A, Wall J, Asch M и Sniderman K (
2003
) Исследование эмболизации миомы матки в Онтарио. Часть 2. Уменьшение миомы матки и облегчение симптомов после эмболизации маточной артерии по поводу миомы.Fertil Steril
79
,120
–127., Garratt AM, Chadha YC, Flett GM, Hall MH и Russell IT (
1995
) Оценка пациентов с меноррагией: насколько обоснован структурированный клинический анамнез как показатель состояния здоровья?Qual Life Res
4
,33
–40.
