инструкция, отзывы. Бактериофаг стафилококковый от прыщей
Бактериофаг относится к биопрепаратам, которые содержат в своем составе полезные вирусы, воздействующие на болезнетворные микроорганизмы. Особенность этих средств в том, что определенное лекарство способно бороться лишь с одним типом вирусов. Бактериофаг стафилококковый, отзывы врачей о котором характеризуют его как действенное средство от многих болезней, относится именно к таким медикаментам. О нем и пойдет речь дальше.
Сразу следует отметить, что без назначения врача подобное лекарство принимать нельзя. Самолечение может плохо отразиться на здоровье. Доктор назначает такое лекарство лишь после установления точного диагноза и определения вида вредоносных вирусов в организме.
Общая информация
Абсолютно все вирусы относятся к паразитам, которые выживают за счет поедания других организмов. Бактериофаги – это полезные вирусы, которые живут за счет плохих. Они всегда там, где есть вредоносные бактерии и микроорганизмы. Принцип уничтожения заключается в том, что бактериофаги нападают на вирус, растворяют его оболочку и пускают внутрь свои ДНК и РНК. После полного растворения внутреннего содержимого вредоносного вируса в среду выходят молодые бактериофаги. Слабые места подобной терапии в том, что они воздействуют лишь на определенный тип вирусов.
Принцип уничтожения заключается в том, что бактериофаги нападают на вирус, растворяют его оболочку и пускают внутрь свои ДНК и РНК. После полного растворения внутреннего содержимого вредоносного вируса в среду выходят молодые бактериофаги. Слабые места подобной терапии в том, что они воздействуют лишь на определенный тип вирусов.
Применение препаратов с бактериофагами
Насколько хорошо воздействуют на организм данные препараты, расскажут отзывы. Бактериофаг стафилококковый хорошо справляется с гнойными инфекциями. Применяется он для лечения слизистых, кожи и висцелярных органов.
Кроме стафилококковой инфекции, определенные виды бактериофагов способны справиться с синегнойной палочкой, стрептококками, сальмонеллами, энтерококковыми бактериями и рядом других вредоносных микроорганизмов.
Когда применяют бактериофаг стафилококковый
Отзывы врачей говорят о том, что данное лекарство поможет при следующих заболеваниях:
- синусит;
- ангина;
- отит;
- ларингит и фарингит;
- пневмония, бронхит и трахеит;
- плеврит;
- гнойные раны, абсцесс, панариций, фурункул, сложные ожоги с нагноением;
- воспалительные процессы мочевой системы, включая циститы, нефриты и пиелонефриты;
- болезни органов пищеварения, вызванные стрептококковой инфекцией, в том числе гастриты, холециститы, гастроэнтероколиты;
- дисбактериоз кишечника.

Форма выпуска
Бактериофаг стафилококковый выпускается в виде раствора, упакованного во флаконы по 100 мл в картонной коробке или по 20 мл в пачке. В каждой коробке имеется детальная инструкция по применению.
Препарат также выпускается в таблетках, в виде ректальных суппозиториев и аэрозоля для комфортного применения при различных заболеваниях.
Способы применения медикамента и отзывы
Бактериофаг стафилококковый в зависимости от типа воспалительного очага может применяться так:
- Раствор вводят в рану при абсцессе после оперативного вмешательства в виде пункции по удалению гнойного содержимого. Количество препарата зависит от объема удаленного гноя и может достигать 200 мл. Также лекарство действенно при остеомиелите, о чем свидетельствуют отзывы. Бактериофаг стафилококковый вливают в рану после обработки по 20 мл. Действие лекарства усиливается, если вдобавок к этому делают орошения и примочки.
- Препарат вводят в ограниченные полости, такие как плевральная и суставная, при этом оставляют специальный капельный дренаж, по которому через некоторое время добавляют раствор.

- Также лекарство может быть назначено врачом для приема внутрь при таких диагнозах, как цистит, уретрит, пиелонефрит. Пациентам с дренированным мочевым пузырем или лоханкой лекарство вводят внутрь посредством цистомы или нефростомы до 2 раз в сутки (от 20 до 50 мл в мочевик и от 5 до 7 мл в лоханку).
- Препарат поможет справиться с рядом гинекологических заболеваний, и это подтверждают многочисленные отзывы. Бактериофаг стафилококковый назначается пациенткам с гнойно-воспалительными очагами. Раствор вводят в вагину или матку по 5-10 мл каждый день. При заболевании под названием кольпит действенными будут орошения по 10 мл и тампонирование по 2 раза в сутки на 2 часа.
- Данное лекарственное средство поможет справиться с заболеваниями ЛОР-органов. Очень часто назначают бактериофаг стафилококковый» при ангине. Отзывы врачей говорят о том, что полоскания данным раствором способствуют быстрому восстановлению пациента. Кроме того, лекарство закапывают в нос и используют для смачивания турунд в уши.

- Как позиционируют стафилококковый бактериофаг отзывы? При дисбактериозе и инфекционных поражениях медикамент показывает высокие результаты. Его назначают по 2-10 мл до трех раз в день за час до трапезы. Кроме этого, практикуется и ректальное введение лекарства для достижения максимального эффекта от терапии.
- Поможет бактериофаг стафилококковый при фурункулезе. Отзывы пациентов говорят о том, что распыление аэрозоля и примочки в виде аппликаций ускоряют процесс восстановления тканей и приводят к скорейшему выздоровлению.
Как назначается бактериофаг стафилококковый взрослым? Отзывы врачей говорят, что при адекватном подходе к терапии с использованием антибиотиков и прочих препаратов наблюдается положительная динамика при таких тяжелых заболеваниях, как абсцесс, сепсис и прочие проявления запущенной инфекции. Однако раннее обращение в медицинское учреждение позволит своевременно диагностировать причину того или иного заболевания и оказать помощь, не дожидаясь осложнений и последствий.
Назначение детям
Препарат широко применяется в педиатрии. Что говорят о таком лекарстве, как бактериофаг стафилококковый отзывы? Для грудничков очень опасными является такое заболевание, как омфалит. Оно проявляется нагноением у пупочной ранки, покраснением кожи около нее и отечностью, а также воспалительным процессом в подкожно-жировом слое. Причиной такого заболевания является стафилококковая инфекция. Прогрессирование болезни может привести к сепсису. Своевременная систематическая обработка ранки таким составом, как бактериофаг стафилококковый, поможет быстро нейтрализовать действие вредных микроорганизмов, что приведет к выздоровлению.
Еще одно распространенное заболевание грудничков – везикулопустулез. Ему характерны поражения кожи, которые сопровождаются образованием пузырьков с мутным содержимым. Состояние маленького пациента зависит от количества высыпаний. Причиной недуга также является стафилококковая инфекция, которая может быть побеждена посредством примочек с таким средством, как бактериофаг стафилококковый.
Отзывы о лечении детей разного возраста
У детей постарше стафилококковые поражения кожных покровов зачастую проявляются фурункулезами и фолликулитами, в отдельных случаях могут наблюдаться гидрадениты и карбункулы. Как советует использовать бактериофаг стафилококковый инструкция? Для детей (отзывы врачей это подтверждают) при лечении кожных проявлений такого типа действенным будет прием аэрозоля, а также использование примочек и аппликации на пораженные участки кожных покровов.
При заболеваниях желудочно-кишечного тракта и дыхательной системы, вызванных стафилококками, которым характерны явные признаки интоксикации, может быть назначено пероральное и ректальное введение препарата.
Что нужно изучить прежде, чем принимать бактериофаг стафилококковый? Отзывы. Для детей очень важна своевременно проведенная антибактериальная терапия, которой должны предшествовать лабораторные исследования для распознавания бактерии, вызвавшей болезнь. Это поможет быстро и без осложнений стабилизировать состояние маленького больного, что приведет к выздоровлению.
Отзывы о лечении прыщей
Довольно часто данный препарат применяется для лечения недостатков кожи, в частности, помогает бактериофаг стафилококковый от прыщей. Отзывы свидетельствуют о том, что после обработки пораженных гнойничковой сыпью участков кожи воспаление быстро сходит, не оставляя после себя шрамов и следов. Данная терапия может применяться при высыпаниях как у грудных младенцев, так и в подростковом возрасте. Естественно, препарат будет действенен, если сыпь вызвана чувствительными к нему микроорганизмами.
Применение у беременных и кормящих
Противопоказаний для лечения в данный период нет, так как лекарство не имеет побочных эффектов. Даже более того, данный биопрепарат станет самым верным помощником в лечении различных заболеваний в период, кода многие другие лекарственные средства принимать противопоказано. Использовать лекарство следует исключительно по рекомендации доктора.
Противопоказания и побочные действия
Ввиду того что лекарство относится к биопрепаратам природного происхождения, оно не имеет побочных эффектов, равно как и не может вызвать передозировку. Кроме того, медикамент может быть частью комплексной терапии и применяться вместе с антибиотиками и прочими лекарственными средствами.
Кроме того, медикамент может быть частью комплексной терапии и применяться вместе с антибиотиками и прочими лекарственными средствами.
Противопоказанием является лишь непереносимость компонентов, входящих в состав препарата.
Особые требования при использовании лекарства
Производитель данного лекарственного средства предупреждает, что ни в коем случае нельзя использовать его, если нарушена целостность флакона. Также нельзя его применять при истекшем сроке годности и помутнении.
Все дело в том, что препарат содержит живые бактерии с особой средой, в которой могут развиться вредоносные микроорганизмы. Именно они и вызывают помутнение раствора. Чтобы не допустить подобного явления, следует придерживаться следующих правил при открывании флакона:
- тщательно вымыть руки и обработать их антисептиком;
- протереть флакон и колпачок спиртовым раствором;
- не допускать соприкосновения внутренней пробки со столом или другими предметами;
- ни в коем случае не оставлять флакон с лекарством открытым;
- хранить препарат в холодильнике.

Чтобы избежать преждевременной порчи раствора, специалисты рекомендуют извлекать содержимое флакона посредством использования стерильного шприца, которым нужно будет аккуратно проколоть резиновую пробку. При соблюдении этих несложных правил удастся избежать помутнений. Это позволит максимально эффективно использовать флакон вплоть до истечения срока годности его содержимого.
Хранить лекарство можно на протяжении двух лет при температуре от 2 до 8 градусов. При необходимости транспортировки допускается диапазон температуры от 9 до 25 градусов. Однако в таком состоянии препарат может находиться не дольше одного месяца. Данное лекарственное средство продается в аптеках без рецепта, поэтому приобрести его не составляет труда.
БАКТЕРИОФАГ СТАФИЛОКОККОВЫЙ раствор: 19 отзывов от реальных людей. Все отзывы о препаратах на сайте
Отзыв: Бактериофаг стафилококковый Микроген жидкий — Стафилококк до конца мы не победили у ребенка!
Никогда не думала, что придется столкнуться с бактериофагам, я даже название такое не слышала, но вот не повезло-у маленького ребенка в два месяца обнаружили золотистый стафилококк в кале.
Видно заработали мы его в род доме, хотя про какие-то плохие анализы не было сказано.
В первый месяц, у ребенка был ужаснейший дисбактериоз, мы плохо какали, вздутие живота мучило, и все лекарства, которые нам выписывал врач, не помогали.
что делать, я обратилась к другому педиатру, меня с ребенком сразу отправили на анализ кала, в котором и обнаружили этот стафилококк. Только месяц был упущен.
Прописали нам бактериофаг стафилококковый Микроген жидкий, так как я обратилось в платную клинику, то и сама за свои денежки покупала этот препарат. И найти его проблема целая была, и стоит он не дешево.
А вот в обычной поликлинике это средство по показаниям выписывают бесплатно.
Начала давать ребенку это средство уже в два месяца.
Жидкость желтоватого цвета, как слабой заварки чай, на вкус неприятная.
Врач мне прописала определенную дозировку. Давала ребенку один раз в день, разбавляя лекарство в водичке. Так как фаг хранится только в холодильнике, соответственно, он был холодный, так не дашь ребенку, а вот с теплой водичкой получается самое то.
И ребенок прямо из соски пил это средство. В принципе, не помню, чтобы он его не допил, процесс протекал нормально.
Жидкость находится в стеклянном пузырьке, объем 100 мл.
Единственное, очень не удобно доставать это лекарство. Нужно брать шприц, протыкать крышку и набирать дозировку лекарства, принцип, как делать укольчик.
Мне было не очень удобно, хотелось бы как-то получше доставать это лекарство.
Инструкция не большая, но очень подробно в ней все изложено. И показание к применению, и дозировки, и как правильно пользоваться средством.
Пропили мы курс этого фага.
Никаких побочных действий, ни аллергии, ни раздражений, ничего негативного я не увидела. Это один из самых безопасных лекарственных препаратов.
Вот только золотистый стафилококк мы не вылечили, пересдали анализы- процент снижен, но не на много.
Но это средство помогло нам облегчить симптомы дисбактериоза, малыш стал чувствовать себя комфортнее, и животик стал менее вздутый, особенно в сочетании с Бифидум-мульти.
Стафилококк ребенка в принципе, больше не беспокоил, не напоминал о себе, лишь в год, ребенок заболел ангиной, вызванной стафилококковыми носителями. И здесь встал вопрос о назначении это препарата снова, мне его уже выписали бесплатно.
Единственно, пока я его повременила давать, проконсультировавшись с педиатром, нужно подождать, чтобы ребенок немного подрос, организм сам может перебороть этот вредный стафилококк.
В общем и целом, сейчас я контролирую содержание в анализах золотистого стафилококка, и конечно в мой аптечке лежит такое средство как Бактериофаг стафилококковый.
Хоть это средство с первого раза не побороло до конца стафилококк, я считаю, что это самое безобидное средство для детского организма, и оно помогло убрать дисбактериоз у маленького ребенка и снизить количество стафилококковых носителей, что есть уже хорошо.
У каждого своя ситуация, быть может, кому-то этот фаг поможет с первого раза, и я все же советовала обратите внимание на данный препарат.
Спасибо за внимание.
Семейство стафилококковых фагов: обзор
1. Lindsay J.A. Геномная изменчивость и эволюция золотистого стафилококка. Междунар. Дж. Мед. микробиол. 2010; 300:98–103. doi: 10.1016/j.ijmm.2009.08.013. [PubMed] [CrossRef] [Google Scholar]
2. Brussow H., Canchaya C., Hardt W.D. Фаги и эволюция бактериальных патогенов: от геномных перестроек до лизогенной конверсии. микробиол. Мол. биол. 2004; 68: 560–602. doi: 10.1128/MMBR.68.3.560-602.2004. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Kwan T., Liu J., DuBow M., Gros P., Pelletier J. Полные геномы и протеомы 27 бактериофагов Staphylococcus aureus. проц. Натл. акад. науч. США. 2005; 102: 5174–5179. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Canchaya C., Proux C., Fournous G., Bruttin A., Brussow H. Prophage Genomics. микробиол. Мол. биол. 2003; 67: 238–276. doi: 10.1128/MMBR.67.2.238-276.2003. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
5. Goerke C., Wirtz C., Fluckiger U., Wolz C. Обширная динамика фагов в Staphylococcus aureus способствует адаптации к человеку-хозяину во время инфекции. Мол. микробиол. 2006; 61: 1673–1685. дои: 10.1111/j.1365-2958.2006.05354.х. [PubMed] [CrossRef] [Google Scholar]
Goerke C., Wirtz C., Fluckiger U., Wolz C. Обширная динамика фагов в Staphylococcus aureus способствует адаптации к человеку-хозяину во время инфекции. Мол. микробиол. 2006; 61: 1673–1685. дои: 10.1111/j.1365-2958.2006.05354.х. [PubMed] [CrossRef] [Google Scholar]
6. Feng Y., Chen C.J., Su L.H., Hu S., Yu J., Chiu C.H. Эволюция и патогенез золотистого стафилококка: уроки, извлеченные из генотипирования и сравнительной геномики. ФЭМС микробиол. 2008; 32:23–37. doi: 10.1111/j.1574-6976.2007.00086.x. [PubMed] [CrossRef] [Google Scholar]
7. Вентворт Б.Б. Бактериофаговое типирование стафилококков. бактериол. 1963; 27: 253–272. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Розенблюм Э.Д., Тайрон С. Серология, плотность и морфология стафилококковых фагов. Дж. Бактериол. 1964; 88: 1737–1742. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Отто М. Молекулярные основы инфекций Staphylococcus epidermidis. Семин. Иммунопатол. 2012;34:201–214. doi: 10. 1007/s00281-011-0296-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
1007/s00281-011-0296-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Otto M. Staphylococcus epidermidis — «случайный» патоген. Нац. Преподобный Микробиолог. 2009; 7: 555–567. doi: 10.1038/nrmicro2182. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
11. Фон Эйфф С., Петерс Г., Хайльманн С. Патогенез инфекций, вызванных коагулазонегативными стафилококками. Ланцет Инфекция. Дис. 2002; 2: 677–685. doi: 10.1016/S1473-3099(02)00438-3. [PubMed] [CrossRef] [Google Scholar]
12. Франк К.Л., Дель Позо Дж.Л., Патель Р. От клинической микробиологии к патогенезу инфекций: как смело работать по-разному для Staphylococcus lugdunensis. клин. микробиол. 2008; 21:111–133. doi: 10.1128/CMR.00036-07. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. Курода М., Ямасита А., Хиракава Х., Кумано М., Морикава К., Хигасиде М., Маруяма А., Иносе Ю., Матоба К., Тох Х., Кухара С., Хаттори М. ., Охта Т. Полногеномная последовательность Staphylococcus saprophyticus раскрывает патогенез неосложненной инфекции мочевыводящих путей. проц. Натл. акад. науч. США. 2005; 102:13272–13277. [Бесплатная статья PMC] [PubMed] [Google Scholar]
проц. Натл. акад. науч. США. 2005; 102:13272–13277. [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. База данных фагов EMBL. Страницы геномов — Фаги. [(по состоянию на 30 октября 2012 г.)]. Доступно в Интернете: http://www.ebi.ac.uk/genomes/phage.html.
15. База данных Patric. Стафилококковая страница. [(по состоянию на 30 октября 2012 г.)]. Доступно в Интернете: http://www.patricbrc.org/portal/portal/patric/Taxon?cType=taxon&cId=1279.
16. Garcia P., Martinez B., Obeso J.M., Lavigne R., Lurz R., Rodriguez A. Функциональный геномный анализ двух фагов Staphylococcus aureus, выделенных из молочной среды. заявл. Окружающая среда. микробиол. 2009; 75: 7663–7673. doi: 10.1128/AEM.01864-09. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17. Ким М.С., Мён Х. Полный геном Staphylococcus aureus Phage SA11. Дж. Вирол. 2012;86:10232. doi: 10.1128/ОВИ.01574-12. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Ackermann H. W. Хвостатые бактериофаги: отряд caudovirales. Доп. Вирус Рез. 1998; 51: 135–201. doi: 10.1016/S0065-3527(08)60785-X. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
W. Хвостатые бактериофаги: отряд caudovirales. Доп. Вирус Рез. 1998; 51: 135–201. doi: 10.1016/S0065-3527(08)60785-X. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Сон Дж. С., Ли С. Дж., Джун С. Ю., Юн С. Дж., Кан С. Х., Пайк Х. Р., Кан Дж. О., Чой Ю. Дж. Антибактериальная активность подовирусов и удаление биопленки Бактериофаг SAP-2 Staphylococcus aureus и производный рекомбинантный фермент, разрушающий клеточную стенку. заявл. микробиол. Биотехнолог. 2010;86:1439–1449. doi: 10.1007/s00253-009-2386-9. [PubMed] [CrossRef] [Google Scholar]
20. O’Flaherty S., Coffey A., Edwards R., Meaney W., Fitzgerald G.F., Ross R.P. Геном стафилококкового фага K: новая линия Myoviridae, инфицирующих Gram. -Положительные бактерии с низким содержанием G+C. Дж. Бактериол. 2004; 186: 2862–2871. doi: 10.1128/JB.186.9.2862-2871.2004. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
21. Педулла М.Л., Форд М.Е., Хаутц Дж.М., Картикеян Т., Уодсворт С., Льюис Дж. А., Джейкобс-Сера Д., Фалбо Дж., Гросс Дж., Паннунцио Н.Р., Брукер В., Кумар В., Кандасами Дж., Кинан Л., Бардаров С., Кряков Дж., Лоуренс Дж.Г., Джейкобс В.Р., мл., Хендрикс Р.В., Хатфулл Г.Ф. Происхождение сильно мозаичных геномов микобактериофагов. Клетка. 2003; 113: 171–182. дои: 10.1016/S0092-8674(03)00233-2. [PubMed] [CrossRef] [Google Scholar]
А., Джейкобс-Сера Д., Фалбо Дж., Гросс Дж., Паннунцио Н.Р., Брукер В., Кумар В., Кандасами Дж., Кинан Л., Бардаров С., Кряков Дж., Лоуренс Дж.Г., Джейкобс В.Р., мл., Хендрикс Р.В., Хатфулл Г.Ф. Происхождение сильно мозаичных геномов микобактериофагов. Клетка. 2003; 113: 171–182. дои: 10.1016/S0092-8674(03)00233-2. [PubMed] [CrossRef] [Google Scholar]
22. Kwan T., Liu J., Dubow M., Gros P., Pelletier J. Сравнительный геномный анализ 18 бактериофагов Pseudomonas aeruginosa. Дж. Бактериол. 2006; 188:1184–1187. doi: 10.1128/JB.188.3.1184-1187.2006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
23. Hatfull G.F. Геномика бактериофагов. Курс. мнение микробиол. 2008; 11: 447–453. doi: 10.1016/j.mib.2008.09.004. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
24. Bae T., Baba T., Hiramatsu K., Schneewind O. Профаги Staphylococcus aureus Newman и их вклад в вирулентность. Мол. микробиол. 2006; 62: 1035–1047. doi: 10.1111/j.1365-2958.2006.05441. x. [PubMed] [CrossRef] [Google Scholar]
x. [PubMed] [CrossRef] [Google Scholar]
25. Выбирал Д., Такак М., Лесснер М., Витте А., фон Ахсен У., Блази У. Полная нуклеотидная последовательность и молекулярная характеристика двух литических фагов Staphylococcus aureus : 44AHJD и P68. ФЭМС микробиол. лат. 2003; 219: 275–283. дои: 10.1016/S0378-1097(03)00028-4. [PubMed] [CrossRef] [Google Scholar]
26. Лобокка М., Хейнович М.С., Домбровски К., Гоздек А., Косаковский Ю., Витковска М., Улатовска М.И., Вебер-Дабровска Б., Квятек М., Парасион С., Гавор Дж., Косовска Х., Гловацка А. Геномика стафилококковых фагов типа Twort — потенциальные терапевтические средства постантибиотической эры. Доп. Вирус Рез. 2012; 83: 143–216. doi: 10.1016/B978-0-12-394438-2.00005-0. [PubMed] [CrossRef] [Google Scholar]
27. Krisch H.M., Comeau A.M. Огромный путь бактериофага Т4 — от д’Эреля до Дельбрюка, затем до Дарвина и дальше. Рез. микробиол. 2008;159: 314–324. doi: 10.1016/j.resmic.2008.04.014. [PubMed] [CrossRef] [Google Scholar]
28. Холден М.Т., Фейл Э.Дж., Линдси Дж.А., Пикок С.Дж., Дэй Н.П., Энрайт М.С., Фостер Т.Дж., Мур С.Е., Херст Л., Аткин Р., Бэррон А., Бейсон Н., Бентли С.Д., Чиллингворт С., Чиллингворт Т., Черчер С., Кларк Л., Кортон С., Кронин А., Доггет Дж., Дауд Л., Фелтуэлл Т., Ханс З., Харрис Б. , Хаузер Х., Холройд С., Джагелс К., Джеймс К.Д., Леннард Н., Лайн А., Майес Р., Мул С., Мангалл К., Ормонд Д., Куэйл М.А., Раббинович Э., Резерфорд К. , Сандерс М., Шарп С., Симмондс М., Стивенс К., Уайтхед С., Баррелл Б.Г., Спратт Б.Г., Паркхилл Дж. Полные геномы двух клинических штаммов золотистого стафилококка: доказательства быстрой эволюции вирулентности и лекарственной устойчивости. проц. Натл. акад. науч. США. 2004;101:9786–9791. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Холден М.Т., Фейл Э.Дж., Линдси Дж.А., Пикок С.Дж., Дэй Н.П., Энрайт М.С., Фостер Т.Дж., Мур С.Е., Херст Л., Аткин Р., Бэррон А., Бейсон Н., Бентли С.Д., Чиллингворт С., Чиллингворт Т., Черчер С., Кларк Л., Кортон С., Кронин А., Доггет Дж., Дауд Л., Фелтуэлл Т., Ханс З., Харрис Б. , Хаузер Х., Холройд С., Джагелс К., Джеймс К.Д., Леннард Н., Лайн А., Майес Р., Мул С., Мангалл К., Ормонд Д., Куэйл М.А., Раббинович Э., Резерфорд К. , Сандерс М., Шарп С., Симмондс М., Стивенс К., Уайтхед С., Баррелл Б.Г., Спратт Б.Г., Паркхилл Дж. Полные геномы двух клинических штаммов золотистого стафилококка: доказательства быстрой эволюции вирулентности и лекарственной устойчивости. проц. Натл. акад. науч. США. 2004;101:9786–9791. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Lindsay J.A., Holden M.T. Staphylococcus aureus: супербактерия, супергеном? Тенденции микробиол. 2004; 12: 378–385. doi: 10.1016/j.tim.2004.06.004. [PubMed] [CrossRef] [Google Scholar]
30. Suzuki H., Lefebure T. , Bitar PP, Stanhope MJ Сравнительный геномный анализ рода Staphylococcus, включая Staphylococcus aureus и его недавно описанный родственный вид Staphylococcus simiae. Геномика BMC. 2012;13:38. дои: 10.1186/1471-2164-13-38. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
, Bitar PP, Stanhope MJ Сравнительный геномный анализ рода Staphylococcus, включая Staphylococcus aureus и его недавно описанный родственный вид Staphylococcus simiae. Геномика BMC. 2012;13:38. дои: 10.1186/1471-2164-13-38. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31. Малахова Н., ДеЛео Ф.Р. Мобильные генетические элементы золотистого стафилококка. Клетка. Мол. Жизнь наук. 2010;67:3057–3071. doi: 10.1007/s00018-010-0389-4. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
32. Coleman D.C., Sullivan D.J., Russell R.J., Arbuthnott J.P., Carey B.F., Pomeroy H.M. Бактериофаги Staphylococcus aureus, опосредующие одновременную лизогенную конверсию бета-лизина, стафилокиназы и энтеротоксина А: молекулярный механизм тройной конверсии. J. Gen. Microbiol. 1989;135:1679–1697. [PubMed] [Google Scholar]
33. ван Вамель В.Дж., Ройяккерс С.Х., Руйкен М., ван Кессель К.П., ван Страйп Дж.А. Модуляторы врожденного иммунитета — стафилококковый ингибитор комплемента и белок, ингибирующий хемотаксис Staphylococcus aureus, расположены на бета-гемолизин-конвертирующих бактериофагах. Дж. Бактериол. 2006; 188:1310–1315. doi: 10.1128/JB.188.4.1310-1315.2006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Дж. Бактериол. 2006; 188:1310–1315. doi: 10.1128/JB.188.4.1310-1315.2006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
34. Wagner P.L., Waldor M.K. Бактериофаговый контроль вирулентности бактерий. Заразить. Иммун. 2002;70:3985–3993. doi: 10.1128/IAI.70.8.3985-3993.2002. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
35. Zou D., Kaneko J., Narita S., Kamio Y. Prophage, phiPV83-pro, несущий гены пантон-валентного лейкоцидина, на стафилококке aureus P83 хромосома: сравнительный анализ геномных структур phiPV83-pro, phiPVL, phi11 и других фагов. Бионауч. Биотехнолог. Биохим. 2000;64:2631–2643. doi: 10.1271/bbb.64.2631. [PubMed] [CrossRef] [Google Scholar]
36. Goerke C., Pantucek R., Holtfreter S., Schulte B., Zink M., Grumann D., Broker B.M., Doskar J., Wolz C. Разнообразие профаги в доминантных клональных линиях Staphylococcus aureus. Дж. Бактериол. 2009 г.;191:3462–3468. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37. Дегорайн М. , Бобай Л.М., Смистерс П.Р., Бусбата С., Вермеерш М., Перес-Морга Д., Дрезе П.А., Роча Э.П., Тушон М., Ван Мелдерен Л. Характеристика новых фагов, выделенных из коагулазонегативных стафилококков, выявляет эволюционные отношения с фагами S. aureus. Дж. Бактериол. 2012;194:5829–5839. doi: 10.1128/JB.01085-12. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
, Бобай Л.М., Смистерс П.Р., Бусбата С., Вермеерш М., Перес-Морга Д., Дрезе П.А., Роча Э.П., Тушон М., Ван Мелдерен Л. Характеристика новых фагов, выделенных из коагулазонегативных стафилококков, выявляет эволюционные отношения с фагами S. aureus. Дж. Бактериол. 2012;194:5829–5839. doi: 10.1128/JB.01085-12. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
38. Goerke C., Koller J., Wolz C. Ципрофлоксацин и триметоприм вызывают индукцию фагов и модуляцию вирулентности у Staphylococcus aureus. Антимикроб. Агенты Чемотер. 2006; 50: 171–177. doi: 10.1128/AAC.50.1.171-177.2006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
39. Сумби П., Уолдор М.К. Транскрипция генов токсинов, присутствующих в стафилококковом фаге phiSa3ms, тесно связана с жизненным циклом фага. Дж. Бактериол. 2003; 185:6841–6851. doi: 10.1128/JB.185.23.6841-6851.2003. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
40. Новик Р.П., Кристи Г.Е., Пенадес Дж.Р. Связанные с фагами хромосомные островки грамположительных бактерий.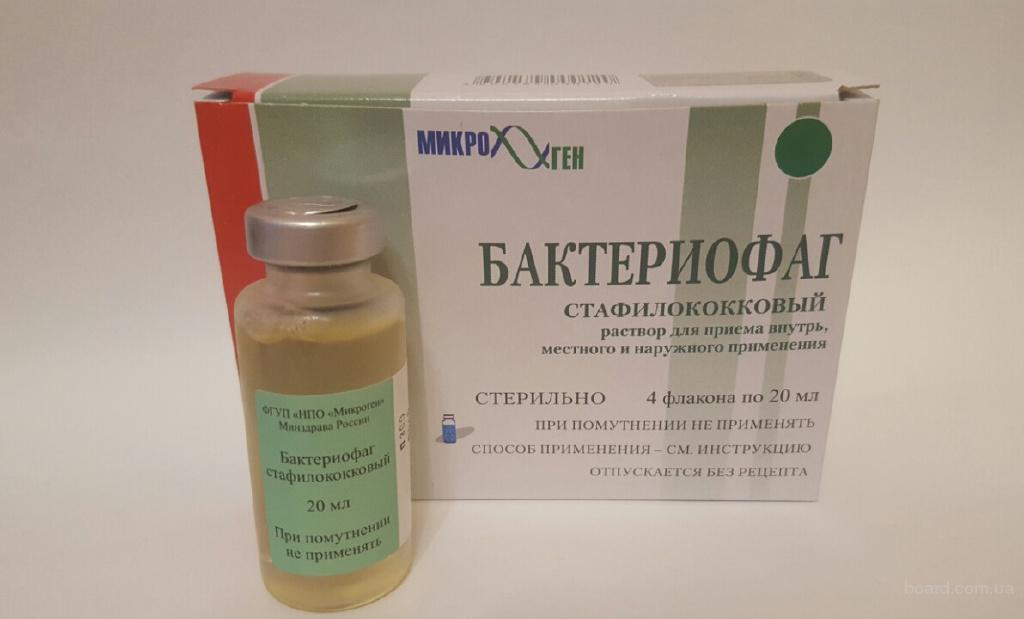 Нац. Преподобный Микробиолог. 2010; 8: 541–551. doi: 10.1038/nrmicro2393. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Нац. Преподобный Микробиолог. 2010; 8: 541–551. doi: 10.1038/nrmicro2393. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
41. Линдсей Дж.А., Рузин А., Росс Х.Ф., Курепина Н., Новик Р.П. Ген токсина токсического шока несет семейство мобильных островков патогенности у Staphylococcus aureus. Мол. микробиол. 1998; 29: 527–543. doi: 10.1046/j.1365-2958.1998.00947.x. [PubMed] [CrossRef] [Google Scholar]
42. Тормо-Мас М.А., Мир И., Шреста А., Таллент С.М., Кампой С., Ласа И., Барбе Дж., Новик Р.П., Кристи Г.Е., Пенадес Дж.Р. Подсобные белки бактериофага дерепрессируют стафилококковые островки патогенности. Природа. 2010;465:779–782. [Бесплатная статья PMC] [PubMed] [Google Scholar]
43. Goerke C., Wolz C. Адаптация золотистого стафилококка к муковисцидозу легкого. Междунар. Дж. Мед. микробиол. 2010; 300:520–525. doi: 10.1016/j.ijmm.2010.08.003. [PubMed] [CrossRef] [Google Scholar]
44. Goerke C., Wolz C. Регуляторная и геномная пластичность Staphylococcus aureus во время персистирующей колонизации и инфекции. Междунар. Дж. Мед. микробиол. 2004; 294:195–202. doi: 10.1016/j.ijmm.2004.06.013. [PubMed] [CrossRef] [Академия Google]
Междунар. Дж. Мед. микробиол. 2004; 294:195–202. doi: 10.1016/j.ijmm.2004.06.013. [PubMed] [CrossRef] [Академия Google]
45. McAdam P.R., Holmes A., Templeton K.E., Fitzgerald J.R. Адаптивная эволюция Staphylococcus aureus при хронической эндобронхиальной инфекции у пациента с муковисцидозом. ПЛОС Один. 2011;6:e24301. [Бесплатная статья PMC] [PubMed] [Google Scholar]
46. Такеучи Ф., Ватанабэ С., Баба Т., Юдзава Х., Ито Т., Моримото Ю., Курода М., Цуй Л., Такахаши М. ., Анкай А., Баба С., Фукуи С., Ли Дж. К., Хирамацу К. Полногеномное секвенирование гемолитического стафилококка раскрывает чрезвычайную пластичность его генома и эволюцию видов стафилококков, колонизирующих человека. Дж. Бактериол. 2005;187:7292–7308. [Бесплатная статья PMC] [PubMed] [Google Scholar]
47. Гилл С.Р., Футс Д.Е., Арчер Г.Л., Монгодин Э.Ф., Дебой Р.Т., Равель Дж., Полсен И.Т., Колонай Дж.Ф., Бринкац Л., Бинан М., Додсон Р.Дж., Догерти С.С., Мадупу Р., Ангиуоли С.В., Дуркин А.С., Хафт Д. Х., Ваматеван Дж., Хури Х., Аттербак Т., Ли С., Димитров Г., Цзян Л., Цинь Х., Вайдман Дж., Тран К., Канг К., Ханс И.Р., Нельсон К.Е., Фрейзер С.М. Взгляд на эволюцию вирулентности и резистентности из полного анализа генома раннего метициллин-резистентного штамма Staphylococcus aureus и биопленкообразующего метициллин-резистентного штамма Staphylococcus epidermidis. Дж. Бактериол. 2005; 187: 2426–2438. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Х., Ваматеван Дж., Хури Х., Аттербак Т., Ли С., Димитров Г., Цзян Л., Цинь Х., Вайдман Дж., Тран К., Канг К., Ханс И.Р., Нельсон К.Е., Фрейзер С.М. Взгляд на эволюцию вирулентности и резистентности из полного анализа генома раннего метициллин-резистентного штамма Staphylococcus aureus и биопленкообразующего метициллин-резистентного штамма Staphylococcus epidermidis. Дж. Бактериол. 2005; 187: 2426–2438. [Бесплатная статья PMC] [PubMed] [Google Scholar]
48. Розенштейн Р., Нерц С., Бисвас Л., Реш А., Раддац Г., Шустер С.С., Готц Ф. Анализ генома бактерии Staphylococcus carnosus TM300 из мясной закваски. заявл. Окружающая среда. микробиол. 2009; 75: 811–822. doi: 10.1128/AEM.01982-08. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
49. Rosenstein R., Gotz F. Геномные различия между пищевым Staphylococcus carnosus и патогенными видами стафилококков. Междунар. Дж. Мед. микробиол. 2010; 300:104–108. doi: 10.1016/j.ijmm.2009.08.014. [PubMed] [CrossRef] [Google Scholar]
50. Лина Б., Бес М., Ванденеш Ф., Гренландия Т., Этьен Дж., Флеретт Дж. Роль бактериофагов в геномной изменчивости родственных коагулазонегативных стафилококков. ФЭМС микробиол. лат. 1993; 109: 273–277. doi: 10.1111/j.1574-6968.1993.tb06180.x. [PubMed] [CrossRef] [Google Scholar]
Лина Б., Бес М., Ванденеш Ф., Гренландия Т., Этьен Дж., Флеретт Дж. Роль бактериофагов в геномной изменчивости родственных коагулазонегативных стафилококков. ФЭМС микробиол. лат. 1993; 109: 273–277. doi: 10.1111/j.1574-6968.1993.tb06180.x. [PubMed] [CrossRef] [Google Scholar]
51. Гутьеррес Д., Мартинес Б., Родригес А., Гарсия П. Геномная характеристика двух бактериофагов Staphylococcus epidermidis с антибиопленочным потенциалом. Геномика BMC. 2012;13:228. дои: 10.1186/1471-2164-13-228. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Асуани В., Тремблей Д.М., Муано С., Шукла С.К. Бактериофаги Staphylococcus epidermidis из носовых ходов человека. заявл. Окружающая среда. микробиол. 2011;77:7853–7855. doi: 10.1128/AEM.05367-11. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
53. Boussard P., Pithsy A., Devleeschouwer MJ, Dony J. Фаговое типирование коагулазонегативных стафилококков. Дж. Клин. фарм. тер. 1992; 17: 165–168. [PubMed] [Google Scholar]
54. Barcs I., Herendi A., Lipcsey A., Bognar C., Hashimoto H. Фаговый паттерн и паттерн устойчивости к антибиотикам коагулазонегативных стафилококков, полученных от пациентов с ослабленным иммунитетом. микробиол. Иммунол. 1992;36:947–959. [PubMed] [Google Scholar]
Barcs I., Herendi A., Lipcsey A., Bognar C., Hashimoto H. Фаговый паттерн и паттерн устойчивости к антибиотикам коагулазонегативных стафилококков, полученных от пациентов с ослабленным иммунитетом. микробиол. Иммунол. 1992;36:947–959. [PubMed] [Google Scholar]
55. Бес М., Акерманн Х.В., Брун Ю., Флеретт Дж. Морфология бактериофагов Staphylococcus saprophyticus. Рез. Вирол. 1990; 141: 625–635. doi: 10.1016/0923-2516(90)
-H. [PubMed] [CrossRef] [Google Scholar]56. Бес М. Характеристика тринадцати бактериофагов Staphylococcus epidermidis и S. saprophyticus. Рез. Вирол. 1994; 145:111–121. doi: 10.1016/S0923-2516(07)80013-6. [PubMed] [CrossRef] [Google Scholar]
57. Гутьеррес Д., Мартинес Б., Родригес А., Гарсия П. Выделение и характеристика бактериофагов, инфицирующих Staphylococcus epidermidis. Курс. микробиол. 2010; 61: 601–608. doi: 10.1007/s00284-010-9659-5. [PubMed] [CrossRef] [Google Scholar]
58. Даниэль А., Боннен П.Е., Фишетти В.А. Первая полная последовательность генома двух бактериофагов Staphylococcus epidermidis. Дж. Бактериол. 2007;189:2086–2100. doi: 10.1128/JB.01637-06. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Дж. Бактериол. 2007;189:2086–2100. doi: 10.1128/JB.01637-06. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
59. Madhusoodanan J., Seo K.S., Remortel B., Park J.Y., Hwang S.Y., Fox L.K., Park YH, Deobald C.F., Wang D., Liu С., Догерти С.К., Гилл А.Л., Бохач Г.А., Гилл С.Р. Островок патогенности, несущий энтеротоксин, у Staphylococcus epidermidis. Дж. Бактериол. 2011;193: 1854–1862. [PMC free article] [PubMed] [Google Scholar]
60. Ackermann H.W., DuBow M.S., Jarvis A.W., Jones L.A., Крылов В.Н., Maniloff J., Rocourt J., Safferman R.S., Schneider J., Seldin L., и другие. Концепция вида и ее применение к хвостатым фагам. Арка Вирол. 1992; 124:69–82. doi: 10.1007/BF01314626. [PubMed] [CrossRef] [Google Scholar]
61. Lee J.S., Stewart P.R. Белки вириона и ультраструктура бактериофагов Staphylococcus aureus. Дж. Генерал Вирол. 1985;66:2017–2027. дои: 10.1099/0022-1317-66-9-2017. [PubMed] [CrossRef] [Google Scholar]
62. Стюарт П.Р., Уолдрон Х.Г. , Ли Дж.С., Мэтьюз П.Р. Молекулярные отношения между бактериофагами серогруппы B золотистого стафилококка. Дж. Вирол. 1985; 55: 111–116. [PMC free article] [PubMed] [Google Scholar]
, Ли Дж.С., Мэтьюз П.Р. Молекулярные отношения между бактериофагами серогруппы B золотистого стафилококка. Дж. Вирол. 1985; 55: 111–116. [PMC free article] [PubMed] [Google Scholar]
63. Пантучек Р., Доскар Ю., Ружичкова В., Каспарек П., Оракова Е., Квардова В., Росыпаль С. Идентификация типов бактериофагов и их носительство у золотистого стафилококка. Арка Вирол. 2004; 149:1689–1703. doi: 10.1007/s00705-004-0335-6. [PubMed] [CrossRef] [Академия Google]
64. Brussow H., Desiere F. Сравнительная геномика фагов и эволюция Siphoviridae: выводы из молочных фагов. Мол. микробиол. 2001; 39: 213–222. doi: 10.1046/j.1365-2958.2001.02228.x. [PubMed] [CrossRef] [Google Scholar]
65. Ле Маррек С., Ван Синдерен Д., Уолш Л., Стэнли Э., Флегелс Э., Муано С., Хайнце П., Фитцджеральд Г., Файард Б. На основе способа упаковки и генетических детерминант основных структурных белков можно выделить две группы бактериофагов, инфицирующих Streptococcus thermophilus. заявл. Окружающая среда. микробиол. 1997;63:3246–3253. [Бесплатная статья PMC] [PubMed] [Google Scholar]
микробиол. 1997;63:3246–3253. [Бесплатная статья PMC] [PubMed] [Google Scholar]
66. Lavigne R., Darius P., Summer E.J., Seto D., Mahadevan P., Nilsson A.S., Ackermann H.W., Kropinski A.M. Классификация бактериофагов Myoviridae по сходству белковых последовательностей. БМС микробиол. 2009; 9:224. дои: 10.1186/1471-2180-9-224. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
67. Lavigne R., Seto D., Mahadevan P., Ackermann H.W., Kropinski A.M. Объединение классической и молекулярной таксономической классификации: анализ Podoviridae с использованием инструментов на основе BLASTP. Рез. микробиол. 2008;159: 406–414. doi: 10.1016/j.resmic.2008.03.005. [PubMed] [CrossRef] [Google Scholar]
68. Chibani-Chennoufi S., Dillmann M.L., Marvin-Guy L., Rami-Shojaei S., Brussow H. Бактериофаг Lactobacillus plantarum LP65: новый член SPO1- как род семейства Myoviridae. Дж. Бактериол. 2004; 186:7069–7083. doi: 10.1128/JB.186.21.7069-7083.2004. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
69. Grossi P.A. Ранняя адекватная терапия грамположительных инфекций кровотока: консервативное применение новых препаратов. Междунар. Дж. Антимикроб. Агенты. 2009 г.;34(Приложение 4):S31–34. doi: 10.1016/S0924-8579(09)70563-1. [PubMed] [CrossRef] [Google Scholar]
Grossi P.A. Ранняя адекватная терапия грамположительных инфекций кровотока: консервативное применение новых препаратов. Междунар. Дж. Антимикроб. Агенты. 2009 г.;34(Приложение 4):S31–34. doi: 10.1016/S0924-8579(09)70563-1. [PubMed] [CrossRef] [Google Scholar]
70. Каханкова Дж., Пантучек Р., Гёрке С., Ружичкова В., Холохова П., Доскар Дж. Стратегия типирования методом мультилокусной ПЦР для дифференциации сифовирусов Staphylococcus aureus, отражающая их модульность. структура генома. Окружающая среда. микробиол. 2010;12:2527–2538. doi: 10.1111/j.1462-2920.2010.02226.x. [PubMed] [CrossRef] [Google Scholar]
71. Ровер Ф., Эдвардс Р. Протеомное дерево фагов: таксономия фагов на основе генома. Дж. Бактериол. 2002;184:4529–4535. doi: 10.1128/JB.184.16.4529-4535.2002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
72. Lima-Mendez G., Toussaint A., Leplae R. Модульное представление геномного пространства бактериофагов: идентификация модулей маркеров хозяина и образа жизни. Рез. микробиол. 2011; 162:737–746. doi: 10.1016/j.resmic.2011.06.006. [PubMed] [CrossRef] [Google Scholar]
Рез. микробиол. 2011; 162:737–746. doi: 10.1016/j.resmic.2011.06.006. [PubMed] [CrossRef] [Google Scholar]
73. Hatfull GF, Hendrix RW Бактериофаги и их геномы. Курс. мнение Вирол. 2011; 1: 298–303. doi: 10.1016/j.coviro.2011.06.009. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
74. Ma XX, Ito T., Kondo Y., Cho M., Yoshizawa Y., Kaneko J., Katai A., Higashiide M., Ли С., Хирамацу К. В Японии преобладают две разные линии лейкоцидиновых фагов Пантон-Валентин. Дж. Клин. микробиол. 2008;46:3246–3258. doi: 10.1128/JCM.00136-08. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
75. Ma X.X., Ito T., Chongtrakool P., Hiramatsu K. Преобладание клонов, несущих гены лейкоцидина Panton-Valentine среди выделенных метициллин-резистентных штаммов Staphylococcus aureus в японских больницах с 1979 по 1985. Дж. Клин. микробиол. 2006;44:4515–4527. doi: 10.1128/JCM.00985-06. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
76. Нарита С., Канеко Дж. , Чиба Дж., Пьемонт Ю., Жарро С., Этьен Дж., Камио Ю. Фаговая конверсия Пантона -Лейкоцидин Валентина в Staphylococcus aureus: молекулярный анализ фага, превращающего PVL, phiSLT. Ген. 2001; 268:195–206. doi: 10.1016/S0378-1119(01)00390-0. [PubMed] [CrossRef] [Google Scholar]
, Чиба Дж., Пьемонт Ю., Жарро С., Этьен Дж., Камио Ю. Фаговая конверсия Пантона -Лейкоцидин Валентина в Staphylococcus aureus: молекулярный анализ фага, превращающего PVL, phiSLT. Ген. 2001; 268:195–206. doi: 10.1016/S0378-1119(01)00390-0. [PubMed] [CrossRef] [Google Scholar]
77. Яндоло Дж. Дж., Уоррелл В., Гройхер К. Х., Цянь Ю., Тиан Р., Кентон С., Дорман А., Джи Х., Лин С., Ло П. ., Qi S., Zhu H., Roe B.A. Сравнительный анализ геномов умеренных бактериофагов phi 11, phi 12 и phi 13 Staphylococcus aureus 8325. Gene. 2002;289: 109–118. doi: 10.1016/S0378-1119(02)00481-X. [PubMed] [CrossRef] [Google Scholar]
78. Zhang M., Ito T., Li S., Jin J., Takeuchi F., Lauderdale T.L., Higashide M., Hiramatsu K. Идентификация третьего типа Фаг PVL в штаммах ST59, устойчивых к метициллину Staphylococcus aureus (MRSA). ФЭМС микробиол. лат. 2011; 323:20–28. doi: 10.1111/j.1574-6968.2011.02355.x. [PubMed] [CrossRef] [Google Scholar]
79. Белкейд М., Бержерон А., Пуассон Г. Мозаичные графики и сравнительная геномика в фаговых сообществах.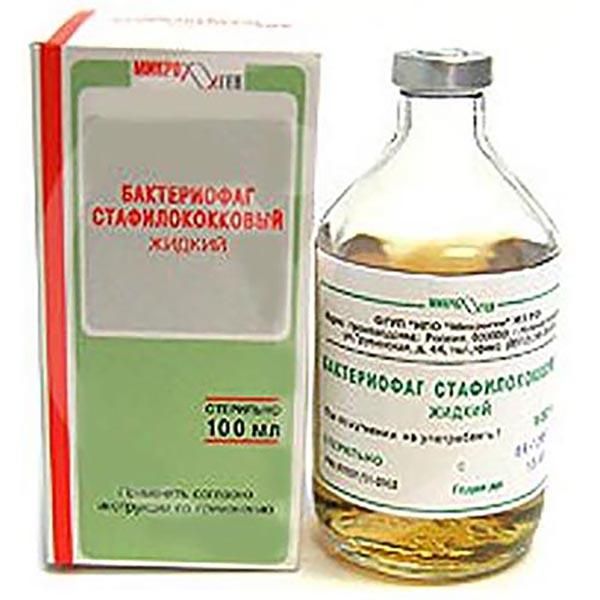 Дж. Вычисл. биол. 2010;17:1315–1326. дои: 10.1089/смб.2010.0108. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
Дж. Вычисл. биол. 2010;17:1315–1326. дои: 10.1089/смб.2010.0108. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
80. Зюскинд М.М., Ботштейн Д. Молекулярная генетика бактериофага Р22. микробиол. 1978; 42:385–413. [Бесплатная статья PMC] [PubMed] [Google Scholar]
81. Clark A.J., Inwood W., Cloutier T., Dhillon T.S. Нуклеотидная последовательность колифага HK620 и эволюция лямбдоидных фагов. Дж. Мол. биол. 2001; 311: 657–679. doi: 10.1006/jmbi.2001.4868. [PubMed] [CrossRef] [Google Scholar]
82. Хендрикс Р. В. Бактериофаги: эволюция большинства. Теор. Народ. биол. 2002; 61: 471–480. doi: 10.1006/tpbi.2002.1590. [PubMed] [CrossRef] [Google Scholar]
Намбури С., Пайчини К.В., Попович М.Г., Шлейхер Д.Т., Симанек Б.З., Смит А.Л., Зданович Г.М., Кумар В., Пиблз К.Л., Джейкобс В.Р., младший, Лоуренс Дж.Г., Хендрикс Р.В. Изучение метапротеома микобактериофагов: фаговая геномика как образовательная Платформа. Генетика PLoS. 2006;2:e92. doi: 10.1371/journal. pgen.0020092. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
pgen.0020092. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
84. Глазко Г., Макаренков В., Лю Дж., Мушегян А. Эволюционная история бактериофагов с двухцепочечными геномами ДНК. биол. Прямой. 2007; 2:36. doi: 10.1186/1745-6150-2-36. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
85. Хьюсон Д.Х., Брайант Д. Применение филогенетических сетей в эволюционных исследованиях. Мол. биол. Эвол. 2006; 23: 254–267. doi: 10.1093/molbev/msj030. [PubMed] [CrossRef] [Академия Google]
86. Лоуренс Дж. Г., Хатфулл Г. Ф., Хендрикс Р. В. Запутанная таксономия вирусов: генетический обмен и недостатки фенетических подходов. Дж. Бактериол. 2002; 184:4891–4905. doi: 10.1128/JB.184.17.4891-4905.2002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
87. Лима-Мендез Г., Ван Хелден Дж., Туссен А., Лепла Р. Сетчатое представление эволюционных и функциональных отношений между фаговыми геномами. Мол. биол. Эвол. 2008; 25: 762–777. doi: 10.1093/molbev/msn023. [PubMed] [CrossRef] [Академия Google]
[PubMed] [CrossRef] [Академия Google]
88. Манн Н.Х. Потенциал фагов для предотвращения инфекций MRSA. Рез. микробиол. 2008; 159:400–405. doi: 10.1016/j.resmic.2008.04.003. [PubMed] [CrossRef] [Google Scholar]
89. Lu T.K., Koeris M.S. Бактериофаговая терапия нового поколения. Курс. мнение микробиол. 2011; 14: 524–531. doi: 10.1016/j.mib.2011.07.028. [PubMed] [CrossRef] [Google Scholar]
90. Мацудзаки С., Ясуда М., Нишикава Х., Курода М., Уджихара Т., Шуин Т., Шен Ю., Джин З., Фудзимото С., Насимуззаман М.Д., Вакигучи Х., Сугихара С., Сугиура Т., Кода С., Мураока А., Имаи С. Экспериментальная защита мышей от смертельной инфекции Staphylococcus aureus с помощью нового бактериофага phi MR11. Дж. Заразить. Дис. 2003; 187: 613–624. дои: 10.1086/374001. [PubMed] [CrossRef] [Академия Google]
91. Квиатек М., Парасион С., Мизак Л., Грико Р., Бартоще М., Коцик Дж. Характеристика бактериофага, выделенного от коровы с маститом, литического против штаммов Staphylococcus aureus.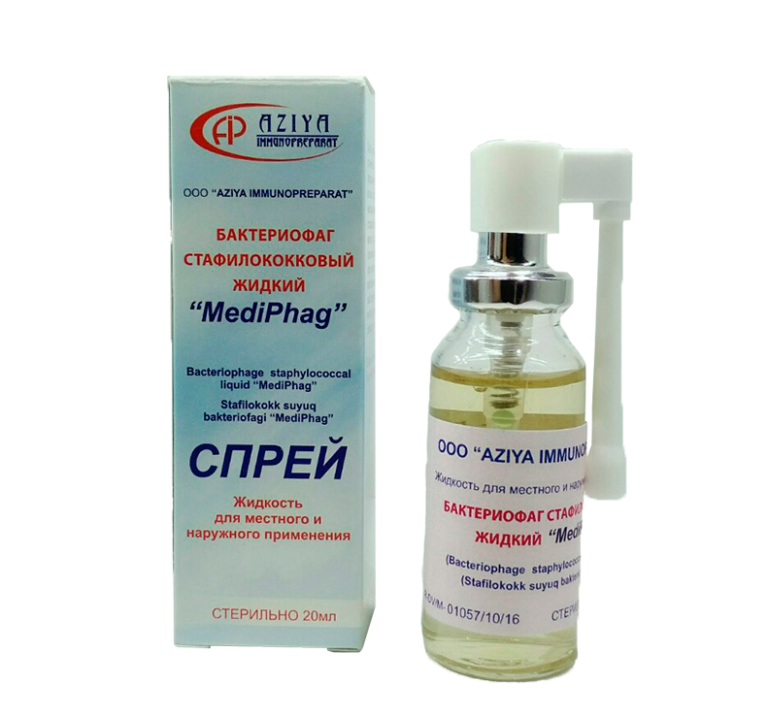 Арка Вирол. 2012; 157: 225–234. doi: 10.1007/s00705-011-1160-3. [PubMed] [CrossRef] [Google Scholar]
Арка Вирол. 2012; 157: 225–234. doi: 10.1007/s00705-011-1160-3. [PubMed] [CrossRef] [Google Scholar]
92. Hagens S., Loessner MJ Бактериофаги для биоконтроля пищевых патогенов: расчеты и соображения. Курс. фарм. Биотехнолог. 2010;11:58–68. дои: 10.2174/138920110790725429. [PubMed] [CrossRef] [Google Scholar]
93. Bueno E., Garcia P., Martinez B., Rodriguez A. Фаговая инактивация Staphylococcus aureus в свежих и твердых сырах. Междунар. Дж. Пищевая микробиология. 2012; 158:23–27. doi: 10.1016/j.ijfoodmicro.2012.06.012. [PubMed] [CrossRef] [Google Scholar]
94. Гарсия П., Мадера К., Мартинес Б., Родригес А., Эваристо Суарес Дж. Распространенность бактериофагов, заражающих золотистый стафилококк, в образцах молочных продуктов и их потенциал в качестве агентов биологической борьбы. Дж. Молочная наука. 2009 г.;92:3019–3026. doi: 10.3168/jds.2008-1744. [PubMed] [CrossRef] [Google Scholar]
95. Гарсия П., Мартинес Б., Обесо Дж. М., Родригес А. Бактериофаги и их применение в пищевой безопасности. лат. заявл. микробиол. 2008; 47: 479–485. doi: 10.1111/j.1472-765X.2008.02458.x. [PubMed] [CrossRef] [Google Scholar]
лат. заявл. микробиол. 2008; 47: 479–485. doi: 10.1111/j.1472-765X.2008.02458.x. [PubMed] [CrossRef] [Google Scholar]
96. Фишетти В.А. Эндолизины бактериофагов: новое противоинфекционное средство для контроля грамположительных патогенов. Междунар. Дж. Мед. микробиол. 2010; 300:357–362. doi: 10.1016/j.ijmm.2010.04.002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
97. O’Flaherty S., Coffey A., Meaney W., Fitzgerald G.F., Ross R.P. Рекомбинантный фаговый лизин LysK обладает широким спектром литической активности в отношении клинически значимых стафилококков, включая метициллин-резистентный Staphylococcus aureus. Дж. Бактериол. 2005; 187:7161–7164. doi: 10.1128/JB.187.20.7161-7164.2005. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
98. O’Flaherty S., Ross R.P., Meaney W., Fitzgerald G.F., Elbreki MF, Coffey A. Потенциал поливалентного антистафилококкового бактериофага K для борьбы с устойчивыми к антибиотикам стафилококками из больниц. заявл. Окружающая среда. микробиол. 2005; 71: 1836–1842. doi: 10.1128/AEM.71.4.1836-1842.2005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Окружающая среда. микробиол. 2005; 71: 1836–1842. doi: 10.1128/AEM.71.4.1836-1842.2005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
99. Се С.Э., Ло Х.Х., Чен С.Т., Ли М.К., Ценг Ю.Х. Широкий круг хозяев и сильная литическая активность лизирующего фага Staphylococcus aureus Stau2. заявл. Окружающая среда. микробиол. 2011; 77: 756–761. doi: 10.1128/AEM.01848-10. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
100. O’Flaherty S., Ross R.P., Flynn J., Meaney WJ, Fitzgerald G.F., Coffey A. Выделение и характеристика двух антистафилококковых бактериофагов специфичен для патогенного золотистого стафилококка, связанного с инфекциями крупного рогатого скота. лат. заявл. микробиол. 2005; 41: 482–486. doi: 10.1111/j.1472-765X.2005.01781.x. [PubMed] [CrossRef] [Академия Google]
101. Мерабишвили М., Пирнай Ж.П., Вербекен Г., Чанишвили Н., Тедиашвили М., Лашхи Н., Глонти Т., Крылов В., Маст Дж., Ван Парис Л., Лавин Р., Волкерт Г. ., Маттеус В. , Вервин Г., Де Корте П., Роуз Т., Дженнес С., Зизи М., Де Вос Д., Ванихутте М. Мелкосерийное производство четко определенного коктейля бактериофагов с контролем качества для использование в клинических испытаниях на людях. ПЛОС Один. 2009;4:e4944. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Вервин Г., Де Корте П., Роуз Т., Дженнес С., Зизи М., Де Вос Д., Ванихутте М. Мелкосерийное производство четко определенного коктейля бактериофагов с контролем качества для использование в клинических испытаниях на людях. ПЛОС Один. 2009;4:e4944. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Экспериментальная фаготерапия против золотистого стафилококка у мышей
1. Adams, M.H. 1959. Методы изучения бактериальных вирусов, с. 447-448. В Бактериофаги. Издательство Interscience, Лондон, Великобритания.
2. Беккер, К., Р. Рот и Г. Петерс. 1998. Быстрое и специфическое обнаружение токсигенного Staphylococcus aureus : использование двух иммуноферментных анализов мультиплексной ПЦР для амплификации и гибридизации генов стафилококкового энтеротоксина, генов эксфолиативного токсина и гена токсина синдрома токсического шока 1. Дж. Клин. микробиол. 36 : 2548-2553. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Бинетти, А. Г., Б. Дель Рио, М. Круз Мартин и М. А. Альварес. 2005. Обнаружение и характеристика бактериофагов Streptococcus thermophilus с использованием последовательности гена антирецептора. заявл. Окружающая среда. микробиол. 71
Бинетти, А. Г., Б. Дель Рио, М. Круз Мартин и М. А. Альварес. 2005. Обнаружение и характеристика бактериофагов Streptococcus thermophilus с использованием последовательности гена антирецептора. заявл. Окружающая среда. микробиол. 71
4. Biswas, B., S. Adhya, P. Washart, B. Paul, A.N. Trostel, B. Powell, R. Carlton и CR Merril. 2002. Бактериофаговая терапия спасает мышей с бактериемией от клинического изолята устойчивого к ванкомицину Enterococcus faecium . Заразить. Иммун. 70 : 204-210. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Броксмейер Л., Д. Сосновска, Э. Милтнер, О. Чакон, Д. Вагнер, Дж. МакГарви, Р. Г. Барлетта и Л. Э. Бермудес. 2002. Уничтожение Mycobacterium avium и Mycobacterium tuberculosis микобактериофагом, доставляемым невирулентной микобактерией: модель фаговой терапии внутриклеточных бактериальных патогенов. Дж. Заразить. Дис. 186 : 1155-1160. [PubMed] [Google Scholar]
Дж. Заразить. Дис. 186 : 1155-1160. [PubMed] [Google Scholar]
6. Bull, JJ, B.R. Levin, T. DeRouin, N. Walker, and C.A. Bloch. 2002. Динамика успеха и неудачи фаго- и антибиотикотерапии при экспериментальных инфекциях. БМС микробиол. 2 : 35. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Bull, JJ, and R.R. Regoes. 2006. Фармакодинамика нереплицирующихся вирусов, бактериоцинов и лизинов. проц. биол. науч. 273 : 2703-2712. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Каппарелли Р., И. Вентимилья, С. Роперто, Д. Фениция и Д. Яннелли. 2006. Селекция бактериофага Escherichia coli O157:H7 на персистенцию в кровеносной системе мышей, инфицированных экспериментально. клин. микробиол. Заразить. 12 : 248-253. [PubMed] [Google Scholar]
9. Клеман С., П. Водо, П. Франсуа, Дж. Шренцель, Э. Хагглер, С. Кампф, К. Шапонье, Д. Лью и Дж. С. Лакруа.
Кампф, К. Шапонье, Д. Лью и Дж. С. Лакруа.
10. Dixon, B. 2004. Новый рассвет фаговой терапии. Ланцет Инфекция. Дис. 4 : 186. [PubMed] [Google Scholar]
11. Fischetti, V. 2004. Vincent Fischetti — следование фагам на всю жизнь. Ланцет Инфекция. Дис. 4 : 246-249. [PubMed] [Google Scholar]
12. Foster, JF 2005. Уклонение от иммунитета стафилококками. Нац. Преподобный Микробиолог. 3 : 948-958. [PubMed] [Google Scholar]
13. Jarraud, S., C. Mougel, J. Thioulouse, G. Lina, H. Meugnier, F. Forey, X. Nesme, J. Etienne и F. Vandenesch. 2002. Взаимосвязь между генетическим фоном Staphylococcus aureus
, факторами вирулентности, группами agr (аллелями) и заболеванием человека. Заразить. Иммун. 70 : 631-641. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Заразить. Иммун. 70 : 631-641. [Бесплатная статья PMC] [PubMed] [Google Scholar]14. Lederberg, J. 1996. Меньшие блохи… до бесконечности: терапевтический бактериофаговый редукс. проц. Натл. акад. науч. США 93 : 3167-3168. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15. Leeb, M. 2004. Антибиотики: укол в руку. Природа 431 : 892-893. [PubMed] [Google Scholar]
16. Лейд, Дж. Г., М. Э. Ширтлифф, Дж. В. Костертон и П. Стадли. 2002. Лейкоциты человека прикрепляются к биопленкам Staphylococcus aureus , проникают в них и реагируют на них. Заразить. Иммун. 70 : 6339-6345. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Левин Б.Р., Розен Д.Е. 2006. Ненаследуемая устойчивость к антибиотикам. Нац. Преподобный Микробиолог. 4 : 556-561. [PubMed] [Google Scholar]
18. Левин Б. Р. и Р. Антиа. 2001. Почему мы не болеем: внутрихозяинная динамика бактериальных инфекций. Наука 292 : 1112-1115. [PubMed] [Google Scholar]
Р. и Р. Антиа. 2001. Почему мы не болеем: внутрихозяинная динамика бактериальных инфекций. Наука 292 : 1112-1115. [PubMed] [Google Scholar]
19. Леви С. Б. и Б. Маршалл. 2004. Устойчивость к антибиотикам во всем мире: причины, проблемы и ответы. Нац. Мед. 10 : 122-129. [PubMed] [Google Scholar]
20. Lowy, F.D. 1998. Staphylococcus aureus инфекции. Н. англ. Дж. Мед. 339 : 520-532. [PubMed] [Google Scholar]
21. Mason, WJ, JS Blevins, K. Beenken, N. Wibowo, N. Ojma, and M.S. Smeltzer. 2001. Протокол мультиплексной ПЦР для диагностики стафилококковых инфекций. Дж. Клин. микробиол. 39 : 3332-3338. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Мацудзаки С., М. Ясуда, Х. Нисикава, М. Курода, Т. Уджихара, Т. Шуин, Ю. Шен, З. Джин, С. Фуймото, М. Д. Насимуццан, Х. Вакигути, С. Сугухара, Т. Сугиура, С. Кода, А. Мураока и С. Имаи. 2003. Экспериментальная защита мышей от смертельной инфекции Staphylococcus aureus новым бактериофагом φMR11. Дж. Заразить. Дис. 187 : 613-624. [PubMed] [Google Scholar]
Кода, А. Мураока и С. Имаи. 2003. Экспериментальная защита мышей от смертельной инфекции Staphylococcus aureus новым бактериофагом φMR11. Дж. Заразить. Дис. 187 : 613-624. [PubMed] [Google Scholar]
23. McClean, KL, GJ Sheehan, and KM Harding. 1994. Интраабдоминальная инфекция: обзор. клин. Заразить. Дис. 19 : 100-116. [PubMed] [Google Scholar]
24. Мехротра, М., Г. Ван и В. М. Джонсон. 2000. Мультиплексная ПЦР для выявления генов энтеротоксинов
25. Merril, C.R., B. Biswas, R. Carlton, NC Jensen, GJ Creed, S. Zullo и S. Adhya. 1996. Длительно циркулирующие бактериофаги как антибактериальные средства. проц. Натл. акад. науч. США 93 : 3188-3192. [Бесплатная статья PMC] [PubMed] [Google Scholar]
США 93 : 3188-3192. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Паллисер Д., Д. Чоудхури, К.Ю. Ван, С.Дж. Ли, Р.Т. Бронсон, Д.М. Найп и Дж. Либерман. 2006. Микробицид на основе миРНК защищает мышей от смертельной инфекции вирусом простого герпеса 2. Природа 439 : 89-94. [PubMed] [Google Scholar]
27. Пейн, Дж. Х. и В. А. Янсен. 2000. Фаговая терапия: своеобразная кинетика самовоспроизводящегося лекарственного препарата. клин. Фармакол. тер. 68 : 225-229. [PubMed] [Google Scholar]
28. Кази, С. Н., С. Э. Харрисон, Т. Селф, П. Уильямс и Дж. Хилл. 2004. Мониторинг внутриклеточной репликации Staphylococcus aureus в режиме реального времени. Дж. Бактериол. 186 : 1065-1077. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Sambrook, J., EF Fritsch, and T. Maniatis. 1989. Молекулярное клонирование: лабораторное пособие, 2-е изд. Лабораторный пресс Колд-Спринг-Харбор, Колд-Спринг-Харбор, Нью-Йорк.
Лабораторный пресс Колд-Спринг-Харбор, Колд-Спринг-Харбор, Нью-Йорк.
30. Smith, H.W., M.B. Huggins, and K.M. Shaw. 1987. Борьба с экспериментальной диареей Escherichia coli у телят с помощью бактериофагов. J. Gen. Microbiol. 133 : 1111-1126. [PubMed] [Google Scholar]
31. Stearne, L.E., IC Gyssens, WH Goessens, JW Mouton, WJ Oyen, JW Van der Meer и HA Verbrugh. 2001. Эффективность тровафлоксацина in vivo в отношении Bacteroides fragilis при смешанной инфекции либо с Escherichia coli , либо с устойчивым к ванкомицину штаммом Enterococcus faecium на мышиной модели установленного абсцесса. Антимикроб. Агенты Чемотер. 45 : 1394-1401. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Сулаквелидзе А., Алавидзе З. и Моррис Дж. Г. 2001. Бактериофаговая терапия. Антимикроб. Агенты Чемотер. 45 : 649-659. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Tenover, F.C., L.M. Weigel, PC Appelbaum, LK McDougal, J. Chaitram, S. McAllistar, N. Clark, G. Killgore, C.M. O’Hara , Л. Джевитт, Дж. Б. Патель и Б. Боздоган. 2004. Устойчивый к ванкомицину изолят от пациента в Пенсильвании. Антимикроб. Агенты Чемотер. 48 : 275-280. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Tenover, F.C., L.M. Weigel, PC Appelbaum, LK McDougal, J. Chaitram, S. McAllistar, N. Clark, G. Killgore, C.M. O’Hara , Л. Джевитт, Дж. Б. Патель и Б. Боздоган. 2004. Устойчивый к ванкомицину изолят от пациента в Пенсильвании. Антимикроб. Агенты Чемотер. 48 : 275-280. [Бесплатная статья PMC] [PubMed] [Google Scholar]
34. Вейгель, Л. М., Д. Б. Клеуэлл, С. Р. Гилл, Н. К. Кларк, Л. К. Макдугал, С. Э. Фланнаган, Дж. Ф. Колонай, Дж. Шетти, Г. Э. Киллгор и Ф. К. Теновер. 2003. Генетический анализ высокорезистентного к ванкомицину изолята Staphylococcus aureus . Наука 302 : 1569-1571. [PubMed] [Google Scholar]
35. Вестуотер, К., Л. М. Касман, А. Шофилд, П. А. Вернер, Дж. В. Долан, М. Г. Шмидт и Дж. С. Норрис. 2003. Использование генно-инженерного фага для доставки противомикробных агентов к бактериям: альтернативная терапия для лечения бактериальных инфекций. Антимикроб. Агенты Чемотер.





