Антибиотики при ротовирусе у детей и взрослых
Антибиотики при ротавирусной инфекции не принимаются, так как они предназначены для борьбы с бактериями, а не вирусами. Заболевшие часто занимаются самолечением и назначают препараты себе сами, не подозревая, что лечение ротавируса антибиотиками совершенно не эффективно.
Антибиотики назначают при появлении бактериальной инфекции, в случаях, когда организм не справляется с болезнью самостоятельно, а применение препаратов иных фармакологических групп не дает положительного эффекта. Также следует знать, что антибиотики совершенно не эффективны при вирусных инфекциях.

Отличие Вируса от Бактерии
В своих интервью доктор Комаровский так же говорит, что антибиотик при ротовирусе не нужен. По мнению Комаровского лечение антибиотиками должно расцениваться, как перестраховка врача и нежелание брать на себя ответственность за пациента, или некомпетентность.
Антибиотики при ротовирусе у детей и взрослых
Применение антибиотиков в случае вирусной кишечной инфекции оправдано в следующих случаях:
- фрагменты крови в кале;
- диарея, не прекращающаяся более 10 дней.
Антибиотик так же оправдан в случае, когда например в инфекционной больнице к ротавирусной инфекции добавляется бактериальная.
Решение о применении антибиотиков при ротавирусной инфекции у детей принимает только педиатр или лечащий врач в больнице.
Злоупотребление антибиотиками уменьшает их эффективность, стимулирует рост устойчивых к антибиотикам бактерий, что является серьезной и актуальной проблемой сегодня во всем мире. Постоянно нужны все более сильные антибиотики, чтобы лечить те бактериальные осложнения, с которыми раньше справлялся даже пенициллин.
ЗАПОМНИТЕ, что антибиотик не снижает температуру, не лечит на кашель, не уменьшает интоксикацию, не устраняет головную боль при ротавирусе. Если бактерии нет, то антибиотик ничем не поможет.
Чем отличается ротавирус от отравления. Отличия в лечении
Ротавирус и отравление – заболевания, которые часто возникают в детском возрасте, но встречаются и у взрослых. Такие состояния сходны по симптоматике и очень опасны, если не предпринять вовремя правильных мер по улучшению самочувствия человека и восстановлению баланса в его организме. Давайте узнаем, как отличить ротавирус от отравления, что делать в каждом случае.
Ротавирус – одна из форм кишечной инфекции. Болезнь имеет и другие названия – кишечный грипп и ротавирусный гастроэнтерит. Источником заражения обычно является больной человек, а само заболевание распространяется очень быстро по группе тесно общающихся между собой людей.
Основной способ передачи инфекции – фекально-оральный. Из-за характера распространения ротавирус чаще всего возникает именно в детском возрасте. Ведь этот период жизни – время особенной любознательности, когда ребёнок тянет всё в рот, изучает предметы на вкус, тесно общается с другими детьми.
Что такое отравление
Отравление – попадание в организм токсинов и ядов, а также вызванное этим нарушение работы органов и систем человеческого тела. Такое состояние может быть нескольких видов в зависимости от пути проникновения вредных веществ в организм:
- ингаляционным, то есть когда яды и токсины попадают через дыхательные пути, например отравление газом;
- пероральным, когда ядовитое вещество попало в тело человека через рот, в том числе самые распространённые пищевые отравления;
- инъекционным, когда яд попал через внутримышечные и внутривенные инъекции;
- перкутанным, когда токсины и вредные вещества поступили в организм через кожные поры и открытые раневые поверхности.
Обычно люди разного возраста страдают именно от пищевых отравлений. Вызваны они употреблением в пищу несвежих и некачественных продуктов и напитков. Выяснение у человека, что он перед ухудшением своего самочувствия ел, пил, делал, чаще всего помогают врачу отличить отравление от ротавирусной инфекции и поставить предварительный диагноз.
Чем отличается ротавирус от отравления
Отличия в причинах заболеваний
Ротавирус – инфекция, которая быстро передаётся от заболевшего или от носителя вируса человека к контактирующему с ним здоровому. В этом случае заболевание поражает весь детский или взрослый коллектив, быстро распространяется на всех домочадцев.
Причинами отравления становятся химикаты, токсины, выделяемые микроорганизмами, а также другие вредные вещества. Основной источник возникновения этого состояния – продукты питания и напитки с истёкшим сроком годности, неправильно хранившиеся или же содержащие в составе вредные вещества (например, алкоголь). Иногда причиной отравления становится неаккуратность, когда взрослый или ребёнок по ошибке или из-за любознательности съедает что-то заведомо вредное, например, одеколон, моющие средства, лекарственные препараты в недопустимых дозировках.
Отличия симптомов
Симптоматика ротавируса и отравления очень похожи. Именно из-за своих проявлений эти два состояния часто путают между собой. Причём в обоих случаях признаки могут быть как яркими, так и едва заметными. Иногда ротавирус и отравление протекают бессимптомно и сопровождаются лишь незначительной слабостью, разовым поносом или же небольшим снижением аппетита. Тем не менее и в симптомах есть отличия.
Основные симптомы ротавирусной инфекции такие:
- изменение цвета слизистой во рту и глотке, налёт на языке;
- покашливание и заложенность носа;
- вялость, сонливость и апатия;
- лихорадочное состояние;
- высокая температура, особенно характерное для детского возраста;
- слабость и снижение работоспособности;
- заложенность носа и покашливание;
- боли в животе;
- полный отказ от пищи;
- частая рвота;
- покраснение горла и глазной конъюнктивы;
- жидкий стул с неприятным кислым запахом.
Спустя сутки без проведения правильного лечения ротавируса организм человека начинает страдать от интоксикации и обезвоживания, что может привести к серьёзным последствиям. За несколько дней больной теряет в весе. При подборе подходящего лечения симптомы отступают уже на следующий день. А полное выздоровление наступает через 3-7 дней.
Отравление имеет сходные, но несколько другие симптомы, чем у ротавируса. Воспаление слизистой оболочки кишечника приводит к появлению таких симптомов интоксикации организма и обезвоживания, как:
- лихорадочное состояние;
- слабость и вялость;
- боли в мышцах и в голове;
- сокращение количества мочеиспусканий;
- рвота, тошнота, головокружение;
- повышение температуры тела;
- появление жажды и сухости во рту;
- частый понос;
- учащение сердцебиения;
- нервные и зрительные расстройства;
- западание родничка в детском возрасте.
При правильном лечении восстановление организма после простого отравления длится около 5-7 дней. Но в особо сложных случаях этот период может затянуться на несколько недель и даже месяцев. В отличие от ротавируса отравления у взрослых и детей чаще всего начинается быстро и сразу у всех, кто питался вместе. При инфекции обычно болеет либо 1 член семьи, либо все, но симптомы начинают проявляться у всех по очереди. Инкубационный период при отравлении — 1,5-3 часа.
Важно! Если вы обнаружили эти симптомы у себя или своих близких, не стоит ждать – необходимо сразу обратиться к врачу. Когда отравление или заражение ротавирусом произошло у ребёнка – позвоните в скорую помощь.
Отличия в течении болезни
Также существуют отличия протекания ротовирусной инфекции от отравления:
- Отличается ротавирус высокой температурой. Отравлению это свойственно только в сложных случаях и в детском возрасте.
- Ротавирус — сезонная болезнь, а отравление может произойти в любое время года.
- Помогут отличить ротавирусную инфекцию и симптомы, которые вы наблюдаете у больного или у себя. В случае ротавируса кроме слабости, тошноты и рвоты, жидкого стула появляются симптомы вируса – заложенность носа, покашливание и головная боль. При отравлении этого не наблюдается, но может появляться боль в мышцах и голове.
- Если вы не знаете, что перед вами – отравление или ротавирус, то обратите внимание на стул, который отличается по запаху и частоте позывов. При ротавирусе он более зловонный, имеющий серовато-жёлтый оттенок. Моча также меняет свой цвет и становится тёмной
- Ротавирус обычно поражает весь школьный или детсадовский коллектив, всех домочадцев, вступающих друг с другом в тесный контакт. А отравление проявляется лишь у тех, кто питался одними и теми же продуктами сомнительного качества.
- Отравление не заразно, чем отличается от энтеровирусной инфекции.
- Отличить инфекцию от отравления можно и по состоянию слизистых оболочек. В первом случае страдают все слизистые, а во втором — только пищеварительной системы.
Отличия в лечении
Различие есть и в лечении обоих заболеваний. При отравлении необходимо как можно скорее промыть желудок, а при ротавирусе это мероприятие не проводится. Причём при отравлении промывание проводится до тех пор, пока не пойдёт обратно только чистая вода. Лечение такого состояния заключается в снятии симптомов интоксикации организма и восстановлении баланса в нём. Для этого применяются:
- препараты сорбенты, выводящие токсины и яды, например, Энтеросгель, активированный уголь, Смекта, Полисорб;
- очистительные клизмы;
- препараты для восстановления водного баланса, например, Регидрон;
- средства для восстановления микрофлоры кишечника, например, Бифдумбактерин, Линекс.
Ротавирус также лечится приёмом медикаментов, но их набор немного отличается:
- жаропонижающие для устранения температуры выше 38,5C, что обычно необходимо только в детском возрасте;
- средства-сорбенты, в том числе Смекта, активированный уголь, Полисорб, Энтеросгель;
- препараты для восстановления водного баланса Регидрон, Тригидрон и другие;
- противодиарейные средства, например, Нифуроксазид, Стопдиар, Энтрофурил;
- препараты для устранения болей в животе, в том чисел Баралгин и Спазмолгон.
Важно! Отличие отравления от ротавируса не всегда явное. Неправильно подобранное лечение может стать причиной осложнений. Поэтому назначить необходимые лекарства может только врач. До его прихода можно при подозрении на ротавирус принять средство-сорбент, препараты для восстановления водного баланса и жаропонижающее. При подозрении на пищевое отравление необходимо вызвать скорую и попытаться промыть желудок. Если симптомы этого недуга не яркие и наблюдаются у взрослых, то можно обойтись только приёмом средств-сорбентов.
Как видите, отравление и ротавирус очень похожи, но являются абсолютно разными по причинам возникновения и мет
Стоит ли давать антибиотики при кишечной инфекции у детей: при ротовирусе, при инфекции

Кишечные инфекции — неприятная реальность. Чаще этот недуг поражает именно детей, а не взрослых, причем, подобно эпидемии, охватывает большие детские коллективы (целые группы в садике или отряды в детских оздоровительных лагерях). Всем родителям, чьи дети посещают дошкольные и школьные учреждения, это знакомо и понятно. Кишечная инфекция у ребенка протекает значительно тяжелее, чем у взрослого. К тому же она чревата обезвоживанием и даже летальным исходом для малыша.
Многие родители, столкнувшись с такой проблемой у ребенка, задаются вопросом, а можно ли принимать антибиотики при кишечной инфекции. Чтобы дать ответ, нужно понимать, что кишечная инфекция – это не какое-то одно конкретное заболевание, это несколько совершенно разных диагнозов. И лечить их тоже надо по-разному.

Нужны ли антибиотики?
Антибиотики при кишечной инфекции назначают, если возбудитель заболевания – бактерия. Если же причиной стал вирус или отравление пищей, антибиотики не нужны. Они не просто не помогут справиться с недугом, но и могут серьезно навредить.
Антибиотики, не способные разрушить вирус при ротавирусной или энтеровирусной инфекции, довольно быстро «расправятся» с полезной кишечной микрофлорой, и организм крохи лишится последних «защитников» при вирусном поносе и рвоте. А сильная интоксикация и обезвоживание после поноса и рвоты могут быть смертельными, особенно для маленьких детей.
Бактериальная кишечная инфекция, или как ее еще называют, «болезнь грязных рук» развивается, если в организм ребенка попадают болезнетворные бактерии. В основном это происходит из-за немытых рук, грязных овощей, непригодной для питья воды, а также во время общения ребенка с зараженными людьми или животными. Бактериальными считают дизентерию, синегнойную палочку, сальмонеллез, холеру, брюшной тиф, ботулизм.

Кишечная инфекция, вызванная вирусом — это всем родителям хорошо знакомые ротавирус, аденовирус и энтеровирус. Чаще всего это сезонные болезни, и атакуют они детей по осени и весной.
Пищевые отравления чаще всего происходят летом, когда из-за жаркой погоды продукты питания портятся быстрее.
Если у ребенка началась диарея, он сильно потеет, его бросает в жар, начинается рвота, а в каловых массах большое количество слизи и даже примеси крови – все это свидетельствует о наличии бактериальной инфекции кишечника, и вопрос применения антибиотиков вполне рационален.


Показания
Обычно лечение кишечной инфекции начинают не сразу, а после установления типа и семейства возбудителя недуга. Но даже если анализы подтверждают, что болезнь имеет бактериальное происхождение, далеко не все всех случаях врач назначит ребенку антибиотики.
Легкие формы кишечной инфекции не нуждаются в сильнодействующих антибактериальных препаратах, с незначительными расстройствами иммунитет ребенка вполне сможет справиться при лечении, основанном на антидиарейных и антирвотных средствах.
По статистике, антибиотики при кишечном недуге врач прописывает в каждом пятом случае (около 20% от общего числа больных бактериальной инфекцией ребят нуждаются в мощной терапии антибиотиками).

Антибиотики необходимы в следующих случаях:
- Инфекции тяжелого протекания. Это дизентерия, брюшной тиф, сальмонеллез, холера и др.
- При сложном протекании инфекции. К примеру, при жидком стуле чаще 10 раз в день в возрасте от 3 лет. Если взрослым антибактериальную терапию назначат при тяжелом состоянии, то ребенку антибиотики показаны уже при средней степени тяжести недуга.
- Если в кале у ребенка есть кровь. Это признак воспаления кишечника. И без антибиотиков вылечить такое воспаление невозможно.
- При состоянии иммунодефицита ребенка.
- При наличии у ребенка опухолей в организме.

Лечение
Лечение антибиотиками при кишечной инфекции обязательно будет комплексным. Такой же подход врачи применяют и к вирусным инфекциям, комплекс препаратов вам назначат и при ротавирусе.
Доктор, помимо антибактериальной терапии, может назначит противорвотные, противодиарейные препараты, а также средства нормализации баланса воды и соли в организме во избежание обезвоживания, например, «Регидрон».
Кроме того, при лечении кишечной инфекции врач обязательно порекомендует давать ребенку бактериофаги «Бактисубтил», «Хилак форте», «Лактулозу», «Бифидумбактерин», «Лактиале» для восстановления естественной защиты кишечника и профилактики дисбактериоза.
Список препаратов
Самыми эффективными «борцами» с микроорганизмами – возбудителями кишечных недугов являются антибиотики цефалоспориновой группы. Но медики сначала назначают тетрациклины (детям старше 8 лет) или пенициллины, и если они не оказывают нужного действия, то переходят к «тяжелой артиллерии» — цефалоспоринам.
Антибиотики – тетрациклины для лечения кишечной инфекции:
- «Доксал». Антибиотик, который довольно эффективно справляется с кишечными микробами разного происхождения. Но этот препарат противопоказан детям до 8 лет, поскольку он образует специфические химические соединения, которые «откладываются» в костном скелете малыша и в эмали еще формирующихся зубов. Детям от 9 до 12 лет (при условии, что их вес не превышает 45 килограммов) назначают суточную дозу 4 мг. на один килограмм массы тела в первый день заболевания, да далее по 2 мг. на килограмм веса ( в два суточных приема). Препарат выпускается в таблетках, капсулах и формах для инъекций. При тяжелой кишечной инфекции антибиотик назначают именно в уколах, но затем рекомендуется перейти на таблетированные формы.
- «Тетрадокс». Антибиотик, выпускаемый в капсулах. Это средство противопоказано детям, не достигшим возраста 9 лет. Дозировку «Тетрадокса» определяет врач строго индивидуально, обязательно учитывая возраст ребенка, его массу тела и тяжесть болезни.
- «Вибрамицин». Антибиотик, который также не рекомендуется принимать детям до 8 лет. Схема приема и дозировки этого препарата – такие же как у «Доксала».

Антибиотики –пенициллины для лечения кишечной инфекции:
- «Ампициллин». Антибиотик назначают детям с 1 месяца. Если инфекция крохи довольно тяжелая, доктор порекомендует индивидуальную дозировку препарата в диапазоне от 50 до 100 мг. на килограмм массы тела ребенка. Полученное количество придется разделить на несколько равных приемов за сутки. Если вес ребенка перевалил за 20 кило – ему можно применять взрослую дозировку (от 250 до 500 мг.четырежды в день.
- «Мономицин». Антибиотик, способный справиться с большинством грамположительных и грамотрицательных бактерий, в том числе и тех, которые устойчивы к кислоте. Именно они, не погибая в желудке, «добираются» до кишечника. Детям препарат назначают из расчета 4-5 мг на каждый килограмм веса ребенка. Общее суточное количество делится на 3 приема. Не рекомендуется малышам до года.


Антибиотики – цефалоспорины для лечения кишечной инфекции:
- «Клафоран». Антибиотик третьего поколения. Его не рекомендуют применять для детей до 2,5 лет. Ребятам, чей вес не достиг 50 килограммов, назначают уколы в дозировке 50-100 мг на один килограмм веса каждые 6-8 часов. При тяжелых инфекциях врач вправе увеличить дозу в два раза. Детям с весом свыше 50 кг дозировка идентична взрослой.
- «Цефабол». Достаточно мощный антибиотик с довольно обширным списком побочных действий. Производители не рекомендуют давать его детям до 2,5 лет, однако в педиатрии сложилась практика применения «Цефбола» у деток, начиная с 1 месяца, если их состояние требует срочной и сильной антибактериальной терапии. У детей от 1 мес. до 12 лет суточная доза – от 50 до 180 мг на каждый килограмм веса. Препарат делают в уколах 4-6 раз в сутки. Для детей с массой тела более 50 кг дозировка по взрослой схеме.


- «Роцефим». Антибиотик третьего поколения. Новорожденным малышам его дают по 20-50 мг на килограмм массы тела один раз в день. Грудничкам, детям в возрасте 2 года, и ребятам старше (вплоть до 12 лет) врач назначит индивидуальную дозу в диапазоне от 20 до 80 мг. препарата на каждый килограмм веса ребенка один раз в день. Подросткам старше 12 лет, препарат также можно принимать 1 раз в сутки по 1-2 гр (на усмотрение врача).
- «Цефтриаксон». Этот антибактериальный препарат с большой осторожностью следует применять при лечении недоношенных детей. Лучше, если такое лечение пройдет в стационаре под наблюдением врача. У лекарства есть свои плюсы и минусы. Плюс в том, что его можно принимать детям любого возраста всего лишь один раз в день. А минус в том, что ни в таблетках, ни в суспензии, «Цефтриаксон» не выпускается. Возможны лишь уколы. Детям старше 12 лет- 1-2 гр. препарата. Новорожденных крохам до 2 недель максимальная дозировка составляет 20-50 мг. на каждый килограмм веса. Детям до 12 лет суточная дозировка от 20 до 75 мг на килограмм массы тела.


Антибиотики других групп для лечения кишечной инфекции:
- «Фуразолидон». Антибиотик, представляющий семейство нитрофуранов. Выпускается в таблетках, гранулах для суспензии и порошках. Противопоказан детям до 1 года. Обычно назначается в дозировке 10 мг. на каждый килограмм веса ребенка, полученное количество делится на 4 приема в сутки. Малышам рекомендован в форме суспензии.

- «Эрсефурил». Еще один антибиотик – нитрофуран. Детям от 1 месяца препарат дают два или три раза в день по 100 мг. Малышам от 2,5 лет и подросткам до 14 лет назначают по 100мг. трижды в сутки. Подросткам от 14 и старше по 200мг в 4 приема (через каждые шесть часов). Препарат подросткам можно давать в капсулах, а малышам – в форме 4% суспензии.

- «Интетрикс». Этот антибиотик, синтезированный во Франции сравнительно недавно, по действующему веществу не имеет аналогов. Антибиотик выпускается в капсулах. Производители заявляют, что лекарство противопоказано детям до 14 лет, однако педиатры используют «Интетрикс» для лечения кишечных инфекций, правда, дозировку устанавливают индивидуально каждому ребенку. В 2 года, в 4 года или в 7 лет разовая доза будет различной.

- «Фталазол». Это настоящий «долгожитель» среди антибиотиков кишечного действия. Им лечат такие заболевания уже более полувека. Современные педиатры утверждают, что нет никакой необходимости давать «Фталазол» детям до 3 лет, тем более, что сейчас появилось много новых и более эффективных антибиотиков. Однако все специалисты согласны с тем, что «старый-добрый» Фталазол вполне безопасен для детей. Суточная доза антибиотика детям до 3 лет -0,2 гр на каждый килограмм веса, детям старше 6 лет можно давать по 0,4-0,8г. на килограмм веса. Выпускается антибиотик только в таблетках.

- «Бисептол». Этот антибиотик доступен в таблетках, порошках для инъекций и суспензии или готовом растворе для применения внутрь. Препарат можно давать детям с полутора месяцев Малышам можно давать 5 мл суспензии или готового раствора однократно в сутки. Школьникам до 12-летнего возраста дают 460-480 мг дважды в сутки.

Также врачом могут быть назначен «Азитромицин», «Кларитромицин» или относительно молодой препарат «Лекор».
Общие правила лечения антибиотиками инфекций ЖКТ у детей:
- Средней курс терапии от 3 до 14 дней. Врач определит продолжительность лечения в каждом конкретном случае, опираясь на тяжесть симптомов, диагноз и возраст малыша. При наступлении улучшения не стоит самостоятельно снижать дозировку или вообще отменять прием препарата. Выжившие бактерии станут резистентными к данному виду антибиотика. И в следующий раз вам будет сложно подобрать действенный препарат.
- При лечении антибиотиками ребенок должен соблюдать диету, пить больше жидкости.
О кишечной инфекции можно узнать, посмотрев видео доктора Комаровского:
Лекарство от ротавируса – таблетки для лечение вирусной инфекции
Несмотря на то, что мы привыкли считать вирусы возбудителями скорее респираторных инфекций, ротавирус провоцирует проблему совсем другую – бурно протекающее расстройство кишечника, называемое в народе кишечным гриппом.
Интересно, что молва верно подметила некоторые его качества. Кишечный грипп действительно начинается симптомами ОРЗ – заложенностью носа, першением в горле, кашлем, чиханием и повышением температуры. Кроме того, он еще и передается воздушно-капельным путем – совсем как вирус ветряной оспы и непосредственно гриппа. Но в остальном сходства между ними мало.
Этап «респираторных» признаков при заражении ротавирусом заканчивается очень быстро – с началом потери аппетита, болей и урчания в животе, тошноты, рвоты и диареи. Именно они считаются его истинными проявлениями.
А первичная реакция на его попадание в организм со стороны верхних дыхательных путей объясняется тем, что рядом с ними располагается один из важнейших «центров» иммунной защиты тела – в виде пористой ткани миндалин.
Так что, если вирус проник в организм воздушно-капельным путем или с пищей (немытыми руками, плохо вымытыми/обработанными продуктами), наш иммунитет поначалу просто путает его с возбудителем обычного гриппа. Отсюда и сходство первичных признаков. Но в дальнейшем все становится на свои места, и ротавирусную инфекцию определяют по особым, свойственным только ей, характеристикам.
В их числе желто-серые каловые массы, имеющие консистенцию глины, устойчиво высокая температура в пределах 38°С, неудержимая рвота и диарея, которые совместно вызывают сильное обезвоживание организма.
Препаратов, способных бороться с каким-то конкретным вирусом или их группой, в настоящее время не существует. Антибиотики, как известно, ничего здесь не решают, поскольку они предназначены для лечения бактериальных инфекций, а вирусы – это паразиты совсем другого типа. Поэтому лечение уже существующей ротавирусной инфекции остается симптоматическим.
Зато наука успела разработать ряд противовирусных средств с профилактической направленностью. Их прием позволяет временно, но заметно повысить устойчивость организма к действию подавляющего большинства вирусов, включая кишечный грипп. И хотя попытки лечиться ими после заражения мало влияют на течение заболевания, с этой группой препаратов не помешает познакомиться поближе.
Первый в списке лекарств, подходящих для лечения ротавируса и ряда других инфекций – «Арбидол», действующим веществом в котором заявлен умифеновир. Он был разработан давно, в середине 70-х гг. прошлого века, в СССР. Предполагается, что он эффективно блокирует один из белков, которые образуют тело вируса, разрушая его ДНК и, следовательно, уничтожая сам вирус.
Кроме того, он стимулирует синтез интерферонов (иммунных белков на поверхности клеток – единственного средства их защиты от вторжения) и лимфоцитов – телец лимфы, целенаправленно «охотящихся» на зараженные чем бы то ни было клетки тела.
Кстати, один из видов лимфоцитов (все они вызревают и проходят обучение в тимусе – вилочковой железе прямо за грудиной) под названием «Т-киллеры» известен своей способностью уничтожать клетки злокачественных опухолей. Поэтому «Арбидолу» приписывают и частичную эффективность в борьбе с раком.
Это лекарство выпускают в желатиновых капсулах. Если они окрашенные в желтый цвет полностью, значит, они содержат 50 мг действующего вещества. А если они белые с желтой «крышкой», это значит, что в них содержится 100 мг умифеновира.
Препарат показан для лечения ротавируса и некоторых респираторных инфекций детям от 3 лет, взрослым и пожилым пациентам:
- В возрасте от 3 до 6 лет следует пить по 50 мг (по 1 капсуле, полностью окрашенной в желтый цвет) препарата в сутки;
- С 6 до 12 лет – по 100 мг (1 бело-желтая или 2 полностью желтые капсулы) действующего вещества;
- Всем остальным возрастным группам – по 200 мг в сутки.
И детям, и взрослым, и пациентам старше 60 лет нужно принимать указанную дозировку средства 1 раз в день, за 15-20 мин до еды, в течение 5 дней. «Арбидол» противопоказан в первые 3 мес. беременности и период лактации, при наличии аллергии на умифеновир.
Противовирусные средства как класс появились совсем недавно (10 лет не прошло), поэтому в подавляющем большинстве побочные эффекты от их применения людьми, да еще и при различных комбинациях существующих патологий, почти не изучены.
Казалось бы, «Арбидол» не совсем из их числа, поэтому с ним все должно быть по-другому, но список противопоказаний и побочных эффектов, который к нему прилагается, тоже подозрительно краток.
С одной стороны, может, это и хорошо – что, если их действительно нет или почти нет?..
С другой же, его противовирусная активность и впрямь была замечена только недавно. Да и в целом, в истории с этим препаратом немало настораживающих моментов. Например, в 2007 г. он был исключен из списка лекарств, продающихся по льготным ценам в РФ, так как доказательств его эффективности оказалось недостаточно.
По этим причинам некоторые инфекционисты назначают его при заражении ротавирусом как детям, так и взрослым, но среди них немало и тех, кто советует вообще не давать его:
- детям младше 10 лет;
- беременным (то есть в течение всех 9 мес. беременности, а не только первых 3, указанных производителем) и кормящим мамам;
- пациентам, страдающим серьезными заболеваниями печени, почек, иммунитета (аллергия, ВИЧ).
Еще одно лекарство от ротавируса – стимулятор выработки интерферонов клетками, в основе которого содержится тилаксин. В целом «Амиксин» и другие препараты на основе тилаксина (тилорона) не проявляют какой-то особой активности именно против ротавируса – в отличие от «Арбидола», назначение которого при кишечном гриппе упомянуто в инструкции к нему. Обычно их назначают при вирусных гепатитах, герпесе и заражении цитомегаловирусом (один из видов герпеса), обычном гриппе и ОРЗ, хламидиозе.
И все же, тилорон обладает свойством активизировать синтез интерферонов как раз клетками кишечника, печени и вилочковой железы. Поэтому, хоть прямых показаний к лечению им кишечных инфекций нет, они считаются одной из его дополнительных «специализаций».
«Амиксин» выпускают в форме таблеток, так как именно благодаря ей его полное растворение происходит в кишечнике – так сказать, по месту назначения.
Курс «Амиксина» для лечения ротавируса и ряда инфекций печени, начиная с гепатита, выглядит так:
- Детям от 7 лет его назначают в количестве 60 мг, 1 раз в день, после приема пищи. Сначала нужно принимать его по 1 таблетке в течение 2 дней подряд, затем – еще 2 таблетки, но уже через день. Таким образом, курс лечения для ребенка составит 4 дня, за это время будет принята доза препарата общим объемом в 240 мг. А по дням это будет выглядеть как 1-й, 2-й, 4-й и 6-й дни;
- Взрослые должны принимать «Амиксин» 2 раза в день, после еды, по 60 мг действующего вещества (то есть по 120 мг в сутки) в течение первых 2 дней. Затем им, как и детям, рекомендуется перейти на прием все той же дозы (120 мг за 2 приема по 60 мг), но уже через 1 день. Схема лечения по дням у взрослых выглядит так же, как и у детей: прием средства нужно назначать на 1-й, 2-й, 4-й и 6-й дни от начала курса. Просто общая дозировка препарата, принятая за 1 курс лечения против ротавируса, должна составить 480 мг.
Этот препарат противопоказан детям до 7 лет, в период беременности и лактации, при наличии сформированной аллергии (на компоненты препарата или какие бы то ни было другие вещества).
В самом начале лечение «Амиксином» может спровоцировать симптомы дисбактериоза, поскольку местное повышение иммунитета нередко приводит к частичной гибели микрофлоры кишечника. Впрочем, при ротавирусной инфекции их легко не заметить, поскольку там достаточно других проявлений со стороны желудка и кишечника.
К тому же, иммуностимуляторы этого типа не являются антибиотиками, способными уничтожить микрофлору «под корень». Так что, это временное и не слишком ярко выраженное явление, которое проходит само.
Прочие вероятные побочные эффекты от его приема заключаются в тоже проходящем самостоятельно повышении температуры и легком ознобе. Зато он способен провоцировать устойчивые аллергические реакции. Это проблема всех препаратов данного класса.
Они взаимодействуют с иммунной защитой тела, побуждая ее к действию. И если она изначально работала неправильно (потому и иммунитет был снижен), эта активизация часто заканчивается аллергией.
Материалы, размещённые на данной странице, носят информационный характер и предназначены для образовательных целей. Посетители сайта не должны использовать их в качестве медицинских рекомендаций. Определение диагноза и выбор методики лечения остаётся исключительной прерогативой вашего лечащего врача.
антибиотик при ротавирусной инфекции — 25 рекомендаций на Babyblog.ru
Понравилась статья. Может кому то еще она будет полезна.
Авторы: Щербина Е. А.
Что такое острая кишечная инфекция?
Острая кишечная инфекция (ОКИ) — это инфекционное воспаление желудка и кишечника, которое проявляется диареей (жидкий стул более 3 раз в сутки), иногда тошнотой, рвотой и повышением температуры тела. Примерно в 80% случаев кишечная инфекция вызывается вирусами (очень часто это ротавирус), то есть применение антибиотиков не будет иметь никакого эффекта. 
Чего нужно бояться при кишечной инфекции и как не попасть в больницу
Самое опасное для ребенка с поносом и рвотой — обезвоживание. Именно из-за него приходится госпитализировать ребенка, если родители не смогли его отпоить. Как этого не допустить, мы с вами очень подробно разберем ниже.
Что мне делать, если мой ребенок заболел ОКИ?
Чаще всего нетяжелые кишечные инфекции можно лечить в домашних условиях. При появлении симптомов заболевания желательно связаться со своим врачом и предупредить его, что ваш ребенок заболел, и подробно описать всю ситуацию. Диарея и рвота (плюс еще и повышение температуры) — это потеря воды и солей, а значит, первое и основное, что должны сделать родители — восполнить уже имеющиеся потери и постоянно компенсировать то, что будет теряться дальше.
Сколько давать жидкости?
В среднем для отпаивания ребенка при острой кишечной инфекции нужно примерно 100 мл на каждый килограмм массы тела (1000 мл для малыша весом 10 кг), но может понадобиться и больше. Чтобы было более удобно, вам нужно следить за тем, чтобы у ребенка была влажная кожа и писал он примерно раз в три часа. Если писаете реже — значит, недоработали, давайте больше пить, пока мочеиспускания не участятся.
Чем отпаивать?
Идеальный раствор для восполнения жидкости при кишечной инфекции — солевые растворы. Они продаются в аптеках или же их можно приготовить дома: три чайные ложки сахара без верха плюс 1/2 чайной ложки соли на литр кипяченой воды. Далеко не все, особенно маленькие дети, в восторге от этих напитков, но потери восполнять все равно нужно. Если маленький пациент отказывается пить солевой раствор, сварите ему компот из сухофруктов. Если и это не помогает, тогда можно давать абсолютно любую жидкость, которую ребенок будет пить: хоть обычную воду, хоть чай, хоть арбуз дать поесть, хоть сладкую воду из магазина — лишь бы пил! (Вред от выпитой ребенком «Кока-колы» не так опасен, как смерть от обезвоживания, поверьте.) Детям на грудном вскармливании (в основном до 12 месяцев) нужно как можно чаще предлагать грудь (грудное молоко на 95 % состоит из воды), особенно, если они не хотят пить солевой раствор. Итого у нас сформировались следующие приоритеты: 1) солевые растворы; 2) компот; 3) любая другая жидкость.
Чем кормить?
Пока у ребенка рвота, ему вообще нет смысла давать еду — только жидкость. Когда рвота прекратится, то параллельно с отпаиванием вы можете предлагать уже и еду, но строго по аппетиту! Не нужно кормить насильно — это только вызовет рвоту и усилит понос. Дети на грудном вскармливании прекрасно обходятся грудным молоком + солевые растворы или компот при необходимости. Более старшие дети могут начинать с легко усваиваемых продуктов: фруктовые кисели, сухари с чаем, галетное печенье, рисовая каша (с компотом, например), супы не на бульоне.
Основное правило — давайте часто, но понемногу. Через день-два уже можно возвращаться к прежним продуктам (тому, что ел до болезни), исключив на некоторое время жареное, жирное и острое.
Какое еще лечение эффективно при кишечной инфекции?
Всемирная организация здравоохранения и другие крупные медицинские организации рекомендуют помимо восполнения жидкости и продолжения кормления принимать препараты цинка. Многочисленные исследования показали, что прием препаратов цинка (10-20 мг в сутки вплоть до прекращения диареи) существенно снижает тяжесть и продолжительность диареи у детей младше 5 лет. В настоящее время на основании проведенных исследований рекомендуется вводить цинк (10-20 мг/день) в рацион всех детей с диареей в течение 10-14 дней.
Также вы много слышали о пробиотиках. Доказано, что пробиотики снижают длительность диареи у детей на фоне кишечной инфекции в среднем на 24 часа. Это все, на что вы можете рассчитывать.
Можно ли детям назначать противодиарейный препарат лоперамид?
Нет. Это лекарство запрещено для применения детям в связи с риском развития угрожающих жизни побочных эффектов.
А как насчет сорбентов (активированный уголь, «Атоксил», «Смекта»)?
Эти препараты не влияют на длительность заболевания. Они лишь могут в некоторых случаях ослабить диарею за счет «закрепления» каловых масс, однако нередко это приводит к формированию каловой «пробки», которая выходит довольно-таки болезненно. В связи с этим сорбенты не входят в протоколы лечения острой кишечной инфекции у детей.
Если почти 80 % всех кишечных инфекций вызываются вирусами, значит, будут очень полезны противовирусные препараты?
Эффективность «противовирусных» и «иммуномодулирующих» лекарств при лечении острых кишечных инфекций не доказана.
Ну хоть «Нифуроксазид» дать можно?
«Нифуроксазид» (энтерофурил) — кишечный антисептик, который запретили применять у детей, больных кишечными инфекциями в той стране, которая его впервые начала производить (Франция). В 2003 году, после переоценки соотношения польза/риск от применения «Нифуроксазида» и длительных дискуссий между производителями и Французским медицинским агентством (FMA), использование оральной суспензии было ограничено и запрещено у детей младше двух лет. Это явилось долгожданной мерой, однако наилучшим подходом представляется прекращение назначения «Нифуроксазида» вообще.
А когда нужно давать антибиотики?
Антибиотики при острых кишечных инфекциях показаны довольно редко, в основном это так называемые инвазивные диареи, когда в кале появляется кровь. Еще их применяют в случае заболевания холерой, а также внекишечными бактериальными инфекциями, которые приводят к развитию диареи (пневмония, средний отит и т. д.). Как вы уже поняли, примерно в 80 % всех случаев кишечных инфекций антибиотики назначаются зря. И это как минимум.
Я не хочу, чтобы мой ребенок заболел. Как предотвратить это?
Во-первых, вы всегда можете сделать вакцинацию от ротавирусной инфекции (до 6- или 8-месячного возраста, в зависимости от вакцины), так как именно она является наиболее частой причиной госпитализации и даже смерти от обезвоживания у маленьких детей. Во-вторых, о способах профилактики заражения кишечными инфекциями я уже подробно рассказывал — почитайте соответствующую статью Профилактика кишечных инфекций.
Как все запутано! А можно на примере объяснить, как же все-таки правильно лечить острую кишечную инфекцию?
Конечно можно. Представим, что у вашего годичного ребенка вдруг началась рвота. Однократная рвота не страшна, причин у нее множество и зачастую они не страшны, однако в случае повторения или если у ребенка уже начался понос, вам стоит по возможности предупредить об этом своего врача. Сразу же разведите 1-2 пакетика купленного солевого раствора (можно сделать самому) и на всякий случай приготовьте любимый напиток ребенка (компот, сок, вода), если он откажется от солевого раствора. Рвота при кишечных инфекциях обычно непродолжительная — в пределах нескольких часов. Пока рвота интенсивная, не нужно ничего давать, так как все сразу же «вернется» назад. Если рвоты
Ротавирусная инфекция. Памятка для родителей
Способы передачи ротавируса
Содержание статьи
Неприятно познакомиться, вирус!
Как не подхватить инфекцию?
С чего все начинается и к чему приводит?
Скорее, еще скорее! Когда нужно вызывать неотложку?
Давайте лечиться
А как быть с профилактикой?
Ротавирусной инфекцией хотя бы раз в жизни заражается каждый ребенок на нашей планете. Это довольно опасное заболевание, к тому же иммунитет после него вырабатывается нестойкий. Как же проявляется «болезнь грязных рук» и как ее вылечить? Давайте разберемся.
Неприятно познакомиться, вирус!
«Сверх популярную» кишечную инфекцию вызывает ротавирус. Он похож на микроскопическое велосипедное колесо со спицами («rota» в переводе с латыни это и есть «колесо»).
Возбудитель заболевания неплохо приспособлен к жизни. Он долгое время сохраняется в окружающей среде, выдерживает замораживание и не исчезает после обработки дезрастворами. Хорошая новость: ротавирус быстро распадается при кипячении.
Эту инфекцию можно подхватить в любое время года. Устойчивый вирус распространяется даже при высокой температуре воздуха. Заразиться можно на отдыхе, прямо на пляже, ведь ротавирус неплохо чувствует себя в воде и песке. Поэтому осторожность нужна и на каникулах.
Как не подхватить инфекцию?
Основные способы передачи ротавируса — фекально-оральный и контактно-бытовой. Активный возбудитель легко переходит с грязных рук на обиходные предметы. Эту кишечную инфекцию можно подхватить в любом возрасте, но чаще всего болеют крохи — от 6 месяцев до 3 лет. Дело в том, что маленькие дети то и дело пробуют мир на вкус — проще говоря, тянут в рот все, что плохо лежит. При этом в организме малышей нет антител к ротавирусу.
А вот грудничков некоторое время защищают материнские антитела, которые поступают в организм вместе с молоком. Дети, которые находятся на искусственном вскармливании, лишены естественной защиты от заражения.
Очень распространен водный путь передачи, поэтому некипяченую воду давать малышам нельзя. Через пищу эта инфекция передается гораздо реже, в основном, через молоко и молочные продукты.
С чего все начинается и к чему приводит?
У ротавируса короткий инкубационный период — от 12 часов до 4 дней. Обычно болезнь стартует внезапно и остро — столбик термометра взлетает до 39-40 градусов. У ребенка появляется урчание и боль в животе, вскоре присоединяется обильный водянистый стул. Малыш может испытывать до 20 позывов на дефекацию — и это за одни сутки!
В первые же часы начинается рвота, даже если ребенок ничего не ел и не пил. Рвота не прекращается, а жар не спадает. Даже при использовании жаропонижающих высокая температура может держаться 5-6 дней. Грудных детей беспокоит сильное урчание в животе, к тому же они стремительно теряют в весе.
Постоянная изнуряющая рвота на фоне общей интоксикации вызывает слабость и сонливость. Но самое опасное — это обезвоживание. Важно знать, что при диарее и рвоте организм ребенка теряет не только воду, но и электролиты. Это полезные соли калия, натрия, магния, фосфора. Их недостаток может привести к ухудшению обмена веществ, нарушению работы сердца, появлению тревожности, мышечных спазмов и судорог.
Обезвоживание очень опасно для малышей младше 5 лет, а особенно — для грудничков. Ведь развитие водно-электролитного дефицита может стать не только причиной госпитализации, но, и с случае позднего обращения за помощью, летального исхода. Поэтому нужно как можно скорее вызвать врача и начать правильное лечение с использованием готовых водно-солевых растворов.
Мучительная диарея всегда сопровождает эту инфекцию, Ротавирусную диарею можно отличить от бактериальной (сальмонеллезной или дизентерийной). Каловые массы не приобретают зеленоватый оттенок и в них нет слизи и примесей крови. Все эти проявления сигнализируют о присоединении бактериальной инфекции.
Как правило, диарея длится 5 — 6 дней. Уже в первые 2-3 суток частый водянистый стул сильно раздражает кожу в перианальной области и приводит к развитию дерматита, усугубляющего и без того тяжелое самочувствие ребенка. Из-за боли он не может спокойно сидеть и лежать. Необходимо тщательно следить за состоянием кожных покровов и соблюдать все гигиенические рекомендации по уходу.
Скорее, еще скорее! Когда нужно вызывать неотложку?
Обезвоживание — веская причина для возможной госпитализации. Сухие слизистые оболочки: обложенный сухой язык и губы, малыш не может плакать (нет слез), бледная и сухая кожа, кожная складка расправляется не сразу, плохой аппетит и отказ от пищи и питья, урежение мочеиспускания, общая вялость и слабость – эти симптомы должны насторожить родителей и сразу обратиться за медицинской помощью.
Обезвоживание
При развитии обезвоживания ребенок теряет вес. Если его вес снижается более чем на 5%, а количество мочеиспусканий уменьшается: до 5-7 раз в сутки у младенцев и до 3 — 5 раз — у детей старше года, нарастает слабость – ребенок не может встать с постели, высока вероятность развития тяжёлой степени обезвоживания.
Частая рвота и диарея (до 5 — 6 раз в сутки) у ребенка, которому еще не исполнилось пяти лет, — прямая угроза для жизни малыша. Медлить в таком случае нельзя, необходимо вызывать скорую помощь.
Особенно внимательно следует отнестись к маленьким пациентам, у которых есть сахарный диабет или хронические заболевания сердца.
Давайте лечиться
Основные задачи терапии — справиться с диареей, рвотой, интоксикацией и предупредить обезвоживанием. При легкой и средней степени ротавирусной инфекции можно лечить ребенка дома.
Остановить диарею помогают специальные средства, нормализующие работу кишечника, например, «Адиарин ®». Его действующее вещество — желатина таннат, имеет органическое происхождение. Он не всасывается в системный кровоток и работает только в кишечнике, не подвергая организм ребенка дополнительной нагрузке. Желатина таннат создает на поверхности кишечника специальную пленку — биобарьер, защищающий слизистую от агрессивного действия вирусов, бактерий и токсинов. В результате уменьшается воспаление слизистой оболочки кишечника, снижается частота эпизодов диареи и сокращается ее продолжительность уже в первые 12 часов применения. * У ребенка проходит тошнота, рвота и боль в животе. Адиарин удобно давать детям: разовая доза помещается в ложке, а нейтральный вкус не вызывает дискомфорта при приеме.
При диарее и рвоте очень важно своевременно восполнить потери жидкости и солей, чтобы у малыша не развилось обезвоживание. Начинать нужно с момента появления первых симптомов инфекции и продолжать до полного прекращения рвоты и диареи.
Помните, что жизненно важные микроэлементы не содержатся в обычной воде, чае и компотах. Необходимо использовать специальные водно-солевые растворы, предназначенные для детей.
Хороший пример такого средства — «Адиарин ® Регидрокомплекс ®». Это раствор с низкой концентрацией солей (гипоосмолярный), который содержит сбалансированную смесь глюкозы и электролитов. Его состав полностью соответствует стандартам ВОЗ, он подходит для малышей с первых дней жизни. Адиарин ® Регидрокомплекс ® предупреждает развитие обезвоживания и быстро устраняет уже развившийся водно-электролитный дисбаланс при ротавирусной инфекции. Адиарин имеет приятный вкус и не вызывает рвоту у ребенка. Это средство можно давать малышам маленькими порциями — чайными ложками каждые 10-15 мин.
Ротавирусная инфекция всегда угнетает полезную кишечную микрофлору. Ее нужно начать восстанавливать как можно быстрее — как только прекратится рвота. Для этого предназначены специальные средства — пробиотики. При кишечной инфекции эффективны особые штаммы бактерий, которые не только восстанавливают микрофлору, но и уменьшают продолжительность диареи. Адиарин Пробио ® обладает антидиарейным эффектом и содержит штаммы лактобактерий LGG и бифидобактерий BB-12. Они эффективно восстанавливают, нарушенную инфекцией микрофлору, и подходят для детей любого возраста, начиная с рождения.
Бактерии в составе Адиарин Пробио самые изученные в педиатрии, используются более 30 лет. Доказано что LGG и ВВ-12 потенцируют и дополняют действие друг друга. Так штамм LGG уменьшает продолжительность диареи и усиливает иммунный ответ слизистой оболочки кишечника, а ВВ-12, в свою очередь, обеспечивает устойчивость кишечника к патогенам и защищает от негативного влияния антибиотиков, в случае их назначения. Масляные капли «Адиарин Пробио ®» удобны в применении: достаточно 6 капель 1 раз в день, их можно принимать отдельно или добавлять в жидкую пищу, грудное молоко и молочные смеси.
А вот антибиотики при ротавирусе использовать бесполезно, ведь они не убивают вирус. Врач выпишет антибиотик, если заболевание осложнится присоединением бактериальной инфекции.
А как быть с профилактикой?
Здоровая микрофлора кишечника, восстановленная при помощи пробиотика, снижает риск повторного заражения. Но что еще помогает для профилактики?
Ротавирусная инфекция — это типичная болезнь «грязных рук», поэтому нужно научить малыша как можно чаще и тщательнее мыть эти самые руки, особенно, после посещения туалета.
Маленьким детям нельзя пить сырую воду и есть немытые овощи и фрукты. Перед тем, как угостить ребенка сочным десертом, нужно почистить овощи под краном специально предназначенной щеткой.
Тщательно мойте руки и правильно термически обрабатывайте пищу
Но самый действенный способ профилактики — это вакцинация. Безболезненную прививку в виде капель малыши получают, начиная с 6 месяцев. До 8 месяцев важно успеть сделать 3 такие прививки. Это поможет избежать встречи с ротавирусом!
Соблюдайте простые правила гигиены и будьте здоровы!
Если вы хотите узнать больше полезной информации о том, как лечить ротавирус правильно, как остановить диарею и избежать обезвоживания, что должно быть в аптечке малыша и что брать с собой в отпуск — присоединяйтесь к нашему полезному марафону в Инстаграм: #МарафонАдиарин #МарафонЗдоровыйЖивотик. Первый пост уже в понедельник 15 июня, не пропустите! В конце недели особо внимательные подписчики получают призы!
Имеются противопоказания. Необходимо ознакомиться с инструкцией по применению или получить консультацию специалиста.
Библиотека ресурсов по вакцинам PATH: ротавирус

Ротавирус — самая частая причина тяжелых диарейных заболеваний у детей во всем мире. Недавнее исследование показало, что 37 процентов из 578 000 случаев смерти детей от диареи в 2013 году были вызваны ротавирусом, в общей сложности 215 000 случаев смерти от ротавируса во всем мире. Более 90 процентов этих смертей произошло в развивающихся странах. Ротавирусное заболевание нельзя лечить антибиотиками или другими лекарствами, и большинство детей подвержены риску заражения независимо от соблюдения гигиены или доступа к чистой воде.Вакцинация — лучший способ защитить детей от ротавируса и смертельно опасной обезвоживающей диареи, которую он может вызвать. В 2009 году Всемирная организация здравоохранения рекомендовала всем странам включить ротавирусные вакцины в свои национальные программы иммунизации. В настоящее время две вакцины против этой болезни доступны во всем мире, четыре вакцины доступны только на национальных рынках, а еще несколько находятся в стадии разработки.
Просмотреть ресурсы по ротавирусу
На сайтах PATH
Ротавирусная болезнь
- Ротавирус — самая частая причина тяжелых диарейных заболеваний у детей во всем мире.Недавнее исследование показало, что 37 процентов из 578 000 случаев смерти детей от диареи в 2013 году были вызваны ротавирусом, в общей сложности 215 000 случаев смерти от ротавируса во всем мире. Более 90 процентов этих смертей произошло в развивающихся странах.
- Ротавирус встречается во всех странах. Независимо от правил гигиены или доступа к чистой воде, почти каждый ребенок в мире подвергается риску заражения ротавирусом в возрасте до пяти лет.
- У маленьких детей ротавирусная болезнь характеризуется диареей, рвотой, лихорадкой и сильным обезвоживанием.В смертельных случаях смерть наступает в результате сильного обезвоживания, вызванного ротавирусной инфекцией.
- Ротавирусную болезнь нельзя лечить антибиотиками или другими лекарствами. Регидратационная терапия — важная часть лечения обезвоживания, вызванного диарейными заболеваниями, включая ротавирус.
- Вакцинация — лучший способ предотвратить тяжелое ротавирусное заболевание, особенно в условиях, когда доступ к медицинской помощи ограничен или недоступен.
Ротавирусные вакцины
- В настоящее время во всем мире доступны две вакцины против ротавируса: RotaTeq® от Merck и Rotarix® от GlaxoSmithKline.Исследования этих вакцин продемонстрировали их безопасность и эффективность среди детей во всех регионах мира. Клинические испытания эффективности в Африке и Азии показали, что вакцины резко снизили количество тяжелых заболеваний среди младенцев в развивающихся странах, где происходит большинство случаев смерти от ротавирусов.
- Существует четыре пероральных ротавирусных вакцины, лицензированных только для национальных рынков: ROTAVAC®, производимый Bharat Biotech, был лицензирован для использования в Индии в 2014 году; ROTASIIL®, выпускаемый Индийским институтом сыворотки, Pvt.Ltd., была лицензирована для использования в Индии в 2016 году; Ротавин-М1®, производимый Центром исследований и производства вакцин, был лицензирован для использования во Вьетнаме в 2007 году; и вакцина против ротавируса ягненка Ланьчжоу, производимая Институтом биологических продуктов Ланьчжоу, была лицензирована для использования в Китае в 2000 году.
- Всемирная организация здравоохранения рекомендует включить ротавирусные вакцины в программы иммунизации каждой страны.
- На сегодняшний день почти 100 стран включили ротавирусные вакцины в свои национальные программы иммунизации.Гави, Альянс по вакцинам, глобальное партнерство в области здравоохранения, направленное на расширение доступа к вакцинам, поддерживает внедрение ротавирусных вакцин во многих беднейших странах мира. При поддержке Гави более 45 стран внедрили ротавирусные вакцины.
- Научные исследования показывают, что ротавирусные вакцины оказывают серьезное влияние на здоровье населения. Быстрое и значительное снижение количества госпитализаций и смертей из-за ротавируса и диареи от всех причин наблюдалось во многих странах, которые включили ротавирусные вакцины в свои национальные программы иммунизации.В некоторых странах, где были внедрены ротавирусные вакцины, исследователи обнаруживают значительное сокращение госпитализаций против ротавирусной диареи среди невакцинированных взрослых и детей, предполагая, что преимущества ротавирусных вакцин распространяются не только на младенцев, но и обеспечивают косвенную защиту непривитых детей и взрослых за счет снижения распространения вируса ( эффект, называемый коллективным иммунитетом).
- В то время как существующие производители играют важную роль в удовлетворении глобального спроса на существующие вакцины, дополнительные варианты вакцин и производители имеют решающее значение для обеспечения устойчивых и доступных поставок.Несколько производителей разрабатывают новые ротавирусные вакцины, в том числе многие в странах с развивающейся экономикой.
- Ротавирусные вакцины являются важной частью комплексной стратегии профилактики и лечения, направленной на борьбу с диарейными заболеваниями. Другие элементы этой стратегии включают пероральную регидратационную терапию; обработка цинком; исключительно грудное вскармливание; Правильное питание; безопасная вода; и улучшенные методы санитарии и гигиены.
Сопутствующие болезни
Диарейные заболевания — основная причина смерти детей в развивающихся странах.Помимо ротавируса, существует множество других патогенов, которые способствуют заболеваемости и смертности от диарейных заболеваний, включая Shigella и энтеротоксигенный Escherichia coli (ETEC), основные бактериальные причины диареи. Узнайте больше о Shigella и ETEC.
Список литературы
- Armah GE, Sow SO, Брейман РФ и др. Эффективность пятивалентной ротавирусной вакцины против тяжелого ротавирусного гастроэнтерита у младенцев в развивающихся странах Африки к югу от Сахары: рандомизированное, двойное слепое, плацебо-контролируемое исследование.
- Мадхи С.А., Канлифф Н.А., Стил Д. и др. Влияние вакцины против ротавируса человека на тяжелую диарею у африканских младенцев.
- ПУТЬ. Данные о воздействии ротавирусной вакцины.
- Tate JE, Burton AH, Boschi-Pinto C, Parashar UD. Глобальные, региональные и национальные оценки смертности от ротавирусов у детей младше 5 лет, 2000–2013 гг.
- Детский фонд ООН. Приверженность выживанию детей: новое обещание — Отчет о ходе работы за 2013 г.
- Всемирная организация здравоохранения.Ротавирусные вакцины: программный документ ВОЗ — январь 2013 г.
- Заман К., Данг Д.А., Виктор Дж.С. и др. Эффективность пятивалентной ротавирусной вакцины против тяжелого ротавирусного гастроэнтерита у младенцев в развивающихся странах Азии: рандомизированное, двойное слепое, плацебо-контролируемое исследование.
Последнее обновление страницы: август 2019 г.
Фото: PATH / Майк Ван.
Ротавирус — лучший канал здоровья
Ротавирус — частая причина вирусного гастроэнтерита у младенцев и детей дошкольного возраста в Австралии.Большинство детей к трем годам перенесли хотя бы одну инфекцию.
Ротавирусный гастроэнтерит обычно протекает тяжелее, чем другие типы гастроэнтерита. До внедрения ротавирусной вакцины в Австралии, по наиболее достоверным имеющимся оценкам, ежегодно на нее приходилось около 10 000 госпитализаций и 115 000 посещений врача для детей в возрасте до пяти лет. С момента включения ротавирусных вакцин в Национальный график иммунизации в 2007 году количество госпитализаций снизилось более чем на 70 процентов.
Иммунизация против ротавирусадоступна бесплатно для всех младенцев викторианской эпохи. За дополнительной информацией обращайтесь к своему терапевту или местному поставщику услуг иммунизации.
Симптомы ротавируса
Симптомы и признаки ротавирусного гастроэнтерита варьируются от легких до потенциально опасных для жизни и могут включать:
- рвота
- внезапное начало диареи
- лихорадка
- обезвоживание
- сонливость.
Причины ротавируса
В Виктории и других регионах Австралии с умеренным климатом ротавирусный гастроэнтерит чаще встречается зимой. Инфекция вызывается близким личным контактом и прикосновением к зараженным рукам, фекалиям (фекалиям) и рвоте. Симптомы появляются через один-три дня после заражения. Когда ребенок выздоравливает, его фекалии могут оставаться заразными до двух месяцев.
Ротавирусная инфекция может повторяться несколько раз
Заразиться ротавирусом можно несколько раз.Первая инфекция обычно самая тяжелая. Повторные инфекции повышают естественный иммунитет человека. Например, после первого заражения около четырех из 10 детей никогда больше не болеют ротавирусным гастроэнтеритом. У остальных, вероятно, будут менее серьезные симптомы после более поздних инфекций.
Группы высокого риска по ротавирусу
Некоторые люди подвергаются повышенному риску серьезных или даже опасных для жизни симптомов. В группы высокого риска входят:
- Дети аборигенов
- дети или взрослые с проблемами иммунной системы
- реципиентов трансплантатов
- человек с проблемами желудочно-кишечного тракта, такими как синдром короткой кишки.
Лечение ротавируса
Лечение зависит от тяжести симптомов. У большинства детей легкое заболевание, которое можно вылечить дома, проходит в течение пяти дней. Варианты лечения могут включать обильное питье (например, напитки для пероральной регидратации, которые можно купить у фармацевта) и много отдыха.
Немедленно обратитесь к врачу или обратитесь в отделение неотложной помощи ближайшей больницы, если ваш ребенок отказывается пить или у него появляются тревожные симптомы, например, очень частая диарея или рвота, вялость или сонливость.В тяжелых случаях может потребоваться госпитализация и внутривенное замещение жидкости.
Профилактика ротавируса
Иммунизация может значительно снизить риск будущих инфекций, но общие советы по предотвращению распространения болезни, если кто-то инфицирован, включают:
- После смены подгузника тщательно вымойте руки.
- Используйте одноразовые подгузники, когда ребенок болен — эластичные повязки для ног помогают предотвратить вытекание загрязненных фекалий.
- Осторожно утилизируйте подгузники и использованные салфетки.
- Часто мойте и дезинфицируйте пеленальный столик.
- Регулярно мойте и дезинфицируйте игрушки и другие предметы общего пользования.
- Держите больных младенцев и детей дома — ротавирусный гастроэнтерит может быстро распространиться через ясли или детский сад.
- Вымойте руки перед тем, как брать в руки, готовить или принимать пищу или питье.
Иммунизация против ротавируса
В Виктории всем детям доступна бесплатная вакцина.Вакцина содержит ослабленную форму ротавируса и побуждает организм вырабатывать антитела. В большинстве случаев вакцинированные дети защищены от инфекции. Однако ни одна вакцина не эффективна на 100 процентов. Иногда иммунизированный ребенок заболевает ротавирусным гастроэнтеритом, но симптомы обычно легкие.
До того, как ротавирусная вакцина стала доступной в Австралии, почти каждый ребенок был инфицирован ротавирусом в возрасте пяти лет. Ежегодно около 10 000 детей младшего возраста находились в больницах с ротавирусным гастроэнтеритом, и до одного ребенка в год умирали от осложнений.
Вакцинация против ротавируса началась в 2007 году, и теперь ежегодно предотвращается более 7000 госпитализаций по поводу ротавируса. Те люди, которые попадают в больницу, теперь обычно менее больны.
С 1 июля 2017 г. Виктория сменила марку ротавирусной вакцины, в результате чего младенцы получали курс из двух доз вместо предыдущего курса из трех доз. Это изменение произошло во всех штатах и территориях Австралии, которые использовали курс из трех доз.
Ротавирусная вакцина
Вакцина против ротавируса доставляется перорально (перорально) и состоит из двух отдельных доз, вводимых в возрасте двух и четырех месяцев.Для обеспечения эффективности важно, чтобы вакцина вводилась как можно ближе к этому возрасту. Первую дозу можно давать с шестинедельного возраста.
Если ребенок не получил первую дозу до 14 недель и шести дней, он не должен получать никаких доз вакцины. Ребенку, который начал, но еще не закончил вакцинацию против ротавируса и который старше 24 недель и шести дней, не должны вводиться дополнительные дозы.
Оральная ротавирусная вакцина вводится одновременно с другими бесплатными вакцинами в рамках Национальной программы иммунизации.Никакой специальной диеты или диетических ограничений до или после вакцинации не требуется.
Вводить ротавирусную вакцину детям старшего возраста («наверстывающая» вакцинация) не рекомендуется, поскольку безопасность и эффективность пероральной ротавирусной вакцины для детей старшего возраста не подтверждены.
Как правило, количество необходимых прививок зависит от вашего здоровья, возраста, образа жизни и рода занятий. Вместе эти факторы называются HALO.
Перед вакцинацией против ротавируса
Перед вакцинацией обязательно сообщите своему врачу или медсестре, если у вашего ребенка:
- старше рекомендованного возрастного диапазона для первой или второй дозы
- — недомогание (температура выше 38.5 ° С)
- имел серьезную реакцию на любую вакцину
- имел серьезную аллергию на что-либо
- страдает хроническим желудочно-кишечным заболеванием
- имел инвагинацию или врожденную аномалию, которая может привести к инвагинации
- принимает стероидные препараты
- получил переливание крови или продуктов крови
- имеет пониженный иммунитет из-за иммунодефицита, аномальных состояний или нарушений крови, рака, ВИЧ или некоторых лекарств
- живет в семье с человеком с пониженным иммунитетом.
Побочные эффекты ротавирусной вакцины
Пероральная ротавирусная вакцина в целом эффективна и безопасна, хотя все лекарства могут иметь нежелательные побочные эффекты.
Обратитесь к врачу за дополнительной информацией, если вы беспокоитесь о своем ребенке.
Редкие побочные эффекты ротавирусной вакцины
Существует очень небольшой риск серьезной аллергической реакции, называемой анафилаксией, на любую вакцину. Вот почему вам рекомендуется держать ребенка в клинике или в хирургическом отделении не менее 15 минут после иммунизации на случай, если потребуется дальнейшее лечение.
Существует очень небольшой риск инвагинации (непроходимости кишечника), которая, по-видимому, возникает в основном в первые один-семь дней после первой или второй дозы ротавирусной вакцины. Отведите ребенка к врачу или в больницу, если они:
- Приступы плача
- подтягивают ноги к животу
- бледный вид
- рвота
- выделяют кровь в стуле (фекалии).
Вакцина против ротавируса и инвагинации
Инвагинация — это когда одна часть кишечника проникает в другую, как части телескопа.Когда это происходит, в кишечнике возникает закупорка. Закупорка вызывает боль, похожую на сильную колику.
Имеются данные из исследований в Австралии и за рубежом, свидетельствующие о небольшом повышении риска инвагинации кишечника у младенцев после вакцинации против ротавируса. Риск составляет примерно шесть дополнительных случаев инвагинации на каждые 100 000 вакцинированных младенцев или 14 дополнительных детей в год, получающих инвагинацию в Австралии.
В большинстве случаев у младенцев причина неизвестна, и связь с ротавирусной вакциной отсутствует.Ребенку, у которого уже была инвагинация, не следует делать ротавирусную вакцину.
Инвагинация встречается редко. В Австралии около 200 детей в возрасте до 12 месяцев заболевают этим заболеванием каждый год. Чаще всего встречается у детей в возрасте от пяти до 10 месяцев и чаще встречается у мальчиков.
Куда обратиться за помощью
Ротавирус | Вакцины
Ротавирус — это болезнь, от которой ежегодно заболевали тысячи младенцев и маленьких детей. Благодаря вакцине против ротавируса количество детей, заболевших этой болезнью, в США снизилось.
Вакцина против ротавируса вводится перорально, что означает, что ваш ребенок ее проглотит.
- Почему вакцина против ротавируса важна?
Ротавирус — это заразное заболевание, оно легко передается от ребенка к ребенку. Ротавирус может вызвать диарею (водянистые фекалии), что может привести к обезвоживанию (недостатку воды в организме). Детей, заболевших ротавирусом в тяжелой форме, может потребоваться госпитализация.
Вакцина против ротавируса защищает 9 из 10 детей от тяжелых заболеваний, вызванных ротавирусом.
Вакцина против ротавируса — лучший способ защитить вашего ребенка от ротавируса.
- Что такое ротавирус?
Ротавирус вызывается вирусом и в основном поражает младенцев и детей младшего возраста. Симптомы ротавируса включают:
- Сильная диарея
- Рвота
- Обезвоживание
- Лихорадка
- Боль в животе
- Изменения в поведении
Ротавирус распространяется, когда человек контактирует с экскрементами человека, у которого есть ротавирус, а затем касается своего рта.Например, ротавирус может распространяться, когда ребенок, заболевший ротавирусом, не моет руки должным образом после посещения туалета, а затем касается еды или других предметов.
Узнайте больше о ротавирусе.
- Кому нужна вакцина против ротавируса?
Все дети в возрасте от 2 до 6 месяцев должны пройти вакцинацию против ротавируса как часть их обычного графика вакцинации.
См. График плановой вакцинации младенцев и детей.
Дети получают 2 или 3 дозы, в зависимости от марки ротавирусной вакцины.Им нужна доза вакцины в следующем возрасте:
- 2 месяца для первой дозы
- 4 месяца для второй дозы
- 6 месяцев для третьей дозы (если они получают 3 дозы)
Поговорите с врачом вашего ребенка о том, как защитить его от ротавируса.
- Кому нельзя делать ротавирусную вакцину?
Некоторым младенцам не следует делать прививку от ротавируса, в том числе младенцам, которые:
- Имелись тяжелые аллергические реакции на ротавирусную вакцину в прошлом
- У вас сильная аллергия на любой из ингредиентов вакцины.
- Имеете тяжелый комбинированный иммунодефицит (группа редких генетических нарушений, влияющих на иммунную систему)
- Инвагинация (своего рода закупорка кишечника)
Если ваш ребенок заболел, ему, возможно, придется подождать, пока ему станет лучше, чтобы ему сделали ротавирусную вакцину.И поговорите с лечащим врачом перед вакцинацией, если ваш ребенок:
- Имеет ВИЧ / СПИД
- Рак
- Принимает лекарства, ослабляющие иммунную систему
- Каковы побочные эффекты ротавирусной вакцины?
У большинства детей, получающих вакцину против ротавируса, нет побочных эффектов. Если это вызывает побочные эффекты, они обычно легкие и проходят через несколько дней. Они могут включать:
- Суетиться
- Диарея (водянистые фекалии)
- Рвота
Также существует небольшая вероятность того, что вакцина против ротавируса может вызвать инвагинацию, очень редкое заболевание, вызывающее закупорку кишечника.Это происходит примерно между 1 из 20 000 и 1 из 100 000 младенцев, получивших вакцину. Инвагинация поддается лечению. Но это может быть смертельно опасным, если не лечить.
Как и любое лекарство, существует очень небольшая вероятность того, что вакцина против ротавируса может вызвать другие серьезные реакции. Имейте в виду, что вакцинация против ротавируса намного безопаснее, чем заражение ротавирусом. Узнайте больше о побочных эффектах вакцины.
- Где я могу получить дополнительную информацию о ротавирусной вакцине?
- Информационные бюллетени
о вакцинах (VIS) содержат подробную информацию о рекомендуемых вакцинах.
Ротавирус
Generalità
ротавирус является вирусным вирусным ответвлением от гастроэнтерита.
Avente на геномную разнообразную молекулу РНК a doppia elica, questo comune virus è trasmissibile в различных модификациях: attato la via oro-fecale (modalità di trasmissione Principale), per contatto fisico (con oggetti, mani o cibi contaminatiie) и атраверсо ле v респираторы.
В общем, язвы гастроэнтерита от ротавируса состоят из: тошноты, рвоты, лихорадочного состояния и водного диареи.
Самая сложная тема — это дезидратация, последовавшая за всеми эпизодами рвоты и инакомыслящих.
Nella maggior parte dei casi, per personare un’infezione da rotavirus sono sufficienti l’esame obiettivo e l’anamnesi.
Non esistono cure specifiche, ma solo trattamenti di tipo sintomatico.
Fondamentale, per Evitare Gravi Computing, è la reidratazione del paziente.
Cos’è il rotavirus?
ротавирусов является биологическим биологическим веществом, которое представляет собой основную причину гастроэнтерита nei neonati e nei bambini.
На каждую молекулу геномы, изменяющуюся с РНК, и на doppia elica, или на вирусный вирус семейства, на Reoviridae .
Cos’è la gastroenterite
Con il termine gastroenterite, i medici indicano un’infiammazione a carico dello dentaco e dell’intestino.
In genere, la gastroenterite ha un’origine infettiva; tuttavia, в alcuni casi, очень хорошо для каждого эффекта, сделанного металлическими tossici, farmaci, piante o грибами.
SPECIE DI ROTAVIRUS
Ad oggi, i virologi hanno Individual 8 видов ротавируса , идентифицировать с первыми письмами maiuscole dell’alfabeto, quindi A, B, C, D, E, F, G e H.
Delle 8 specie di Rotavirus finora индивидуальный, вид Ротавируса A — quella più diffusa. Это, инфатти, отвечает на 90% заразных инфекций ротавируса.
ALCUNE CARATTERISTICHE DEL ROTAVIRUS
Генома ротавируса состоит из 11 молекул РНК a doppia elica, идентифицируемых как con i numeri arabi da 1 a 11.
Tutte insieme, queste 11 молекул ди РНК a doppia elica Possiedono esattamente 18,555 нуклеотидов .
Tranne la molcola di RNA numero 9 — che codifica per due geni — все другие молекулы, кодирующие РНК для единственного гена.
Ротавирус — это частицы диаметром 76,5 нанометров .
STORIA DEL ROTAVIRUS
Заслуга исследователя ротавируса в Австралийском вирусе Рут Бишоп и за свою команду коллег.Era l’anno 1973.
L’introduzione nel gergo medico del termine «rotavirus», risale al 1974: a coniare story parola fu un altro virologo, un certo Thomas Henry Flewett , che al microscopio elettronico not la частной формы a ruota del ротавирус («ротавирус» — это латиноамериканский термин, по-итальянски, значение «руота»).
Частично в 1980 году было проведено исследование ротавирусов, связанных с отдельными видами вирусов, существующих в естественных условиях и способностях заражения.
ЭПИДЕМИОЛОГИЯ
В базовой статистике исследований ротавируса вызвано миллионов и миллионов инфекций , ответственных за 2 миллиона пациентов и определено случаев квази 9 453,000 за 9000 лет.
Tuttavia, это точная вакцинация против ротавируса, ежегодная инфекция, вызванная вирусом ротавируса, в явном виде (без вакцинации).
Вирус ротавируса является общим, второстепенным, медицинским и вирусным, почти полностью и однозначно противодействующим вирусам.
Вероятность заражения ротавирусом è больше всего поражает фредди е / о секше.
Nella popolazione adulta, инфекция ротавируса очень редко.
Негативный ротавирус США, при вакцинировании
Приведенный к применению вакцины ad hoc , Негли США, только год, в казино заражения ротавирусной инфекцией около 2,7 миллиона человек.
Di questi 2,7 миллиона casi d’infezione, 60,000 около богатых медикаментов и 37 около causavano la morte dell’individuo interessato.
Причина
La trasmissione del rotavirus può avvenire in diversi modi:
- Tramite la cosiddetta via oro-fecale ( trasmissione oro-fecale ). Questa modalità di trasmissione comporta che l’agente patogeno sia in grado di ritrovarsi nelle feci.
Nel caso specifico, il rotavirus ha la suddetta capacity. - Tramite il contatto fisico con mani, superfici, cibi od oggetti contaminati.
- Tramite le vie респиратор . В questo caso, trasmettere l’agente virale sono piccole goccioline volatili di saliva, che espellono le persone contagiate quando parlano, starnutiscono, tossiscono ecc.
La trasmissione oro-fecale è, in assoluto, la più diffusa e quella che causa il maggior numero di infzioni. Del resto, si pensi che le feci di un soggetto infettato dal rotavirus context около 10 триллионов отдельных вирусов на грамм e, для того, чтобы избавиться от гастроэнтерита ротавируса, достаточно 100 частиц вируса на грамм.
ALCUNE CURIOSITÀ SULLA TRASMISSIONE DEL ROTAVIRUS
Rotavirus è abbastanza stabile nell’ambiente ed è capace di sopravvivervi, in attesa di infettare qualcuno, per un periodo di tempo che va dai 9 ai 19 giorni.
Inoltre, è curioso come, nei Paesi del Mondo in cui le misure sanitarie sono inadeguate, il tasso d’incidenza delle influenza da rotavirus sia equiparabile al tasso d’incidenza delle infzioni da rotavirus calcolato per i Paesi del Mondo dove le misure all’avanguardia.
FATTORI DI RISCHIO
Я получил вирусную инфекцию от ротавирусной инфекции, обнаруженной в bambini di età compresa tra i 3 e i 35 mesi .
Sintomi e Complicanze
Я знаю, что заражение ротавирусной инфекцией было подтверждено приблизительно в связи с установленной ситуацией на всем патогенезе. Это период инкубации ротавируса 14-15 лет примерно.
Деривант гастроэнтерита, который является производным от градации умеренного или северо-восточного, in un primo momento defineda un lieve stato febbrile , тошнота e vomito ; in un secondo momento (di solito dopo 3-7 giorni), compaiono episodi ricorrenti di diarrea acquosa (o dissenteria) и forti dolori addominali .
Secondo alcune indagini cliniche, i bambini di età compresa tra i 6 mesi e i due anni di vita sono i soggetti che sviluppano la sintomatologia più grave.
РОТАВИРУС НЕГЛИ ВЗРОСЛЫЙ
Negli adulti che godono di buona salute, инфекционные заболевания ротавируса, вызванные выявлением заражения, spesso quasi impercettibili.
in altre parole, sono parzialmente o totalmente asintomatiche .
Perché gli adulti sono meno soggetti all инфекция ротавируса?
Другие причины предрасположенности ко всем инфекциям ротавируса на все случаи жизни:
- Нет, вероятно, вирус в этом вирусе, но не имеет антикорпусного иммунитета, который защищен от инфекции.
- Hanno un sistema immmunitario maturo e più efficace di quello di un bambino.
ПРИХОДИТЕ РОТАВИРУС КАУЗА ГАСТРОЭНТЕРИТ
Dal punto di vista patofisiologico, il rotavirus causa la gastroenterite perché, quando penetra nell’organismo, agredisce e distrugge gli enterociti .
Gli enterociti sono le cellule epiteliali che rivestono la parete interna dell’intestino tenue; nella fattispecie, sono gli elementi celli che tappezzano i кишечные ворсинки .
QUANDO RIVOLGERSI AL MEDICO?
In caso di pazienti di età giovane o molto giovane, è Bene contattare il medico in presenza di:
In caso di pazienti di età adulta, rivolgersi al medico in presenza di:
- Episodi di diarrea almeno due volte al giorno
- Incapacità di trattenere i liquidi ingeriti per più di 24 ore
- Vomito con sangue
- Ripetuti movimenti кишечника
- Февраль при 39 ° C или выше
- Disidratazione
ОСОБЕННОСТИ
Важнейшее осложнение заражения ротавирусом — дезидратации последовательных эпизодов заражения бактериальной диареей.
Se non trattata per tempo e con le giuste modalità, la disidratazione può portare anche alla morte il soggetto interessato.
Диагностика
Il rotavirus provoca un’infezione che i medici Diagnosticano, в общем, tramite un accurato esame obiettivo e un’attenta anamnesi (storia Clinica).
Qualora permanessero dei dubbi, l’esame che permette di chiarire Definitivamente l’origine della diarrea e degli altri sintomi della gastroenterite и l ‘ analysis di un campione di feci del paziente.
L’analisi del campione fecale comprende una serie di test di labratorio, finalizzati alla ricerca del rotavirus.
Траттаменто
I trattamenti disponibili, per la cura delle influeni da rotavirus, sono aspecifici econstonzialmente in terapie di tipo sintomatico . Типовая синтоматическая терапия — это финальная промежуточная терапия в области квадратной синтоматологии.
Tra i varmedi sintomatici, является наиболее важным для управления idratazione del soggetto infetto.Se l’apporto di liquidi è adeguato all richieste del paziente, il rischio di затруднительно и минимально, и дает возможность повысить уровень гарантии.
REIDRATAZIONE: IN COSA CONSISTE?
La reidratazione di un soggetto con un’infezione da rotavirus consiste nella somministrazione di liquidi на основе воды, минеральных солей и цуккери .
Я соленые минералы, которые очень важны, in quanto il vomito e la diarrea neterminano una grande perdita.
COSA FARE IN CASO DI DISIDRATAZIONE SEVERA?
Инфекция ротавируса вызвана серьезным нарушением, необходимо , чтобы получить человек, инфицированных и подозреваемых в заражении, и жидкости для повторного заражения через эндовенозу.
SERVONO I FARMACI CONTRO LA DIARREA?
В целом, возбудители инфекционных заболеваний ротавируса не предотвращают заболевания, вызванные заболеванием, противодействующим диарее (farmaci antidiarroici).
Индикация сказки действительна для того, чтобы узнать, каковы были инфетивные признаки серьезного несогласия.
Prognosi
В целом, это заболевание, выздоравливающее и ликвидирующее заболевание, вызывающее диарею и / или рвоту, является классической инфекцией ротавируса, связанной с заражением 3-7 человек , зараженным другим видом.
Prevenzione
Приходите с акцентом на вакцину против ротавируса .
A voler essere più Precisi, esistono due tipologie di Vacini, Entrambe molto efficaci e sicure. Этот тип вакцины, защищенной от специфических вирусов ротавируса вида A, имеет аттенуированных вакцин против и предположительно на через orrale . За консультацией по относительной схеме технологий, приведены сведения о характеристиках вакцины Rotarix и RotaTeq .
La messa in commercio dei vacini contro il rotavirus A è abbastanza Последние. Risale, infatti, al 2006 (dopo ovviamente unaunga serie di sperimentazioni).
Attualmente, per.
PPT — Презентация PowerPoint по ротавирусной инфекции, скачать бесплатно
Ротавирусная инфекция Детская больница, Медицинский факультет Чжэцзянского университета Цзян Мизу
Что такое ротавирус? Электронно-микроскопический вид ротавируса «Рота» на латыни означает колесо Впервые обнаружен в апреле 1973 года Р. Бишопом и его командой при биопсии австралийского ребенка с тяжелым гастроэнтеритом.Частицы ротавируса в фильтрате стула Фото: F.P. Уильямс, Агентство по охране окружающей среды США; По материалам Parashar et al. Emerg Inft Dis 1998,14 (4) 561–570
Электронно-микроскопические проявления ротавируса
Что такое гастроэнтерит? • Гастроэнтерит занимает второе место после респираторных заболеваний как причина детской заболеваемости во всем мире. • Гастроэнтерит: тошнота, рвота, диарея, спазмы в животе и лихорадка возникают через 6-48 часов после воздействия.• Большинство гастроэнтеритов вызвано вирусной инфекцией; бактериальные, паразитарные и протозойные заболевания встречаются реже, но нередки.
Ротавирусный гастроэнтерит • Вирусный гастроэнтерит • Самостоятельное заболевание с тошнотой, рвотой, диареей • Дети в возрасте от 6 месяцев до 2 лет • Ротавирус может вызывать острую диарею у взрослых
Что такое диарея? • Определение: повышенный общий суточный диурез (> 10 г / кг / сут) , обычно связан с повышенным содержанием воды в стуле.• Рыхлая консистенция (性状 改变): водянистая диарея, слизистая диарея, кровавый понос • Частота стула (次数 增多) • Продолжительность • Острая (<14 дней) • Постоянная (от 14 дней до 2 месяцев) • Хроническая (> 2 минут)
Ротавирус и диарея • Вирусы являются наиболее частой причиной острого гатроэнтерита в развивающихся и развитых странах, такие как ротавирус, астровирус, аденовирус и калицивирусы (агент Norwalk) • Ротавирус, вирус с двухцепочечной РНК длиной 67 нм по крайней мере, с восемью серотипическими вариантами, является наиболее распространенным.• Как и большинство вирусных патогенов, ротавирус поражает тонкий кишечник, вызывая объемную водянистую диарею без лейкоцитов и крови.
REOviridae Группа B VP6 C, D, E, F, G (7) Семейство I Подгруппа II (2) Серотип VP7 VP4 GP (1-14) (1-8) G1P [8] G2P [4] G3P [8] G4P [8] 病毒 — 分类 呼 肠 病毒 科 A G9 (64%) (12%) (3%) (9%) Santos et al, Rev Med Virol 2005, январь — 15 февраля (1) 29-56
Введение Эпидемиология ротавируса • Ротавирус — самый распространенный диарейный патоген у детей во всем мире1 • В мире более 125 миллионов случаев младенческого гастроэнтерита2 • 440 000 случаев смерти в год, главным образом в менее развитых странах3 Расчетное глобальное распределение 440 000 смертей в год у детей младше 5 лет, вызванная ротавирусной диареей31 dot = 1000 смертей 1Parashar et al, Emerg Infect Dis 1998 4 (4) 561–570; 2Linhares и Bresee, Pan Am J Public Health 2000 8 (5) 305–331; 3Parashar et al, Emerg Infect Dis 2003 9 (5) 565–572
Развитые страны Менее развитые страны Паразиты Неизвестный Ротавирус Неизвестный Ротавирус Другие бактерии Escherichia coli Бактерии Аденовирус Аденовирус Астровирус Калицивирус Распространение возбудителя Астровирус Калицивирус эпидемия эндемический / эпидемический гастроэнтерит и детская рвота и диарея От Kapikian AZ, Chanock RM.Ротавирусы. В: Поля вирусологии, 3-е изд. Филадельфия, Пенсильвания: Липпинкотт-Рэйвен; 1996: 1659.
Все дети заразятся хотя бы одной ротавирусной инфекцией в начале жизни 1,0 1-я инфекция 0,9 0,8 2-я инфекция 0,7 0,6 Вероятность ротавирусной инфекции 0,5 3-я инфекция 0,4 0,3 4-я инфекция 0,2 0,1 5-я инфекция 9 12 15 18 21 24 3 6 Возраст (мес.) Воспроизведено с разрешения Velázquez et al. N Engl J Med. 1996; 335: 1022-1028.
Смертность, связанная с ротавирусами, на 1000 детей в возрасте до 5 лет лет 0.0-0,1 0,2-0,5 0,6-0,9 1,0-1,9 2,0-3,4
Эпидемиология • Вспышки распространены в детских больницах и детских учреждениях. • Заболевание обычно бывает наиболее тяжелым у пациентов в возрасте от 6 до 24 месяцев, хотя 25% случаев тяжелого заболевания возникают после 2-летнего возраста, при этом серологические признаки инфекции развиваются практически у всех детей к 4-5 годам. • Младенцы младше 3 месяцев относительно защищены трансплацентарными антителами и, возможно, кормят грудью.
Эпидемиология • Передача: фекально-оральный путь через зараженную пищу, воду, игрушку или респираторную каплю, требуется всего 10 частиц от человека к человеку. • Вирус устойчив к кислоте желудка, прикрепляется к бета-рецепторам. • Пик сезона в умеренном климате — зима, в тропиках чаще во времена низкой влажности. • Большое количество вируса выделяется со стулом в течение первой недели заражения, и может сохраняться до 2 месяцев. • Вирус выживает часами на руках и в течение 6-60 дней на сухих неодушевленных поверхностях.
Фекально-оральная передача Зараженный человек Зараженное животное Игрушка Вода Пища Восприимчивый человек
Патофизиология ротавирусной инфекции • При вирусной инфекции диарея не вызывает воспаления и возникает в результате зрелой энтеропатии, в результате которой происходит смерть ворсинок. верхние клетки (ответственные за переваривание дисахаридов и всасывание моносахаридов) вызывают осмотическую диарею из-за мальабсорбции сахаров.
Анатомия кишечника
Патогенез • Вирусы, вызывающие диарею человека, избирательно инфицируют и разрушают клетки кончика ворсинок в тонком кишечнике.• Биопсия тонкой кишки показывает различную степень притупления ворсинок и инфильтрата круглых клеток в собственной пластинке. • Патологические изменения могут не коррелировать с серьезностью клинических симптомов и обычно проходят до того, как клиническое исчезновение диареи.
Патогенез Ротавирусы прикрепляются к эпителию желудочно-кишечного тракта (слизистая оболочка тощей кишки) * * Атрофия ворсинок кишечника Потеря абсорбционной области Поток воды и электролитов Рвота и диарея Энтеротоксин энтеротоксина энтеротоксина энтеротоксина животная модель инфекции.Фотографии взяты с экспериментально зараженного теленка. Воспроизведено с разрешения Zuckerman et al, eds. Принципы и практика клинической вирусологии. 2-е изд. Лондон: John Wiley & Sons; 1990: 182. Микрофотографии любезно предоставлены доктором Грэмом Холлом, Беркшир, Великобритания.
Главное беспокойство • Острая диарея, ограниченная самим собой • Тошнота • Рвота • Большинство инфекций у новорожденных протекает бессимптомно или в легкой форме
Клиническое проявление • Наиболее частая причина острого гастроэнтерита у младенцев и детей ясельного возраста.• Пик сезона приходится на более прохладные осенние и зимние месяцы (круглый год). • Пик заболеваемости составляет от 3 до 24 месяцев. • Инкубационный период RV составляет 24-48 часов. • Рвота — первый симптом у 80–90% пациентов, за которым в течение 24 часов следует субфебрильная температура и объемная водянистая диарея без крови.
Клинические проявления • Диарея обычно проходит самостоятельно, проходит через 4–8 дней, но может длиться дольше у младенцев или пациентов с ослабленным иммунитетом. • До одной трети имеют лихорадку> 39 ° C. • Количество лейкоцитов повышено редко.• Стул не содержит крови или лейкоцитов. • Осложнение • Обезвоживание • Дисбаланс электролитов
Оценка состояния обезвоживания • Наиболее частыми причинами обезвоживания у детей являются рвота и диарея. • Обезвоживание классифицируется по проценту общей потери воды в организме: легкое (<5%), умеренное (5-10%) и тяжелое (> 10%). • Различные признаки и симптомы, а также дополнительные данные помогают оценить степень обезвоживания.
Степень обезвоживания Клинические признаки легкая умеренная тяжелая Снижение массы тела 3-5% 5-10% 10-15% Кожа Тургор в норме снижен Заметно снижен Цвет нормальный бледный заметно уменьшен Слизистые оболочки Сухие Пятнистые или серые; пересохшие Гемодинамические признаки Пульс нормальный незначительное усиление тахикардия Наполнение капилляров 2-3 с 3-4 с> 4 с артериальное давление нормальная низкая перфузия нормальная циркуляторная недостаточность Потеря жидкости диурез легкая олигурия олигурия анурия слезы Снижение отсутствует Индексы мочи удельный вес> 1.020 анурия Моча [Na +] <20 мЭкв / л анурия
Клиническая шкала обезвоживания (CDS) • Баллы, присвоенные на основе 4 клинических пунктов • Общий вид • 0, нормальный • 1, жажда, беспокойство, вялость, но раздражительность при прикосновении • 2, сонливость, вялость, холод, потливость, коматозное состояние • Глаза • 0, нормальное состояние; 1, слегка вдавленный; 2, очень впалые • Слизистые оболочки (язык) • 0, влажные; 1, липкий; 2, сухие • Слезы • 0, есть; 1, уменьшилось; 2, отсутствует • CDS классифицирует детей по 3 степени обезвоживания • 0 баллов, обезвоживание отсутствует • 1-4 балла, небольшое обезвоживание • 5-8 баллов, умеренное / тяжелое обезвоживание
Электролитные расстройства • Нарушения натрия Изотоническое обезвоживание: [Na +] 130-150 ммоль / л Гипотоническая дегидратация: [Na +] <130 ммоль / л Гипертоническая дегидратация: [Na +]> 150 ммоль / л • Калийные расстройства Гиперкалиемия: [K +]> 5.5 ммоль / л Гипокалиемия: [K +] <3,5 ммоль / л
Метаболический ацидоз Согласно AG = [Na +] — ([HCO3-] + [Cl-]) • Нормальный тип: 8-16 ммоль / л [ HCO3-] • Повышенный тип:> 16 ммоль / л [H +] Согласно [HCO3-] • Легкий [HCO3-] 18-13 ммоль / л • Умеренный [HCO3-] 13-9 ммоль / л • Тяжелый [HCO3-] <9 ммоль / L
Диагноз • В большинстве случаев удовлетворительный диагноз может быть поставлен на основании клинических и эпидемиологических признаков. • Специфическая идентификация ротавируса требуется не во всех случаях, особенно во время вспышек.• Стул для ELISA, который обеспечивает чувствительность примерно 70-80% и специфичность 71-100%. • Анализы крови: газы и электролиты крови, анализ крови, азот мочевины в крови, креатинин • Выполните микробиологические исследования стула при кровавой диарее или тяжелой болезни. • Дополнительные анализы: рентген брюшной полости, стул (посев, электронная микроскопия, ПЦР)
Исследования стула Выводы Значение Общий анализ Кровь, слизь, гной Бактериальная инфекция Микроскопическое исследование> 5 лейкоцитов / HPF Бактериальная инфекция Химическое исследование • Стул pH pH <5 Вирусная инфекция, мальабсорбция углеводов • Вещества, снижающие стул + вирусная инфекция, мальабсорбция углеводов
Дифференциальный диагноз • В младенчестве дифференциальный диагноз острого гастроэнтерита включает диарею, связанную с другими инфекциями, такими как инфекция мочевыводящих путей, отит, сепсис и пневмония.• В зависимости от географического положения кишечные аденовирусы или калицивирусы являются следующими по распространенности вирусными патогенами у младенцев. • Другие потенциально патогенные вирусы включают астровирусы, короноподобные вирусы, вирусы Коксаки и другие небольшие круглые вирусы.
Норовирус • Калицивирус — это вирус с малой РНК, который вызывает эпидемические вспышки гастроэнтерита • Поражает детей школьного возраста, подростков и взрослых. • После 24-часового инкубационного периода (от 12 до 72 часов) у пациентов наблюдаются лихорадка, рвота, диарея и часто недомогание и миалгии.• Стул жидкий, водянистый, без крови, слизи и лейкоцитов. • Продолжительность симптомов короткая, обычно 12-60 часов.
一些 胃肠 道 病毒 的 特征
Управление • Цели • Контроль диареи, предотвращение рвоты, контроль других симптомов • Распознавание, профилактика и лечение обезвоживания • Поддержание нутритивного статуса пациенты. • Поддерживающее лечение • Восполнение дефицита жидкости и электролитов и продолжающихся потерь имеет решающее значение, особенно у маленьких детей.• В большинстве случаев уместно использование раствора для пероральной регидратации (ПРС).
Раствор для пероральной регидратации (ПРР) Компонент (低渗) г / л (标准) г / л NaCl 2,6 3,5 Глюкоза 13,5 20 KCl1,5 1,5 Цитрат натрия 2,9 2,9 Общий вес 20,5 27,9
Управление обезвоживанием • Для детей с легким или умеренным обезвоживанием • Рекомендуется быстрое восполнение жидкости пероральной регидратационной терапией (ПРТ) • Расчетное количество ПРС 75 мл / кг в течение первых 4 часов • ПРТ через рот или назогастральный зонд (НГ) может иметь аналогичная общая безопасность и эффективность, как при внутривенной регидратационной терапии.• Для детей с тяжелым обезвоживанием • Рекомендуется немедленная и быстрая регидратация внутривенно. • Детей с острой диареей следует продолжать кормить.
Отсутствие или минимальные признаки обезвоживания • Рекомендуется введение жидкости в домашних условиях • Увеличьте потребление жидкости, чтобы компенсировать потери и предотвратить развитие обезвоживания • Если возможно, заменяйте жидкость после каждого эпизода диареи или рвоты • 50–120 мл у детей <2 лет • 100–240 мл детям в возрасте 2–10 лет • Поощряйте ПРС • Избегайте коммерческих соков и газированных напитков • Продолжайте обычное кормление • Поощряйте опекунов приносить ребенка в медицинское учреждение при появлении признаков обезвоживания
Легкая и умеренная обезвоживание • Быстрая замена жидкости с помощью ОРТ в медицинском учреждении • Обеспечьте 50-100 мл / кг ПРС в течение первых 4 часов (давая часто в небольших количествах) • Рекомендации по ОРТ • Рассмотрите возможность введения ПРТ на НГ ребенку с нормальным психическим статусом, который не может выпивает или постоянно рвет при пероральном введении ПРС • Рассмотрите возможность внутривенной терапии ребенку с пониженным сознанием или при отсутствии реакции на пероральное введение или введение НГ. ПРС • Немедленно начните внутривенную инфузию, если у ребенка появляются признаки тяжелого обезвоживания или клинического ухудшения • Поощряйте введение жидкости в домашних условиях после исправления обезвоживания
Тяжелое обезвоживание • Начните быструю внутривенную инфузию болюсом 10-20 мл / кг физиологического раствора ( NS) от 20 до 30 мин.• Оценка их жидкостного статуса. • Получите кровь на электролиты, азот мочевины крови (АМК), креатинин, глюкозу и общий анализ мочи • Если реакция на начальный болюс плохая, повторите инфузию. • При плохой реакции на два болюса внутривенно рассмотрите другое сопутствующее заболевание органов (септический шок или метаболические, сердечные и неврологические заболевания) или необходимость мониторинга центральной венозной крови перед введением третьего болюса. • Отек век и конечностей может указывать на гипергидратацию
Диетическая терапия • Дети, получающие полутвердую или твердую пищу, должны продолжать обычную диету во время эпизодов диареи • Предлагать детское питание каждые 3-4 часа • Рекомендации по кормлению младенцев кормить грудью по требованию • Младенцы, находящиеся на искусственном вскармливании, должны продолжать обычное питание после регидратации • Младенцы должны продолжать обычную диету во время диареи после диареи • Никогда не следует отказываться от еды; • Пищу нельзя разбавлять. • Грудное вскармливание следует всегда продолжать. • Безлактозное молоко или детские смеси не улучшают исходы у большинства маленьких детей с острой диареей.• Рекомендации по питанию детей в развивающихся странах
Лекарства • Пробиотики: было показано, что такие виды, как лактобациллы, несколько снижают интенсивность и продолжительность болезни. • Добавки цинка • Рацекадотрил, ингибитор энкефалиназы с антисекреторным действием • Смектития • Глютамин
Лекарств не принимаются • Нет роли в лечении противовирусными препаратами. • Нет пользы от антибиотиков • Нет пользы от противорвотных или противодиарейных препаратов, и существует значительный риск серьезных побочных эффектов.• Следует избегать агентов, снижающих моторику.
Профилактика ротавирусной инфекции • Хорошая гигиена (регулярная дезинфекция игровых площадок и игрушек) снижает передачу RV. • Частое мытье рук и процедуры изоляции могут помочь контролировать внутрибольничные вспышки. • Кормление грудью для профилактики или облегчения инфекции RV может быть незначительным. • Возникают повторные инфекции, но обычно менее тяжелые. • Разработка ротавирусных вакцин
Вакцинация против ротавируса • Имитация иммунного ответа естественной ротавирусной инфекции для: • защиты от умеренного / тяжелого заболевания • предотвращения госпитализации и смерти • снижения заболеваемости и социально-экономического бремени • уменьшения тяжести и продолжительности болезни
Здоровье азиатских ротавирусов
Frontiers | Преимущества и полезные свойства молочнокислых бактерий и их бактериоцинов как альтернативы стимуляторам роста антибиотиков при производстве продуктов питания и животных
Введение
Животноводство — один из наиболее быстрорастущих аспектов сельскохозяйственного сектора.За последние десятилетия производство и потребление продуктов животноводства значительно увеличилось (Speedy, 2003). Это увеличение продолжится в ближайшем будущем, чтобы удовлетворить высокий спрос на продукты животноводства, такие как мясо, молоко, яйца и рыба, особенно в промышленно развитых странах (OECD / FAO, 2018). Преобладающими видами домашнего скота являются свиньи (112,33 млн тонн), домашняя птица (109,02 тонн) и крупный рогатый скот, включая говядину и мясо буйвола (67,99 тонн), что составляет 91,80% мирового производства мяса (FAOSTAT, 2013).В то время как вылов рыбы и производство аквакультуры достигли 158 тонн (FAOSTAT, 2013).
В ветеринарии антибиотики используются для борьбы с клиническими и субклиническими инфекционными заболеваниями. Примечательно, что в некоторых странах они также используются в качестве противомикробных стимуляторов роста (AGP). С этой целью антибиотики поставляются в субтерапевтических дозах, чтобы принести пользу домашнему скоту за счет повышения скорости роста, снижения смертности и улучшения репродуктивной способности животных (Marshall and Levy, 2011). Антибиотики, в основном используемые для применения с AGP, включают тетрациклины, ионофоры и пенициллины (American Meat Institution, 2013).В Европе использовались различные противомикробные препараты (Butaye et al., 2003), но Регламент (ЕС) № 1831/2003 гласил, что «Антибиотики, кроме кокцидиостатов или гистомоностатов, не должны разрешаться в качестве кормовых добавок», и теперь они разрешены. запрещен в ЕС. По оценкам, глобальное потребление антибиотиков животноводством составляет примерно от 63 000 до более 240 000 метрических тонн в год (World Bank, 2017), и эти количества, безусловно, могут увеличиваться из-за высокого уровня потребления, зарегистрированного в странах с развивающейся экономикой (World Bank, 2017).Однако в некоторых странах наблюдается значительное снижение продаж противомикробных препаратов для пищевых продуктов (ESVAC, 2017). Как следствие, такое чрезмерное использование антибиотиков будет способствовать распространению устойчивости к противомикробным препаратам во всем мире.
Антибиотики могут влиять на микробиоту кишечника и физиологию хозяина путем (i) предотвращения колонизации патогенными микроорганизмами, (ii) воздействия на иммунную систему, (iii) увеличения абсорбции жира за счет уменьшения гидролиза конъюгированных солей желчных кислот и (iv) увеличения использования питательных веществ. в результате изменения стенки кишечника и собственной пластинки (Niewold, 2007; Lee et al., 2011). Баланс, существующий между полезными и вредными бактериями в желудочно-кишечном тракте (ЖКТ) здорового животного, может быть изменен при изменении пропорций бактерий, вызывающих инфекции патогенными микроорганизмами из различных внешних источников (Kers et al., 2018; Pluske et al., 2018). Патогенные бактерии могут негативно влиять на здоровье и благополучие животных, а также на их рост и воспроизводство. Некоторые из них могут попасть в желудочно-кишечный тракт человека через пищевую цепь (Newell et al., 2010), что между тем может привести к передаче устойчивости к антибиотикам (Soucy et al., 2015). Устойчивость к антибиотикам — серьезная проблема для человечества. Чтобы уменьшить это явление, запрет на использование антибиотиков в качестве стимуляторов роста в ЕС должен быть глобальным. Следовательно, некоторые страны, такие как Мексика, Новая Зеландия и Южная Корея, приняли подход ЕС. Другие страны, такие как США, Канада или Япония, разработали руководящие принципы и рекомендации по сокращению использования AGP в животноводстве (Laxminarayan et al., 2015; Браун и др., 2017; Ляо и Ньячоти, 2017). Чтобы помочь в борьбе с устойчивостью к антибиотикам, международные организации разработали глобальные планы действий, направленные на обеспечение лечения и профилактики инфекционных заболеваний безопасными и эффективными лекарствами (ВОЗ, 2015).
Запрет на использование антибиотиков в качестве AGP оказывает экономическое и негативное влияние на сектор животноводства из-за различных неконтролируемых бактериальных заболеваний (Laxminarayan et al., 2015). Чтобы помочь контролировать растущую устойчивость к антибиотикам, срочно необходимы инновационные альтернативы для производства продуктов питания животного происхождения (Seal et al., 2013; Cheng et al., 2014; Когут, 2014; Czaplewski et al., 2016). В связи с этим ЕС недавно рекомендовал использование альтернативных стратегий в отношении сельскохозяйственных животных для ограничения устойчивости к противомикробным препаратам (УПП), и это привело к временным и удовлетворительным результатам, наблюдаемым в некоторых странах ЕС. Принятые стратегии включали (i) национальные цели по сокращению, (ii) сравнительный анализ использования противомикробных препаратов и (iii) меры контроля за назначением и ограничениями использования конкретных критически важных противомикробных препаратов, вместе с улучшениями в животноводстве и мерами профилактики и контроля болезней (Мерфи и другие., 2017). Согласно исследованиям Allen et al. (2013), Czaplewski et al. (2016), Сил и др. (2018), ожидается, что дополнительными средствами замены AGP в животноводстве являются пребиотики, антимикробные пептиды (AMP), бактериофаги и их генные продукты, антитела, вакцины и природные соединения, такие как полифенолы и особенно пробиотики. Текущее принятое определение пробиотиков от ФАО / ВОЗ (2002) гласит, что пробиотики — это «живые микроорганизмы, приносящие пользу здоровью хозяина при введении в адекватных количествах».«Микроорганизмы с пробиотической чистотой должны быть лишены каких-либо побочных эффектов (цитотоксичность, устойчивость к антибиотикам, гемолиз) и должны иметь полезные свойства. Известно, что пробиотики действуют штамм-зависимым образом и подавляют патогенные бактерии с помощью различных механизмов, как сообщалось в различных исследованиях (Kabir, 2009; Alloui et al., 2013; Pandiyan et al., 2013; Dowarah et al., 2017). Что касается функций, возложенных на пробиотики, было установлено, что многочисленные филогенетические анализы, связанные с экспериментальными данными, выявили некоторую парадигму адаптации хозяина (Frese et al., 2011).
По данным Krajmalnik-Brown et al. (2012), кишечная микробиота животных является ключевым органом, который играет определяющую роль в сборе, хранении и расходе энергии, получаемой с пищей. Примечательно, что эти функции могут влиять на здоровье и изменение веса животного (Krajmalnik-Brown et al., 2012). Поэтому обратите внимание, что в другом отчете ФАО (2013) сообщается о возможности применения пробиотиков для питания животных в качестве усилителей экосистемы кишечника. Интересно, что Йирга (2015) и Сил и др.(2018) сообщили и аргументировали использование пробиотиков молочнокислых бактерий (LAB) для улучшения показателей роста и воспроизводства, а также выживаемости и состояния здоровья животных. В отношении LAB-пробиотиков в таблице 1 приведен список этих штаммов, потенциально применимых в качестве заменителей антибиотиков из-за их многогранности.

Таблица 1. Родов пробиотиков, используемых в животноводстве ∗ .
Молочнокислые бактерии подходят для животноводства в качестве пробиотиков из-за их способности изменять среду, в которой они были доставлены, путем продуцирования различных метаболитов, среди которых широкий спектр ингибирующих веществ и даже конкурентное исключение (Gaggìa et al., 2010; ФАО, 2016). Следует отметить, что LAB-пробиотики относятся к Lactobacillus ( Lb. ), , Pediococcus ( Ped. ) , Lactococcus ( Lc. ) , Enterococcus (18) Ent. , Streptococcus ( Str .) И Leuconostoc ( Leuc. ). Тем не менее, видов Lactobacillus остаются наиболее изученными и используемыми (Martínez Cruz et al., 2012). Механизмы ингибирования патогенов пробиотиками LAB включают (i) продукцию ингибирующих соединений, (ii) предотвращение адгезии патогенов, (iii) конкуренцию за питательные вещества, (iv) модуляцию иммунной системы хозяина, (v) улучшение усвояемости питательных веществ. , конверсия корма и (vi) снижение биодоступности токсина (рис. 1).
Рисунок 1. Механизмы ингибирования возбудителя LAB-пробиотиками.
Подавление патогенов
Наиболее часто встречающимися патогенными или зоонозными бактериями в животноводстве являются: Escherichia coli , Salmonella enterica , Campylobacter jejuni , Vibrio anguillarum , Clostridium perfringens , salmonudicas Aeromonasidae и Edwardsiella spp.(Таблица 2). Хотя некоторые из этих патогенов, такие как V. anguillarum и C. jejuni , чаще всего встречаются у рыб и птиц, соответственно, другие бактерии могут поражать различных хозяев, вызывая различные патологии у нескольких животных-производителей пищевых продуктов. Это случаи E. coli и S. enterica , которые могут поражать домашнюю птицу, свиней, жвачных животных и людей (таблица 2). Как указывалось выше, LAB-пробиотики могут ограничивать распространение патогенных бактерий с помощью механизмов, включающих продукцию ингибирующих соединений и конкурентное исключение.
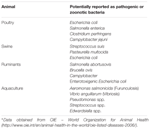
Таблица 2. Наиболее часто встречающиеся бактериальные инфекции среди производителей в животноводстве ∗ .
Производство ингибирующих соединений
LAB может производить широкий спектр ингибирующих соединений для уменьшения инвазии патогенов (таблица 3). К ним относятся AMP, такие как бактериоцины, органические кислоты, этанол, диацетил, диоксид углерода и перекись водорода (Liao and Nyachoti, 2017).
Таблица 3. Примеры антимикробных соединений, производимых LAB.
Бактериоцины — это синтезированные рибосомами АМП, продуцируемые как грамотрицательными, так и грамположительными бактериями (Drider and Rebuffat, 2011). Бактериоцины, продуцируемые LAB, называемые здесь LAB-бактериоцинами, чаще всего лишены цитотоксических свойств (Belguesmia et al., 2010) и наделены антагонистическими функциями, а также дополнительными полезными свойствами (Drider et al., 2016; Chikindas et al., 2018). LAB-бактериоцины появляются как новая волна антибиотиков с высокой активностью in vitro и in vivo (Stern et al., 2008; Рихакова и др., 2010; Аль-Атья и др., 2016; Цзян и др., 2016; Caly et al., 2017; Седдик и др., 2017). В отличие от традиционных антибиотиков, LAB-бактериоцины нацелены на определенные виды и не влияют на другие популяции в пределах той же экосистемы. Известно, что LAB-бактериоцины проявляют бактериостатическую или бактерицидную активность в отношении чувствительных организмов. Их способы действия были широко, но не досконально исследованы. Недавние исследования способов действий рассмотрены в другом месте (Cavera et al., 2015; Драйдер и др., 2016; Woraprayote et al., 2016; Бен Лага и др., 2017; Perez et al., 2018). Комбинации LAB-бактериоцинов и антибиотиков становятся новыми терапевтическими вариантами для животных, производящих пищу (Naghmouchi et al., 2010, 2011, 2013; Al Atya et al., 2016). В различных отчетах установлены основные преимущества и синергетическое действие LAB-бактериоцинов с другими биомолекулами. Это случай энтероцина AS-48 и этамбутола против Mycobacterium tuberculosis (Aguilar-Pérez et al., 2018), низин и лимонная кислота против Staphylococcus aureus и Listeria monocytogenes (Zhao et al., 2017), низин и бета-лактамы против Salmonella enterica серовар Typhimurium (Rishi et al., 2014; Singh et al. ., 2014), и Гарвицин КА-фарнезол против набора грамположительных и грамотрицательных бактерий (Chi and Holo, 2018). Пероральное введение этих веществ является проблемой из-за их ферментативного разложения. Об этом случае сообщалось in vivo для лактицина 3147 и низина (Gardiner et al., 2007; Gough et al., 2018).
Органические кислоты, включая короткоцепочечные жирные кислоты, молочную и муравьиную кислоты, подавляют потенциально патогенные бактерии, важные для сельскохозяйственных животных. LAB производят молочную кислоту как основной продукт метаболизма сахара (Russo et al., 2017). Однако LAB, метаболически известные как гетероферментативные виды, могут одновременно продуцировать другие конечные продукты, такие как уксусная кислота (Oude Elferink et al., 2001; Schnürer and Magnusson, 2005). Известно, что органические кислоты действуют путем снижения внутриклеточного pH и ингибирования активного транспорта избыточных внутренних протонов, что требует потребления клеточного аденозинтрифосфата (АТФ), что приводит к истощению клеточной энергии (Ricke, 2003).Основными мишенями органических кислот являются клеточная стенка бактерий, цитоплазматическая мембрана и определенные метаболические функции (например, репликация и синтез белка) патогенных микроорганизмов, ведущие к их нарушению и гибели (Surendran Nair et al., 2017; Zhitnitsky et al., 2017). Молочная кислота, продуцируемая LAB, создает неблагоприятную локальную микросреду для патогенных бактерий (Dittoe et al., 2018). Wang C. et al. (2015) показали, что концентрация молочной кислоты 0,5% (об. / Об.) Может полностью подавлять рост патогенов, таких как Salmonella spp., E. coli или L. monocytogenes . Тем не менее эти кислоты не влияют на эпителиальные клетки животных из-за слоя слизи, который создает градиент pH (Allen and Flemström, 2005). Кормление органическими кислотами, такими как пропионовая, имеет некоторые ограничения, поскольку их диссоциация до достижения тонкой кишки (Hume et al., 1993).
Этанол, продуцируемый гетероферментативными LAB, образуется путем гликолиза (Elshaghabee et al., 2016). Этанол влияет на текучесть и целостность мембраны, что приводит к гибели бактериальных клеток из-за утечки через плазматическую мембрану (Ingram, 1989).О и Маршалл (1993) сообщили, что концентрация этанола при 5% ингибирует репликацию L. monocytogenes .
Диацетил образуется в результате поглощения цитрата и метаболизма в LAB. В частности, фунтов. plantarum, Lb. helveticus, Lb. bulgaricus, Ent. faecalis , и в основном Leuc. mesenteroides и Lc. lactis biovar diacetylactis — наиболее известные виды LAB, продуцирующие диацетил (García-Quintáns et al., 2008; Singh, 2018). Диацетил препятствует утилизации аргинина, реагируя с аргинин-связывающим белком грамотрицательных бактерий (Lindgren and Dobrogosz, 1990), в то время как углекислый газ, выделяемый LAB в ближайшем окружении, создает анаэробную среду, в которой аэробные бактерии не могут расти (Singh, 2018). .
Некоторые виды LAB способны производить перекись водорода (H 2 O 2 ) и могут подавлять патогенные бактерии, лишенные каталазы (Mitchell et al., 2015), посредством цепной реакции супероксид-аниона, усиливающей токсическое окисление. H 2 O 2 Бактерицидное действие зависит от концентраций и факторов окружающей среды, таких как pH и температура (Surendran Nair et al., 2017). Lc. lactis и Ent. faecium , как сообщалось, продуцируют H 2 O 2 с сильным антимикробным действием (Yang et al., 2012).
Реутерин — вторичный метаболит, связанный с метаболизмом глицерина фунтами. реутери. Это сильнодействующее ингибирующее соединение обладает широким спектром активности, проявляющейся независимо от pH. Известно, что реутерин ингибирует репликацию ДНК и устойчив к протеолитическим и липолитическим ферментам (Singh, 2018). Что касается спектра активности, реутерин оказался активным против E. coli , Staphylococcus aureus и Candida spp.(Helal et al., 2016).
Конкурентное исключение
Конкурентное исключение (CE) может произойти после добавления любой культуры, содержащей хотя бы одну непатогенную бактерию, в желудочно-кишечный тракт животных. Это уменьшит количество патогенных бактерий за счет прямой или косвенной конкуренции за питательные вещества и адгезии за участки в кишечнике (Callaway et al., 2008). Эти LAB-пробиотики способны образовывать биопленки и общаться через Quorum Sensing (QS) при продуцировании и высвобождении аутоиндукторов (Tannock et al., 2005). Патогены не способны прилипать к слизистой оболочке кишечника, что блокирует развитие их популяции за счет постоянного потока пищеварительного тракта (Callaway et al., 2008; Yirga, 2015; Liao, Nyachoti, 2017). Некоторые исследования, направленные на выявление этого механизма, кратко описаны ниже. Картер и др. (2017) сообщили о защитном эффекте, оказываемом комбинацией 5 × 10 7 КОЕ / мл фунтов. salivarius 59 и Ent. faecium PXN33 за счет уменьшения колонизации Salmonella Enteritidis S1400 у цыплят.Penha Filho et al. (2015) сообщили об эффекте 1 × 10 5 КОЕ фунтов. Суспензия пробиотиков на основе при уменьшении колонизации Salmonella при введении этого штамма цыплятам в возрасте от 1 до 7 дней. Arruda et al. (2016) показали, что коммерческий пробиотик Lactobacillus spp. снижение распространенности инфекции Clostridium difficile у свиней при введении в концентрации 7,5 × 10 9 КОЕ. Sha et al. (2016a) с помощью пробных анализов кормления показали, что 1 × 10 9 КОЕ / мл фунтов.pentosus HC-2 сильно подавлял рост Vibrio parahaemolyticus в кишечнике креветок.
Модуляция иммунной системы хозяина
Молочнокислые бактерии широко описаны благодаря своей способности усиливать иммунную систему животных, положительно влияя на врожденный и адаптивный иммунный ответ (Tellez et al., 2012; Tsai et al., 2012; Ashraf and Shah, 2014), помогая защищают от патогенных заболеваний (Ashraf and Shah, 2014). Врожденная иммунная система вызывает немедленную защиту от инфекции, но также активирует долговременный адаптивный иммунитет.Компоненты врожденной системы распознают молекулярные паттерны, связанные с патогенами, через рецепторы распознавания образов (PRR). Распознавание этих паттернов с помощью PRR приводит к индукции воспалительных реакций и врожденной защиты хозяина. Кроме того, обнаружение микробов с помощью PRR, экспрессируемой в антигенпрезентирующих клетках, особенно дендритных клетках (DC), приводит к активации адаптивных иммунных ответов с помощью Т- и В-клеток (Iwasaki and Medzhitov, 2015). Различные типы иммунных клеток, включая гранулоциты, макрофаги, DC и T- и B-лимфоциты, вовлечены в воспалительные реакции, которые опосредуются несколькими цитокинами, такими как TNFα, IL-1β, IL-6, IL-8 и интерлейкины IL-15.Противовоспалительные / супрессивные ответы, со своей стороны, опосредуются IL-10, IL-12 и TGFβ (Hardy et al., 2013). LAB обладают различными иммуномодулирующими свойствами, связанными с их способностью индуцировать продукцию цитокинов, влиять на иммуномодуляцию за счет врожденных или адаптивных иммунных ответов (Kiczorowska et al., 2017a). Эти способности к иммуномодуляции рассматриваются как решающий критерий оценки пробиотиков с помощью различных механизмов (Wells, 2011; Hardy et al., 2013).
Повышение врожденного иммунного ответа
Первичным механизмом врожденного иммунитета являются физические и химические барьеры, такие как кишечные эпителиальные клетки (IEC), которые предотвращают распространение патогенов и последующие инфекции (Riera Romo et al., 2016). В зависимости от наличия изменяющегося слоя слизи пробиотики могут взаимодействовать с IEC и DC (Lebeer et al., 2010). IEC являются первыми защитными барьерами (Dowarah et al., 2017), и предполагается, что они являются первыми и наиболее важными клетками-мишенями для действия пробиотиков (Lebeer et al., 2008). Было показано, что штаммы пробиотиков оказывают благотворное влияние на функцию питания кишечного эпителия (Lebeer et al., 2008). Они также улучшают барьерную функцию кишечника, стимулируя: (i) выработку антимикробной слизи и пептидов, таких как дефенсины (Yang et al., 1999; Schlee et al., 2008), (ii) усиление иммунных ответов, (iii) улучшение экспрессии и / или локализации белков плотных контактов, (iv) предотвращение апоптоза эпителиальных клеток и (v) индукция цитопротекторных молекул (Ewaschuk et al. ., 2008; Андерсон и др., 2010; Матиас и др., 2010; Мадсен, 2012). У цыплят, фунтов. plantarum LTC-113 (1 × 10 9 КОЕ) может активировать клеточные соединения, чтобы препятствовать колонизации патогенов, таких как Salmonella (Wang et al., 2018).
Кроме того, другие клеточные компоненты врожденной иммунной системы, такие как моноциты и макрофаги, предотвращают вторжение патогенов, секретируя провоспалительные цитокины и цитотоксические молекулы. Клетки Natural Killer (NK) продуцируют цитокины, такие как интерферон (IFN-γ) и различные интерлейкины (IL): IL-10, IL-3 и др. (Vivier et al., 2011). У поросят-отъемышей введение фунтов. brevis ZLB004 (2 × 10 9 КОЕ / кг корма) повышал уровень IFN-γ (Liu et al., 2015). Штаммы Lactobacilli как Lb. fermentum, фунт. salivarius, фунт. crispatus и Lb. Сообщалось, что gasseri положительно модулирует уровень секреции про и противовоспалительных интерлейкинов IL-6, IL-8 и IL-10, чтобы регулировать воспаление и восстанавливать физиологическое равновесие у животных, производящих пищу (Pérez- Cano et al., 2010; Luongo et al., 2013; Sun et al., 2013; Rizzo et al., 2015). ИЛ-8 представляет собой провоспалительный цитокин, который напрямую привлекает макрофаги и лейкоциты в воспалительные области посредством химиочувствительности (Riera Romo et al., 2016). A фунтов. acidophilus стимулировал противовоспалительные свойства у поросят, инфицированных энтеротоксигенными E. coli (ETEC), при введении в корм 1 × 10 8 КОЕ. Этот штамм также был способен подавлять провоспалительные цитокины IL-8 и TNF-α in vivo на основании экспериментов на животных (Li et al., 2016). Такая же тенденция в уровнях IL-8 наблюдалась и у карпа, инфицированного Aeromonas hydrophila ( Cyprinus carpio Huanghe var.) при кормлении 1 × 10 7 КОЕ г / л фунтов. delbrueckii (Zhang et al., 2017). И наоборот, комбинация из Lc в количестве 1 × 10 7 КОЕ на г гранулы корма. lactis BFE920 и фунтов. plantarum FGL0001 индуцировал повышение уровня IL-8 и IL-6 у японской камбалы, инфицированной Streptococcus iniae (Beck et al., 2015). Уолтер (2008) и Брисбин и др. (2011) подтверждают, что расхождения в эффектах иммуномодуляции были приписаны выбранным штаммам Lactobacillus , их дозировкам, а также условиям содержания животных.Zhang et al. (2017) установили, что Lb. delbrueckii при 1 × 10 7 КОЕ г / л повышали уровни противовоспалительных цитокинов IL-10 и TGF-β в кишечнике и повышали иммунитет A. hydrophila- , инфицированных Cyprinus carpio Huanghe var.
Повышение адаптивного иммунного ответа
Адаптивный иммунный ответ зависит от В- и Т-лимфоцитов, которые вызывают антиген-специфический ответ. Ассоциация Lb. plantarum (1 × 10 7 КОЕ / кг корма) и Clostridium butyricum (1 × 10 6 КОЕ / кг корма) на продуктивность и иммунную функцию у бройлеров выявили повышение уровней IgG и IgA в цыплята, которых кормили этими полезными пробиотиками (Han et al., 2018). По прямой линии, фунтов. plantarum B2984, как было показано, стимулирует выработку иммуноглобулинов (IgM и IgA) против инфекции Salmonella у свиней во время испытаний на животных с пероральным введением (Naqid et al., 2015). Кормление поросят штаммом Lb. rhamnosus ATCC 7469, в концентрации 10 9 КОЕ / мл, предотвращал острую инфекционную диарею путем стимуляции адаптивной иммунной системы, что впоследствии приводило к увеличению концентрации собственной пластинки CD3 + CD4 + CD8 — Т-клетки (Zhu et al., 2014). Для цыплят добавка к корму с 1 × 10 9 КОЕ / кг фунтов. acidophilus LA5 увеличивал продукцию CD4 + , CD8 + и TCR1 + Т-клеток в желудочно-кишечном тракте, но также и в периферической крови (Asgari et al., 2016). Введение 10 10 КОЕ / мл Lactobacillus spp. может эффективно активировать иммунитет слизистой оболочки цыплят за счет повышения уровней IgA и IgG (Rocha et al., 2012). Молодым телятам введение 1.85 × 10 7 КОЕ / л видов Lactobacillus , как было показано, улучшают набор веса и иммунокомпетентность (Al-Saiady, 2010). Таким образом, сообщалось, что LAB улучшают резистентность хозяина и продуктивность, как описано в разделе «Производственные характеристики», за счет усиления иммунного ответа (Kiczorowska et al., 2017a).
Улучшение усвояемости питательных веществ и конверсии корма
Усвояемость корма отражает количество поглощенного корма и доступность питательных веществ, используемых для роста и воспроизводства животных (ILCA, 1990).Можно измерить кажущуюся или реальную перевариваемость путем сравнения питательных веществ, содержащихся в фекалиях, с питательными веществами, содержащимися в рационе, или добавлением внешних маркеров (таких как диоксид титана, оксид хрома и редкоземельные элементы) в корм (ILCA, 1990; Safwat et al., 2015). Улучшение усвояемости питательных веществ измеряется косвенным методом: коэффициент конверсии корма, корреляция между весом корма, вводимого в течение всей жизни животного, и прибавленным весом, который является ценным показателем эффективности систем кормления (Wenk et al., 1980; Fry et al., 2018). LAB-пробиотики улучшают усвояемость питательных веществ из-за их высокой ферментативной активности. Действительно, они могут улучшить весь процесс пищеварения, метаболическое использование питательных веществ и повысить эффективность корма за счет производства пищеварительных ферментов (например, амилазы, хитиназы, липазы, фитазы, протеазы) или просто путем выработки летучих жирных кислот и витаминов группы B. рибофлавин, биотин, витамин B12 (Russo et al., 2014; Liao, Nyachoti, 2017; Sharifuzzaman, Austin, 2017).Кроме того, LAB-пробиотики могут косвенно модифицировать микросистему кишечника (FAO, 2016), помогая усвоению питательных веществ за счет активации иммунных клеток хозяина и увеличения количества антител, что приводит к улучшению благополучия животных (Forte et al., 2016) .
Снижение биодоступности токсина
Защитные эффекты LAB-пробиотиков могут приводить к подавлению экспрессии токсина в патогенах (Liao and Nyachoti, 2017). Также сообщалось, что LAB могут представлять собой естественные барьеры против микотоксинов, которые считаются потенциально опасными для животных соединениями (Tsai et al., 2012; Peng et al., 2018). Несколько исследователей сообщили, что Lb. plantarum, Lb. acidophilus, Lb. paracasei и Ent. faecium может смягчить эффект афлатоксинов для улучшения здоровья человека и животных (Gratz et al., 2007; Ahlberg et al., 2015; Abbès et al., 2016; Damayanti et al., 2017; Li et al., 2017) .
Молочнокислые бактерии действуют как биологический барьер в кишечном тракте, уменьшая доступность микотоксинов и нейтрализуя их побочные эффекты.Детоксифицирующие способности LAB связаны с их способностью связывать и изолировать микотоксины, повышая их выведение пищеварительной системой с фекалиями (Zoghi et al., 2014; Damayanti et al., 2017; Li et al., 2017). Микотоксины могут связываться с жизнеспособной и нежизнеспособной бактериальной поверхностью за счет адгезии к компонентам их клеточной стенки (Damayanti et al., 2017; Li et al., 2017), а афлатоксин B1 (AFB1), например, был связан с LAB не -ковалентные взаимодействия (Haskard et al., 2001). Испытания, направленные на борьбу с микотоксинами, были проведены с фунтами.casei DSM20011, фунтов. casei Shirota (Liew et al., 2018), Lb. rhamnosus штаммы LGG и LC 705 (El-Nezami et al., 1998, 2002; Nybom et al., 2007), Lb. acidophilus 24 (Pizzolitto et al., 2012) и Lb. plantarum Lb. brevis , фунтов. sanfranciscensis , из коллекции LOCK (Piotrowska, 2014). Пиотровска (2014) предположила, что связывание с микотоксинами, в частности с охратоксином, приписывается гидрофобным свойствам клеточной стенки, а также взаимодействиям донорно-акцепторных электронов и кислотно-основным взаимодействиям Льюиса.У LAB есть дополнительные механизмы антимикотоксина, основанные на исследовании, проведенном на мышах, в рацион которых добавляли фунтов. plantarum C88 (1 × 10 10 КОЕ / мл). Эта добавка ослабляла окислительный стресс, вызванный афлатоксином AFB1. Точно так же этот штамм уменьшал перекисное окисление липидов в сыворотке и печени из-за повреждения печени, вызванного токсичностью AFB1 (Li et al., 2017). LAB продуцируют экзополисахариды, которые являются важными соединениями, способными ингибировать бактериальные токсины, как сообщалось Ruas-Madiedo et al.(2010) для взаимодействий между Lb. rhamnosus GG против Bacillus cereus. О других механизмах, включая снижение pH и блокировку QS, сообщалось во время сосуществования C. perfringens типа A и LAB, в частности Lb. acidophilus CGMCC 11878 и Lb. fermentum CGMCC12029 (Guo et al., 2017).
Преимущества для животных и пищевой цепи
В дополнение к перечисленным выше положительным эффектам, приписываемым LAB, потенциально используемым в качестве пробиотиков, мы отметили дальнейшее положительное влияние на здоровье различных сельскохозяйственных животных и качество продуктов животноводства.Эти эффекты зависят от животных и включают увеличение массы тела, улучшение баланса кишечных микробов, улучшение репродуктивной функции и повышение общей продуктивности (рис. 2).

Рисунок 2. Благоприятные эффекты от введения пробиотиков LAB.
Ведение болезней
Различные исследователи сообщили о потенциальном эффекте LAB для снижения риска инфекций и кишечных расстройств, связанных с патогенами, такими как Salmonella spp., E. coli, Campylobacter или Clostridium spp. LAB-пробиотики использовались в профилактических и терапевтических целях для лечения инфекций, вызываемых этими патогенами (Tellez et al., 2012; Layton et al., 2013; O’Bryan et al., 2014; Gómez et al., 2016; Park et al., 2016).
Птица
Множество исследований было посвящено LAB, используемым в птицеводстве. Действительно, Ван и др. (2018) инокулировали вылупившихся цыплят 1 × 10 9 КОЕ Lb. plantarum LTC-113, который обеспечивал защиту против Salmonella Typhimurium, ограничивая колонизацию кишечника и стабилизируя экспрессию генов плотных контактов в эпителиальных клетках кишечника среди обработанных цыплят, делая их более устойчивыми к инфекции.Как упоминалось ранее, ХЭ является эффективным механизмом защиты только что вылупившихся птиц от колонизации энтеропатогенными микроорганизмами домашней птицы (Kabir, 2009). Аналогичным образом Olnood et al. (2015) показали, что 5 × 10 8 КОЕ из фунтов. johnsonii уменьшил количество Salmonella enterica серовара Sofia и C. perfringens у зараженных однодневных бройлеров Cobb (Olnood et al., 2015). В другом исследовании сообщалось, что введение 1 × 10 9 КОЕ (50:50) Lb. salivarius 59 и Ent.faecium PXN33 в сочетании снижали уровни колонизации у птиц на Salmonella (Carter et al., 2017). С другой стороны, штаммы C. perfringens ответственны за продукцию токсинов и / или ферментов некротического энтерита. Колонизация слизистой оболочки домашней птицы C. perfringens происходит в молодом возрасте птиц (M’Sadeq et al., 2015). Несколько Lactobacillus ( Lb. acidophilus, Lb. fermentum, Lb. plantarum, Lb. reuteri и Lb.salivarius ) и штаммы Enterococcus ( Ent. faecium и Ent. faecalis ) могут ингибировать C. perfringens in vitro (Caly et al., 2015). Введение определенных штаммов LAB не приносит систематической пользы домашней птице, как это было подтверждено для Lb. plantarum PCS 20 против Campylobacter jejuni (Santini et al., 2010), или Lb. johnsonii FI9785 против Salmonella Enteritidis (La Ragione et al., 2004). Следовательно, скрининг должен проводиться в определенных условиях, а результаты строго зависят от деформации.
Молочнокислые бактерии-бактериоцины улучшают показатели роста цыплят, пораженных C. perfringens , что позволяет восстанавливать вес на уровне, аналогичном здоровым птицам. Например, этот эффект наблюдался, когда цыплят, зараженных C. perfringens , лечили педиоцином A из Ped. pentosaceus (Grilli et al., 2009), или когда E.coli инфицированных цыплят получали плантарицин из фунтов. plantarum F1 (Ben Lagha et al., 2017). Примечательно, что бактериоцин против C. perfringens divercin, продуцируемый Carnobacterium divergens AS7, улучшал показатели роста и благополучие обработанных цыплят (Józefiak et al., 2012).
Свинья
Многочисленные преимущества были описаны у свиней при введении LAB, в частности, лактобацилл (Yang F. et al., 2015; Valeriano et al., 2016; Dowarah et al., 2017). У свиней самый высокий уровень смертности связан с диареей, вызванной ETEC и Salmonella (Liao and Nyachoti, 2017). Кормовая добавка с различными видами Lactobacillus , включая Lb. johnsonii, Lb. mucosae и Lb. plantarum улучшил микробный профиль кишечника и продукцию микробных метаболитов, что привело к улучшению здоровья кишечника и уменьшило колонизацию патогенными микроорганизмами слизистой оболочки кишечника (Dowarah et al., 2017). Впоследствии эти исследователи показали, что поросята-отъемыши, обработанные 2 × 10 9 КОЕ / г Ped.acidilactici FT28, а не Lb. acidophilus NCDC-15 привело к снижению диареи из-за изменений в питании и окружающей среде (Dowarah et al., 2018). Снижение количества ЕТЕС наблюдалось при использовании ферментированного корма от производителя реутерана Lb. reuteri LTH5794 в концентрации 1 × 10 7 КОЕ / г вводили свиньям-отъемышам. Исследуемый штамм был способен продуцировать экзополисахариды, такие как реутеран или леван, препятствующие адгезии ETEC к слизистой оболочке (Yang Y.и др., 2015). Однако исследование Andersen et al. (2017) показали, что у новорожденных поросят, получавших коммерчески доступный пробиотик Lb. paracasei F19 (2,6 × 10 8 КОЕ / кг) и недавно охарактеризованный штамм Ped. pentosaceus (1,3 × 10 10 КОЕ / кг), разработанный для подавления E. coli F18-индуцирующей диареи (Andersen et al., 2017).
Streptococcus suis вызывает широкий спектр инфекций у свиней, таких как менингит, артрит, эндокардит, пневмония и сепсис (Ben Lagha et al., 2017). Сообщается, что эта бактерия чувствительна к низину, хорошо известному и единственному бактериоцину, продаваемому в настоящее время (Lebel et al., 2013).
Жвачные
Введение LAB может предотвратить развитие ацидоза рубца путем создания оптимальных условий для бактерий, потребляющих молочную кислоту, таких как Megasphaera elsdenii или Propionibacterium spp. (Чаучейрас-Дюран и Дюран, 2010). Добавление фунтов. acidophilus, Lb. salivarius и Lb.plantarum в концентрациях 10 7 –10 8 КОЕ / г снижал частоту диареи у молодых телят (Signorini et al., 2012). LAB виды, включая Lb. paracasei и Lb. plantarum , а выделенные из меда, такие как Lb. kunkeei, Lb. apinorum, Lb. mellis, Lb. mellifer, фунт. apis имел in vitro, активностей против возбудителей мастита, таких как Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus uberis или E.coli (Piccart et al., 2016; Diepers et al., 2017). LAB-пробиотики также успешно использовались для облегчения симптомов таких заболеваний, как кокцидиоз, важное паразитарное заболевание молодняка жвачных животных, вызываемое Eimeria . Эти LAB-пробиотики минимизировали воздействие этого заболевания за счет снижения риска распространения этого паразита (Giannenas et al., 2012). С другой стороны, Cao et al. (2007) сообщили об эффективности внутримолочной инфузии низина для лечения мастита, вызванного Staphylococcus aureus у дойных коров.
Аквакультура
В аквакультуре, фунтов. штаммов, таких как Lb. murinus или Lb. pentosus проявлял антагонизм против V. harveyi и V. parahaemolyticus . Другие потенциальные LAB-пробиотики, такие как Ent. faecium NRW-2 (1 × 10 7 КОЕ / г корма), как сообщается, был активен против Vibrio spp. штаммы из-за их очень высокой способности к адгезии и конкуренции за питательные вещества. Сообщалось, что эти бактерии уменьшают присутствие Vibrio в креветках (Sha et al., 2016б). Рыбу кормят фунтами. delbrueckii стал более устойчивым к инфекциям Aeromonas . Было предложено, чтобы 1 × 10 6 КОЕ / г из фунтов. delbrueckii было связано с их стимулирующими свойствами иммунной системы кишечника личинок креветок (Zhang et al., 2017). Araújo et al. (2016) выделили несколько штаммов Ped. acidilactici из корма радужной форели ( Oncorhynchus mykiss ) и личинок. Некоторые из этих штаммов обладают широким спектром действия и проявляют антагонистическую активность против нескольких патогенов рыб, включая Lc.garvieae, Streptococcus iniae, Carnobacterium maltaromaticum и A. salmonicida .
Nisin Z-production Lc. lactis WFLU12 обеспечивает защиту от инфекций, вызываемых Streptococcus parauberis , у оливковой камбалы (Nguyen et al., 2017). В то время как Lb. pentosus 39 продуцирует бактериоцин, активный против патогена рыб A. hydrophila , что позволяет предположить, что этот LAB может использоваться в качестве природного биоконсерванта (Anacarso et al., 2014).
LAB-пробиотики в лечении вирусных инфекций
Молочнокислые бактерии-пробиотики были описаны как эффективные организмы для лечения вирусных инфекций (Al kassaa et al., 2014; Arena et al., 2018a, b). Лейва-Мадригал и др. (2011) сообщили о возможностях Ped. pentosaceus и Staphylococcus haemolyticus (1 × 10 6 КОЕ / г корма) для лечения вируса синдрома белых пятен (WSSV) у белых креветок ( Litopenaeus vannamei ). Модифицированный Lb.plantarum придает устойчивость креветок к вирусу желтой головы (Thammasorn et al., 2017). У поросят фунтов. plantarum N4 показал свою активность в отношении трансмиссивного вируса гастроэнтерита при профилактическом применении (Yang Y. et al., 2017) и Lb. plantarum 25F, снижает вирусную инфекционность вируса эпидемической диареи свиней (PEDV) (Sirichokchatchawan et al., 2018). Эффекты Lb. casei CMPUJ 415 и B. adolescentis DSM 20083 на ротавирусе было продемонстрировано снижение продукции вирусного белка энтеротоксина (NSP4) (Olaya Galán et al., 2016). Roselli et al. (2017) перечислили многочисленные примеры LAB-пробиотиков с противовирусной активностью, такие как Lb. casei MEP221106 или MEP221114, фунтов. rhamnosus CRL1505. Тем не менее, Sachsenrödder et al. (2014) выдвинули гипотезу о применении пробиотиков как Ent. faecium NCIMB10415 не влияет на вирусный состав, присутствующий в кишечнике свиней. По этой причине несколько исследований сосредоточены на получении рекомбинантных LAB для вакцинации, как в случае рекомбинантного Lb.casei ATCC 393 против PEDV (Wang X. et al., 2017) или Lb. plantarum NC8 против вируса птичьего гриппа H9N2 (Yang W. et al., 2017), усиливая иммунную систему, представляющую антигены.
Производительность
Lactobacilli продуцируют молочную кислоту и протеолитические ферменты, которые улучшают переваривание питательных веществ в ЖКТ, и добавление к корму штаммов Lactobacillus может вызывать увеличение веса у сельскохозяйственных животных (Angelakis, 2017) в зависимости от штамма (Drissi et al., 2017). Например, Lb. delbrueckii, Lb. acidophilus, Lb. casei, фунт. agilis, Lb. salivarius , Lb. fermentum и Lb. ingluviei были описаны как усилители веса (Drissi et al., 2017). Последние два вида ассоциировались со значительным эффектом набора веса у уток и цыплят (Million et al., 2012; Drissi et al., 2017). LAB-пробиотики улучшили эффективность преобразования корма, изменив микробиоту кишечника, ограничив рост патогенов, способствуя развитию непатогенных бактерий и улучшив использование питательных веществ и пищеварение (Yang Y.и др., 2015). Некоторые LAB-пробиотики обеспечивали те же преимущества, что и антибиотики, с точки зрения увеличения веса, потребления корма и эффективности корма, как в случае Lb. plantarum P-8 (2 × 10 6 КОЕ / мл) (Wang L. et al., 2015).
Baldwin et al. (2018) показали, что консорциум LAB-пробиотиков, содержащий Lb. ingluviei, Lb. agilis и Lb. reuteri улучшили прибавку в весе, когда они были инокулированы на ранней стадии инкубатория, изменив кишечную микробиоту и уменьшив количество патогенных таксонов у цыплят (Baldwin et al., 2018). С другой стороны, добавка к корму с 1 × 10 6 КОЕ / г корма фунтов. johnsonii BS15 у бройлеров улучшает пищеварение, способствует росту и снижению содержания жира в организме (Wang H. et al., 2017).
Еще одно исследование было проведено на свиньях, получавших фунтов. plantarum ATCC 4336, фунт. fermentum DSM 20016 и Ent. faecium ATCC 19434 в концентрациях 10 11 КОЕ / кг приводил к увеличению веса из-за способности этих штаммов, в основном Lb. единиц, чтобы производить ферменты, улучшающие переваривание кормов, помимо производства молочной кислоты (Veizaj-Delia et al., 2010). Lan et al. (2016) показали, что штамм Lb. acidophilus увеличил усвояемость у поросят-отъемышей в возрасте 14 дней и улучшил их показатели роста.
Однако добавление в корм LAB-пробиотиков не оказывало никакого влияния на вес животных во всех случаях. Wang et al. (2012) показали, что ферментированный кукурузный корм Lactobacillus или Pediococcus может изменять микробиоту, но не влияет на продуктивность свиней.Эта вариабельность связана с неоднородностью исследований. Тем не менее, для свиней такие факторы окружающей среды, как загон, подстилка… свиноматка и поросенок тесно связаны между собой, согласно Zimmermann et al. (2016).
Что касается жвачных животных, телят, которых кормили смесью 1 × 10 9 КОЕ фунтов. casei DSPV 318T, фунтов. salivarius DSPV 315T и Ped. acidilactici DSPV 006T продемонстрировал более высокий дневной привес, общее потребление корма и потребление стартового рациона (Frizzo et al., 2010). Кроме того, телятам давали 6,8 × 10 8 КОЕ фунтов. acidophilus и Lb. plantarum обогащенное молоко (Gupta et al., 2015) или 1 × 10 10 КОЕ из фунтов. plantarum DSPV 354T (Soto et al., 2014) потребляли больше молока, помимо увеличения массы тела и показателей роста. Подобный эффект был зарегистрирован для ягнят после отъема. Когда их кормили педиококками (1 × 10 6 КОЕ / г), было показано повышенное потребление сухого вещества корма и лучшие показатели роста (Saleem et al., 2017).
В секторе аквакультуры Zheng et al. (2017) показали увеличение размера белых креветок ( Litopenaeus vannamei ), когда их рацион был дополнен 1 × 10 9 КОЕ / мл фунтов. plantarum. Кроме того, Lb. delbrueckii также повысил продуктивность Cyprinus carpio Huanghe var. при добавлении в корм в концентрации 10 6–7 КОЕ / г (Zhang et al., 2017). У морских ушек ( Haliotis Discus hannai Ino) потребление корма и увеличение роста наблюдались, когда Lb.pentosus поставлялся в концентрации 10 3–5 КОЕ / г (Gao et al., 2018).
Повышение качества продукции животноводства
Существует несколько примеров Lactobacillus spp. как пробиотик, улучшающий качество мяса цыплят, включая нежность, внешний вид, текстуру и сочность среди других параметров (Park et al., 2016). Известно, что добавление ЛАБ к корму бройлеров снижало содержание холестерина в мясе (Попова, 2017). Администрация Lb.salivarius SMXD51, в концентрации 10 7 КОЕ / мл, может частично предотвращать воздействие Campylobacter на цыплят из-за способности этого штамма продуцировать бактериоцин против Campylobacter с высокой активностью против четырех протестированных кампилобактерий jejuni (Messaoudi et al., 2012; Saint-Cyr et al., 2017). Кроме того, пробиотики могут улучшить производство и качество яиц. Таким образом, добавка Ped. acidilactici MA 18 / 5M (10 8 КОЕ / кг корма) в корме для кур выявило влияние на качество яиц за счет увеличения их веса, толщины яичной скорлупы и снижения уровня холестерина в яичном желтке (Mikulski et al., 2012).
У свиней, Пед. acidilactici улучшает качество мяса (Dowarah et al., 2018). Kiczorowska et al. (2017b) сравнили четыре группы коров и продемонстрировали, что коровы в условиях интенсивной производственной системы получали лечение пробиотиками [ Lb. casei , Lb. plantarum (5 × 10 6 КОЕ / мл)] и S. cerevisiae (5 × 10 3 КОЕ / мл) давали молоко более высокого качества с более высоким содержанием белка и жира, которые содержали большее количество ненасыщенных жиров. кислоты, наоборот, коровы в системе интенсивного производства.Было показано, что добавление в корм 4 × 10 9 КОЕ Lb. acidophilus NP51 и Propionibacterium freudenreichii NP24 увеличивают производство молока и улучшают очевидную усвояемость пищевых питательных веществ (Boyd et al., 2011).
Размножение рыб
Пробиотики связаны с воспроизводством рыб за счет повышения их плодовитости (Banerjee and Ray, 2017; Carnevali et al., 2017). Сообщается, что прямые эффекты обусловлены увеличением экспрессии генов, кодирующих несколько гормонов, и усилением роста гонад, плодовитости и выживаемости эмбрионов (Gioacchini et al., 2010, 2012). Пробиотики также улучшают созревание и развитие фолликулов, а также качество эмбриона. Например, несколько штаммов Lb. rhamnosus может улучшить плодовитость рыбок данио ( Danio rerio) модели (Hai, 2015; Banerjee and Ray, 2017).
Качество воды
Качество воды на рыбоводческих фермах, несомненно, является важным фактором предотвращения распространения болезней. Параметры для измерения этого качества основаны на pH воды и количествах CO 2 , аммиака, нитратов и фосфора, содержащихся в ней. фунтов plantarum и Lb. casei , как сообщается, поддерживал или улучшал качество воды в процессе производства рыбы (Banerjee and Ray, 2017).
Основная проблема связана с загрязнением воды тяжелыми металлами, вызывающими болезни рыб. Этого можно избежать, используя некоторые LAB-пробиотики, такие как Lb. plantarum CCFM639, который восстанавливает целостность поврежденных белков плотных контактов и поддерживает кишечную проницаемость, что приводит к снижению вызванных алюминием повреждений кишечника (Yu et al., 2016). Yu et al. (2017) также сообщили о снижении накопления алюминия в тканях тилапии и более низкой смертности при включении 10 8 КОЕ / г фунтов. plantarum в корм.
Синбиотики
Синбиотики определяются как комбинация пробиотиков и пребиотиков, которые благотворно влияют на хозяина, улучшая выживаемость и оседание живых микробных пищевых добавок в желудочно-кишечном тракте. Это происходит за счет выборочной стимуляции роста и / или активации метаболизма одной или ограниченного числа полезных для здоровья бактерий и, таким образом, улучшения благополучия хозяина (Gibson et al., 2004). Пребиотик, который приносит пользу здоровью желудочно-кишечного тракта, может поддерживать рост пробиотика, который обладает активностью против потенциального патогена (Allen et al., 2013).
Guerra-Ordaz et al. (2014) сообщили о синергетическом эффекте, когда Lb. plantarum (2 × 10 10 КОЕ) и лактулозу (10 г / кг корма) одновременно использовали для лечения колибактериоза у свиней, уменьшения диареи и улучшения среднесуточного привеса. Ясуда и др. (2007) показали, что фунтов.casei subsp. casei (1 × 10 7 КОЕ / кг корма) и декстран (5%, мас. / Мас.) В комбинации улучшили надой и компоненты молока у коров, и они предполагают, что симбиотическая ассоциация имела профилактический эффект, ингибируя развитие мастита. . Данные Naqid et al. (2015) предложили соблюдать осторожность при использовании синбиотиков, поскольку внутри комбинации может происходить внутривзаимодействие и снижать ожидаемую активность. Mookiah et al. (2014) показали такое же увеличение массы тела у цыплят, получавших мультиштамм Lactobacillus пробиотиком в дозе 1 × 10 9 КОЕ / г или пребиотиком (изомальтоолигосахариды; 5 или 10 г / кг корма) по отдельности или их объединение в виде синбиотик.Szczurek et al. (2018) показали, что синбиотик, состоящий из сывороточной лактозы и Lb. agilis не показал никаких преимуществ по сравнению с каждым соединением в отдельности.
В рыбной администрации Ent. faecalis и маннан-олигосахариды усиливали рост, иммунный ответ и выживаемость радужной форели ( Oncorhynchus mykiss ) при заражении A. salmonicida (Rodriguez-Estrada et al., 2013). В тилапии наблюдается эффект против A. hydrophila , когда комбинация 1 × 10 8 КОЕ Lb.brevis JCM 1170 или фунтов. plantarum JCM 1149 и фруктоолигосахариды (1 г / кг корма) были добавлены в корм, но та же комбинация не улучшила рост животных или конверсию корма (Liu et al., 2017).
Заключение и будущий дизайн лабораторных пробиотиков
В этом обзоре выявлены многочисленные преимущества LAB-пробиотиков, используемых в животноводстве и производстве. После неизбирательного использования антибиотиков в животноводстве для повышения продуктивности животных устойчивость к этим молекулам резко возросла.Чтобы уменьшить эту обеспокоенность во всем мире, использование пробиотиков LAB является эффективной и многообещающей альтернативой. Различные преимущества наблюдались у животных, которых кормили различными LAB-пробиотиками. Согласно многочисленным исследованиям, LAB-пробиотики могут контролировать развитие бактериальных заболеваний, увеличивать прибавку в весе у здоровых и пораженных животных, стимулировать качество (побочных) продуктов этой отрасли или даже улучшать качество воды для аквакультуры. LAB-пробиотики могут контролировать бактериальные инфекции путем выделения ингибирующих соединений или с помощью других механизмов, включая конкурентное исключение, снижение биодоступности токсинов, укрепление кишечного барьера или положительную стимуляцию иммунной системы.Их действия проявляются напряженно и специфично для хозяина. Наконец, существует множество синергетических эффектов при сочетании LAB с другими видами пробиотиков, пребиотиками или ферментами. С точки зрения будущего дизайна рекомбинантные LAB-пробиотики могут иметь дополнительные преимущества. Новаторские исследования уже открыли этот путь. Действительно, сообщалось, что Lb. plantarum NC8 может продуцировать рекомбинантный пептид, нацеленный на дендритные клетки, с активностью против вируса птичьего гриппа H9N2 у кур (Shi et al., 2016; Wang X. et al., 2017). Кроме того, этот рекомбинантный пептид, нацеленный на дендритные клетки, можно синергетически использовать для усиления гуморального иммунного ответа вакцины и для уменьшения репликации вируса в легких курицы (Shi et al., 2016).
Заявление об этике
Все авторы этой статьи прочитали и одобрили представленную окончательную версию. Содержание этой рукописи ранее не защищалось авторским правом и не публиковалось. Никакие процедуры, выполняемые в этих исследованиях, не проводились на людях и / или животных.
Авторские взносы
Все перечисленные авторы внесли существенный, прямой и интеллектуальный вклад в работу и одобрили ее к публикации.
Финансирование
NV-S получил докторскую степень ANRT. грант финансируется подразделением Phileo Business Unit от Lesaffre International. Эта работа была частично поддержана грантом Sincolistin ANR, координируемым DD (ANR-15-CE21-0015).
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Редактор обработки заявил о прошлом соавторстве с одним из авторов DD.
Благодарности
Авторы признательны доктору Брюсу Силу (Каскады Университета штата Орегон) за его постоянное восторженное критическое прочтение рукописи и улучшение английского языка.
Список литературы
Аббес, С., Бен Салах-Аббес, Дж., Джебали, Р., Юнес, Б. Р., и Уэслати, Р. (2016). Взаимодействие афлатоксина B1 и фумонизина B1 у мышей вызывает иммунотоксичность и окислительный стресс: возможная защитная роль при использовании молочнокислых бактерий. J. Immunotoxicol. 13, 46–54. DOI: 10.3109 / 1547691X.2014.997905
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Агилар-Перес, К., Грасиа, Б., Родригес, Л., Витория, А., Себриан, Р., Дебузер, Н. и др. (2018). Синергизм циркулярного бактериоцина AS-48 и этамбутола против Mycobacterium tuberculosis . Антимикробный. Агенты Chemother. 62: e00359-18. DOI: 10.1128 / AAC.00359-18
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Альберг, С.Х., Йоутсйоки В., Корхонен Х. Дж. (2015). Потенциал молочнокислых бактерий в снижении риска афлатоксина. внутр. J. Food Microbiol. 207, 87–102. DOI: 10.1016 / j.ijfoodmicro.2015.04.042
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Аль-Атья, А. К., Белгуэсмия, Ю., Чатень, Г., Раваллек, Р., Ваше, А., Шунериц, С., и др. (2016). Активность энтероцинов DD28 и DD93 против MRSA и данные об их роли в ингибировании образования биопленок. Фронт. Microbiol. 7: 817. DOI: 10.3389 / fmicb.2016.00817
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Аль-кассаа, И., Хобер, Д., Чихиб, Н., и Драйдер, Д. (2014). Противовирусный потенциал молочнокислых бактерий и их бактериоцинов. Probiotics Antimicrob. Белки 6, 177–185. DOI: 10.1007 / s12602-014-9162-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Аллен А. и Флемстрем Г. (2005). Бикарбонатный барьер гастродуоденальной слизи: защита от кислоты и пепсина. Am. J. Physiol. Cell Physiol. 288, C1 – C19. DOI: 10.1152 / ajpcell.00102.2004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Аллен, Х. К., Левин, У. Ю., Лоофт, Т., Бандрик, М., и Кейси, Т. А. (2013). Лечение, продвижение, беспокойство: альтернативы антибиотикам у сельскохозяйственных животных. Trends Microbiol. 21, 114–119. DOI: 10.1016 / j.tim.2012.11.001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Аллуи, М.Н., Щурек В., Святкевич С. (2013). Польза пребиотиков и пробиотиков в современном питании птицы: обзор. Ann. Anim. Sci. 13, 17–32. DOI: 10.2478 / v10220-012-0055-x
CrossRef Полный текст | Google Scholar
Ас-Сайади, М. Ю. (2010). Влияние пробиотических бактерий на концентрацию иммуноглобулина G и другие компоненты крови новорожденных телят. J. Anim. Вет. Sci. 9, 604–609. DOI: 10.3923 / javaa.2010.604.609
CrossRef Полный текст | Google Scholar
Анакарсо, И., Месси, П., Кондо, К., Исеппи, Р., Бонди, М., Сабиа, К. и др. (2014). Бактериоциноподобное вещество, продуцируемое из Lactobacillus pentosus 39, является естественным антагонистом для борьбы с Aeromonas hydrophila и Listeria monocytogenes в свежем филе лосося. LWT — Пищевая наука. Technol. 55, 604–611. DOI: 10.1016 / j.lwt.2013.10.012
CrossRef Полный текст | Google Scholar
Андерсен, А.Д., Силиборг, М.С., Лауридсен, К., Моркбак, А.Л., Сангильд П. Т. (2017). Добавление Lactobacillus paracasei или Pediococcus pentosaceus не предотвращает диарею у новорожденных свиней, инфицированных Escherichia coli F18. Br. J. Nutr. 118, 109–120. DOI: 10.1017 / S000711451700160X
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Андерсон, Р. К., Куксон, А. Л., Макнабб, В. К., Парк, З., Макканн, М. Дж., Келли, В. Дж. И др. (2010). Lactobacillus plantarum MB452 усиливает функцию кишечного барьера за счет увеличения уровней экспрессии генов, участвующих в образовании плотных контактов. BMC Microbiol. 10: 316. DOI: 10.1186 / 1471-2180-10-316
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Аракава, К., Йошида, С., Айкава, Х., Хано, К., Болорма, Т., Буренджаргал, С., и др. (2016). Продукция бактериоцин-подобного ингибирующего вещества Leuconostoc mesenteroides subsp. dextranicum 213M0 выделено из ферментированного кобыльего молока в Монголии, айраг. Аним. Sci. J. 87, 449–456. DOI: 10.1111 / asj.12445
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Араужо, К., Muñoz-Atienza, E., Poeta, P., Igrejas, G., Hernández, P.E., Herranz, C., et al. (2016). Характеристика штаммов Pediococcus acidilactici , выделенных из корма и личинок радужной форели ( Oncorhynchus mykiss ): безопасность, ДНК-отпечатки пальцев и бактериоциногенность. Dis. Акват. Орган. 119, 129–143. DOI: 10.3354 / dao02992
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Arena, M. P., Capozzi, V., Russo, P., Drider, D., Spano, G., и Фиокко, Д. (2018a). Иммунобиоз и пробиоз: антимикробная активность молочнокислых бактерий с акцентом на их противовирусные и противогрибковые свойства. Заявл. Microbiol. Biotechnol. 102, 9949–9958. DOI: 10.1007 / s00253-018-9403-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Arena, M. P., Elmastour, F., Sane, F., Drider, D., Fiocco, D., Spano, G., et al. (2018b). Ингибирование вируса Коксаки В4 с помощью Lactobacillus plantarum . Microbiol.Res. 210, 59–64. DOI: 10.1016 / j.micres.2018.03.008
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Арруда, П. Х., Мэдсон, Д. М., Рамирес, А., Роу, Э. У., и Сонгер, Дж. Г. (2016). Бактериальные пробиотики как средство борьбы с заболеванием Clostridium difficile у неонатальных свиней. Банка. Вет. J. 57, 183–188.
Google Scholar
Асгари Ф., Маджд З., Фалак Р., Бахар М. А., Насрабади М. Х., Райани М. и др.(2016). Кормление пробиотиками влияет на популяции Т-лимфоцитов в крови и лимфоидных органах кур. Benef. Микробы 7, 669–675. DOI: 10.3920 / BM2016.0014
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Болдуин, С., Хьюз, Р. Дж., Хао Ван, Т. Т., Мур, Р. Дж., И Стэнли, Д. (2018). Введение пробиотика цыплятам при выводе может привести к положительным изменениям в микробиоте кишечника. PLoS One 13: e0194825. DOI: 10.1371 / journal.pone.0194825
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Банерджи, Г., и Рэй А.К. (2017). Развитие исследований пробиотиков и их применение в рыбоводстве. Res. Вет. Sci. 115, 66–77. DOI: 10.1016 / j.rvsc.2017.01.016
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бек, Б. Р., Ким, Д., Чон, Дж., Ли, С. М., Ким, Х. К., Ким, О. Дж. И др. (2015). Влияние комбинированных диетических пробиотиков Lactococcus lactis BFE920 и Lactobacillus plantarum FGL0001 на врожденный иммунитет и устойчивость к болезням камбалы оливковой ( Paralichthys olivaceus ). Fish Shellfish Immunol. 42, 177–183. DOI: 10.1016 / j.fsi.2014.10.035
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Belguesmia, Y., Choiset, Y., Prevost, H., Dalgalarrondo, M., Chobert, J., and Drider, D. (2010). Частичная очистка и характеристика механизма действия энтероцина S37: бактериоцина, продуцируемого Enterococcus faecalis S37, выделенным из фекалий домашней птицы. J. Environ. Общественное здравоохранение 2010: 986460. DOI: 10.1155/2010/986460
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бен Лага, А., Хаас, Б., Готшалк, М., и Гренье, Д. (2017). Антимикробный потенциал бактериоцинов в птицеводстве и свиноводстве. Вет. Res. 48, 1–12. DOI: 10.1186 / s13567-017-0425-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бойд, Дж., Уэст, Дж. У., Бернард, Дж. К., Аоак, Г., Бергнер, Х., Киджора, К. и др. (2011). Влияние добавления микробов прямого кормления и глицерина в рацион лактирующих дойных коров на удои и очевидную эффективность надоя. J. Dairy Sci. 94, 4616–4622. DOI: 10.3168 / jds.2010-3984
PubMed Аннотация | CrossRef Полный текст | Google Scholar
.
