Диагностика зрительных вызванных потенциалов — ранняя диагностика ЗВП в глазной клинике «Ясный Взор»
- Главная
- Услуги
- Диагностика
- Зрительно-вызванные потенциалы
Записаться на прием
Зрительно-вызванные потенциалы (ЗВП) проводятся для оценки функционального состояния зрительной системы и выявления тонких специфических отклонений.
Это электрофизиологический метод исследования, который незаменим для выявления меридианальной амблиопии, атрофии зрительного нерва, для оценки результатов лечения и динамического наблюдения состояния зрительной системы при косоглазии, нистагме, амблиопии, атрофии зрительного нерва.
Мы проводим ЗВП детям с 3 месяцев.
У детей до 2-х лет ЗВП используется как исследование, которое помогает следить за созреванием зрительного пути, поэтому исследование может проводиться раз в 3 месяца, после 2-х лет — в среднем 1 раз в год.
Исследование длится от 30 минут до 1 часа.
Как подготовить ребенка к исследованию ЗВП:
- Накануне вечером вымойте ребенку голову без применения бальзамов.
- Ребенок должен хорошо выспаться.
- Если Ваш ребенок носит очки, обязательно возьмите их с собой. Если ребенок носит контактные линзы, также лучше взять их с собой или приехать в них (некоторые виды исследований лучше проводить в контактной коррекции). Не забудьте взять контейнер с раствором на случай, если понадобится снять линзы.
- Если Ваша дочь носит сережки, снимите их заблаговременно.
- Если вы принимаете какие-либо препараты регулярно, примите их в обычном режиме. Другие препараты, которые Вы принимаете периодически, перед исследованием лучше не использовать. Обо всех применяемых Вами медикаментах сообщите проводящему исследование врачу.
- Приезжайте на прием заблаговременно и постарайтесь сделать так, чтобы ребенок расслабился перед исследованием.

Рекомендации зависят от вида электрофизиологического исследования и могут меняться.
Как проводится ЗВП
ЗВП — процедура безопасная и неинвазивная. Подготовьте Вашего ребенка к проведению ЗВП:
- Перед началом исследования врач приложит несколько электродов на мочки ушей и на голову. Иногда для этого используется физиологический раствор, контактный гель или паста.
- Врач будет давать Вам или ребенку инструкции, что необходимо делать во время исследования. Обычно каждый глаз исследуется отдельно (закрывается при помощи окклюдера или заслонки).
- После процедуры электроды и контактный гель убираются.
После исследования доктор проанализирует результаты и обсудит с Вами заключение.
Возврат к списку
Электрофизиологические методы исследования в офтальмологии.
Клиническая электрофизиология зрительной системы изучает электрическую активность основных отделов зрительного анализатора.
Электрофизиологические методы позволяют объективно оценить функциональное состояние зрительного анализатора на уровне различных слоев и нейронов сетчатки и зрительного пути и используются для диагностики различных заболеваний сетчатки и зрительного пути.
Возможности электрофизиологических методов:
- Объективная оценка функционального состояния сетчатки и зрительного пути
- Возможность ранней диагностики на субклиническом уровне ряда заболеваний сетчатки и зрительного нерва и зрительного пути в целом, в том числе и наследственных, а также в ряде случаев выявлять носителей патологических генов. Это особенно важно, если еще нет достаточно выраженных офтальмоскопических изменений и нарушений зрительных функций.
- Дифференциальная диагностика заболеваний сетчатки и зрительного нерва.
- Объективный контроль в динамике за течением заболевания и эффективностью проводимого лечения.
- Возможность достаточно точно характеризовать функциональное состояние сетчатки и зрительного нерва при помутнениях прозрачных сред глаза, что является прогностическим критерием перед различными хирургическими вмешательствами на глазном яблоке.

- Возможность оценить функциональное состояние органа зрения у детей раннего возраста, когда субъективные исследования неэффективны.
Основными электрофизиологическими методами исследования органа зрения в клинике являются
ЭРГ используется для оценки функционального состояния сетчатки, ЭОГ – для оценки функции пигментного эпителия, ЗВКП – для оценки зрительного пути от сенсорной сетчатки до зрительных центров.
Методы дополняют друг друга, а их выбор определяется необходимостью дифференциального диагноза и уточнения локализации патологического процесса.
Часто необходимо использовать все ЭФ методы исследования для оценки всего зрительного пути.
Противопоказаниями для проведения электрофизиологических исследований являются беспокойное поведение больных, эпилепсия, а для регистрации ЭРГ сюда добавляются конъюнктивиты, воспалительные заболевания роговицы и склеры, ранние сроки после оперативного лечения на глазном яблоке и придаточном аппарате глаза.
ЭЛЕКТРОРЕТИНОГРАФИЯ (ЭРГ)
ЭРГ представляет собой графическое отображение изменений биоэлектрической активности клеточных элементов сетчатки в ответ на световое раздражение и используется для оценки функционального состояния сетчатки.
Показания к проведения электроретинографии:
1. Необходимость оценки функционального состояния сетчатки, том числе и в тех случаях, когда определить зрительные функции обычным методом невозможно, а глазное дно не офтальмоскопируется, при помутнении сред глаза (бельмо роговицы, катаракта, гемофтальм), в том числе для прогноза зрительных функций в результате предполагаемого оперативного лечения.
2. Диагностика и дифференциальная диагностика заболеваний сетчатки, в том числе наследственных, так как в ряде случаев изменения ЭРГ являются патогномоничными симптомами заболевания. Диагностика поражения палочковой и колбочковой систем сетчатки. Амблиопия.
3. Оценка глубины, распространенности, локализации и степени поражения сетчатки (в том числе при отслойке сетчатки, диабетической ретинопатии, травме, хороидитах и т.
4. Дифференциальная диагностика заболеваний сетчатки и зрительного нерва различного генеза.
5. Выявление начальных функциональных изменений сетчатки, предшествующих клиническим проявлениям заболевания (медикаментозная интоксикация, металлозы, симпатическая офтальмия, сосудистые нарушения и пр.).
6. Контроль за динамикой патологического процесса и эффективностью лечения, определение прогноза.
7. Мониторинг больных, получающих лекарственные препараты с возможным побочным ретинотоксическим действием при длительном их применении.
8. Неожиданная потеря зрения.
9. Педиатрическая практика.
В основе принятой в электроретинографии классификации ЭРГ лежат амплитудные характеристики основных а- и b-волн ЭРГ, а также их временные параметры. Различают следующие виды ЭРГ: нормальную, супернормальную, субнормальную (плюс- и минус-негативную), угасшую, или нерегистрируемую (отсутствующую). Таким образом, при патологических состояниях сетчатки возможно как изменение отдельных компонентов ЭРГ, так и полное её исчезновение.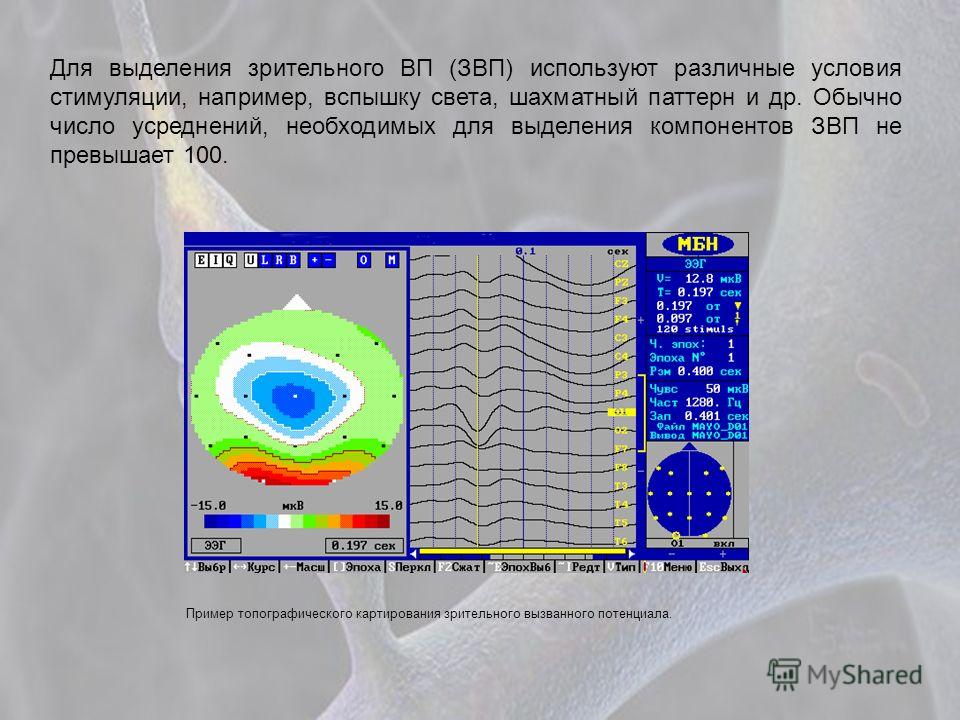
Виды ЭРГ.
- Максимальный или смешанный ответ (общая или ганцфельд-ЭРГ), состоящий из комбинации компонентов палочковой и колбочковой систем, отражает функцию всей сетчатки. Хотя в этих условиях участие колбочек достаточно велико, доминирует ответ палочковой системы. Поражения макулярной области с локализацией патологического процесса в пределах до 6-15° не влияют на величину общей ЭРГ.
- Оценка палочковой системы – скотопическая (палочковая) ЭРГ.
- Оценка колбочковой системы – фотопическая (колбочковая) ЭРГ и мелькающая (ритмическая) ЭРГ на частоту стимула 30 Гц.

- Паттерн-ЭРГ является ответом сетчатки на структурированные стимулы с постоянной освещенностью (реверсивные шахматные или решетчатые паттерны). ПЭРГ используется для диагностики дисфункции макулы и заболеваний, сопровождающихся нарушением функции ганглиозных клеток сетчатки (глаукома).
Электроокулография
позволяет выявить патологические изменения пигментного эпителия сетчатки и фоторецепторов. Для регистрации нормальной электроокулограммы необходимо нормальное функционирование фоторецепторов и пигментного эпителия, контакт между этими слоями, а также адекватное хориоидальное кровоснабжение.Для клинических целей используют расчётную величину – коэффициент Ардена.
Коэффициент Ардена (КА) считают нормальным, если он превышает 185 %. (Обычно 180-250%). С целью оценки патологических состояний сетчатки КА подразделяют на субнормальный (135—185%), анормальный (110—135%), погасший (100—110%), извращенный (ниже 100 %).
Электроокулографию используют в диагностике различных заболеваний сетчатки дистрофической, воспалительной и токсической природы, при циркуляторных нарушениях и другой патологии когда в процесс вовлекается пигментный эпителий
Зрительные вызванные потенциалы (ЗВП) позволяют оценить функциональное состояние зрительных путей на всём протяжении до центральных отделов зрительного анализатора.
Метод регистрации ЗВП используется в клинике для диагностики патологии зрительного нерва и ретрохиазмальных поражений зрительных путей и зрительных центров; при отеке зрительного нерва, воспалении, атрофии, компрессионных повреждениях травматического и опухолевого генеза, метаболических или токсических оптических нейропатиях, для оценки функции зрительного нерва и зрительных путей после орбитальной и интракраниальной хирургии, для диагностики амблиопии.
ЗВП дополняют результаты электроретинографии и могут являться единственным источником информации о зрительной системе в тех случаях, когда ЭРГ невозможно зарегистрировать по тем или иным причинам.
Виды ЗВП зависят от характера стимула: ЗВП на вспышку света называется вспышечным (ВЗВП), на паттерн-стимул — паттерн-ЗВП (ПЗВП). В качестве стимуляции чаще используется реверсивный шахматный паттерн. Генерируемый при этом ответ является наиболее стабильным, наименее вариабельным по амплитуде и латентности пиков.
Зрительные ВП исследуются также в ответ на стандартную фотостимуляцию («вспышку»). Ответ на такую стимуляцию менее стабильный, чем при стимуляции реверсивным шахматным паттерном, изменчив в популяции даже в норме, менее специфичен для оценки центрального зрения. Однако зрительные ВП на вспышку обладают одним важным преимуществом перед шахматным паттерном – они не требуют кооперации пациента, могут регистрироваться у пациентов, которым не может быть проведена регистрация паттерн-ЗВП в связи с очень низкой остротой зрения и отсутствием фиксации взора.
Критериями нарушения проведения по зрительным путям при оценке ЗВП являются отсутствие ответа или значительное снижение амплитуды, удлинение латентности пиков, значительные различия в амплитуде и латентности при стимуляции правого и левого глаз.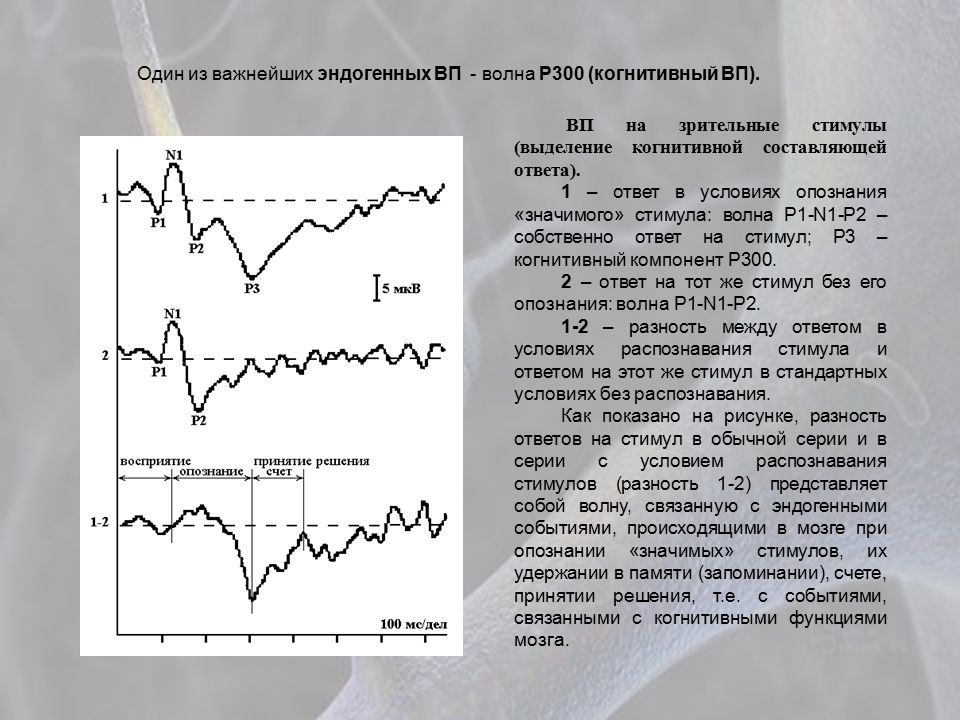 В целом, латентность – более стабильный показатель, амплитуда пиков более вариабельна, чем латентность.
В целом, латентность – более стабильный показатель, амплитуда пиков более вариабельна, чем латентность.
Изменения ПЗВП могут быть связаны и с патологией макулярной области сетчатки, поэтому информативность результатов значительно повышается при одновременной регистрации ЗВП с ЭРГ.
Таким образом, по результатам электрофизиологических исследований (ЭФИ) можно отличить норму от патологии, определить уровень поражения, а также подтвердить или уточнить клинический диагноз. В ряде случаев ЭФ-изменения являются патогномоничными симптомами заболевания. Однако ЭФИ не являются самостоятельным диагностическим инструментом и интерпретация результатов электрофизиологических методов исследования должна всегда проводиться в контексте клинической картины заболевания.
Зрительные вызванные потенциалы — StatPearls
Непрерывное обучение
Зрительные вызванные потенциалы (ЗВП) представляют собой надежный электрофизиологический инструмент при неврологических патологиях. ЗВП являются выражением электрической активности зрительных путей вплоть до зрительного нерва до шпорной коры. Эти потенциалы обеспечивают неинвазивный метод исследования функциональности зрительной системы человека путем обнаружения активности нейронного пула, реагирующего на стимулы, независимо от состояния сознания и внимания пациента. ЗВП имеют клиническое применение при офтальмологической патологии сетчатки и неврологической патологии, связанной со зрительным нервом и/или головным мозгом. ЗВП использовались в качестве альтернативного метода для оценки остроты зрения у невербальных младенцев и взрослых с низкими интеллектуальными способностями или потенциальными симулянтами, а также для хирургического интраоперационного мониторинга. В данном мероприятии описывается роль данного инструментального обследования в диагностике и последующем наблюдении неврологической и офтальмологической патологии межпрофессиональной командой.
ЗВП являются выражением электрической активности зрительных путей вплоть до зрительного нерва до шпорной коры. Эти потенциалы обеспечивают неинвазивный метод исследования функциональности зрительной системы человека путем обнаружения активности нейронного пула, реагирующего на стимулы, независимо от состояния сознания и внимания пациента. ЗВП имеют клиническое применение при офтальмологической патологии сетчатки и неврологической патологии, связанной со зрительным нервом и/или головным мозгом. ЗВП использовались в качестве альтернативного метода для оценки остроты зрения у невербальных младенцев и взрослых с низкими интеллектуальными способностями или потенциальными симулянтами, а также для хирургического интраоперационного мониторинга. В данном мероприятии описывается роль данного инструментального обследования в диагностике и последующем наблюдении неврологической и офтальмологической патологии межпрофессиональной командой.
Цели:
Опишите основной тип ЗВП, используемый при изучении неврологических патологий, поражающих зрительные пути.

Укажите основное дегенеративное заболевание, изучаемое ЗВП.
Объясните изменения ЗВП при рассеянном склерозе.
Обобщить технические принципы VEP.
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Зрительные вызванные потенциалы (ЗВП) представляют собой действенный электрофизиологический инструмент при неврологических патологиях. ЗВП являются выражением электрической активности зрительных путей от зрительного нерва до коры калькарина.[1]
Эти потенциалы обеспечивают неинвазивный метод исследования функциональности зрительной системы человека путем обнаружения активности пула нейронов, реагирующей на стимулы, независимо от состояния сознания и внимания пациента. Измерение ЗВП стало возможным путем наложения электродов на кожу головы в затылочной области и подачи визуальных стимулов пациенту с открытыми глазами.[1][2]
В зависимости от характеристик стимула паттерн зрительных вызванных потенциалов может предоставить различную информацию о функциональности различных секторов поля зрения и целостности оптических путей.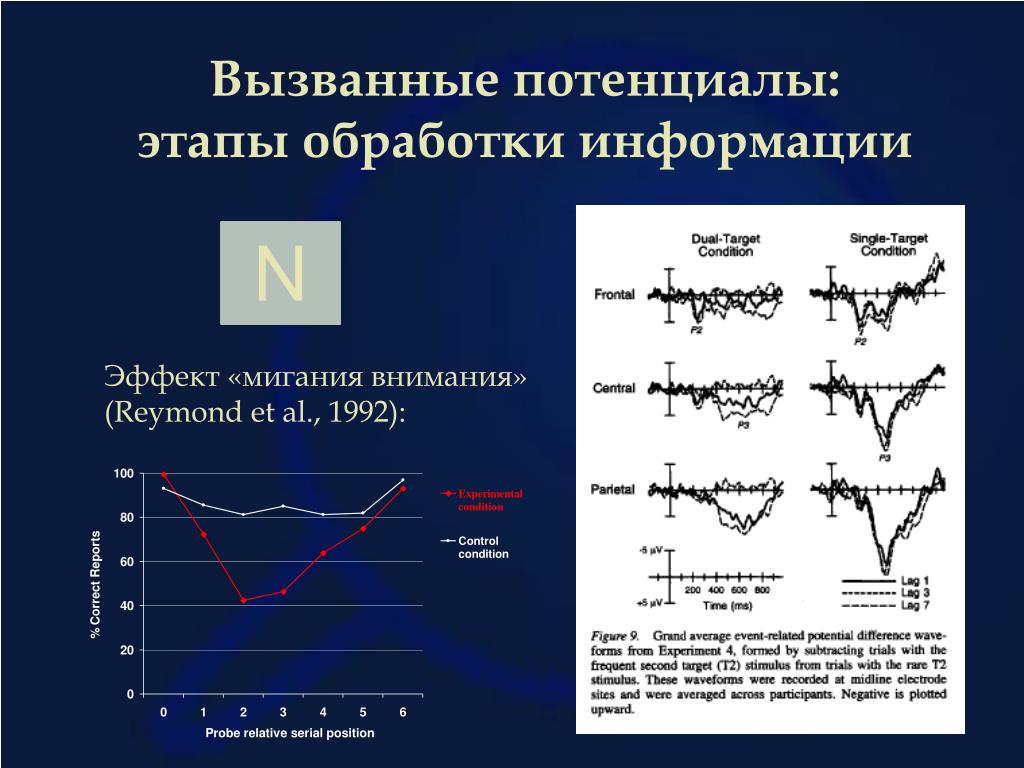 Этот вид инструментального исследования имеет клиническое применение при офтальмологической патологии сетчатки и неврологической патологии, связанной со зрительным нервом и/или головным мозгом (воспалительные, атрофические, токсические, опухолевые и генетические заболевания). VEP использовался в качестве альтернативного метода для оценки остроты зрения у невербальных младенцев и взрослых с низкими интеллектуальными способностями или потенциальной симуляцией.
Этот вид инструментального исследования имеет клиническое применение при офтальмологической патологии сетчатки и неврологической патологии, связанной со зрительным нервом и/или головным мозгом (воспалительные, атрофические, токсические, опухолевые и генетические заболевания). VEP использовался в качестве альтернативного метода для оценки остроты зрения у невербальных младенцев и взрослых с низкими интеллектуальными способностями или потенциальной симуляцией.
Функция
Технические понятия
Основным типом ЗВП, используемым при изучении неврологических патологий, влияющих на зрительные пути, являются ЗВП, структурированные по модели стимуляции (паттерн-ЗВП или П-ЗВП). Как правило, это «разворотный» паттерн (разворот-P-VEP), в котором светлые и темные элементы модели организованы в виде шахматной доски или баров. Стимулы меняются местами, что позволяет варьировать контраст с постоянной средней яркостью. Другой тип ЗВП с паттерном «начало-смещение» (начало-смещение-П-ЗВП) основан на зрительном стимуле, который появляется и исчезает в последовательности, всегда характеризующейся постоянной средней яркостью.
ЗВП, в которых используется диффузный импульсный стимул (вспышка-ЗВП или F-ЗВП), характеризующийся изменением яркости, однако, имеют довольно ограниченную область применения в области неврологических патологий, влияющих на зрительные пути, учитывая, что этот метод тестирования предлагает чрезвычайно изменчивы реакции у нормальных людей и менее чувствительны, чем P-VEP. Кроме того, P-VEP позволяют выбирать характеристики наиболее подходящего стимула при клиническом анализе различных компонентов зрительной системы, которые могут активироваться по-разному в зависимости от пространственных, временных, хроматических и контрастных свойств изображения. [6] [7] (См. Рисунки инструментов, тестирования, стимулятора и результаты ЗВП)
Пространственная частота (SF) шаблонного стимула измеряет, сколько раз контрастность изображения изменяется от минимального до максимального значения в градусах угла зрения, которое затем измеряется в циклах на градус (c/d), где 1 ц/г соответствует полному чередованию светлого элемента с темным в градусе угла зрения.
Размер бара (w) можно рассчитать по формуле: w = 60/2f, где w выражено в угловых минутах, а f — SF, выраженное в c/d. Если вместо баров используется модель шахматной доски, то размеры шахматных досок измеряются в угловых минутах градуса угла зрения. Различные SF позволяют исследовать различные сектора поля зрения, физиологически стимулируя различные нейронные системы зрительного пути.[8]
Электрофизиологический ответ, полученный с помощью потенциала, зависит от яркости стимула, контраста между двумя стимулами (яркостная разница) и временной частоты. Амплитуда P-VEP линейно увеличивается с увеличением контраста и исчезает при контрастах, равных или менее 10%, когда разница между светлыми и темными элементами становится неразличимой. Если ЗВП записываются в соответствии со смещенным/начальным стимулом, фоновая яркость смещенного стимула должна быть идентична яркости структурированного стимула (начального стимула).
Контрастность (С) между элементами рисунка соответствует разнице яркости между светлыми и темными элементами и выражается в процентах. Электрофизиологический ответ, полученный с помощью P-VEP, зависит от временной частоты, то есть от скорости, с которой паттерн появляется или исчезает (начало-смещение-набор-P-VEP) или с которой элементы модели меняют свое положение. (реверс-П-ВЭП). Изменение временной частоты, с которой элементы меняют друг друга на низких частотах (<4 Гц), считается реакцией «переходного» типа, тогда как на высоких частотах (>4 Гц) тип реакции определяется как «устойчивое состояние». .»[9]
Электрофизиологический ответ, полученный с помощью P-VEP, зависит от временной частоты, то есть от скорости, с которой паттерн появляется или исчезает (начало-смещение-набор-P-VEP) или с которой элементы модели меняют свое положение. (реверс-П-ВЭП). Изменение временной частоты, с которой элементы меняют друг друга на низких частотах (<4 Гц), считается реакцией «переходного» типа, тогда как на высоких частотах (>4 Гц) тип реакции определяется как «устойчивое состояние». .»[9]
В реверсивном P-VEP в настоящее время используются ФП с низкой стимуляцией (от 1 Гц до 4 Гц), что позволяет точно записывать данные из затылочной коры. Этот электрофизиологический ответ известен как «переходный» ответ. «Переходный» потенциал реверсивного П-ВЭП состоит из трех отклонений электрического сигнала с чередующейся полярностью воспроизводимой латентности и морфологии, в которых можно распознать положительный главный компонент с латентностью около 100 мс (потенциал P 100), которым предшествуют и за которыми следуют два отрицательных компонента с задержкой примерно от 70 до 75 мс (потенциал N 75) и от 130 до 145 мс (потенциал N 140) соответственно. Положительный компонент Р100 представляет собой наиболее стабильный и повторяемый ответ этого Р-потенциала, регистрируемый на всех участках скальпа, соответствующих затылочной коре, с максимальной амплитудой по средней линии, в области иниона.
Положительный компонент Р100 представляет собой наиболее стабильный и повторяемый ответ этого Р-потенциала, регистрируемый на всех участках скальпа, соответствующих затылочной коре, с максимальной амплитудой по средней линии, в области иниона.
Многочисленные исследования идентифицировали P100 как электрический коррелят активности первичной зрительной коры. При поражении зрительных путей с корковым сохранением еще возможно зарегистрировать интактный Р100. Два других отрицательных компонента потенциала (N140 и N70) вместо этого могут иметь генераторы на уровне стриарной коры (N70) и внеполосатой коры (N140), что, как правило, бесполезно в клинической практике. ][11] (См. рисунки результатов ЗВП)
приложений
В обычных клинических условиях схема стимуляции P-VEP достигается за счет одновременной стимуляции двух зрительных полуполей по сторонам от центра фиксации (стимуляция всего поля), в то время как регистрирующие электроды располагаются на затылочной части черепа в точке Oz (Международная электроэнцефалографическая система 10-20) и на двух симметричных точках, расположенных латерально на расстоянии 5–7 см от центральной.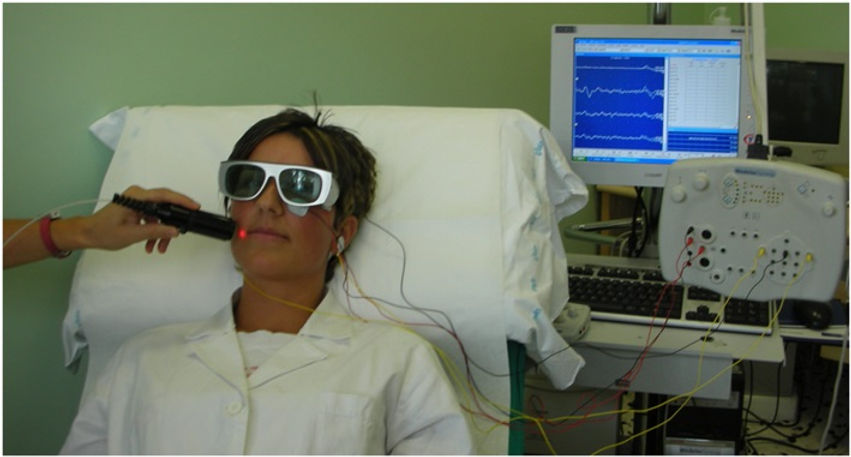
Потенциалы, регистрируемые латерально расположенными электродами, обычно изменчивы и менее представлены; поэтому параметры амплитуды и латентности регулярно получают с учетом центрального электрода. Оценка морфологии, амплитуды и, прежде всего, латентного периода (ретинокортикального времени проведения) потенциала Р100 представляет собой фундаментальный элемент для электрофизиологического исследования целостности оптических путей, особенно на прехиазматическом уровне.
Снижение чувствительности поля зрения вследствие поражения структур ретроорбитального нерва (зрительного нерва) определяет изменения P-PEV, которые отражаются в уменьшении амплитуды и/или удлинении латентного времени различных компонентов, составляющих потенциал. Изменения амплитуды и латентности PEV точно представляют собой электрофизиологический коррелят различных патологических явлений, влияющих на оптические пути.
Топографическое положение, размер и степень кампиметрического дефицита строго обусловливают любые аномалии, обнаруженные при анализе P-PEV. Поражение зрительного нерва, связанное с относительными скотомами в макулярной области, может вызывать значительные изменения P-ЗВП, регистрируемые скальпом, тогда как абсолютная скотома, даже обширная, но локализованная в периферической области поля зрения, может модифицировать P -VEP минимальным или даже нулевым способом.[12]
Поражение зрительного нерва, связанное с относительными скотомами в макулярной области, может вызывать значительные изменения P-ЗВП, регистрируемые скальпом, тогда как абсолютная скотома, даже обширная, но локализованная в периферической области поля зрения, может модифицировать P -VEP минимальным или даже нулевым способом.[12]
Клиническое значение
P-ЗВП представляют собой чувствительный индикатор нарушений целостности всей зрительной системы, которая может быть предметом демиелинизирующих или аксональных патологий. В зависимости от типа патогенетического механизма П-ЗВП могут сигнализировать о наличии явлений демиелинизации, выражающихся изменением латентного периода и увеличением времени ретинол-кортикальной проводимости, а также указывать на наличие аксонального повреждения, о чем свидетельствуют изменения амплитуды и Морфология полученных ответов. В соответствии с этими принципами P-VEP используются для диагностики прехиазматических, хиазматических и ретрохиазматических неврологических патологий. [13][14][15]
[13][14][15]
Нейроптальмологическое поле
ЗВП используются в области нейроофтальмологии для нескольких клинических применений, которые включают: количественную оценку и мониторинг функциональных повреждений при оптических нейропатиях различных воспалительных, демиелинизирующих, компрессионных, ишемических, травматических, наследственных, дегенеративных и/или токсических -метаболического происхождения; дифференциальная диагностика между патологиями зрительного нерва и патологиями сетчатки с использованием результатов, связанных с функциональными исследованиями сетчатки; и в различии между корковой слепотой и симуляцией.
Неврологическое поле
Рассеянный склероз — воспалительное заболевание белого вещества, характеризующееся многоочаговым поражением белого вещества головного мозга. Клинические проявления очень разнообразны в зависимости от локализации и распространенности вспышек демиелинизации; однако поражения, по-видимому, имеют преимущественное распространение в некоторых областях центральной нервной системы. Более чем в 20% случаев симптомом начала заболевания является неврит зрительного нерва, а более чем у 50% больных имеется клинический эпизод неврита зрительного нерва. Исследования показали, что латентность ЗВП и оптическая когерентная томография измерения толщины нервного слоя сетчатки коррелируют с измерениями инвалидности и могут быть полезны при лечении этих пациентов.] Ранние клинические признаки рассеянного склероза позволяют выявить «доброкачественные» фенотипы, характеризующиеся почти полным восстановлением зрения и потерей чувствительности сетчатки в острой фазе.[20][21]
Более чем в 20% случаев симптомом начала заболевания является неврит зрительного нерва, а более чем у 50% больных имеется клинический эпизод неврита зрительного нерва. Исследования показали, что латентность ЗВП и оптическая когерентная томография измерения толщины нервного слоя сетчатки коррелируют с измерениями инвалидности и могут быть полезны при лечении этих пациентов.] Ранние клинические признаки рассеянного склероза позволяют выявить «доброкачественные» фенотипы, характеризующиеся почти полным восстановлением зрения и потерей чувствительности сетчатки в острой фазе.[20][21]
При демиелинизирующих патологиях зрительного нерва П-ЗВП показывают задержку латентных ответов, часто при отсутствии значительных изменений амплитуды, связанных со снижением остроты зрения пациентов. Латентные изменения П-ЗВП могли сохраняться длительное время, даже после полного восстановления остроты зрения. Иногда можно наблюдать задержку латентного периода P-PEV и в контралатеральном глазу. Этот тип изменений может выявить наличие субклинических изменений проведения импульса по зрительному нерву даже до того, как проявятся клинические признаки или симптомы поражения нерва. [22]
[22]
При ишемической нейропатии зрительного нерва передняя ишемическая оптическая нейропатия или AION возникает вследствие инфаркта ламинарной или ламинарной части диска зрительного нерва, вызванного окклюзией коротких задних цилиарных артерий. Клиническое начало этого изменения, как правило, неожиданное, безболезненное, а потеря зрения может прогрессировать в течение многих дней. Исследования показали, что ЗВП полезны при лечении таких пациентов.[23]
Дефицит кампиметрии обычно носит высотный характер и может затрагивать центральную зону фиксации, что оправдывает серьезную потерю остроты зрения. Что касается изменений ЗВП, то можно наблюдать преобладающее изменение, которое оказывается выраженным снижением амплитуды Р100, связанным с плохой модификацией латентности.[24]
Причиной сдавления зрительного нерва являются частые глиомы зрительного пути детского возраста. Клиническое начало характеризуется постепенной потерей зрения без болей в орбите, которые могут быть даже бессимптомными в течение длительного времени. Ранний клинический диагноз и точное последующее наблюдение за пациентами с компрессионной невропатией зрительного нерва, особенно при наличии менингиом или глиом, имеют принципиальное значение для улучшения терапевтического подхода, основанного на хирургической резекции и/или процедурах лучевой терапии [25]. ] В этих случаях PEV постоянно демонстрируют десинхронизированный P100 низкой амплитуды с очевидной латентной задержкой.
Ранний клинический диагноз и точное последующее наблюдение за пациентами с компрессионной невропатией зрительного нерва, особенно при наличии менингиом или глиом, имеют принципиальное значение для улучшения терапевтического подхода, основанного на хирургической резекции и/или процедурах лучевой терапии [25]. ] В этих случаях PEV постоянно демонстрируют десинхронизированный P100 низкой амплитуды с очевидной латентной задержкой.
Что касается нейродегенеративных заболеваний, то ЗВП исследования обычно не играют диагностической роли. Однако эти методы тестирования могут дать возможность исследовать физио- и патофизиологические механизмы и участие различных систем нейротрансмиссии, участвующих в патогенезе этих патологических состояний, точным и неинвазивным способом.
Нейропатия зрительного нерва Лебера (LON) и доминантный неврит зрительного нерва типа Kjer (DON) являются наиболее распространенными наследственными формами первичной болезни ганглиозных клеток сетчатки. LON обычно представляет собой прогрессирующую потерю двустороннего зрения, не связанную с тканью орбиты и связанную с митохондриальными мутациями. В этих случаях заметно задерживаются P-VEP, но возможно относительное сохранение морфологии P100 на начальных стадиях заболевания.
В этих случаях заметно задерживаются P-VEP, но возможно относительное сохранение морфологии P100 на начальных стадиях заболевания.
Изменения амплитуды Р100 связаны со стадией и клинической формой заболевания. Изменениям P-PEV обычно предшествует снижение амплитуды или даже отсутствие воспроизводимости потенциала N95.
При атаксии Фридриха PEV используются для оценки развития зрительной функции при этом нейродегенеративном заболевании, которое имеет тенденцию быть ненормальным у двух третей пациентов. Замедленная латентность и увеличенная амплитуда волны р100 являются наиболее частыми электрофизиологическими изменениями при этой патологии.[28][29]]
Прочие вопросы
Хирургический интраоперационный мониторинг
В последние несколько лет ЗВП рассматривались для интраоперационного мониторинга зрительной функции с использованием нескольких протоколов; однако текущая литература и клинические данные в этой области очень ограничены. Использование тотальной внутривенной анестезии, внедрение светодиодной технологии, электроретинографии и электроэнцефалографии повысили надежность нейромониторинга ЗВП за счет улучшения воспроизводимости и интерпретируемости метода, а также работы над тем, чтобы сделать его более надежным и упростить его интеграцию в операционный процесс. .
.
В недавних исследованиях эти инструменты применялись в орбитальной и транссфеноидальной хирургии.[30][31][32] (См. рисунки интраоперационного хирургического мониторинга с помощью VEP)
Улучшение результатов медицинского персонала
Для применения VEP требуется межпрофессиональная команда медицинских работников, включая медсестер, техников нейрофизиопатологии, неврологов и офтальмологов. Эта команда имеет основополагающее значение для правильного применения этого инструмента как в клинической сфере, так и при интраоперационном хирургическом мониторинге. ЗВП регулярно используются при диагностике прехиазматических, хиазматических и ретрохиазматических неврологических патологий.[13] [Уровень 3]
В этом сценарии техник-нейрофизиопатолог обеспечивает подготовку и контроль инструментов оборудования, которым он оснащен, и полностью управляет сбором и оптимизацией различных диагностических методов, по которым, по запросу, он должен составить описательный отчет из технический аспект. (уровень I)
(уровень I)
Недавние исследования применяли ЗВП в орбитальной и транссфеноидальной хирургии, но без стандартизированных протоколов и однородных результатов.[30][31][32] [Уровень 3]
Межпрофессиональная команда, обеспечивающая комплексный подход к уходу за пациентами и всестороннее диагностическое управление, может помочь в достижении наилучших возможных результатов. Сотрудничество, междисциплинарное совместное принятие решений и открытое общение между членами команды являются ключевыми элементами для правильной диагностики и хорошего результата. Межпрофессиональная помощь, оказываемая пациенту, должна использовать комплексный подход в сочетании с научно обоснованным подходом к планированию и оценке всех совместных действий.[33] Чем раньше выявляются признаки и симптомы осложнения, тем лучше прогноз и исход. [Уровень 3]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.

Рисунок
Зрительные вызванные потенциалы (ЗВП) с использованием стимуляции в виде шахматной доски. Могут использоваться разные электроды, которые размещаются на коже головы. Прибор оснащен стимулятором для регулирования частоты и интенсивности световых раздражителей. Предоставлено (подробнее…)
Рисунок
Результаты паттерновых и импульсных зрительных вызванных потенциалов (ЗВП). Предоставлено Марко Цеппиери, доктором медицинских наук. Изображения предоставлены Элисой Экоретти и Джадой Паулетто, докторами медицины.
Рисунок
Подушечки для импульсной стимуляции, используемые для хирургического интраоперационного мониторинга. Результаты интраоперационных зрительных вызванных потенциалов (ЗВП). Предоставлено Марко Цеппиери, доктором медицинских наук. Изображения предоставлены Элисой Экоретти и Джадой Паулетто, докторами медицины.
Ссылки
- 1.
Hoffmann MB, Brands J, Behrens-Baumann W, Bach M.
 Оценка остроты зрения на основе ЗВП при слабом зрении. Док Офтальмол. 2017 декабрь; 135(3):209-218. [PubMed: 28980154]
Оценка остроты зрения на основе ЗВП при слабом зрении. Док Офтальмол. 2017 декабрь; 135(3):209-218. [PubMed: 28980154]- 2.
Гамильтон Р., Бах М., Генрих С.П., Хоффманн М.Б., Одом Дж.В., Маккалох Д.Л., Томпсон Д.А. VEP-оценка остроты зрения: систематический обзор. Док Офтальмол. 2021 фев; 142(1):25-74. [Бесплатная статья PMC: PMC7907051] [PubMed: 32488810]
- 3.
Patterson Gentile C, Joshi NR, Ciuffreda KJ, Arbogast KB, Master C, Aguirre GK. Влияние развития на паттерн зрительных вызванных потенциалов, характеризуемый анализом главных компонентов. Transl Vis Sci Technol. 2021 01 апр;10(4):1. [Бесплатная статья PMC: PMC8024780] [PubMed: 34003980]
- 4.
Zheng X, Xu G, Zhang K, Liang R, Yan W, Tian P, Jia Y, Zhang S, Du C. Оценка остроты зрения человека с использованием зрительного вызванного потенциала: обзор. Датчики (Базель). 28 сентября 2020 г., 20(19) [бесплатная статья PMC: PMC7582995] [PubMed: 32998208]
- 5.

Соареш Т.С., Сакаи П.Ю., Березовский А., Роча Д.М., Ватанабэ С.Е., Саломао С.Р. Зрительные вызванные потенциалы с обращением паттерна как инструмент диагностики глазной симуляции. Арк Брас Офтальмол. 2016 сен-октябрь;79(5):303-307. [PubMed: 27982208]
- 6.
Махаджан Ю., Чинг А., Уотсон Т., Ким Дж., Дэвис С. Влияние устойчивого избирательного внимания на стационарные зрительные вызванные потенциалы. Опыт Мозг Res. 2022 янв; 240(1):249-261. [PubMed: 34727219]
- 7.
Хасанкарими Х., Джафарзадехпур Э., Мохаммади А., Нури С.М.Р. Низкоконтрастный визуальный вызванный потенциал обращения паттерна в различных пространственных частотах. J Офтальмологический Vis Res. 2020 июль-сен;15(3):362-371. [Бесплатная статья PMC: PMC7431726] [PubMed: 32864067]
- 8.
Монтгомери Д.П., Хейден Д.Дж., Чалонер Ф.А., Кук С.Ф., Беар М.Ф. Пластичность селективной реакции на стимулы в первичной зрительной коре: прогресс и загадки.
 Передние нейронные цепи. 2021;15:815554. [PMC free article: PMC8841555] [PubMed: 35173586]
Передние нейронные цепи. 2021;15:815554. [PMC free article: PMC8841555] [PubMed: 35173586]- 9.
Ян М., Юнг Т.П., Хан Дж., Сюй М., Мин Д. [Обзор исследований алгоритмов декодирования стационарных зрительных вызванных потенциалов ]. Шэн У И Сюэ Гун Ченг Сюэ За Чжи. 2022 25 апреля; 39 (2): 416-425. [Бесплатная статья PMC: PMC9927346] [PubMed: 35523564]
- 10.
Котари Р., Сингх С., Сингх Р., Шукла А.К., Бокария П. Влияние угла зрения на изменение зрительных вызванных потенциалов. Оман Дж. Офтальмол. 2014 сен;7(3):120-5. [Бесплатная статья PMC: PMC4220397] [PubMed: 25378875]
- 11.
Dymond AM, Coger RW, Serafetinides EA. Предварительная обработка данных применялась к средней амплитуде зрительного вызванного потенциала P100-N140 человека, латентности и наклону. Психиатрия рез. 1980 декабрь; 3(3):315-22. [В паблике: 6936725]
- 12.
Ядав Н.К., Лудлам Д.П., Чуффреда К.Дж. Влияние различных конфигураций стимулов на зрительный вызванный потенциал (ЗВП).
 Док Офтальмол. 2012 июнь; 124(3):177-96. [PubMed: 22426575]
Док Офтальмол. 2012 июнь; 124(3):177-96. [PubMed: 22426575]- 13.
Park SH, Park CY, Shin YJ, Jeong KS, Kim NH. Низкоконтрастные визуальные вызванные потенциалы для раннего выявления неврита зрительного нерва. Фронт Нейрол. 2022;13:804395. [Бесплатная статья PMC: PMC9099025] [PubMed: 35572925]
- 14.
Тирунаву В.М., Мохаммад Л.М., Кандула В., Беструм М., Лам С.К. Результаты зрения для педиатрических пациентов с глиомами зрительного пути, связанными с нейрофиброматозом типа I: систематический обзор клинических данных. J Pediatr Hematol Oncol. 2021 01 мая; 43 (4): 135-143. [PubMed: 33480655]
- 15.
Leocani L, Guerrieri S, Comi G. Зрительные вызванные потенциалы как биомаркер рассеянного склероза и ассоциированного оптического неврита. J Нейроофтальмол. 2018 сен; 38 (3): 350-357. [В паблике: 30106802]
- 16.
Ван Ю, Ву ДЗ, Ву ЛЗ, Чен ЮЗ. Поле зрения в сравнении со зрительными вызванными потенциалами при макулопатиях и оптических нейропатиях.
 Ян Кэ Сюэ Бао. 1989 июнь; 5 (1-2): 52-9. [PubMed: 2485746]
Ян Кэ Сюэ Бао. 1989 июнь; 5 (1-2): 52-9. [PubMed: 2485746]- 17.
Юркуте Н., Робсон А.Г. Электрофизиология в нейроофтальмологии. Handb Clin Neurol. 2021;178:79-96. [PubMed: 33832688]
- 18.
Маркар В.Л., Баттегай Э., Шмидт Д., Читам М. Параллельная обработка в зрительной коре человека проявляется через влияние их нейронных реакций на зрительный вызванный потенциал. Видение Рез. 2022 апр;193:107994. [PubMed: 34979298]
- 19.
Эклунд А., Хуанг-Линк Ю., Ковачович Б., Дале С., Вретем М., Линд Дж. ОКТ и ВЭП коррелируют с инвалидностью при вторично-прогрессирующем рассеянном склерозе. Мульт Склер Релят Расстройство. 2022 дек;68:104255. [PubMed: 36544315]
- 20.
Oh J, Vidal-Jordana A, Montalban X. Рассеянный склероз: клинические аспекты. Карр Опин Нейрол. 2018 дек; 31 (6): 752-759. [PubMed: 30300239]
- 21.
де Сез Дж., Биго К. Диагностические критерии рассеянного склероза: от проблемы до пересмотренных критериев Макдональда 2017 года.
 Пресс Мед. 2021 июнь;50(2):104089. [PubMed: 34718114]
Пресс Мед. 2021 июнь;50(2):104089. [PubMed: 34718114]- 22.
Backner Y, Petrou P, Glick-Shames H, Raz N, Zimmermann H, Jost R, Scheel M, Paul F, Karussis D, Levin N. Видение и связанные с видением Меры при прогрессирующем рассеянном склерозе. Фронт Нейрол. 2019;10:455. [Бесплатная статья PMC: PMC6509148] [PubMed: 31130910]
- 23.
Барбано Л., Зиккарди Л., Паризи В. Корреляции между визуальными морфологическими, электрофизиологическими изменениями и изменениями остроты зрения при хронической неартериальной ишемической оптической нейропатии. Graefes Arch Clin Exp Офтальмол. 2021 май; 259(5):1297-1308. [PubMed: 33415352]
- 24.
Джаяраман М., Ганди Р.А., Рави П., Сен П. Мультифокальный зрительный вызванный потенциал при оптическом неврите, ишемической оптической нейропатии и компрессионной оптической нейропатии. Индийский Дж. Офтальмол. 2014 март; 62(3):299-304. [Бесплатная статья PMC: PMC4061667] [PubMed: 24088641]
- 25.

Дотто П.Ф., Березовский А., Сакаи П.Ю., Роча Д.М., Фернандес А.Г., Саломао С.Р. Оценка зрительных функций по зрительно-вызванным потенциалам у взрослых с орбитальными и другими первичными внутричерепными опухолями. Eur J Офтальмол. 2021 май; 31(3):1351-1360. [PubMed: 32468859]
- 26.
Боуман Р., Уолтерс Б., Смит В., Приз К.Л., Хэндли С.Э., Грин К., Манкад К., О’Хара П., Даль С., Йоргенсен М., Опочер Э., Харгрейв Д. , Томпсон Д.А. Зрительные исходы и предикторы глиомы зрительного пути: исследование в одном центре. Глаз (Лонд). 2022 13 мая; [В паблике: 35562551]
- 27.
Табакару Б., Станка Х.Т. Дальнейшие достижения в диагностике и лечении наследственной оптической нейропатии Лебера — обзор. Ром Дж. Офтальмол. 2022 г., январь-март; 66(1):13-16. [Бесплатная статья PMC: PMC
47] [PubMed: 35531455]- 28.
Ziccardi L, Cioffi E, Barbano L, Gioiosa V, Falsini B, Casali C, Parisi V. Функциональная оценка макулярных морфо-функциональных и зрительных путей у пациентов со спиноцеребеллярной атаксией 1 типа с неврологическими симптомами или без них.
 Дж. Клин Мед. 2021 12 ноября; 10 (22) [бесплатная статья PMC: PMC8625180] [PubMed: 34830553]
Дж. Клин Мед. 2021 12 ноября; 10 (22) [бесплатная статья PMC: PMC8625180] [PubMed: 34830553]- 29.
Родригес-Лабрада Р., Веласкес-Перес Л., Ортега-Санчес Р., Пенья-Акоста А., Васкес-Мохена Ю., Каналес-Очоа Н., Медрано-Монтеро Х., Торрес-Вега Р., Гонсалес- Залдивар Ю. Взгляд на снижение когнитивных функций при спиноцеребеллярной атаксии 2 типа: исследование потенциала мозга, связанное с событием P300. Атаксия мозжечка. 2019;6:3. [Бесплатная статья PMC: PMC6399884] [PubMed: 30873287]
- 30.
MacDonald DB, Dong CC, Uribe A. Интраоперационные техники вызванных потенциалов. Handb Clin Neurol. 2022;186:39-65. [PubMed: 35772897]
- 31.
Zhu H, Qiao N, Yang X, Li C, Ma G, Kang J, Liu C, Cao L, Zhang Y, Gui S. Клиническое применение интраоперационных визуальных вызванных потенциал при рецидивирующих краниофарингиомах, удаленных расширенной эндоскопической эндоназальной хирургией. Клиника Нейрол Нейрохирург. 2022 март; 214:107149.
 [PubMed: 35151969]
[PubMed: 35151969]- 32.
Clauser LC, Tieghi R, Galie’ M, Franco F, Carinci F. Хирургическая декомпрессия при эндокринной орбитопатии. Визуальная оценка вызванных потенциалов и влияние на зрительный нерв. J Краниомаксиллофак Хирург. 2012 Октябрь;40(7):621-5. [В паблике: 22424910]
- 33.
Гутовский К.А. Доказательная медицина: Абдоминопластика. Plast Reconstr Surg. 2018 г., февраль; 141(2):286e-299e. [PubMed: 29373443]
Зрительные вызванные потенциалы — StatPearls
Непрерывное обучение
Зрительные вызванные потенциалы (ЗВП) представляют собой надежный электрофизиологический инструмент при неврологических патологиях. ЗВП являются выражением электрической активности зрительных путей вплоть до зрительного нерва до шпорной коры. Эти потенциалы обеспечивают неинвазивный метод исследования функциональности зрительной системы человека путем обнаружения активности нейронного пула, реагирующего на стимулы, независимо от состояния сознания и внимания пациента. ЗВП имеют клиническое применение при офтальмологической патологии сетчатки и неврологической патологии, связанной со зрительным нервом и/или головным мозгом. ЗВП использовались в качестве альтернативного метода для оценки остроты зрения у невербальных младенцев и взрослых с низкими интеллектуальными способностями или потенциальными симулянтами, а также для хирургического интраоперационного мониторинга. В данном мероприятии описывается роль данного инструментального обследования в диагностике и последующем наблюдении неврологической и офтальмологической патологии межпрофессиональной командой.
ЗВП имеют клиническое применение при офтальмологической патологии сетчатки и неврологической патологии, связанной со зрительным нервом и/или головным мозгом. ЗВП использовались в качестве альтернативного метода для оценки остроты зрения у невербальных младенцев и взрослых с низкими интеллектуальными способностями или потенциальными симулянтами, а также для хирургического интраоперационного мониторинга. В данном мероприятии описывается роль данного инструментального обследования в диагностике и последующем наблюдении неврологической и офтальмологической патологии межпрофессиональной командой.
Цели:
Опишите основной тип ЗВП, используемый при изучении неврологических патологий, поражающих зрительные пути.
Укажите основное дегенеративное заболевание, изучаемое ЗВП.
Объясните изменения ЗВП при рассеянном склерозе.
Обобщить технические принципы VEP.
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Зрительные вызванные потенциалы (ЗВП) представляют собой действенный электрофизиологический инструмент при неврологических патологиях. ЗВП являются выражением электрической активности зрительных путей от зрительного нерва до коры калькарина.[1]
Эти потенциалы обеспечивают неинвазивный метод исследования функциональности зрительной системы человека путем обнаружения активности пула нейронов, реагирующей на стимулы, независимо от состояния сознания и внимания пациента. Измерение ЗВП стало возможным путем наложения электродов на кожу головы в затылочной области и подачи визуальных стимулов пациенту с открытыми глазами.[1][2]
В зависимости от характеристик стимула паттерн зрительных вызванных потенциалов может предоставить различную информацию о функциональности различных секторов поля зрения и целостности оптических путей. Этот вид инструментального исследования имеет клиническое применение при офтальмологической патологии сетчатки и неврологической патологии, связанной со зрительным нервом и/или головным мозгом (воспалительные, атрофические, токсические, опухолевые и генетические заболевания). VEP использовался в качестве альтернативного метода для оценки остроты зрения у невербальных младенцев и взрослых с низкими интеллектуальными способностями или потенциальной симуляцией.
VEP использовался в качестве альтернативного метода для оценки остроты зрения у невербальных младенцев и взрослых с низкими интеллектуальными способностями или потенциальной симуляцией.
Функция
Технические понятия
Основным типом ЗВП, используемым при изучении неврологических патологий, влияющих на зрительные пути, являются ЗВП, структурированные по модели стимуляции (паттерн-ЗВП или П-ЗВП). Как правило, это «разворотный» паттерн (разворот-P-VEP), в котором светлые и темные элементы модели организованы в виде шахматной доски или баров. Стимулы меняются местами, что позволяет варьировать контраст с постоянной средней яркостью. Другой тип ЗВП с паттерном «начало-смещение» (начало-смещение-П-ЗВП) основан на зрительном стимуле, который появляется и исчезает в последовательности, всегда характеризующейся постоянной средней яркостью.
ЗВП, в которых используется диффузный импульсный стимул (вспышка-ЗВП или F-ЗВП), характеризующийся изменением яркости, однако, имеют довольно ограниченную область применения в области неврологических патологий, влияющих на зрительные пути, учитывая, что этот метод тестирования предлагает чрезвычайно изменчивы реакции у нормальных людей и менее чувствительны, чем P-VEP. Кроме того, P-VEP позволяют выбирать характеристики наиболее подходящего стимула при клиническом анализе различных компонентов зрительной системы, которые могут активироваться по-разному в зависимости от пространственных, временных, хроматических и контрастных свойств изображения. [6] [7] (См. Рисунки инструментов, тестирования, стимулятора и результаты ЗВП)
Кроме того, P-VEP позволяют выбирать характеристики наиболее подходящего стимула при клиническом анализе различных компонентов зрительной системы, которые могут активироваться по-разному в зависимости от пространственных, временных, хроматических и контрастных свойств изображения. [6] [7] (См. Рисунки инструментов, тестирования, стимулятора и результаты ЗВП)
Пространственная частота (SF) шаблонного стимула измеряет, сколько раз контрастность изображения изменяется от минимального до максимального значения в градусах угла зрения, которое затем измеряется в циклах на градус (c/d), где 1 ц/г соответствует полному чередованию светлого элемента с темным в градусе угла зрения.
Размер бара (w) можно рассчитать по формуле: w = 60/2f, где w выражено в угловых минутах, а f — SF, выраженное в c/d. Если вместо баров используется модель шахматной доски, то размеры шахматных досок измеряются в угловых минутах градуса угла зрения. Различные SF позволяют исследовать различные сектора поля зрения, физиологически стимулируя различные нейронные системы зрительного пути. [8]
[8]
Электрофизиологический ответ, полученный с помощью потенциала, зависит от яркости стимула, контраста между двумя стимулами (яркостная разница) и временной частоты. Амплитуда P-VEP линейно увеличивается с увеличением контраста и исчезает при контрастах, равных или менее 10%, когда разница между светлыми и темными элементами становится неразличимой. Если ЗВП записываются в соответствии со смещенным/начальным стимулом, фоновая яркость смещенного стимула должна быть идентична яркости структурированного стимула (начального стимула).
Контрастность (С) между элементами рисунка соответствует разнице яркости между светлыми и темными элементами и выражается в процентах. Электрофизиологический ответ, полученный с помощью P-VEP, зависит от временной частоты, то есть от скорости, с которой паттерн появляется или исчезает (начало-смещение-набор-P-VEP) или с которой элементы модели меняют свое положение. (реверс-П-ВЭП). Изменение временной частоты, с которой элементы меняют друг друга на низких частотах (<4 Гц), считается реакцией «переходного» типа, тогда как на высоких частотах (>4 Гц) тип реакции определяется как «устойчивое состояние». .»[9]
.»[9]
В реверсивном P-VEP в настоящее время используются ФП с низкой стимуляцией (от 1 Гц до 4 Гц), что позволяет точно записывать данные из затылочной коры. Этот электрофизиологический ответ известен как «переходный» ответ. «Переходный» потенциал реверсивного П-ВЭП состоит из трех отклонений электрического сигнала с чередующейся полярностью воспроизводимой латентности и морфологии, в которых можно распознать положительный главный компонент с латентностью около 100 мс (потенциал P 100), которым предшествуют и за которыми следуют два отрицательных компонента с задержкой примерно от 70 до 75 мс (потенциал N 75) и от 130 до 145 мс (потенциал N 140) соответственно. Положительный компонент Р100 представляет собой наиболее стабильный и повторяемый ответ этого Р-потенциала, регистрируемый на всех участках скальпа, соответствующих затылочной коре, с максимальной амплитудой по средней линии, в области иниона.
Многочисленные исследования идентифицировали P100 как электрический коррелят активности первичной зрительной коры. При поражении зрительных путей с корковым сохранением еще возможно зарегистрировать интактный Р100. Два других отрицательных компонента потенциала (N140 и N70) вместо этого могут иметь генераторы на уровне стриарной коры (N70) и внеполосатой коры (N140), что, как правило, бесполезно в клинической практике. ][11] (См. рисунки результатов ЗВП)
При поражении зрительных путей с корковым сохранением еще возможно зарегистрировать интактный Р100. Два других отрицательных компонента потенциала (N140 и N70) вместо этого могут иметь генераторы на уровне стриарной коры (N70) и внеполосатой коры (N140), что, как правило, бесполезно в клинической практике. ][11] (См. рисунки результатов ЗВП)
приложений
В обычных клинических условиях схема стимуляции P-VEP достигается за счет одновременной стимуляции двух зрительных полуполей по сторонам от центра фиксации (стимуляция всего поля), в то время как регистрирующие электроды располагаются на затылочной части черепа в точке Oz (Международная электроэнцефалографическая система 10-20) и на двух симметричных точках, расположенных латерально на расстоянии 5–7 см от центральной.
Потенциалы, регистрируемые латерально расположенными электродами, обычно изменчивы и менее представлены; поэтому параметры амплитуды и латентности регулярно получают с учетом центрального электрода. Оценка морфологии, амплитуды и, прежде всего, латентного периода (ретинокортикального времени проведения) потенциала Р100 представляет собой фундаментальный элемент для электрофизиологического исследования целостности оптических путей, особенно на прехиазматическом уровне.
Оценка морфологии, амплитуды и, прежде всего, латентного периода (ретинокортикального времени проведения) потенциала Р100 представляет собой фундаментальный элемент для электрофизиологического исследования целостности оптических путей, особенно на прехиазматическом уровне.
Снижение чувствительности поля зрения вследствие поражения структур ретроорбитального нерва (зрительного нерва) определяет изменения P-PEV, которые отражаются в уменьшении амплитуды и/или удлинении латентного времени различных компонентов, составляющих потенциал. Изменения амплитуды и латентности PEV точно представляют собой электрофизиологический коррелят различных патологических явлений, влияющих на оптические пути.
Топографическое положение, размер и степень кампиметрического дефицита строго обусловливают любые аномалии, обнаруженные при анализе P-PEV. Поражение зрительного нерва, связанное с относительными скотомами в макулярной области, может вызывать значительные изменения P-ЗВП, регистрируемые скальпом, тогда как абсолютная скотома, даже обширная, но локализованная в периферической области поля зрения, может модифицировать P -VEP минимальным или даже нулевым способом. [12]
[12]
Клиническое значение
P-ЗВП представляют собой чувствительный индикатор нарушений целостности всей зрительной системы, которая может быть предметом демиелинизирующих или аксональных патологий. В зависимости от типа патогенетического механизма П-ЗВП могут сигнализировать о наличии явлений демиелинизации, выражающихся изменением латентного периода и увеличением времени ретинол-кортикальной проводимости, а также указывать на наличие аксонального повреждения, о чем свидетельствуют изменения амплитуды и Морфология полученных ответов. В соответствии с этими принципами P-VEP используются для диагностики прехиазматических, хиазматических и ретрохиазматических неврологических патологий.[13][14][15]
Нейроптальмологическое поле
ЗВП используются в области нейроофтальмологии для нескольких клинических применений, которые включают: количественную оценку и мониторинг функциональных повреждений при оптических нейропатиях различных воспалительных, демиелинизирующих, компрессионных, ишемических, травматических, наследственных, дегенеративных и/или токсических -метаболического происхождения; дифференциальная диагностика между патологиями зрительного нерва и патологиями сетчатки с использованием результатов, связанных с функциональными исследованиями сетчатки; и в различии между корковой слепотой и симуляцией.
Неврологическое поле
Рассеянный склероз — воспалительное заболевание белого вещества, характеризующееся многоочаговым поражением белого вещества головного мозга. Клинические проявления очень разнообразны в зависимости от локализации и распространенности вспышек демиелинизации; однако поражения, по-видимому, имеют преимущественное распространение в некоторых областях центральной нервной системы. Более чем в 20% случаев симптомом начала заболевания является неврит зрительного нерва, а более чем у 50% больных имеется клинический эпизод неврита зрительного нерва. Исследования показали, что латентность ЗВП и оптическая когерентная томография измерения толщины нервного слоя сетчатки коррелируют с измерениями инвалидности и могут быть полезны при лечении этих пациентов.] Ранние клинические признаки рассеянного склероза позволяют выявить «доброкачественные» фенотипы, характеризующиеся почти полным восстановлением зрения и потерей чувствительности сетчатки в острой фазе. [20][21]
[20][21]
При демиелинизирующих патологиях зрительного нерва П-ЗВП показывают задержку латентных ответов, часто при отсутствии значительных изменений амплитуды, связанных со снижением остроты зрения пациентов. Латентные изменения П-ЗВП могли сохраняться длительное время, даже после полного восстановления остроты зрения. Иногда можно наблюдать задержку латентного периода P-PEV и в контралатеральном глазу. Этот тип изменений может выявить наличие субклинических изменений проведения импульса по зрительному нерву даже до того, как проявятся клинические признаки или симптомы поражения нерва.[22]
При ишемической нейропатии зрительного нерва передняя ишемическая оптическая нейропатия или AION возникает вследствие инфаркта ламинарной или ламинарной части диска зрительного нерва, вызванного окклюзией коротких задних цилиарных артерий. Клиническое начало этого изменения, как правило, неожиданное, безболезненное, а потеря зрения может прогрессировать в течение многих дней. Исследования показали, что ЗВП полезны при лечении таких пациентов. [23]
[23]
Дефицит кампиметрии обычно носит высотный характер и может затрагивать центральную зону фиксации, что оправдывает серьезную потерю остроты зрения. Что касается изменений ЗВП, то можно наблюдать преобладающее изменение, которое оказывается выраженным снижением амплитуды Р100, связанным с плохой модификацией латентности.[24]
Причиной сдавления зрительного нерва являются частые глиомы зрительного пути детского возраста. Клиническое начало характеризуется постепенной потерей зрения без болей в орбите, которые могут быть даже бессимптомными в течение длительного времени. Ранний клинический диагноз и точное последующее наблюдение за пациентами с компрессионной невропатией зрительного нерва, особенно при наличии менингиом или глиом, имеют принципиальное значение для улучшения терапевтического подхода, основанного на хирургической резекции и/или процедурах лучевой терапии [25]. ] В этих случаях PEV постоянно демонстрируют десинхронизированный P100 низкой амплитуды с очевидной латентной задержкой.
Что касается нейродегенеративных заболеваний, то ЗВП исследования обычно не играют диагностической роли. Однако эти методы тестирования могут дать возможность исследовать физио- и патофизиологические механизмы и участие различных систем нейротрансмиссии, участвующих в патогенезе этих патологических состояний, точным и неинвазивным способом.
Нейропатия зрительного нерва Лебера (LON) и доминантный неврит зрительного нерва типа Kjer (DON) являются наиболее распространенными наследственными формами первичной болезни ганглиозных клеток сетчатки. LON обычно представляет собой прогрессирующую потерю двустороннего зрения, не связанную с тканью орбиты и связанную с митохондриальными мутациями. В этих случаях заметно задерживаются P-VEP, но возможно относительное сохранение морфологии P100 на начальных стадиях заболевания.
Изменения амплитуды Р100 связаны со стадией и клинической формой заболевания. Изменениям P-PEV обычно предшествует снижение амплитуды или даже отсутствие воспроизводимости потенциала N95.
При атаксии Фридриха PEV используются для оценки развития зрительной функции при этом нейродегенеративном заболевании, которое имеет тенденцию быть ненормальным у двух третей пациентов. Замедленная латентность и увеличенная амплитуда волны р100 являются наиболее частыми электрофизиологическими изменениями при этой патологии.[28][29]]
Прочие вопросы
Хирургический интраоперационный мониторинг
В последние несколько лет ЗВП рассматривались для интраоперационного мониторинга зрительной функции с использованием нескольких протоколов; однако текущая литература и клинические данные в этой области очень ограничены. Использование тотальной внутривенной анестезии, внедрение светодиодной технологии, электроретинографии и электроэнцефалографии повысили надежность нейромониторинга ЗВП за счет улучшения воспроизводимости и интерпретируемости метода, а также работы над тем, чтобы сделать его более надежным и упростить его интеграцию в операционный процесс. .
.
В недавних исследованиях эти инструменты применялись в орбитальной и транссфеноидальной хирургии.[30][31][32] (См. рисунки интраоперационного хирургического мониторинга с помощью VEP)
Улучшение результатов медицинского персонала
Для применения VEP требуется межпрофессиональная команда медицинских работников, включая медсестер, техников нейрофизиопатологии, неврологов и офтальмологов. Эта команда имеет основополагающее значение для правильного применения этого инструмента как в клинической сфере, так и при интраоперационном хирургическом мониторинге. ЗВП регулярно используются при диагностике прехиазматических, хиазматических и ретрохиазматических неврологических патологий.[13] [Уровень 3]
В этом сценарии техник-нейрофизиопатолог обеспечивает подготовку и контроль инструментов оборудования, которым он оснащен, и полностью управляет сбором и оптимизацией различных диагностических методов, по которым, по запросу, он должен составить описательный отчет из технический аспект. (уровень I)
(уровень I)
Недавние исследования применяли ЗВП в орбитальной и транссфеноидальной хирургии, но без стандартизированных протоколов и однородных результатов.[30][31][32] [Уровень 3]
Межпрофессиональная команда, обеспечивающая комплексный подход к уходу за пациентами и всестороннее диагностическое управление, может помочь в достижении наилучших возможных результатов. Сотрудничество, междисциплинарное совместное принятие решений и открытое общение между членами команды являются ключевыми элементами для правильной диагностики и хорошего результата. Межпрофессиональная помощь, оказываемая пациенту, должна использовать комплексный подход в сочетании с научно обоснованным подходом к планированию и оценке всех совместных действий.[33] Чем раньше выявляются признаки и симптомы осложнения, тем лучше прогноз и исход. [Уровень 3]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.

Рисунок
Зрительные вызванные потенциалы (ЗВП) с использованием стимуляции в виде шахматной доски. Могут использоваться разные электроды, которые размещаются на коже головы. Прибор оснащен стимулятором для регулирования частоты и интенсивности световых раздражителей. Предоставлено (подробнее…)
Рисунок
Результаты паттерновых и импульсных зрительных вызванных потенциалов (ЗВП). Предоставлено Марко Цеппиери, доктором медицинских наук. Изображения предоставлены Элисой Экоретти и Джадой Паулетто, докторами медицины.
Рисунок
Подушечки для импульсной стимуляции, используемые для хирургического интраоперационного мониторинга. Результаты интраоперационных зрительных вызванных потенциалов (ЗВП). Предоставлено Марко Цеппиери, доктором медицинских наук. Изображения предоставлены Элисой Экоретти и Джадой Паулетто, докторами медицины.
Ссылки
- 1.
Hoffmann MB, Brands J, Behrens-Baumann W, Bach M.
 Оценка остроты зрения на основе ЗВП при слабом зрении. Док Офтальмол. 2017 декабрь; 135(3):209-218. [PubMed: 28980154]
Оценка остроты зрения на основе ЗВП при слабом зрении. Док Офтальмол. 2017 декабрь; 135(3):209-218. [PubMed: 28980154]- 2.
Гамильтон Р., Бах М., Генрих С.П., Хоффманн М.Б., Одом Дж.В., Маккалох Д.Л., Томпсон Д.А. VEP-оценка остроты зрения: систематический обзор. Док Офтальмол. 2021 фев; 142(1):25-74. [Бесплатная статья PMC: PMC7907051] [PubMed: 32488810]
- 3.
Patterson Gentile C, Joshi NR, Ciuffreda KJ, Arbogast KB, Master C, Aguirre GK. Влияние развития на паттерн зрительных вызванных потенциалов, характеризуемый анализом главных компонентов. Transl Vis Sci Technol. 2021 01 апр;10(4):1. [Бесплатная статья PMC: PMC8024780] [PubMed: 34003980]
- 4.
Zheng X, Xu G, Zhang K, Liang R, Yan W, Tian P, Jia Y, Zhang S, Du C. Оценка остроты зрения человека с использованием зрительного вызванного потенциала: обзор. Датчики (Базель). 28 сентября 2020 г., 20(19) [бесплатная статья PMC: PMC7582995] [PubMed: 32998208]
- 5.

Соареш Т.С., Сакаи П.Ю., Березовский А., Роча Д.М., Ватанабэ С.Е., Саломао С.Р. Зрительные вызванные потенциалы с обращением паттерна как инструмент диагностики глазной симуляции. Арк Брас Офтальмол. 2016 сен-октябрь;79(5):303-307. [PubMed: 27982208]
- 6.
Махаджан Ю., Чинг А., Уотсон Т., Ким Дж., Дэвис С. Влияние устойчивого избирательного внимания на стационарные зрительные вызванные потенциалы. Опыт Мозг Res. 2022 янв; 240(1):249-261. [PubMed: 34727219]
- 7.
Хасанкарими Х., Джафарзадехпур Э., Мохаммади А., Нури С.М.Р. Низкоконтрастный визуальный вызванный потенциал обращения паттерна в различных пространственных частотах. J Офтальмологический Vis Res. 2020 июль-сен;15(3):362-371. [Бесплатная статья PMC: PMC7431726] [PubMed: 32864067]
- 8.
Монтгомери Д.П., Хейден Д.Дж., Чалонер Ф.А., Кук С.Ф., Беар М.Ф. Пластичность селективной реакции на стимулы в первичной зрительной коре: прогресс и загадки.
 Передние нейронные цепи. 2021;15:815554. [PMC free article: PMC8841555] [PubMed: 35173586]
Передние нейронные цепи. 2021;15:815554. [PMC free article: PMC8841555] [PubMed: 35173586]- 9.
Ян М., Юнг Т.П., Хан Дж., Сюй М., Мин Д. [Обзор исследований алгоритмов декодирования стационарных зрительных вызванных потенциалов ]. Шэн У И Сюэ Гун Ченг Сюэ За Чжи. 2022 25 апреля; 39 (2): 416-425. [Бесплатная статья PMC: PMC9927346] [PubMed: 35523564]
- 10.
Котари Р., Сингх С., Сингх Р., Шукла А.К., Бокария П. Влияние угла зрения на изменение зрительных вызванных потенциалов. Оман Дж. Офтальмол. 2014 сен;7(3):120-5. [Бесплатная статья PMC: PMC4220397] [PubMed: 25378875]
- 11.
Dymond AM, Coger RW, Serafetinides EA. Предварительная обработка данных применялась к средней амплитуде зрительного вызванного потенциала P100-N140 человека, латентности и наклону. Психиатрия рез. 1980 декабрь; 3(3):315-22. [В паблике: 6936725]
- 12.
Ядав Н.К., Лудлам Д.П., Чуффреда К.Дж. Влияние различных конфигураций стимулов на зрительный вызванный потенциал (ЗВП).
 Док Офтальмол. 2012 июнь; 124(3):177-96. [PubMed: 22426575]
Док Офтальмол. 2012 июнь; 124(3):177-96. [PubMed: 22426575]- 13.
Park SH, Park CY, Shin YJ, Jeong KS, Kim NH. Низкоконтрастные визуальные вызванные потенциалы для раннего выявления неврита зрительного нерва. Фронт Нейрол. 2022;13:804395. [Бесплатная статья PMC: PMC9099025] [PubMed: 35572925]
- 14.
Тирунаву В.М., Мохаммад Л.М., Кандула В., Беструм М., Лам С.К. Результаты зрения для педиатрических пациентов с глиомами зрительного пути, связанными с нейрофиброматозом типа I: систематический обзор клинических данных. J Pediatr Hematol Oncol. 2021 01 мая; 43 (4): 135-143. [PubMed: 33480655]
- 15.
Leocani L, Guerrieri S, Comi G. Зрительные вызванные потенциалы как биомаркер рассеянного склероза и ассоциированного оптического неврита. J Нейроофтальмол. 2018 сен; 38 (3): 350-357. [В паблике: 30106802]
- 16.
Ван Ю, Ву ДЗ, Ву ЛЗ, Чен ЮЗ. Поле зрения в сравнении со зрительными вызванными потенциалами при макулопатиях и оптических нейропатиях.
 Ян Кэ Сюэ Бао. 1989 июнь; 5 (1-2): 52-9. [PubMed: 2485746]
Ян Кэ Сюэ Бао. 1989 июнь; 5 (1-2): 52-9. [PubMed: 2485746]- 17.
Юркуте Н., Робсон А.Г. Электрофизиология в нейроофтальмологии. Handb Clin Neurol. 2021;178:79-96. [PubMed: 33832688]
- 18.
Маркар В.Л., Баттегай Э., Шмидт Д., Читам М. Параллельная обработка в зрительной коре человека проявляется через влияние их нейронных реакций на зрительный вызванный потенциал. Видение Рез. 2022 апр;193:107994. [PubMed: 34979298]
- 19.
Эклунд А., Хуанг-Линк Ю., Ковачович Б., Дале С., Вретем М., Линд Дж. ОКТ и ВЭП коррелируют с инвалидностью при вторично-прогрессирующем рассеянном склерозе. Мульт Склер Релят Расстройство. 2022 дек;68:104255. [PubMed: 36544315]
- 20.
Oh J, Vidal-Jordana A, Montalban X. Рассеянный склероз: клинические аспекты. Карр Опин Нейрол. 2018 дек; 31 (6): 752-759. [PubMed: 30300239]
- 21.
де Сез Дж., Биго К. Диагностические критерии рассеянного склероза: от проблемы до пересмотренных критериев Макдональда 2017 года.
 Пресс Мед. 2021 июнь;50(2):104089. [PubMed: 34718114]
Пресс Мед. 2021 июнь;50(2):104089. [PubMed: 34718114]- 22.
Backner Y, Petrou P, Glick-Shames H, Raz N, Zimmermann H, Jost R, Scheel M, Paul F, Karussis D, Levin N. Видение и связанные с видением Меры при прогрессирующем рассеянном склерозе. Фронт Нейрол. 2019;10:455. [Бесплатная статья PMC: PMC6509148] [PubMed: 31130910]
- 23.
Барбано Л., Зиккарди Л., Паризи В. Корреляции между визуальными морфологическими, электрофизиологическими изменениями и изменениями остроты зрения при хронической неартериальной ишемической оптической нейропатии. Graefes Arch Clin Exp Офтальмол. 2021 май; 259(5):1297-1308. [PubMed: 33415352]
- 24.
Джаяраман М., Ганди Р.А., Рави П., Сен П. Мультифокальный зрительный вызванный потенциал при оптическом неврите, ишемической оптической нейропатии и компрессионной оптической нейропатии. Индийский Дж. Офтальмол. 2014 март; 62(3):299-304. [Бесплатная статья PMC: PMC4061667] [PubMed: 24088641]
- 25.

Дотто П.Ф., Березовский А., Сакаи П.Ю., Роча Д.М., Фернандес А.Г., Саломао С.Р. Оценка зрительных функций по зрительно-вызванным потенциалам у взрослых с орбитальными и другими первичными внутричерепными опухолями. Eur J Офтальмол. 2021 май; 31(3):1351-1360. [PubMed: 32468859]
- 26.
Боуман Р., Уолтерс Б., Смит В., Приз К.Л., Хэндли С.Э., Грин К., Манкад К., О’Хара П., Даль С., Йоргенсен М., Опочер Э., Харгрейв Д. , Томпсон Д.А. Зрительные исходы и предикторы глиомы зрительного пути: исследование в одном центре. Глаз (Лонд). 2022 13 мая; [В паблике: 35562551]
- 27.
Табакару Б., Станка Х.Т. Дальнейшие достижения в диагностике и лечении наследственной оптической нейропатии Лебера — обзор. Ром Дж. Офтальмол. 2022 г., январь-март; 66(1):13-16. [Бесплатная статья PMC: PMC
47] [PubMed: 35531455]- 28.
Ziccardi L, Cioffi E, Barbano L, Gioiosa V, Falsini B, Casali C, Parisi V. Функциональная оценка макулярных морфо-функциональных и зрительных путей у пациентов со спиноцеребеллярной атаксией 1 типа с неврологическими симптомами или без них.
 Дж. Клин Мед. 2021 12 ноября; 10 (22) [бесплатная статья PMC: PMC8625180] [PubMed: 34830553]
Дж. Клин Мед. 2021 12 ноября; 10 (22) [бесплатная статья PMC: PMC8625180] [PubMed: 34830553]- 29.
Родригес-Лабрада Р., Веласкес-Перес Л., Ортега-Санчес Р., Пенья-Акоста А., Васкес-Мохена Ю., Каналес-Очоа Н., Медрано-Монтеро Х., Торрес-Вега Р., Гонсалес- Залдивар Ю. Взгляд на снижение когнитивных функций при спиноцеребеллярной атаксии 2 типа: исследование потенциала мозга, связанное с событием P300. Атаксия мозжечка. 2019;6:3. [Бесплатная статья PMC: PMC6399884] [PubMed: 30873287]
- 30.
MacDonald DB, Dong CC, Uribe A. Интраоперационные техники вызванных потенциалов. Handb Clin Neurol. 2022;186:39-65. [PubMed: 35772897]
- 31.
Zhu H, Qiao N, Yang X, Li C, Ma G, Kang J, Liu C, Cao L, Zhang Y, Gui S. Клиническое применение интраоперационных визуальных вызванных потенциал при рецидивирующих краниофарингиомах, удаленных расширенной эндоскопической эндоназальной хирургией. Клиника Нейрол Нейрохирург. 2022 март; 214:107149.







 Оценка остроты зрения на основе ЗВП при слабом зрении. Док Офтальмол. 2017 декабрь; 135(3):209-218. [PubMed: 28980154]
Оценка остроты зрения на основе ЗВП при слабом зрении. Док Офтальмол. 2017 декабрь; 135(3):209-218. [PubMed: 28980154]
 Передние нейронные цепи. 2021;15:815554. [PMC free article: PMC8841555] [PubMed: 35173586]
Передние нейронные цепи. 2021;15:815554. [PMC free article: PMC8841555] [PubMed: 35173586] Док Офтальмол. 2012 июнь; 124(3):177-96. [PubMed: 22426575]
Док Офтальмол. 2012 июнь; 124(3):177-96. [PubMed: 22426575] Ян Кэ Сюэ Бао. 1989 июнь; 5 (1-2): 52-9. [PubMed: 2485746]
Ян Кэ Сюэ Бао. 1989 июнь; 5 (1-2): 52-9. [PubMed: 2485746] Пресс Мед. 2021 июнь;50(2):104089. [PubMed: 34718114]
Пресс Мед. 2021 июнь;50(2):104089. [PubMed: 34718114]
 Дж. Клин Мед. 2021 12 ноября; 10 (22) [бесплатная статья PMC: PMC8625180] [PubMed: 34830553]
Дж. Клин Мед. 2021 12 ноября; 10 (22) [бесплатная статья PMC: PMC8625180] [PubMed: 34830553] [PubMed: 35151969]
[PubMed: 35151969]