Нейтропения у детей — Доказательная медицина для всех
Что такое нейтропения?
Нейтропения — это состояние, при котором в периферической крови человека снижается количество нейтрофилов (подкласса лейкоцитов, белых кровяных клеток) ниже определенной нормы. Обратите внимание, что речь идет об абсолютном числе нейтрофилов, а не об относительных единицах (не о процентах). Нередко бывает так, что по процентам нейтрофилов маловато, родителей это пугает, однако при пересчете в абсолютные числа оказывается, что нейтрофилов — совершенно нормальное количество. Как посчитать абсолютное количество нейтрофилов — мы доступно расскажем чуть ниже.Чем опасна нейтропения?
Нейтрофилы — это клетки крови, отвечающие за борьбу с бактериальной инфекцией, а значит, чем ниже уровень нейтрофилов, тем выше риск возникновения, и/или тяжелого течения бактериальных инфекций у человека. Однако этот риск начинает повышаться только при значительном снижении количества нейтрофилов, поэтому нельзя говорить что нейтропения однозначно приводит к частым бактериальным инфекциям.Как выявляется нейтропения?
При рецидивирующих инфекциях, скажем, фурункулезе, упорном импетиго, или повторных средних отитах — врач может заподозрить снижение защитных функций организма, и назначить общий анализ крови (ОАК) с целью посмотреть уровень нейтрофилов. Но чаще всего нейтропения обнаруживается совершенно случайно, при сдаче ОАК по иному поводу, например, при плановом диспансерном обследовании ребенка 1го года жизни.Где именно в ОАК указано количество нейтрофилов?
Если бланк старого образца (такие обычно пишут, когда лейкоцитарную формулу в ОАК считают «вручную», под микроскопом), то на обороте бланка Вы увидите такую картину:
Здесь лейкоциты — абсолютное число, а эозинофилы, нейтрофилы, лимфоциты и моноциты — относительные, то есть проценты от общего количества лейкоцитов. Именно поэтому их сумма всегда равняется 100. То есть в этом анализе 23% нейтрофилов. Чтобы оценить абсолютное количество — составим простую пропорцию. Всего лейкоцитов 8,3 Г/лэто 100%
Из них нейтрофилов — 23%
8,3 = 100%
х = 23%
Произведение крайних членов пропорции всегда равно произведению средних. А значит:
х = (23*8,3)/100
х = 1,9 Гл
Удобнее смотреть на нейтрофилы, переведя их в «клетки на микролитр крови», то есть умножив на 1000.
1,9 Гл = 1900 кл/мкл
Если же у Вас перед глазами бланк из автоанализатора, но в нем нейтрофилы уже посчитаны автоматически, как в относительных величинах (в процентах), так и в абсолютных:

Лейкоцитов (белых кровяных клеток, white blood cells, WBC) здесь 4,2 Гл, из них 42,8% — нейтрофилов. Это 1,8 Гл, или 1800 кл/мкл нейтрофилов.

Здесь лейкоцитов 12,3 Гл
Нейтрофилов 48,7%, то есть 6000 кл/мкл
Обратите внимание, что в данных примерах (1 и 2) указанные нормы относятся ко взрослому человеку, и не подходят к детям. Так бывает нередко. Поэтому не пытайтесь ориентироваться на нормы на бланке, не посоветовавшись с врачом, даже если автоанализатор пометил их стрелочкой вниз (↓) или звездочкой (*).
Каковы нормы нейтрофилов в периферической крови ребенка?
Сайт emedicine.com дает следующие нормы:Перевод:
Нормы нейтрофилов у детей отличаются от взрослых норм. У младенцев в возрасте от 2 недель до 1 года нижний предел нормального количества нейтрофилов составляет 1000 кл/мкл. У детей старше первого года жизни, как и у взрослых, нижний предел составляет 1500 кл/мкл.Степень тяжести нейтропений у детей старше года, и у взрослых, рассчитывают так:
* выше 1500 кл/мкл — норма
* от 1500 до 1000 кл/мкл — легкая степень нейтропении
* от 1000 до 500 кл/мкл — средняя степень нейтропении
* от 500 до 100 кл/мкл — тяжелая степень нейтропении
* при тяжелой степени нейтропении рассчитывается общее количество гранулоцитов в абсолютных числах (нейтрофилы + базофилы + эозинофилы), и если оно ниже 100 кл/мкл — состояние называется агранулоцитоз.
У детей младше года — эти цифры на треть ниже.
Каковы причины нейтропении у детей?
Наиболее частая причина — это доброкачественная нейтропения детского возраста. В этом случае она совершенно не опасна, и проходит за несколько месяцев или несколько лет. Обычно никак себя не проявляет, а значит — не требует никакого лечения, никаких ограничений в быте, диете или вакцинации. Но об этом — чуть ниже. Реже — нейтропения может вызываться приемом некоторых лекарств. Антибиотики (особенно левомицетин), жаропонижающие препараты (особенно анальгин) и многие другие препараты способны вызывать временное (на несколько месяцев) снижение уровня нейтрофилов. Ну и, разумеется, к нейтропении часто приводят препараты, применяемые для лечения злокачественных опухолей и/или препараты, назначаемые после трансплантации органов. Гораздо реже — нейтропения может быть симптомом заболеваний крови, и требовать активного лечения. В случаях, когда нейтропения сопровождается рецидивирующими упорными инфекциями, и/или количество нейтрофилов падает ниже 500-100 кл/мкл — требуется консультация гематолога, для исключения этих редких, но серьезных заболеваний.Если у моего ребенка нейтропения — значит он беззащитен перед болезнетворными бактериями?
Не совсем так. Обычно у нас нейтрофилов «с запасом». Если их количество упадет ниже нормы, но не до критических цифр (не ниже 100 кл/мкл) то у ребенка увеличивается риск бактериальных инфекций. Но это вовсе не значит, что этот риск обязательно реализуется.А если цифры нейтрофилов ниже 100 кл/мкл?
Это довольно опасно. Такие дети требуют особого контроля и изоляции от всякой инфекции. Но даже при таких низких цифрах если ребенок внешне здоров — ему не требуется профилактической антибиотикотерапии, или иных агрессивных мер. В подавляющем большинстве случаев критично тяжелая нейтропения длится всего несколько дней или недель, затем цифры вновь возрастают, без всякого лечения.Как я могу помочь своему ребенку, как ускорить увеличение уровня нейтрофилов?
Никак. То есть, разумеется, есть препараты, увеличивающие количество нейтрофилов, но назначаются они только гематологом, и только при тех заболеваниях, которые мы с Вами выше назвали термином «гораздо реже».
Обычная аутоиммунная доброкачественная нейтропения, или, скажем, циклическая нейтропения — не требуют лечения совсем. Лекарственная нейтропения требует только отмены лекарства, которое ее вызвало.
Но почему бы все же не назначить препарат для увеличения нейтрофилов, раз у ребенка с нейтропенией есть высокий риск бактериальных инфекций?
Лекарства — это не конфеты. Врач исходит из того, что всякое лечение — приносит вред. Если вред от лечения больше, чем вред от выжидательной тактики — лечение не назначается. Доброкачественная нейтропения — классический тому пример. Поэтому обычно мы ждем и наблюдаем, и этого достаточно, и все проходит само.
Вот если гематолог подтвердит у ребенка серьезное заболевание, проявляющееся нейтропенией, например, синдром Костманна, то специфическое лечение будет оправданным, оно будет неизбежным и пожизненным.А помогают ли при нейтропении народные методы? Гомеопатия? Иглоукалывание?
Нет.
А что такое агранулоцитоз, и как он связан с нейтропенией?
Агранулоцитоз — это, если немного упростить, крайняя степень нейтропении. Дословно агранулоцитоз означает отсутствие, или чрезвычайно низкое содержание в периферической крови гранулоцитов. Гранулоциты — это лейкоциты, которые при окрашивании под микроскопом имеют «гранулы» или «зернистость» при их рассмотрении. Все лейкоциты делятся на гранулоциты и агранулоциты (имеющие и не имеющие «гранулы»). К гранулоцитам относятся не только нейтрофилы, но и базофилы, и эозинофилы (см «старый» бланк анализа ОАК выше). Агранулоцитоз ставится в том случае, если общее количество гранулоцитов в крови не превышает 100 кл/мкл (по другим источникам — 500 кл/мкл). Агранулоцитоз — опасное состояние, и обязательно требует консультации гематолога.Мы сдали ОАК ребенку перед плановой вакцинацией, педиатр выявил нейтропению и на этом основании отложил ребенку вакцинацию. Правильно ли это?
На этот вопрос не получится ответить коротко.
Сперва отметим, что сдавать анализы перед прививками — совершенно бессмысленно и даже вредно. Как, например, вредно сдавать мочу на посев у ребенка, не имеющего симптомов. Потому что есть такая штука, как бессимптомная бактериурия, и если даже посев мочи покажет, что моча не стерильна — это не потребует лечения.
Однако выделение бактерий с мочой встревожит родителей, и у них, а иногда даже у врача, начнут «чесаться руки» дать ребенку антибиотик — что с точки зрения современной медицины совершенно бессмысленно. Поэтому в современных международных рекомендациях врачам запрещается сдавать посев мочи ребенку, не имеющему симптомов ИМВП. Точно также и с анализами перед прививкой. Если ребенокЕще один довод против сдачи анализов без показаний: анализы иногда делают неверно. И тогда они уж точно вызывают беспричинное беспокойство и необоснованное лечение.
Ну, и последнее об этом: Вам следует знать, что не существует никаких приказов, которые требовали бы сдавать какие-либо анализы, и проходить какие-либо консультации врачей (кроме педиатра) перед прививкой. Повсеместно распространенная практика «сдайте ОАК, ОАМ и консультацию невролога перед прививкой» — это или ненужная перестраховка, или местечковая необоснованная традиция, или откровенное выколачивание денег из пациента.
Теперь по сути.
С точки зрения доказательной медицины, общепризнанных современных подходов, нейтропения легкой и средней тяжести — не является поводом для откладывания иммунизации. При определенных условиях врач может отложить только введение живых вакцин, например MMR (корь + эпидпаротит + краснуха).
С точки зрения российской медицины все иначе. Бытует мнение, что нейтропения ниже 800 кл/мкл — это временное противопоказание к вакцинации. Это мнение кочует из учебника в учебник, из статьи в статью, например:
Профилактические прививки проводятся по возрасту при абсолютном числе нейтрофилов более 800 в 1 мкл (источник). Вакцинация детей до года с ХДНДВ возможна при уровне нейтрофилов выше 800 клеток в 1 мкл, детей старше года — не менее 1000 клеток в 1 мкл (источник).5.9. Неправомерен отказ от вакцинации ребенка без соответствующей клинической картины, у которого выявлены отклонения показателей иммунного статуса, не достигающих уровней, характерных для конкретного иммунодефицитного состояния. Нерезкое снижение уровней сывороточных иммуноглобулинов, изменения в соотношении субпопуляций лимфоцитов, снижение численности Т-клеток и т.д. закономерно возникают при различных заболеваниях и состояниях, не достигая пороговых уровней и не сопровождаясь соответствующими клиническими проявлениями.
Что тут можно сказать?
Ни для кого не секрет, что российская медицина все больше отстает от медицины развитых стран. Ни для кого не секрет, что юридически врач в России почти никак не защищен от негодующего пациента. Итогом всего этого является «хронический перестраховочный подход» наших врачей.
Если врач не привьет Вашего ребенка из-за нейтропении — это ничем ему не грозит, как минимум. А как максимум — Вы даже сочтете его отличным врачом, мол — вот другие привили бы, а этот с «индивидуальным подходом», сразу видно что заботится о детях, не для галочки прививает. Если даже такой ребенок, скажем, заболеет коклюшем из-за того, что АКДС-вакцинация была отложена ради нейтропении — врачу ничего не будет. Он сошлется на «научные» статьи, где сказано про «ниже 800 — не прививать» и к нему ни один юрист не придерется.
А вот если врач привьет вашего ребенка, то при неудачном стечении обстоятельств, несмотря на вышеупомянутый приказ, он рискует остаться крайним. Поди докажи потом, что это не из-за прививки у ребенка развился агранулоцитоз, хотя на момент прививки нейтропения была вполне безобидной. Понимаете, перед каким выбором оказывается врач? Ну и что, по-Вашему, должно заставить его идти на риск?
Поэтому или ищите другого врача, который более смел, доверяет Вам и не станет откладывать вакцинацию «на всякий случай». Или смиритесь, и ждите пока нейтрофилы поднимутся выше 800 клеток.
Где я могу получить более подробную информацию об этой проблеме?
Выше были приведены пара ссылок на сайт emedicine.com, они дают вполне исчерпывающую информацию, достаточную даже врачу. Помимо этого Вы можете прочесть, например, эту статью:Статья на английском, поэтому хочется перевести несколько наиболее интересных абзацев для людей, не владеющих английским языком перевод:
У детей с нейтропенией (прим.перев) важно соблюдать ежедневную гигиену полости рта и регулярно обращаться к стоматологу для профилактического осмотра, особенно при хронических и длительных формах нейтопении. Это позволит избежать хронических заболеваний десен или зубной инфекции.
Важен также хороший уход за кожей и быстрая антисептическая обработка поверхностных порезов, ссадин и любых повреждений кожных покровов. Вакцинация детей с нейтропениями не только возможна, но и более актуальна, нежели у обычных детей. График вакцинации никак не изменяется, если нейтропения не связана с иммунодефицитным синдромом.
Детям, которые имеют нарушенную функцию Т- или B-лимфоцитов, не следует вводить живые или ослабленные вакцины.
Посещение детского сада или школы не противопоказано большинству детей с легкой или среднетяжелой нейтропенией, хотя контакта с явно больными детьми все же следует избегать. Дети с тяжелой степенью нейтропении или тяжелыми бактериальными инфекциями в анамнезе на фоне нейтропении — нуждаются в изоляции, дабы избежать встречи с инфекционными агентами.…Вместо постскриптума. Завершая нашу статью, еще раз подчеркнем: если у Вашего ребенка нейтропения — не впадайте в панику. У врачей есть поговорка «редкие болезни — бывают редко». Держите руку на пульсе, контролируйте ОАК через интервалы, которые посоветует врач, обсудите с врачом лекарства, которые принимает ребенок, и откажитесь от тех лекарств, которые врач сочтет подозрительными в плане причины нейтропении. Этого, скорее всего, будет вполне достаточно.
В практике педиатра дети раннего возраста с нейтропениями встречаются ежемесячно. При этом злокачественные причины нейтропений педиатры видят всего несколько штук за жизнь. Например, я видел пациента с синдромом Костманна один раз в жизни, а деток без всяких симптомов болезней, но с нейтропенией в ОАК — сотни.
Были детки и с 400кл/мкл, и даже с 120 кл/мкл нейтрофилов. Наблюдали, иногда — откладывали вакцинацию, восстанавливались за 2-5 месяцев и продолжали прививаться и жить как жили. Даже к гематологу не всегда направлял. Потому что чаще всего — это совершенно безобидное состояние, которое проходит само.
Врожденные нейтропении — причины, симптомы, диагностика и лечение

Врожденные нейтропении – это группа генетически детерминированных заболеваний, которые характеризуются снижением уровня нейтрофильных лейкоцитов ниже 1500/мкл, а у детей до 1 года – ниже 1000/мкл. Клинически это проявляется частными бактериальными инфекциями, задержкой в психофизическом развитии. Наиболее распространенным признаком врожденных нейтропений являются частые гингивиты и стоматиты. Диагноз выставляется на основании анамнеза, данных осмотра, общего анализа крови и миелограммы. Тактика лечения зависит от формы патологии. Для стимуляции синтеза нейтрофильных гранулоцитов применяется гранулоцитарный колониестимулирующий фактор (Г-КСФ).
Общие сведения
Врожденные нейтропении – это группа наследственных патологий, которые передаются по аутосомно-доминантному или аутосомно-рецессивному типу и проявляются уменьшением количества нейтрофилов в периферической крови. Все заболевания, входящие в эту группу, были описаны в ХХ веке: синдром Костмана – в 1956 году, семейная доброкачественная нейтропения – в 1939 году, циклическая нейтропения – в 1910 году, синдром «ленивых лейкоцитов» – в 1964 году. Встречаются данные патологии редко. Распространенность колеблется от 1-2:100000 до 1 случая на 1 млн. младенцев. Врожденными нейтропениями с одинаковой частотой болеют как мальчики, так и девочки. Прогноз зависит от формы заболевания, при синдроме Костмана летальность достигает 97-100%, в то время как при семейной доброкачественной нейтропении исход, как правило, благоприятный.

Врожденные нейтропении
Причины врожденных нейтропений
Врожденные нейтропении – это генетически обусловленные заболевания, которые наследуются по аутосомно-доминантному или аутосомно-рецессивному типу. Синдром Костмана проявляется мутацией в гене ELA2, находящемся на 19р13.3. Данный ген кодирует фермент – нейтрофильную эластазу. Точная роль ее неизвестна, но, вероятнее всего, при ее дефекте у нейтрофилов еще в костном мозге запускается процесс апоптоза. Реже данная патология может быть вызвана дефектами генов GFII и 6-CSFR, кодирующих фактор активации эластазы нейтрофилов и рецепторы к гранулоцитарно-макрофагальному колониестимулирующему фактору. Циклическая врожденная нейтропения также развивается на фоне мутации ELA2, однако, апоптоз при данной форме проходит не так интенсивно, что обеспечивает менее выраженный дефицит нейтрофилов. Эти две формы врожденных нейтропении наследуются по аутосомно-рецессивному типу.
Синдром «ленивых лейкоцитов» возникает на фоне нарушения процесса выхода гранулоцитов из костного мозга в системный кровоток. Патогенез данной формы врожденной нейтропении основывается на мутации белка, кодирующего клеточную мембрану нейтрофилов, а также их ускоренном апоптозе. При семейной доброкачественной нейтропении у детей нарушается процесс дифференциации гранулоцитов в костном мозге – нейтрофилы остаются на стадии метамиелоцитов. Также существует целый ряд врожденных синдромов, одним из проявлений которых является уменьшение количества нейтрофильных лейкоцитов. Сюда относятся синдром гипер-IgM, ретикулярная дисгенезия, синдром Чедиака-Хигаси, синдром Швахмана-Даймонда, Барта и др.
Классификация врожденных нейтропений
В педиатрии нейтропении разделяются на врожденные и приобретенные формы. К врожденным относятся:
- Синдром Костмана. В основе заболевания лежит ранний апоптоз и отсутствие в периферической крови зрелых форм нейтрофильных лейкоцитов. В костном мозге определяются пролиферирующие клетки до миелоцитов. Характеризуется тяжелой клинической картиной уже на первых месяцах жизни.
- Циклическая нейтропения. Данная форма врожденной нейтропении проявляется недостаточным гранулоцитопоэзом, который имеет повторяющийся характер. Клинические симптомы возникают одновременно с эпизодами агранулоцитоза.
- Семейная доброкачественная нейтропения. В основе этой формы врожденной нейтропении лежит нарушение дозревания нейтрофильных гранулоцитов. Клинически проявляется редко. Специфического лечения не требует.
- Синдром «ленивых лейкоцитов». Суть заболевания заключается в нарушении хемотаксиса нейтрофилов. Проявляется частыми воспалительными заболеваниями уже с младенчества.
Симптомы врожденных нейтропений
Клинические картины различных форм врожденной нейтропении имеют как общие аспекты, так и определенные различия. При всех видах часто возникают воспалительные заболевания органов, тесно контактирующих с внешней средой и наиболее чувствительных к ослаблению иммунной системы. Сюда относятся кожа, слизистая оболочка рта, трахеобронхиальное дерево, легкие, внешнее и среднее ухо. Также почти всегда присутствуют астеновегетативный и интоксикационный синдромы. Однако возраст, в котором манифестирует врожденная нейтропения, частота и степень тяжести обострений могут существенно варьировать.
Синдром Костмана характеризуется выраженной симптоматикой уже в первые месяцы жизни ребенка. Первичные признаки – лихорадка неясной этиологии, частые бактериальные заболевания кожи и подкожной жировой клетчатки (фурункулы, флегмоны). У таких детей медленно заживают пупочные ранки, плохо поддается лечению омфалит. Может наблюдаться задержка в психическом и физическом развитии. Постепенно присоединяются гепатоспленомегалия и лимфаденопатия. Характерный признак врожденной нейтропении – поражение слизистых оболочек рта и десен (гингивит и стоматит). При синдроме Костмана также отмечаются рецидивирующие пневмонии, абсцессы легких, циститы, отиты, уретриты, пиелонефриты, гастродуодениты, парапроктиты, перитониты и т. д. Все перечисленные патологии склонны к генерализации, что без раннего лечения приводит к развитию сепсиса и смерти.
Циклическая нейтропения проявляется в возрасте до 1 года. Также характеризуется поражением кожи, внешнего уха, слизистых оболочек рта и десен. Типичной особенностью данной формы врожденной нейтропении является периодичность рецидивов. Обострения могут возникать каждые 14-49 дней, зачастую – каждые 3 недели. В тяжелых случаях, особенно при инфицировании анаэробной микрофлорой, развиваются тяжелые осложнения в виде перитонита и сепсиса, однако их вероятность значительно меньше, чем при синдроме Костмана. С возрастом частота и тяжесть рецидивов снижаются.
Семейная доброкачественная нейтропения проявляется в возрасте от 2-3 месяцев до 1 года. В клинической картине этой врожденной нейтропении превалируют редкие гингивиты и стоматиты, фурункулез. Еще реже встречаются отиты и поражения легких. Перечисленные заболевания, как правило, протекают в легкой форме, общее состояние ребенка нарушено мало. Клиническая картина синдрома «ленивых лейкоцитов» наблюдается уже на первых месяцах жизни. Наиболее часто у пациентов диагностируются бактериальные поражения верхних дыхательных путей (ларингиты, фарингиты, трахеиты), пневмонии, гингивиты и стоматиты.
Диагностика врожденных нейтропений
Диагностика врожденных нейтропений основывается на сборе анамнестических данных, физикальном обследовании, результатах лабораторных и инструментальных исследований. Из анамнеза педиатром или неонатологом обязательно устанавливается наличие подобных наследственных заболеваний у родителей или других родственников. Физикальное обследование может выявить умеренное отставание в физическом развитии, лимфаденопатию, гепатоспленомегалию. При развитии бактериальных осложнений будут обнаруживаться другие специфические изменения.
Основа диагностики врожденных нейтропений – общий анализ крови и миелограмма. В ОАК определяется снижение уровня лейкоцитов ниже 4,5х109/л, а нейтрофильных гранулоцитов – до 1000/мкл и ниже у грудных детей и до 1500/мкл и ниже у детей старше 1 года. Врожденные нейтропении почти всегда сопровождаются моноцитозом и эозинофилией. В зависимости от формы уровень нейтрофилов может варьировать, как и изменения в костном мозге при его пункции. В миелограмме при синдроме Костмана выявляются только клетки-предшественники нейтрофилов – миелобласты, промиелоциты, миелоциты.
Циклическая нейтропения также проявляется отсутствием зрелых форм, однако при повторных тестах может обнаруживаться лейкоцитоз. Миелограмма при семейной доброкачественной нейтропении характеризуется большим числом метамиелоцитов и дефицитом зрелых нейтрофилов. Синдром «ленивых лейкоцитов» проявляется чрезмерным насыщением костного мозга клетками всех этапов дифференциации, в том числе и зрелыми. Другие изменения в лабораторных или инструментальных тестах соответствуют возникшим осложнениям врожденных нейтропений.
Лечение врожденных нейтропений
Лечение врожденных нейтропений зависит от формы патологии. Основу терапии составляет гранулоцитарный колониестимулирующий фактор (Г-КСФ). Данный гормональный препарат стимулирует синтез и дифференциацию нейтрофильных гранулоцитов в костном мозге. При синдроме Костмана и условии отсутствия генной мутации Г-КСФ применяется пожизненно. Также при данной форме врожденной нейтропении может проводиться пересадка костного мозга. При циклической нейтропении Г-КСФ назначается за 2-3 дня до развития агранулоцитоза. Доброкачественная семейная нейтропения и синдром «ленивых лейкоцитов», как правило, не требуют использования Г-КСФ за исключением тяжелых форм.
При развитии бактериальных осложнений на фоне врожденной нейтропении осуществляется массивная антибактериальная терапия. Как правило, назначаются антибиотики широкого спектра действия – цефалоспорины III-IV поколения, макролиды. В тяжелых случаях могут применяться внутривенные иммуноглобулины. При необходимости проводят дезинтоксикационную терапию, по показаниям используют симптоматические средства.
Прогноз и профилактика врожденных нейтропений
Прогноз при разных формах врожденных нейтропений различается. При синдроме Костмана большинство детей умирают от тяжелых, резистентных к лечению бактериальных осложнений на протяжении первых месяцев жизни. Циклическая нейтропения и синдром «ленивых лейкоцитов» имеют более благоприятный прогноз – летальный исход возможен только при тяжелых вариантах течения и отсутствии своевременной диагностики. Семейная доброкачественная нейтропения в большинстве случаев не приводит к смерти ребенка – с возрастом число нейтрофилов возрастает, иммунитет стабилизируется.
Специфической профилактики врожденных нейтропений не существует. Неспецифические превентивные меры включают в себя оценку риска развития генетических мутаций у ребенка еще до его рождения путем медико-генетического консультирования. Данное обследование можно пройти у врача-генетика в специализированных центрах. Уже беременным женщинам проводят кордоцентез, амниоцентез, плаценто- или хориоцентез с последующим кариотипированием. С целью профилактики спонтанных мутаций, которые также могут сопровождаться врожденными нейтропениями, на период беременности следует полностью исключить воздействие всех тератогенных факторов на плод. В их число входят алкоголь, наркотики, табачные изделия, химикаты, ионизирующее излучение, некоторые медикаменты и др.
что это такое, таблица по возрасту, причины, симптомы, лечение
При нейтропении у детей в крови снижается уровень нейтрофилов. При общем анализе крови указывают общее количество лейкоцитов – абсолютное число защитных клеток. При развернутом отдельно рассчитывают уровень их подклассов – моноцитов, эозинофилов, лимфоцитов, нейтрофилов.
Для чего нужны нейтрофилы
 Задача всех лейкоцитов – защищать организм от внедрения патогенных возбудителей. Нейтрофилы синтезируются в красном костном мозге в среднем 14 дней. После поступления в кровоток они активны в течение 6 часов и отвечают за неспецифический иммунитет при внедрении патогенной флоры. Если на своем пути клетки обнаруживают болезнетворного возбудителя, они фиксируются на его поверхности, выделяют токсические вещества, поглощают, уничтожают бактерию.
Задача всех лейкоцитов – защищать организм от внедрения патогенных возбудителей. Нейтрофилы синтезируются в красном костном мозге в среднем 14 дней. После поступления в кровоток они активны в течение 6 часов и отвечают за неспецифический иммунитет при внедрении патогенной флоры. Если на своем пути клетки обнаруживают болезнетворного возбудителя, они фиксируются на его поверхности, выделяют токсические вещества, поглощают, уничтожают бактерию.
Один нейтрофил может уничтожить до 25 бактериальных клеток. В норме защитные клетки через 6 часов мигрируют в печень, селезенку, где погибают, их сменяет новая порция клеток из костного мозга. Если она уничтожилась после поглощения бактерий, в кровь выделяются специальные вещества, которые усиливают синтезирование нейтрофилов в костном мозге, ускоряют выход в кровь незрелых нейтрофилов.
Данный процесс отражается на анализ крови – количество юных клеток увеличивается (лейкоцитарный сдвиг влево), что говорит о снижении нейтрофилов. После гибели защитной клетки в кровь выделяются ферменты, привлекающие другие лейкоцитарные клетки. Разрушенные нейтрофилы, патогенные возбудители образуют гной зеленоватого оттенка за счет наличия в нейтрофилах миелопероксидазы.
Важно!Нейтрофилы действуют преимущественно на бактерии, грибы, в отношении вирусных агентов их активность выражена слабо.
Показатели нормы
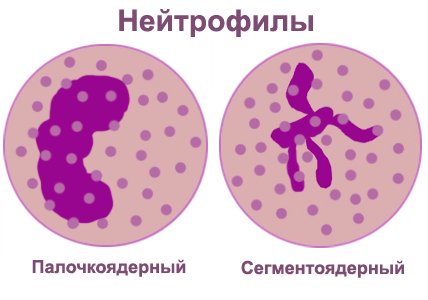
В лейкоцитарной формуле при анализе крови указывают 2 вида нейтрофилов: палочкоядерные (молодые), сегментоядерные (зрелая форма, которая преобладает над другими клетками). В анализе крови их количество указывают в процентах.
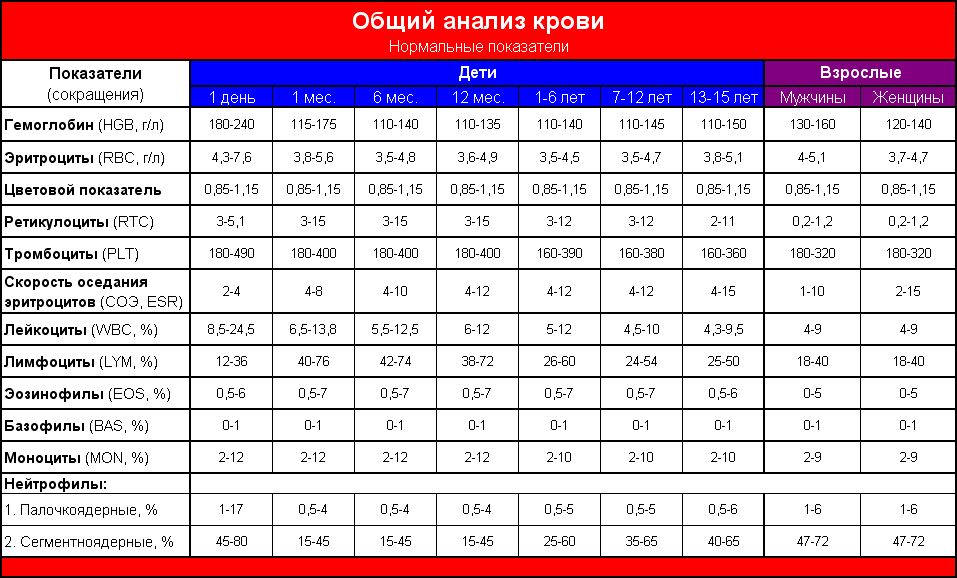
| Возраст | Палочкоядерные | Сегментоядерные |
| 1 сутки | 5-11 | 50-70 |
| 1-5 сутки | 1-6 | 34-55 |
| 5-10 сутки | 1-5 | 25-45 |
| 1 месяц | 1-5 | 18-30 |
| 1 год | 1-4 | 18-25 |
| 1-5 лет | 1-4 | 25-55 |
| 5-10 лет | 1-4 | 25-40 |
| старше 10 лет | 1-4 | 30-45 |
Снижение их количества называется нейтрофильной лейкопенией (нейтропения), повышение – нейтрофильным лейкоцитозом (нейтрофилия).
Причины, формы состояния
 Нейтропения у детей до года считается циклическим состоянием. В младенческом возрасте показатель клеток снижается, повышается – патологическим состоянием это не считается. К трем годам показатели окончательно стабилизируются, приходят в состояние нормы. Исключение составляют случаи, когда уровень клеток снижается в 2 и более раз.
Нейтропения у детей до года считается циклическим состоянием. В младенческом возрасте показатель клеток снижается, повышается – патологическим состоянием это не считается. К трем годам показатели окончательно стабилизируются, приходят в состояние нормы. Исключение составляют случаи, когда уровень клеток снижается в 2 и более раз.
Причины снижения нейтрофилов:
- инфекционные болезни: грипп, ветряная оспа, корь, краснуха, гепатит, бруцеллез, брюшной тиф и другие;
- лечение антибактериальными, противовирусными препаратами;
- болезни крови: лейкоз, апластическая анемия и др.;
- химио-, радиотерапия;
- дефицит витамина В12, фолиевой кислоты;
- повышение уровня гормонов щитовидной железы;
- грибковые инфекции;
- опухоли.
В зависимости от уровня клеток в крови выделяют три степени тяжести: легкую, среднюю, тяжелую.
В основу классификации положен механизм развития состояния:
- Аутоиммунная нейтропения. Возникает при выработке антител против нейтрофилов. Процесс развивается при аутоиммунных заболеваниях либо выработка антител протекает изолированно.
- Лекарственная – на фоне приема препаратов, имеющих токсическое действие в отношении нейтрофилов: антибиотики (цефалоспорины, пенициллины), нейролептики, антиконвульсанты, противосудорожные. После химиотерапии угнетается синтезирование клеток в красном костном мозге, в том числе и нейтрофилов.
- Инфекционная. Связана с проникновением в организм инфекционных возбудителей.
- Врожденная – группа генетических болезней связанных со снижением уровня нейтрофилов.
- Фебрильная (нейтропеническая лихорадка) – опасное состояние, сопровождающееся высокой температурой, интоксикацией, быстрым распространением инфекции по организму. Чаще возникает на фоне приема цитостатиков по поводу онкологических заболеваний.
Также выделяют доброкачественную нейтропению у детей – хроническая форма состояния, которая не проявляется клиническими симптомами. Чаще связана с развитием костного мозга у детей до года.
Симптомы
Проявление нейтропении зависит от степени снижения клеток. При легкой – симптомов не наблюдается. Выявляют ее случайно при лабораторном анализе по поводу заболеваний или на профилактическом обследовании. Незначительное отклонение показателя от нормы может быть связано с перенесенным бактериальным, вирусным заболеванием. При циклической нейтропении симптомов не наблюдается, показатель понижается или повышается на 8-10 дней, затем приходит в норму. При данных формах иммунная защита снижается, поэтому дети склонны к гриппу, ОРВИ.
При средней форме организм ослаблен, его устойчивость к грибковым, бактериальным, вирусным инфекциям снижается. У детей часто повышается температура, возникают воспалительные процессы в полости рта (стоматит, гингивит и др.). При отсутствии лечения, на фоне инфекций уровень нейтрофилов прогрессивно снижается (тяжелая форма).
Возможные проявления:
- язвы во рту;
- пародонтоз;
- грибковые инфекции, поражающие кожу, внутренние органы;
- повышение температуры до 40°С;
- гнойные высыпания на коже;
- пневмония.
Распространение инфекции, подавление иммунных клеток ведет к заражению крови (сепсису), опасному состоянию, имеющему высокие показатели летальности.
Важно!На выраженность симптомов влияет тип возбудителя, вид нейтропении, общее состояние иммунной системы.
Диагностика
 Диагноз нейтропения ставят на основании результатов развернутого анализа крови. При легкой форме снижения клеток у ребенка 1-2 лет, анализ повторяют каждые 10-15 дней, чтобы поставить диагноз – доброкачественная нейтропения. Для определения сопутствующей патологии может потребоваться:
Диагноз нейтропения ставят на основании результатов развернутого анализа крови. При легкой форме снижения клеток у ребенка 1-2 лет, анализ повторяют каждые 10-15 дней, чтобы поставить диагноз – доброкачественная нейтропения. Для определения сопутствующей патологии может потребоваться:
- рентгенография легких;
- УЗИ внутренних органов;
- анализ крови (маркеры) на выявление аутоиммунных, паразитарных, онкологических болезней.
При врожденном заболевании назначают миелограмму с подсчетом миелобластов, промиелоцитов и других клеток. При тяжелой форме делают пункцию костного мозга, исследуют ростковые клетки.
Лечение нейтропении у детей
Выбор метода лечения зависит от вида снижения клеток. Педиатры, в том числе доктор Комаровский, при доброкачественной нейтропении детского возраста лечение не назначают –иммунная система еще формируется. Дети стоят на учете в поликлинике, сдают анализы каждые 3-4 месяца, чтобы выявить транзиторный характер состония При врожденном снижении клеток назначают гранулоцитарный колониестимулирующий фактор (Г-KCФ). Он стимулирует синтезирование, дифференцировку нейтрофилов в костном мозге. В зависимости от типа врожденной патологии его применяют курсами либо в течение всей жизни.
При тяжелых врожденных аномалиях пересаживают костный мозг. При развитии бактериальной инфекции показана антибиотикотерапия, иммуноглобулины, глюкокортикостероиды, дезинтоксикационная терапия. Если снижение клеток связано с анемией, дефицитом витаминов группы В показаны препараты железа, витамины, поливитаминные комплексы. При лекарственной нейтропении отменяют препараты, вызвавшие их снижение, через 1-2 недели повторно делают развернутый анализ крови.
Нейтрофилы – клетки иммунной системы, при их снижении у детей и взрослых повышается вероятность инфекционных, бактериальных инфекций. Изменение показателя у грудничков не считается патологией, лечение не назначают. Но контролировать показатели, состоять на учете у педиатра необходимо до стабилизации уровня всех подвидов лейкоцитарных клеток.
Мне нравитсяНе нравитсяпричины, симптомы, диагностика и лечение
Нейтропения у грудничков принадлежит к группе заболеваний крови. Его основной показатель – сниженное количество нейтрофильных лейкоцитов.
Из-за этого у ребенка падает иммунитет, что приводит к высокой восприимчивости к вирусам, патогенным бактериям и так далее. Нормальным уровнем нейтрофилов считается 1500/1 мкл. Если цифра снижается, начинает развиваться нейтропения.
Причины
Нейтропения может стать следствием различных патологий крови. Также заболевание может быть отдельной аномалией. Есть три основных причины развития недуга.
- Первой причиной является полный сбой количества и соотношения пристеночного пула и циркулирующих клеток. Кроме того, в очаге воспаления может происходить застой нейтрофилов, чем чаще всего характеризуется перераспределительная нейтропения.
- Вторая причина касается полного сбоя продукции нейтрофилов, что происходит в костном мозге. Данный сбой развивается из-за нарушений и дефекта предшествующих клеток. Также имеет значение переход нейтрофилов в состояние периферического характера, что имеет место в случае наследственных нейтропений, синдроме нейтропении и пи апластической анемии.
- Еще одно основная причина кроется в полном изменении нейтрофильной структуры, происходящее в периферическом русле. Такая ситуация наблюдается при секвестрациях в период инфекционного заражения, гемофагоцитарных синдромах, и при иммунных нейтропениях.
Другими причинами могут быть заболевания крови, такие как острый лейкоз, апластическая анемия, синдром Швахмана-Даймонда и миелодиспластический синдром и. Заболевания соединительных тканей также могут привести к нейтропении, например, общая иммунологическая вариабельная недостаточность. Вирусные и бактериальные инфекции тоже влияют на количество нейтрофилов в крови. Нейтропении могут быть наследственными, приобретенными, первичными и вторичными.
до змісту↑Симптомы
Клиническая картина, прежде всего, зависит от выраженности заболевания. Если говорить о течении болезни, он связано с формами и причинами. Как уже было сказано, нейтропения приводит к поражению иммунной системы ребенка, из-за чего его организм попадает под негативное влияние многочисленных бактерий и вирусных инфекций.
В результате этого на слизистых оболочках появляются язвы. Может развиться пневмония и сильно повыситься температура. Если не будет проводиться соответствующее лечение, разовьется токсический шок.
Если количество нейтрофилов в крови очень маленькое, ниже 500, может развиться серьезнейшая форма, которая называется фебрильной нейтропенией. Она характеризуется резко повышенной температурой, сильной слабостью, тремором, выраженной интоксикацией, повышенной потливостью, нарушенной работой сердца, частыми грибковыми инфекциями и инфекциями ротовой полости.
Стоит рассмотреть симптомы в зависимости от формы тяжести заболевания:
- Нейтропения легкой тяжести способна вообще не проявлять себя. Если же она дает о себе знать, то человек часто болеет ОРВИ. Кроме того, он сталкивается с локализованной бактериальной инфекцией, которая хорошо поддается лечению.
- Заболевание средней тяжести проявляется себя частыми рецидивами, ОРВИ, гнойной локализованной инфекцией и инфекциями в ротовой полости. Эта форм может протекать бессимптомно, однако в этом случае присутствует агранулоцитоз.
- Тяжелая форма характеризуется лихорадкой, выраженной интоксикацией, частыми инфекциями, поражениями слизистых или кожи, риском развития сепсиса, деструктивными пневмониями. Если терапия не приносит ожидаемого эффекта, повышен риск летального исхода.
Диагностика
Известный детский врач Е.О. Комаровский в процессе диагностики призывает обращать внимание на такие симптомы, как лихорадка и инфекции: пневмония, синусит, лимфаденит и стоматит.
По его мнению, именно они являются первыми проявлениями нейтропении. Кроме того, важно обращать внимание на провоцирующие факторы, периодичность болезни и инфекции, наблюдаемые у членов семьи.
Болезнь диагностируется путем подсчета клеток кровиНеобходимо провести лабораторные исследования, которые включают в себя сдачу крови два раза в неделю на протяжении полугода. Такой подход позволит выявить периодическую наследственную нейтропению. Важно сравнивать свежие анализы с предшествующими анализами, чтобы исключить врожденную форму. Если есть необходимость, проводят исследование костного мозга и антинейтрофильных антител.
до змісту↑Лечение
Если абсолютное число нейтрофилов менее 500 на единицу, необходимо сразу же приступать к эмпирическому антибактериальному лечению, причем независимо от того, какая причина привела к такому состоянию. Такое лечению должно быть эффективно по отношению к возбудителям, которые становятся причиной инфекции. После этого лечение зависит от течения и характера заболевания.
Циклическая нейтропения лечится гранулоцитарным колониестимулирующим фактором, который вводится подкожно. Его суточная доза составляет от 3 до 5 мкг на кг. Этот препарат вводится за несколько суток до криза. Продолжительность лечения: до того момента, пока не нормализуются показатели крови.
Есть и другая тактика лечения этим же препаратом: он вводится ежедневно или через день в количестве 3 грамм подкожно. Благодаря этому число нейтрофилов будет более 0,5/мкл, а это поможет поддержать качество жизни пациента на удовлетворительном уровне. Если развивается инфекция, назначается местная и антибактериальная терапия.
до змісту↑Генетически детерминированная хроническая нейтропения активно лечится в период обострения инфекции бактериального характера. Лечение основывается на применении антибиотиков, которые обладают широким спектром действия. Не требует специального лечения хроническая доброкачественная нейтропения детского возраста, так как заболевание проходит само собой.
Профилактика
Если у ребенка возникают частые рецидивы инфекции бактериального характера, проводится профилактика триметопримом. Однако врач должен понимать, что дозы, безопасность, эффективность и длительность курса не были изучены до конца. Если все методы не оказывают должного влияния, уровень нейтрофилов может быть повышен глюкокортикоидами, но это делается в редких случаях. Этот метод противопоказан детям, у которых имеется неосложненная ХДНДВ. В целом причин для беспокойств не много. Их вообще не будет, если соблюдать все рекомендации врача.
Нейтропении у детей раннего возраста
Вирусные и бактериальные инфекции, негативное влияние на организм некоторых медикаментов, апластическая анемия, тяжелые воспалительные заболевания, действие химиотерапии – основные причины возникновения нейтропении. Нейтропения у ребенка может развиваться вследствие каких либо проблем в организме и как самостоятельное заболевание.
Нейтропения — это снижение количества нейтрофилов в периферической крови вследствие чего организм теряет способность защищаться от неблагоприятных воздействий окружающей среды (бактерий, вирусов, грибковой инфекции и т.д.). Критерием нейтропении является абсолютное уменьшение количества нейтрофилов (палочкоядерные + сегментоядерные): у детей до 1 года ниже 1 тыс. в 1 мкл, после 1 года – менее 1,5 тыс. в 1 мкл крови.
Иммунная нейтропения
На ранний возраст приходится основное число заболеваний иммунной нейтропении. Механизм заболевания заключается в разрушении нейтрофилов антигранулоцитарными антителами. В результате чего разрушается иммунная система. Среди иммунной нейтропении у детей раннего возраста наибольшее значение имеют трансимммунные, аллоиммунные и первичные аутоиммунные нейтропении.
- Трансиммунная нейтропения встречается достаточно редко, возникает вследствие разрушения нейтрофилов ребенка антителами, проникающими через плаценту от матери, страдающей аутоиммунной нейтропенией.
- Аллоимунная нейтропения обусловлена изоиммунизацией вследствие несовместимости нейтрофильных антигенов плода и матери. Встречается у 3% новорожденных. Симптомы при транс- и аллоиммунной нейтропениях сходны.
- Первичные аутоиммунные нейтропении диагностируются в возрасте от 3-х до 38-ми месяцев (как правило, на 3–7-м месяце жизни). Заболевание может привести к серьезным осложнениям вплоть до развития угрожающих жизни гнойно-септических и некротических осложнений.
Легкие, среднетяжелые и тяжелые нейтропении
Легкие нейтропении могут протекать бессимптомно, или у больных возникают частые ОРВИ, локализованная бактериальная инфекция, хорошо поддающаяся стандартным методам лечения.
Среднетяжелые нейтропении протекают с частыми рецидивами локализованной гнойной инфекции, ОРВИ, рецидивирующей инфекцией ротовой полости (стоматит, гингивит, пародонтоз). Может быть бессимптомное течение болезни, но с агранулоцитозом, который является синдромом какого-либо заболевания. Агранулоцитоз представляет собой патологическое состояние, при котором наблюдается снижение содержания в крови нейтрофилов.
Тяжелые нейтропении сопровождаются выраженной интоксикацией, лихорадкой, частыми тяжелыми бактериальными и грибковыми инфекциями, некротическими поражениями слизистых, в некоторых случаях кожи, деструктивными пневмониями, повышенным риском развития сепсиса и высокой летальностью при неадекватной терапии.
Симптомы
В первые месяцы жизни или в период новорожденности заболевание проявляется в виде тяжелых рецидивирующих бактериальных инфекций — стоматита, гингивита, пневмонии, в том числе деструктивной. У ребенка выраженный агранулоцитоз: количество нейтрофилов менее 300 в 1 мкл. Миелограмма: только промиелоциты и/или миелоциты, увеличено число эозинофилов и моноцитов. В промиелоцитах встречаются атипичные ядра, крупные азурофильные гранулы и вакуоли в цитоплазме. В некоторых случаях у детей выявляется мутация гена (ген ELA-2), кодирующего образование эластазы нейтрофилов. В процессе жизни часть больных синдромом Костмана (13-27%) приобретают точечную мутацию гена рецептора — G-CSF. Больные с этой формой нейтропении относятся к группе высокого риска по развитию острого миелобластного лейкоза и миелодиспластического синдрома.
Хроническая доброкачественная нейтропения детского возраста возникает спонтанно на 1-2 году жизни. Протекает в нетяжелой форме. Количество нейтрофилов 500-1000 в 1 мкл. В пунктате костного мозга снижено количество сегментоядерных нейтрофилов, повышено число палочкоядерных нейтрофилов. При тяжелых формах и хроническом течении тактика лечения индивидуальная.
У детей старшего возраста чаще развивается острая тяжелая абсолютная нейтропения, или острый иммунный агранулоцитоз. Симптомы проявляются лихорадкой, фарингитом, стоматитом, пневмонией, при несвоевременном лечении быстро развивается сепсис. Прогноз неблагоприятный.
Без специального лечения больные нейтропенией еще совсм недавно погибали в раннем возрасте. При своевременно начатом лечении и в зависимости от тяжести и формы заболевания лечение проходит в стационаре или дома.
причины, как проявляется, лечение и профилактика
Есть опасное заболевание, угрожающее в некоторых случаях не только здоровью, но и жизни – нейтропения у детей.
Этот недуг относится к болезням крови и характеризуется значительным снижением иммунитета ребенка. Подобное явление может привести к различным осложнениям, которые требуют срочного лечения, в противном случае дитя может умереть.
Что такое нейтропения?
В крови каждого человека, в том числе и ребенка, есть множество клеточных элементов, подразделяющихся на эритроциты, тромбоциты и лейкоциты. К группе последних относятся нейтрофилы – белые тельца, которые вырабатываются в головном мозге.
С момента начала зарождения клетки до ее полного созревания проходит примерно четырнадцать дней. Нейтрофилы (полиморфноядерные лейкоциты) после этого попадают в кровь, где свободно циркулируют по организму.
Основной задачей белых кровяных клеток является защита человека от различных вирусов и инфекций.

Соответственно, чем меньше в крови у ребенка нейтрофилов, тем больше он уязвим для различных вредоносных организмов.
Нейтропенией называют болезнь, при которой количество этих белых кровяных клеток понижено, и иммунная система работает со сбоями.
Ребенок при этом имеет больше шансов подцепить какую-либо инфекцию. Если при легкой степени нейтропении все может ограничиться ОРВИ (острой респираторной вирусной инфекцией), то тяжелая стадия может вызывать даже сепсис, что несет угрозу жизни.
Нормальное содержание нейтрофилов зависит от возраста ребенка. Младенческий организм в норме должен содержать тысячу и более этих белых кровяных клеток на один микролитр крови.
Ребенок старше года уже имеет полторы тысячи нейтрофилов или даже больше. Легкая степень нейтропении характеризуется снижением количества полиморфноядерных лейкоцитов до 1000 у годовалых детей и до 650 – у младенцев.
При средней форме болезни в микролитре крови малыша старше года содержится от пятиста до тысячи нейтрофилов, в то время как у совсем маленького ребенка – от 350 до 650.
Диагностирование тяжелой степени нейтропении у грудничка происходит при уровне белых кровяных клеток ниже 350 единиц. У детей старше года такая стадия наступает, если анализ показал наличие менее пятиста нейтрофилов в микролитре крови.
При тяжелой степени нейтропении врачи подсчитывают общее количество нейтрофилов, базофилов и эозинофилов.
Эти клетки относятся к группе лейкоцитов и характеризуются способностью к дегрануляции при обнаружении вредоносных организмов.
Если общее количество этих белых кровяных телец ниже ста, то диагностируется агранулоцитоз – тяжелейшее заболевание, довольно часто заканчивающееся летальным исходом по причине развившихся осложнений.
Как правило, нейтропения обнаруживается случайно, во время сдачи общего анализа крови при плановом обследовании ребенка.
Формы заболевания, причины возникновения
Довольно часто диагностируется доброкачественная нейтропения детского возраста. Этот недуг характеризуется периодическим снижением уровня нейтрофилов в крови и дальнейшим возвращением к нормальным показателям.
Как правило, доброкачественная нейтропения детского возраста возникает в два-три года и в четыре-пять лет полностью проходит. Зачастую болезнь протекает в легкой форме и не несет никакой угрозы здоровью ребенка.
Специалисты выделяют еще врожденную нейтропению. Этот недуг развивается по причине недостаточной выработки нейтрофилов головным мозгом.
Как правило, такая форма нейтропении возникает из-за определенных врожденных заболеваний – иммунодефицитов, ацидемии, миелокахексии, гликогеноза, метафизарной хондродисплазии.
Еще одной причиной может быть синдром Костмана – неизлечимая болезнь, нарушающая работу костного мозга. Заболевание довольно часто вызывает лейкоз и требует регулярных инъекций препаратов, повышающих выработку нейтрофилов.
Фебрильная нейтропения – тяжелая форма болезни, характеризующаяся снижением количества всех видов лейкоцитов в крови.
Как правило, недуг сопровождается тахикардией, понижением давления, высокой температурой. Иммунная нейтропения возникает из-за разрушения нейтрофилов антителами. Причинами такой формы болезни могут быть полиомиелит, вирусный гепатит, инфекционный мононуклеоз.
Цикличная нейтропения характеризуется периодическим снижением уровня полиморфноядерных лейкоцитов и дальнейшим восстановлением их количества.
Как правило, полный цикл изменения количества нейтрофилов занимает около трех недель. Заболевание вызывается нарушением в одном из генов и может быть как врожденным, так и приобретенным.
Транзиторная нейтропения возникает у грудных детей и передается им от матери, болеющей любой формой недуга. Зачастую такое заболевание не опасно и проходит само собой за один-два месяца.
Часто встречается развитие нейтропении у детей по причинам, связанным с определенными болезнями.
Возникновение недуга может быть спровоцировано инфекционными заболеваниями (краснухой, туберкулезом, гриппом, ВИЧ, корью, герпесом), нарушениями работы селезенки или костного мозга, проблемами с кровеносной системой (лейкозом, анемией) или авитаминозом.
Как правило, для определения причины развития нейтропении необходимо проводить другие обследования, поскольку недуг может возникнуть из-за большого количества факторов.
Симптомы и диагностика нейтропении
Легкая форма нейтропении протекает у ребенка практически бессимптомно. Обнаружить ее удается только случайно, при плановом обследовании и сдаче общего анализа крови.
Отличительным признаком легкой стадии считается долгое выздоровление после различных инфекционных заболеваний.
В некоторых случаях болезни могут давать осложнения, несвойственные привычной клинической картине.
Видео:
Зачастую особенного лечения такая форма нейтропении не требует, поскольку угрозы жизни и здоровью ребенка нет, и заболевание проходит достаточно быстро.
Средняя стадия болезни характеризуется довольно частыми ОРВИ, гнойными инфекциями (как правило, проявляющимися в ротовой полости).
Анализ крови показывает общее уменьшение количества лейкоцитов. В некоторых случаях средняя форма нейтропении протекает без всяких симптомов, и обнаружить ее можно лишь по снижению уровня полиморфноядерных белых кровяных клеток. Зачастую угрозы жизни ребенка такая стадия болезни не несет.
Тяжелая форма нейтропении дает о себе знать общей интоксикацией организма, повышенной температурой (от 38 градусов по Цельсию), рецидивами инфекционных болезней, лихорадкой.
Довольно часто наблюдается развитие болезней полости рта: гингивита, стоматита, пародонтоза.
Появляются гнойные высыпания на коже и слизистых оболочках, язвочки в области ануса, развивается пневмония.
При отсутствии своевременного лечения у ребенка может развиться сепсис, что в дальнейшем зачастую приводит к летальному исходу.
Для диагностики легкой и средней форм нейтропении хватает общего анализа крови на содержание полиморфноядерных лейкоцитов.
Помимо этого, доктор проводит визуальный осмотр ребенка, выслушивает жалобы родителей. Может быть назначен анализ крови из вены на проверку уровня иммуноглобулинов.
При подозрении на тяжелую степень нейтропении часто проводится миелограмма – проверка материала после пункции костного мозга. Если есть подозрение о врожденной природе заболевания, то проводят генетические исследования.
Как правило, анализы на содержание нейтрофилов в крови берутся два раза в неделю на протяжении минимум полугода. Организм ребенка регулярно проверяется на содержание гемоглобина.
Только при длительном соответствии уровня белых кровяных клеток норме можно считать, что болезнь побеждена. В дальнейшем врачи рекомендуют сдавать анализ крови на содержание нейтрофилов каждые полгода, чтобы своевременно зафиксировать возможные рецидивы.
Лечение заболевания
Нужно отметить, что не существует универсального метода лечения, способного избавить от нейтропении.
Все зависит от причин, вызвавших патологию, и усилия врачей направлены на борьбу с ними. Специалисты подчеркивают, что лекарств, повышающих уровень нейтрофилов в крови, не существует.
Терапия направлена на укрепление иммунитета ребенка, избавление от инфекций и других заболеваний.
Видео:
Легкая и доброкачественная формы нейтропении, как правило, не требуют особенного лечения. Ребенок находится на учете в поликлинике, регулярно сдает анализы и посещает своего лечащего врача.
Если в течение года содержание нейтрофилов в крови не упало ниже нормы, то диагностируют полное излечение маленького пациента от болезни.
В этот период рекомендуется принимать витамины (кушать больше свежих фруктов и овощей, пить специальные лекарственные комплексы) и медикаменты, укрепляющие иммунитет, заниматься спортом.
При диагностике средней формы нейтропении доктор в большинстве случаев назначает специальные препараты против вирусов и грибков, в зависимости от типа поразившей ребенка инфекции.
Если на протяжении полугода уровень содержания нейтрофилов не приходит в норму, то может быть назначена госпитализация с целью проведения дальнейших исследований. Это делается для диагностики тяжелых заболеваний крови.
По результатам исследований может быть назначено медикаментозное лечение, в некоторых случаях даже пожизненное.
Тяжелая форма нейтропении требует обязательной госпитализации ребенка в отдельную палату, в которой регулярно проводят ультрафиолетовую и антибактериальную обработку.
В большинстве случаев маленькому больному назначают курс приема антибиотиков с целью быстрого избавлении от инфекции. Помимо этого, обязательно лечение препаратами, повышающими иммунитет.
Через несколько дней такой терапии, исходя из результатов анализов, специалистами принимается решение, как лечить ребенка дальше.
Если причиной возникновения нейтропении стали проблемы с селезенкой, то назначается спленэктомия – удаление органа хирургическим путем. В некоторых особо тяжелых случаях может потребоваться пересадка костного мозга.
Нужно отметить, что трансплантация проводится только детям старше двенадцати лет. Как правило, после такой операции пациент всю жизнь находится на учете в больнице и вынужден принимать специальные лекарства.
Нейтропения – заболевание крови, характеризующееся понижением количества полиморфноядерных белых кровяных клеток группы лейкоцитов.
Причины снижения уровня нейтрофилов могут быть разными, от врожденных отклонений до инфекционных заболеваний.
Симптомы и лечение болезни зависят от того, в какой форме протекает нейтропения: если доброкачественная, легкая и средняя формы проходят довольно легко, то тяжелая стадия требует срочной госпитализации, поскольку угрожает жизни ребенка.
Вы здесь:
Нейтропения у недоношенных детей
Отделение педиатрии, Первая дочерняя больница Медицинского университета Куньмин, Куньмин, КНР
* Автор для корреспонденции: Хэ Сянъин, Отделение педиатрии, Первая дочерняя больница Медицинского университета Куньмина, Куньмин, Юньнань, Китайская Народная Республика, 650032
Образец цитирования: Субба Четана, Хэ Сяньин. Нейтропения у недоношенных детей. Журнал педиатрии, перинатологии и детского здоровья 3 (2019): 001-009.
Сокращения:
АНК-абсолютное количество нейтрофилов; Г-КСФ-гранулоцитарный колониестимулирующий фактор; GM-CSF-гранулоцитарный макрофагальный колониестимулирующий фактор; ВВИГ-внутривенный иммуноглобулин; мкл-микролитр; NICU — неонатальное отделение интенсивной терапии; РКИ — рандомизированные контролируемые испытания; rG-CSF-рекомбинантный колониестимулирующий фактор гранулоцитов; rGM-CSF-рекомбинантный фактор, стимулирующий колонию макрофагов из гранулоцитов; WBC-лейкоциты
,001. Справочная информация
Нейтрофилы, тип лейкоцитов, составляют более пятидесяти процентов от общего количества лейкоцитов [1].В 1880 году Эрлих разработал метод окрашивания, который упростил идентификацию развивающихся фагоцитов в костном мозге, крови и тканях. Из-за красителей Эрлиха возможность микроскопических наблюдений за клетками крови оказалась обычным явлением, что привело к четкому определению нормального количества, лейкопении, лейкемии, нейтропении и агранулоцитоза [2]. Нейтрофилы являются основным типом эффекторных клеток в системе врожденного иммунитета [3, 4], которые циркулируют в крови и поглощают вторгающиеся микроорганизмы, такие как бактерии и грибы, путем фагоцитоза.Они сравнительно недолговечны, имеют период полураспада в кровотоке от 6 до 8 часов и производятся со скоростью 5 × 10 10 -10 × 10 10 клеток / день [5]. Хотя в педиатрической популяции нормальные диапазоны варьируются в основном в зависимости от возраста, нормальное количество нейтрофилов у недоношенных детей зависит от гестационного возраста при рождении и веса при рождении [1]. Поэтому крайне важно тщательно оценивать количество нейтрофилов у недоношенных и тяжелобольных детей. Хотя нейтропения обычно является доброкачественным заболеванием, которое протекает самостоятельно у большинства младенцев, она может быть стойкой и представлять собой серьезный дефицит противомикробной защиты у некоторых недоношенных детей.Упорядоченное развитие пролиферации, дифференцировки и созревания стволовых клеток от миелобластов до полностью зрелых сегментированных клеток приводит к развитию зрелых нейтрофилов [6]. Развитие нейтрофилов включает три стадии: размножение, созревание и функциональную. В среднем первая стадия занимает 14 дней, митотический период — 7,5 дней, вторая стадия — 6,5 дней и заключительная стадия — 2,5 дня [6]. Первым предшественником, коммитированным гранулоцитами, является миелобласт (обнаруженный в костном мозге), который далее дифференцируется / созревает в промиелоциты.Позже промиелоциты созревают в миелоциты [7]. Клетки на этих трех стадиях развития способны размножаться. Предполагается, что результатом митотического деления должны быть симметричные клетки, в результате которых образуются две клетки, которые либо пролиферируют, либо переходят к дальнейшему созреванию [8]. Митотический пул обозначает коммитированные гранулоцитарные клетки-предшественники, претерпевающие пролиферацию и дифференцировку, тогда как полностью дифференцированные зрелые нейтрофилы составляют постмитотический пул, который формирует резерв костного мозга и доступен для высвобождения [5].Сегментированные клетки костного мозга первоначально запускаются, когда существует более высокая потребность в полиморфно-ядерных клетках (PMN), так что неактивная популяция становится частично активной и производит новые сегментированные клетки. Благодаря этой системе обновления возможен непрерывный выход большего количества полиморфно-ядерных клеток (PMN) [8].
Нейтропения определяется как абсолютное количество нейтрофилов (АНК) менее чем на два стандартных отклонения ниже среднего значения для возраста статистически [9] или, альтернативно, ниже 5-го процентиля для населения определенного возраста [3, 10].Здесь ANC будет рассчитываться как автоматическое значение количества лейкоцитов × (% сегментированных нейтрофилов +% полос) / 100 [11]. Первое исследование, проведенное Manroe et al. [10], используя когорту из 434 младенцев (38,9 ± 2,4 недели беременности), составили контрольные диапазоны для концентраций нейтрофилов в крови, используя данные, полученные в этом исследовании. Исследование показало, что количество нейтрофилов достигло пика через 12-14 часов с минимумом 7800 клеток / мм 3 и максимумом 14500 клеток / мм 3 , а затем стабилизировалось на более низком уровне 1750 общих нейтрофилов / мм 3 к 72 часам жизни.Стабильное максимальное значение 5400 нейтрофилов / мм 3 достигается через 5 дней. Поскольку контрольные диапазоны были более подходящими для доношенных и поздних недоношенных детей, Mouzinho et al. [12] позже провели другое исследование. Согласно исследованию, верхние пределы концентрации нейтрофилов в крови были почти такими же, как у Manroe et al. но нижний предел показал большие вариации. Совсем недавно Schmutz et al. [11] провели исследование на младенцах, родившихся на сроке гестации 23-42 недели, используя 30 354 полных анализа крови.В его исследовании обычный диапазон АНК составлял от 2700 до 13000 / мкл (5 -й -95 -й -й процентиль) для младенцев более 36 недель гестации, между 1000-12 500 / мкл для младенцев 28-36 недель. беременность и 1300-15 300 / мкл для младенцев младше 28 недель в течение 72-240 часов после рождения. Верхние пределы ANC были значительно выше, чем диапазоны, указанные как Manroe, так и Mouzinho.
2. Нейтропения у недоношенных детей
Преждевременные роды определяются как роды до 37 полных недель беременности [13].На преждевременные роды приходится 11% родов во всем мире [14]. Китай занимает второе место после Индии с 1 172 300 недоношенными детьми среди 10 стран, имеющих большинство преждевременных родов [15]. Точно так же нейтропения входит в число наиболее часто выявляемых аномалий в отделениях неонатальной терапии и отделениях интенсивной терапии новорожденных (ОИТН). Из общего числа госпитализированных в ОИТН примерно у 8% новорожденных выявляется количество нейтрофилов в крови <1000 / мкл, а у 6-58% недоношенных детей, по крайней мере, в одном случае, снижается количество нейтрофилов в крови [16].Частота нейтропении зависит от этнической принадлежности, срока беременности и характера роста. Оно обратно пропорционально массе тела при рождении и гестационному возрасту [17], тогда как прямо пропорционально степени гипертонии у матери [12, 18, 19]. Женский пол, высокогорные роды и способ родоразрешения новорожденных являются другими сопутствующими факторами риска [17]. Поскольку иммунная система недоношенных детей имеет относительно меньший пул нейтрофилов и моноцитов, потенциал этих клеток по уничтожению патогенов снижается, а также активация Т-клеток ограничена из-за более низкой продукции цитокинов.Следовательно, это приводит к снижению способности этих клеток бороться с бактериями и обнаруживать вирусы в клетках по сравнению со зрелыми младенцами [20-22]. Хотя ряд общих пренатальных и послеродовых событий, сопровождающих преждевременные роды, обладают способностью модулировать иммунитет [20], родовая деятельность и вагинальные роды были связаны с улучшением функции нейтрофилов, возможно, из-за иммунного прайминга у недоношенных детей [17].
2.1 Причины неонатальной нейтропении
Нейтропения может быть вызвана разными причинами.Три механизма — снижение скорости продукции нейтрофилов, чрезмерная маргинализация нейтрофилов и увеличение скорости разрушения или их комбинации считаются основными причинами [23].
1. Снижение продукции нейтрофилов
- Материнские и внутриутробные состояния — материнская гипертензия, преэклампсия, гипертензия, вызванная беременностью, ограничение внутриутробного развития
- Доноры парных трансфузий
- Младенцы с резус-гемолитической болезнью
- Хроническая нейтропения при синдромах недостаточности костного мозга (синдром Костмана, ретикулярная дисгенезия, циклическая нейтропения, синдром Барта, синдром Швахмана-Даймонда, гипоплазия хрящей и волос)
- Врожденные нарушения обмена веществ
- Болезнь накопления гликогена типа 1b, Органические ацидемии
- Вирусные инфекции
- Краснуха, цитомегаловирус (внутриутробные инфекции)
- Недостаток меди
- Аллоиммунная нейтропения, связанная с антителами против NB1 .
2. Повышенная деструкция (утилизация) нейтрофилов
- Бактериальный или грибковый сепсис (включая некротический энтероколит)
- Иммуноопосредованная (аллоиммунная нейтропения новорожденных, аутоиммунная нейтропения младенцев и изоиммунная или аутоиммунная нейтропения новорожденных) .
- Чрезмерная граница нейтрофилов
- Нейтропения, вызванная лекарственными средствами
- Другое я
- Идиопатическая нейтропения недоношенных .
2.2 Клиническое ведение нейтропении у недоношенных детей
Поскольку риск инфицирования напрямую связан с продолжительностью и тяжестью нейтропении у недоношенных детей, любая нейтропения, которая длится более пяти дней или, в частности, имеет АНК менее 500 / мкл, должна пройти тщательную оценку [17, 24]. Если пациент выживает, нейтропения быстро проходит у большинства недоношенных детей. Например, в большинстве случаев нейтропении, сопровождающей ПВГ, нейтропения обычно проходит через 3-5 дней.Но необходимо рассмотреть дополнительную оценку, если нейтропения сохраняется более 2 или 3 дней у младенца с сепсисом. По-прежнему остается дилемма, использовать или не использовать профилактические антибиотики у младенцев с нейтропенией, поскольку это может привести к грибковому сепсису или сепсису с высокорезистентными бактериями [24]. Тем не менее, сепсис следует рассматривать как часть дифференциального диагноза, и соответствующую антибактериальную терапию следует начинать в ожидании отчетов о посеве у тяжелобольного ребенка [25].Для увеличения выработки нейтрофилов и их функций у недоношенных детей рекомендуются различные методы лечения. Хотя некоторые схемы лечения не показали значительного положительного воздействия на недоношенных детей, они по-прежнему широко применяются для лечения нейтропении у недоношенных детей, а некоторые новые препараты проходят клинические испытания.
2.2.1 Внутривенный иммуноглобулин (ВВИГ): Внутривенный иммуноглобулин (ВВИГ) — препарат, широко используемый в педиатрической практике при иммунных расстройствах.Были проведены многочисленные исследования эффективности ВВИГ у недоношенных детей с нейтропенией. Исследование, проведенное Sandberg et al. [26] показывает, что ВВИГ не играет роли профилактической иммунотерапии для улучшения иммунной компетентности недоношенных детей для предотвращения тяжелых неонатальных инфекций. Аналогичным образом системный обзор, проведенный Ohlsson et al. [27] пришли к выводу, что существенного снижения смертности во время пребывания в больнице у младенцев с подозрением или подтвержденной инфекцией не наблюдается, и исследование не рекомендует рутинное введение ВВИГ или ВВИГ, обогащенного IgM, для предотвращения смертности у младенцев с подозрением или подтвержденной неонатальной инфекцией. инфекция.Однако недавно Liu et al. [28] заявили, что недоношенным детям может быть полезна высокая доза ВВИГ (1-2 г / кг) за счет предотвращения усиления воспаления и восстановления баланса иммунного гомеостаза.
2.2.2 Кортикостероиды: Кортикостероиды широко используются для лечения иммуноопосредованной неонатальной нейтропении [29], но противоречивые результаты не подтверждают их использование у младенцев с нейтропенией. Однако, согласно исследованию, проведенному Bux et al. [30], ответ на терапию кортикостероидами был лучше при первичной аутоиммунной нейтропении (AIN).Введение дексаметазона до искусственного кровообращения (КПБ) приводит к уменьшению воспалительной реакции, но не влияет на абсолютное количество нейтрофилов [31]. Как правило, антенатальные кортикостероиды рекомендуются женщинам, которые подвержены риску преждевременных родов до 34 недель беременности для созревания легких плода [32, 33], но использование постнатальных стероидов у недоношенных детей часто было связано с пагубными последствиями для нервного развития. Точно так же на постнатальный характер роста недоношенных детей влияет лечение кортикостероидами, в большей степени дексаметазоном, чем гидрокортизоном [34], поэтому послеродовые стероиды следует применять только для недоношенных детей, которые остаются зависимыми от ИВЛ после первой недели жизни, а также от дозы и Продолжительность лечения должна быть минимально возможной, необходимой для достижения экстубации [35].
2.2.3 Переливание гранулоцитов: Переливание концентратов гранулоцитов предлагалось в прошлом для новорожденных с тяжелой нейтропенией и тяжелым сепсисом, резистентным к лечению антибиотиками. Однако в настоящее время нет определенных показаний по этому поводу [36]. Переливание гранулоцитов может помочь в острых ситуациях, но долгосрочная польза остается неясной [17]. Согласно системному обзору Кокрановской базы данных, проведенному в 2011 году, в настоящее время недостаточно данных из рандомизированных контролируемых исследований (РКИ) для подтверждения регулярного использования переливаний гранулоцитов у младенцев с нейтропенией и сепсисом, поэтому больше исследователей поощряются к многоцентровым исследованиям [37].Поэтому с учетом возможных побочных эффектов (передачи инфекций) более целесообразно использовать рекомбинантные факторы роста гранулоцитов (рекомбинантный гранулоцитарный колониестимулирующий фактор, рекомбинантный гранулоцитарно-моноцитарный колониестимулирующий фактор) [36].
2.2.4 Рекомбинантный колониестимулирующий фактор гранулоцитов (rG-CSF) и рекомбинантный колониестимулирующий фактор гранулоцитов-макрофагов (rGM-CSF): Гемопоэтические колониестимулирующие факторы G-CSF (фактор, стимулирующий колонии гранулоцитов) и GM -CSF (фактор, стимулирующий колонии гранулоцитов и макрофагов) — это цитокины, которые увеличивают количество циркулирующих нейтрофилов за счет стимуляции клеток-предшественников нейтрофилов в костном мозге, увеличивают резерв костного мозга и уменьшают апоптоз нейтрофилов [38, 39].Гипотетически rG-CSF и rGM-CSF должны снижать уровень смертности младенцев с сепсисом. Чтобы проверить эту гипотезу, был проведен метаанализ с включением 5 исследований, результат показал, что, хотя было небольшое снижение уровня смертности у младенцев-реципиентов rG-CSF / rGM-CSF с предполагаемой сепсисом, но результат был более очевиден в только группа младенцев с нейтропенией [40]. Аналогичным образом, другое исследование показало, что введение rG-CSF недоношенным детям с клиническим диагнозом сепсиса с ранним началом коррелировало с более низкой частотой нозокомиальной инфекции в течение последующих трех недель и повышением концентрации нейтрофилов в периферической крови и костном мозге. но не было разницы в общей смертности [41].Другое исследование, проведенное Miura et al. [42] показали, что пятидневный период терапии Г-КСФ у недоношенных новорожденных с нейтропенией и клиническим сепсисом является безопасным и также сокращает продолжительность пребывания в больнице, но не улучшает уровень смертности. Профилактическое использование лечения rG-CSF и rGM-CSF в более крупных исследованиях не показало какого-либо очевидного снижения инфекционных осложнений или улучшения общей выживаемости, и почти идентичные результаты наблюдались в исследованиях, оценивающих G-CSF и GM-CSF в качестве интервенционной терапии в младенцы с сепсисом.Таким образом, согласно недавним данным, rG-CSF и rGM-CSF не рекомендуются для рутинного использования у недоношенных, а также доношенных детей [43, 44]. Однако rG-CSF очень эффективен при коррекции иммуноопосредованной, а также в случаях врожденной нейтропении [16]. В случаях нейтропении, связанной с преэклампсией матери и идиопатической нейтропенией недоношенных, предпочтения в лечении должны соответствовать стандартному протоколу или индивидуальному решению с учетом продолжительности и тяжести нейтропении [16, 43].
2.2.5 Пентоксифиллин: Иммуномодулирующее свойство пентоксифиллина имеет отчетливую иммунологическую реакцию у недоношенных детей, приводящую к количественным и качественным различиям в уровнях поверхностного маркера и продукции цитокинов [45]. Поперечное исследование с участием 18 недоношенных новорожденных с очень низкой массой тела при рождении (VLBW) с нозокомиальным сепсисом показывает значительное снижение отношения незрелых нейтрофилов к общему количеству нейтрофилов (I / T) и С-реактивного белка (CRP) после терапии пентоксифиллином в качестве средства дополнительная терапия к схемам приема антибиотиков [46].Анализ Кокрановской базы данных в 2015 году также показал, что пентоксифиллин, используемый в дополнение к антибиотикам, снижает смертность при неонатальном сепсисе без каких-либо побочных эффектов. Но из-за минимального качества доказательств относительно небольших исследований хорошо спланированные многоцентровые испытания по-прежнему имеют первостепенное значение для подтверждения эффективности пентоксифиллина в снижении показателей смертности и заболеваемости у младенцев с сепсисом [47]. Большое ретроспективное когортное исследование с участием 311 недоношенных новорожденных пришло к выводу, что пентоксифиллин совместим с обычными неонатальными препаратами в отделении интенсивной терапии интенсивной терапии при введении через ту же внутривенную линию [48].В последнее время многие медицинские центры используют пентоксифиллин в качестве адъювантной терапии для лечения недоношенных детей с такими заболеваниями, как нозокомиальные инфекции, но никаких серьезных побочных эффектов замечено не было. Таким образом, его можно считать безопасным лекарством, но для его повседневного использования необходимы дополнительные клинические испытания.
3. Заключение
Последние достижения в области неонатальной медицины внесли существенный вклад в очевидное снижение неонатальной смертности. Но увеличение выживаемости недоношенных детей привело к увеличению числа недоношенных детей с заболеваниями и длительной инвалидностью.Научные исследования, посвященные нейтропении у недоношенных детей и наиболее подходящим методам лечения этих недоношенных детей, по-прежнему ограничены, и многие из них являются противоречивыми. Следовательно, мы настоятельно рекомендуем дальнейшие исследования в этой области, которые будут направлены на решение проблем у недоношенных детей.
Ссылки
- Шах Б., Бург Н, Пиллинджер М.Х. в Учебнике ревматологии Келли и Файрестайна, (10 th Edn) (2017).
- Дейл, округ Колумбия, Боксер Л, Лайлс WC.Фагоциты: нейтрофилы и моноциты. Кровь 112 (2008): 935-945.
- Боррегаард Н. Нейтрофилы: от костного мозга до микробов. Иммунитет 33 (2010): 657-670.
- Amulic B, Cazalet C, Hayes GL и др. Функция нейтрофилов: от механизмов к болезни. Анну Рев Иммунол 30 (2012): 459-489.
- Саммерс С., Рэнкин С.М., Кондлифф А.М. и др. Кинетика нейтрофилов при здоровье и болезни. Тенденции Immunol 31 (2010): 318-324.
- Da Silva FM, Massart-Leen AM, Burvenich C.Развитие и созревание нейтрофилов. Vet Q 16 (1994): 220-225.
- Tak T, Tesselaar K, Pillay J, et al. Опять сколько тебе лет? Повторное определение периода полураспада нейтрофилов человека. J Leukoc Biol 94 (2013): 595-601.
- Болл И. Т., Фукс Г. Кинетическая модель гранулоцитопоэза. Exp Cell Res 61 (1970): 147-152.
- Афины JW. Нарушения пролиферации и кровообращения нейтрофилов: Патофизиологический взгляд. Clin Haematol 4 (1975): 553-566.
- Манро Б.Л., Вайнберг А.Г., Розенфельд С.Р. и др. Анализ крови новорожденных при здоровье и болезнях. I. Референтные значения для нейтрофильных клеток. J Pediatr 95 (1979): 89-98.
- Шмутц Н., Генри Э., Джоплинг Дж. И др. Ожидаемые диапазоны концентраций нейтрофилов в крови младенцев: пересмотренные графики Манро и Музиньо. Журнал перинатологии 28 (2008): 275-281.
- Mouzinho A, Rosenfeld CR, Sanchez PJ, et al. Пересмотренные контрольные диапазоны циркулирующих нейтрофилов у младенцев с очень низкой массой тела при рождении.Педиатрия 94 (1994): 76-82.
- Beck S, Wojdyla D, Say L, et al. Заболеваемость преждевременными родами во всем мире: систематический обзор материнской смертности и заболеваемости. Bull World Health Organ 88 (2010): 31-38.
- Blencowe H, Cousens S, Oestergaard MZ и др. Национальные, региональные и мировые оценки показателей преждевременных родов в 2010 году с временными тенденциями с 1990 года для отдельных стран: систематический анализ и последствия. Ланцет 379 (2012): 2162-2172.
- Преждевременные роды. ВОЗ (2018).
- Махешвари А. Нейтропения у новорожденного. Curr Opin Hematol 21 (2014): 43-49.
- Moerdler S, LaTuga MS. Неонатальная нейтропения. NeoReviews 19 (2018): 22-28.
- Дорон М.В., Махлуф Р.А., Кац В.Л. и др. Повышенная частота сепсиса при рождении у младенцев с нейтропенией и матерями с преэклампсией. J Pediatr 125 (1994): 452-458.
- Paul DA, Leef KH, Sciscione A, et al. Преэклампсия не увеличивает риск сепсиса, подтвержденного культурой, у младенцев с очень низкой массой тела при рождении.Am J Perinatol 16 (1999): 365-372.
- Мелвилл Дж. М., Мосс TJM. Иммунные последствия преждевременных родов. Front Neurosci 7 (2013): 79.
- Дюранди А. Онтогенез иммунной системы. Трансфус. Med Hemother 30 (2003): 222-227.
- Странк Т., Карри А., Ричмонд П. и др. Врожденный иммунитет у новорожденных: недоношенность означает больше, чем незрелость. J Matern Fetal Neonatal Med 24 (2011): 25-31.
- Hassan M, Yasmeen BHN. Нейтропения у младенцев — обзор.Журнал Северного международного медицинского колледжа 7 (2016): 149-152.
- Christensen RD, Calhoun DA, Rimsza LM. Практический подход к оценке и лечению нейтропении в отделении интенсивной терапии новорожденных. Clin Perinatol 27 (2000): 577-601.
- Ниттала С., Суббарао Г.К., Махешвари А. Оценка нейтропении и нейтрофилии у недоношенных детей. J Matern Fetal Neonatal Med 25 (2012): 100-103.
- Сандберг К., Фаст А., Бергер А. и др. Недоношенные дети с низким уровнем иммуноглобулина G имеют повышенный риск неонатального сепсиса, но не получают пользы от профилактического иммуноглобулина G.J Pediatr 137 (2000): 623-628.
- Ольссон А., Лейси Дж. Б.. Внутривенный иммуноглобулин при подозрении или подтвержденной инфекции у новорожденных. Кокрановская база данных Syst Rev 27 (2015 г.): CD001239.
- Лю П., Ли Л., Фан П. и др. Высокие дозы внутривенного иммуноглобулина модулируют иммунную толерантность у недоношенных детей. BMC Pediatr 18 (2018): 74. .
- Махешвари А., Кристенсен РД, Калхун Д.А. Иммуноопосредованная нейтропения у новорожденных. Acta Paediatr Suppl 91 (2002): 98-103.
- Bux J, Behrens G, Jaeger G и др. Диагностика и клиническое течение аутоиммунной нейтропении в младенческом возрасте: анализ 240 случаев. Кровь 91 (1998): 181-186.
- Bronicki RA, Backer CL, Baden HP, et al. Дексаметазон снижает воспалительную реакцию на искусственное кровообращение у детей. Ann Thorac Surg 69 (2000): 1490-1495.
- Шмитц Т. Профилактика осложнений преждевременных родов с помощью антенатального введения кортикостероидов. Журнал J Gynecol Obstet Biol Reprod (Париж) 45 (2016): 1399-1417.
- Робертс Д., Браун Дж., Медли Н. и др. Антенатальные кортикостероиды для ускорения созревания легких плода у женщин с риском преждевременных родов. Кокрановская база данных Syst Rev 3 (2017 г.): CD004454.
- Tijsseling D, Ter Wolbeek M, Derks JB и др. Неонатальная кортикостероидная терапия влияет на характер роста в раннем младенчестве. PLoS One 13 (2018): 0192162.
- Холлидей HL. Обновленная информация о послеродовых стероидах. Неонатология 111 (2017): 415-422.
- Girelli G, Antoncecchi S, Casadei AM и др.Рекомендации по трансфузионной терапии в неонатологии. Переливание крови 13 (2015): 484-497.
- Pammi M, Brocklehurst P. Переливания гранулоцитов новорожденным с подтвержденным или подозреваемым сепсисом и нейтропенией. Кокрановская база данных Syst Rev 10 (2011 г.): CD003956.
- Коэн-Волковиц М., Бенджамин Д. К. мл., Каппарелли Э. Иммунотерапия при неонатальном сепсисе: достижения в лечении и профилактике. Curr Opin Pediatr 21 (2009): 177-181.
- Калхун Д.А., Кристенсен Р.Д.Биология развития человека колониестимулирующего фактора гранулоцитов. Clin Perinatol 27 (2000): 559-576.
- Bernstein HM, Pollock BH, Calhoun DA, et al. Введение рекомбинантного гранулоцитарного колониестимулирующего фактора новорожденным с септицемией: метаанализ. J Pediatr 138 (2001): 917-920.
- Borjianyazdi L, Froodmand M, NooriShadkam M и др. Эффект от введения гранулоцитарного колониестимулирующего фактора у недоношенных новорожденных с нейтропенией и клиническим сепсисом: рандомизированное клиническое исследование.Иран Дж. Пед Гематол Онкол 13 (2013): 64-68.
- Miura E, Procianoy RS, Bittar C и др. Оценка эффективности рекомбинантного человеческого гранулоцитарного колониестимулирующего фактора «rhG-CSF» в лечении раннего неонатального сепсиса у недоношенных новорожденных. J Pediatr (Rio J) 76 (2000): 193-199.
- Lehrnbecher T. Гематопоэтические факторы роста в профилактике и терапии инфекционных осложнений у недоношенных и новорожденных. Z Geburtshilfe Neonatol 205 (2001): 167-173.
- Castagnola E, Dufour C. Роль G-CSF GM-CSF в лечении инфекций у недоношенных новорожденных: обновленная информация. Early Hum Dev 90 (2014): 15-17.
- Schuller SS, Wisgrill L, Herndl E, et al. Пентоксифиллин модулирует LPS-индуцированное гипервоспаление в моноцитах недоношенных детей in vitro. Педиатр Res 82 (2017): 215-225.
- Hamilcikan S, Can E, Buke O, et al. Лечение пентоксифиллином новорожденных с очень низкой массой тела при нозокомиальном сепсисе.Am J Perinatol 34 (2017): 795-800.
- Pammi M, Haque KN. Пентоксифиллин для лечения сепсиса и некротического энтероколита у новорожденных. Кокрановская база данных Syst Rev 3 (2015 г.): CD004205.
- Лаутербах Р., Странк Т, Патоле С. и др. Совместимость внутривенного пентоксифиллина с другими лекарствами, вводимыми одновременно с недоношенными детьми с поздним началом сепсиса. Acta Paediatr 107 (2018): 1288-1289.
Нейтропения — младенцы | UF Health, Университет здравоохранения Флориды,

Академический медицинский центр Университета Флориды — самый обширный академический медицинский центр на Юго-Востоке — предназначен для высококачественных программ образования, исследований, ухода за пациентами и государственных услуг.
Стоматологический колледж UF является единственной стоматологической школой во Флориде, финансируемой государством, и признан одной из лучших стоматологических школ США за качество образовательных программ, исследовательскую деятельность в области гигиены полости рта и приверженность уходу и обслуживанию пациентов.
Медицинский колледж, крупнейший из шести колледжей Академического медицинского центра Университета Флориды, открылся в 1956 году с целью увеличения количества высококвалифицированных врачей во Флориде, предоставления передовых медицинских услуг жителям Флориды и содействия открытиям в области здравоохранения. исследование.
Колледж медсестер Университета Флориды, основанный в 1956 году, является ведущим учебным заведением для медсестер в штате Флорида и входит в 10% лучших медицинских программ для выпускников в стране. Колледж медсестер UF постоянно привлекает и сохраняет высочайший уровень студентов и преподавателей медсестер, увлеченных наукой и заботой.
Фармацевтический колледж, основанный в 1923 году, является старейшим колледжем Академического медицинского центра UF.Колледж, входящий в число лучших фармацевтических школ страны, поддерживает исследовательские, сервисные и образовательные программы, дополненные онлайн-технологиями.
Колледж общественного здравоохранения и медицинских профессий (PHHP) предназначен для предоставления отличных образовательных программ, которые готовят выпускников к удовлетворению многогранных медицинских потребностей населения, сообществ и отдельных лиц.
UF College of Veterinary Medicine — единственный ветеринарный колледж Флориды, предлагающий множество уникальных образовательных программ для студентов и услуг, направленных на помощь домашним животным, дикой природе и исчезающим видам.Мы предлагаем четырехлетние программы доктора ветеринарной медицины, а также M.S. и к.т.н. степени в области ветеринарной медицины.
Расположенный в одном месте с больницей Shands Jacksonville, Центр медицинских наук Джексонвилля выделяется в области образования, исследований и ухода за пациентами, что отражает наши неизменные ценности сострадания, совершенства, профессионализма и инноваций. Наш современный медицинский центр обслуживает 1 миллионное городское население от северной Флориды до южной Джорджии.
UFCOM-J предлагает аккредитованные программы ординатуры и стипендий для выпускников медицинского образования в дополнение к нестандартным программам стипендий. Клиническая ротация по всем основным дисциплинам предусмотрена для студентов-медиков UFCOM, а выборная ротация — для студентов из других аккредитованных школ.
UFHSC-J — это клинический учебный центр для медицинского колледжа в Гейнсвилле. Студенты поочередно проходят через различные клинические учреждения на территории кампуса, а также центры первичной медико-санитарной помощи и специализированные медицинские учреждения, расположенные по всему Джексонвиллю.
Фармацевтический колледж UF в Джексонвилле предлагает четырехлетнюю программу доктора фармацевтики (Pharm.D.), Полностью завершенную в Джексонвилле. Также на территории кампуса предлагается программа резидентуры в аптеке Shands Jacksonville, аккредитованная Американским обществом фармацевтов системы здравоохранения.
University of Florida Health знает, насколько важно постоянное медицинское обучение для поставщиков медицинских услуг и общества. Вот почему мы предлагаем онлайн-курсы непрерывного медицинского образования (CME), которые вы можете пройти для получения кредитов CME.Эти курсы знакомят с последними медицинскими знаниями, обучают новым навыкам взаимоотношений с пациентами и помогают поставщикам медицинских услуг решать актуальные текущие проблемы.
Нейтропения — младенцы | UF Health, Университет здравоохранения Флориды,

Академический медицинский центр Университета Флориды — самый обширный академический медицинский центр на Юго-Востоке — предназначен для высококачественных программ образования, исследований, ухода за пациентами и государственных услуг.
Стоматологический колледж UF является единственной стоматологической школой во Флориде, финансируемой государством, и признан одним из лучших университетов США.S. Dental School за качество образовательных программ, исследовательскую деятельность в области гигиены полости рта и приверженность уходу и обслуживанию пациентов.
Медицинский колледж, крупнейший из шести колледжей Академического медицинского центра Университета Флориды, открылся в 1956 году с целью увеличения количества высококвалифицированных врачей во Флориде, предоставления передовых медицинских услуг жителям Флориды и содействия открытиям в области здравоохранения. исследование.
Колледж медсестер Университета Флориды, основанный в 1956 году, является ведущим учебным заведением для медсестер в штате Флорида и входит в 10% лучших медицинских программ для выпускников в стране.Колледж медсестер UF постоянно привлекает и сохраняет высочайший уровень студентов и преподавателей медсестер, увлеченных наукой и заботой.
Фармацевтический колледж, основанный в 1923 году, является старейшим колледжем Академического медицинского центра UF. Колледж, входящий в число лучших фармацевтических школ страны, поддерживает исследовательские, сервисные и образовательные программы, дополненные онлайн-технологиями.
Колледж общественного здравоохранения и медицинских профессий (PHHP) предназначен для предоставления отличных образовательных программ, которые готовят выпускников к удовлетворению многогранных медицинских потребностей населения, сообществ и отдельных лиц.
UF College of Veterinary Medicine — единственный ветеринарный колледж Флориды, предлагающий множество уникальных образовательных программ для студентов и услуг, направленных на помощь домашним животным, дикой природе и исчезающим видам. Мы предлагаем четырехлетние программы доктора ветеринарной медицины, а также M.S. и к.т.н. степени в области ветеринарной медицины.
Расположенный в одном месте с больницей Shands Jacksonville, Центр медицинских наук Джексонвилля выделяется в области образования, исследований и ухода за пациентами, что отражает наши неизменные ценности сострадания, совершенства, профессионализма и инноваций.Наш современный медицинский центр обслуживает 1 миллионное городское население от северной Флориды до южной Джорджии.
UFCOM-J предлагает аккредитованные программы ординатуры и стипендий для выпускников медицинского образования в дополнение к нестандартным программам стипендий. Клиническая ротация по всем основным дисциплинам предусмотрена для студентов-медиков UFCOM, а выборная ротация — для студентов из других аккредитованных школ.
UFHSC-J — это клинический учебный центр для медицинского колледжа в Гейнсвилле.Студенты поочередно проходят через различные клинические учреждения на территории кампуса, а также центры первичной медико-санитарной помощи и специализированные медицинские учреждения, расположенные по всему Джексонвиллю.
Фармацевтический колледж UF в Джексонвилле предлагает четырехлетнюю программу доктора фармацевтики (Pharm.D.), Полностью завершенную в Джексонвилле. Также на территории кампуса предлагается программа резидентуры в аптеке Shands Jacksonville, аккредитованная Американским обществом фармацевтов системы здравоохранения.
University of Florida Health знает, насколько важно постоянное медицинское обучение для поставщиков медицинских услуг и общества.Вот почему мы предлагаем онлайн-курсы непрерывного медицинского образования (CME), которые вы можете пройти для получения кредитов CME. Эти курсы знакомят с последними медицинскими знаниями, обучают новым навыкам взаимоотношений с пациентами и помогают поставщикам медицинских услуг решать актуальные текущие проблемы.
Нейтропения — младенцы Информация | Гора Синай
Выберите Failure SpecialtyAddiction MedicineAddiction PsychiatryAdolescent MedicineAdvanced сердца и TransplantAllergy и ImmunologyAlzheimer в DiseaseAnatomic Патология и клиническая PathologyAnesthesiologyBariatric SurgeryBlood Banking / Переливание MedicineBody ImagingBreast Рак — грудиПластика ImagingCancer (онкология) CardiologyCardiovascular компьютерной TomographyCardiovascular DiseaseCardiovascular SurgeryCerebrovascular Болезни / StrokeChild NeurologyChild и подростковая PsychiatryColon и ректальной хирургии / ProctologyCornea, Внешние болезни и Рефракционная хирургияМедицина критических состоянийКлиническая медицина — АнестезиологияСтоматологическая онкологияСтоматологияДерматологияДерматопатология — ДерматологияУхо, нос, горло / отоларингологияЭхокардиографияЭлектродиагностическая медицинаЭкстренная медицинаЭндокринная медицина, диабет и болезни костейГенерикологическая медицинаГенологическая медицина necologic OncologyHand SurgeryHead & шеи SurgeryHeadache MedicineHematology-OncologyHospital MedicineInfectious DiseaseInternal MedicineInterventional CardiologyInterventional NeuroradiologyInterventional RadiologyIntestinal TransplantationKidney / Поджелудочная TransplantationLiver MedicineLiver SurgeryLiver TransplantationMaternal и фетальный MedicineMetabolism / DiabetesNephrologyNeuro-OphthalmologyNeurocritical CareNeurologyNeuropsychologyNeuroradiologyNeurosurgeryNewborn MedicineNuclear CardiologyNuclear MedicineObesity MedicineObstetrics и GynecologyOccupational MedicineOcular OncologyOphthalmic PathologyOphthalmic Пластиковые SurgeryOphthalmologyOptometryOral / челюстно SurgeryOrthopedics & Ортопедические SurgeryPain ManagementPediatric & Подростков Гинекология, Детская аллергия и иммунология врачебный GastroenterologyPediatric Гематология-OncologyPediatric HepatologyPediatric Инфекционного DiseasesPediatric нефрология и HypertensionPediatric NeurologyPediatric NeurosurgeryPediatric OphthalmologyPediatric PulmonologyPediatric RadiologyPediatric RheumatologyPediatric Спорт MedicinePediatric SurgeryPediatric UrologyPediatricsPlastic и реконструктивная SurgeryPodiatryPrimary CarePsychiatryPsychologyPublic здоровье и общий Профилактический MedicinePulmonary MedicineRadiation OncologyRadiologyRehabilitation и физической MedicineReproductive EndocrinologyRetina — Medical & SurgicalRheumatologyShoulder & Elbow SurgerySleep MedicineSpinal шнур Травма MedicineSpine SurgerySports медицина ( Реабилитация) КосоглазиеХирургияХирургическая реанимацияХирургическая онкологияТоракальная хирургияТрансплантацияУрогинекологияУрологияУвеитСосудистая хирургия
Нейтропения (низкое количество нейтрофилов) — Клиника Мэйо
Нейтропения (noo-troe-PEE-nee-uh) возникает, когда у вас слишком мало нейтрофилов, типа белых кровяных телец.В то время как все белые кровяные тельца помогают вашему телу бороться с инфекциями, нейтрофилы важны для борьбы с некоторыми инфекциями, особенно вызванными бактериями.
Вы, вероятно, не узнаете, что у вас нейтропения. Люди часто узнают об этом только после того, как сдали анализ крови по другим причинам.
Один анализ крови, показывающий низкий уровень нейтрофилов, не обязательно означает, что у вас нейтропения. Эти уровни могут меняться изо дня в день, поэтому, если анализ крови показывает, что у вас нейтропения, его необходимо повторить для подтверждения.
Нейтропения может сделать вас более уязвимыми для инфекций. При тяжелой нейтропении даже нормальные бактерии изо рта и пищеварительного тракта могут вызвать серьезное заболевание.
28 декабря 2018 г. Показать ссылки- AskMayoExpert. Нейтропения. Рочестер, Миннесота: Фонд Мейо медицинского образования и исследований; 2017.
- Нейтропения и риск заражения. Центры по контролю и профилактике заболеваний. https://www.cdc.gov/cancer/preventinfections/neutropenia.htm. Проверено 4 декабря 2018 г.
- Берлинер Н. Обращение к взрослому с необъяснимой нейтропенией. https://www.uptodate.com/contents/search. По состоянию на 8 декабря 2018 г.
- Goldman L, et al., Ред. Лейкоцитоз и лейкопения. В: Медицина Гольдмана-Сесила. 25-е изд. Филадельфия, Пенсильвания: Сондерс Эльзевьер; 2016 г. https://www.clinicalkey.com. По состоянию на 8 декабря 2018 г.
- Bope ET, et al. Нейтропения. В: Текущая терапия Конна 2018. Филадельфия, Пенсильвания: Эльзевир; 2018. https: // www.Clinicalkey.com. По состоянию на 8 декабря 2018 г.
- McPherson RA, et al., Eds. Лейкоцитарные нарушения. В: Клиническая диагностика и лечение Генри лабораторными методами. 23-е изд. Сент-Луис, Миссури: Эльзевир; 2017. https://www.clinicalkey.com. По состоянию на 8 декабря 2018 г.
.
Нейтропения
Последний раз просмотрено доктором Мэри 7 августа 2018 г.
что такое нейтропения?
Это атипично низкое количество нейтрофилов.Нейтрофилы — это белые кровяные тельца, которые помогают иммунной системе бороться с инфекциями, особенно грибками, а также бактериями. В организме есть несколько видов лейкоцитов, и примерно от 45% до 70% всех лейкоцитов составляют нейтрофилы.
Границы определения нейтропении несколько различаются в зависимости от медицинской практики. Нейтропения у взрослых обычно определяется как любое количество нейтрофилов 1700 или меньше на микролитр крови. Количество клеток, представляющих нейтропению у детей, меняется с возрастом.
Чем ниже количество нейтрофилов, тем более восприимчивый человек к инфекционным заболеваниям. Если у человека тяжелая нейтропения — например, менее 500 клеток на микролитр крови — бактерии, которые обычно живут в вашей пищеварительной системе или во рту, могут вызывать инфекции.
Симптомы нейтропении
Нейтропению часто не замечают из-за отсутствия каких-либо специфических симптомов. Часто болезнь обнаруживается только после того, как у пораженного человека развиваются серьезные инфекции.Низкие уровни нейтрофилов обычно делают человека очень уязвимым к частым инфекциям. Любые бактерии, обычно присутствующие в организме, могут быстро вызвать инфекции, когда количество нейтрофилов значительно падает. Обычно у людей с нейтропенией наблюдаются лишь очень немногие симптомы, а некоторые симптомы могут быть вызваны и другими проблемами со здоровьем. Симптомы нейтропении включают:
- Частые инфекции
- Озноб
- Необъяснимая лихорадка
- Язвы в анальном проходе и во рту
- Боль в горле
- Увеличение лимфатических узлов
- Диарея
- Кожные инфекции
- Чувство жжения при мочеиспускании
- Редкое покраснение и припухлость вокруг любой раны или участка травмы
У некоторых людей есть циклическая нейтропения, которая проявляет все или только некоторые из симптомов, упомянутых выше, но только тогда, когда есть период низкого нейтрофила.Симптомы будут проявляться только в эти периоды, когда нейтрофилы упадут до значительно низкого уровня.
Причины нейтропении
Нейтропения может быть вызвана:
- Заболевания, которые являются врожденными и характеризуются плохой функцией костного мозга
- Рак или другие проблемы, которые могут повредить костный мозг
- Заболевания, которые являются аутоиммунными проблемами и разрушают клетки костного мозга, а также нейтрофилы
- Вирусные инфекции, нарушающие функцию костного мозга
- Инфекции, которые подавляют нейтрофилы и быстро расходуют их быстрее, чем они производятся
- Препараты, повреждающие костный мозг и разрушающие нейтрофилы
Некоторые возможные причины нейтропении могут включать:
- Алкоголизм
- Пересадка костного мозга
- Апластическая анемия
- Хроническая идиопатическая нейтропения у взрослых
- Химиотерапия
- Лекарственные средства, такие как диуретики и антибиотики
- Гепатит A, B, C
- ВИЧ / СПИД
- Гистоплазмоз
- Лейкемия
- Малярия
- Волчанка
- Мононуклеоз
- Миелофиброз
- Ревматоидный артрит
- Миелодиспластические синдромы
- Лучевая терапия
- Нейтропения, ассоциированная с синдромом
- Сепсис
- Синдром Шегрена
- Туберкулез
- Недостаточность витаминов
Диагноз нейтропении
Диагноз нейтропении ставится на основании анализа крови, при котором клетки крови подсчитываются в образце этой крови.Чтобы определить точную причину нейтропении в конкретном случае, обычно требуются другие тесты.
Некоторые другие тесты, которые также могут быть выполнены, включают:
- Тест на антинейтрофильные антитела
- Скрининг аутоантител
- Витамин B12
- Анализ фолиевой кислоты
- Тест на подкисленную сыворотку
- Тест на системную красную волчанку
Часто биопсия костного мозга выполняется, особенно если считается, что нейтропения вызвана серьезными заболеваниями.При подозрении на циклическую нейтропению проводят серийный подсчет нейтрофилов.
Лечение нейтропении
Лечение нейтропении будет сосредоточено на причинном заболевании или заболевании, наличии сопутствующих инфекций или симптомов, тяжести и общем состоянии здоровья человека. Часто лечение также должно быть направлено на любой основной процесс заболевания. Лечение, направленное непосредственно на нейтропению, может включать:
- Противогрибковые и / или антибиотические препараты для борьбы с инфекциями
- Введение и регулирование фактора роста лейкоцитов — например, «рекомбинантный фактор, стимулирующий колонии гранулоцитов», также называемый G-CSF или филграстим.Это для случаев очень тяжелой нейтропении
- Переливание гранулоцитов
- Кортикостероидная терапия
- Иммуноглобулин для внутривенного введения при нейтропении с подавленным иммунитетом
Меры предосторожности или превентивные меры
Меры, которые являются профилактическими, обычно должны применяться у пациентов с этим заболеванием, чтобы ограничить любой риск инфекций.
Личная гигиена
- Руки необходимо часто мыть антибактериальным мылом, особенно перед едой, после туалета и после рукопожатия.
- Ежедневное принятие ванны или душа с последующим легким похлопыванием по коже
- Для предотвращения проблем, связанных с сухой кожей, используйте увлажняющий крем
- Тщательная очистка прямой кишки после деятельности кишечника. Женщинам необходимо помнить о чистке перианальной области спереди назад.
- Уход за волосами, например стрижка ногтей. Не разрезайте и не рвите кутикулу, используйте крем для кутикулы, а также средство для удаления
- Никаких царапин и выдавливания пятен
- Используйте чистую электрическую бритву вместо безопасной или одноразовой бритвы
- Женщинам необходимо использовать гигиенические прокладки вместо тампонов, чтобы снизить риск заражения.
Техника безопасности
- Следует избегать людей с гриппом, простудой, открытыми язвами или другой инфекцией
- Избегать солнечных ожогов
- Избегайте закрытых, многолюдных общественных мест
- Обувь необходимо носить во избежание порезов
- Избегайте ректальных суппозиториев или термометров
- Беречь руки от ожогов и порезов
- Статус вакцинации необходимо обсудить с врачом. Лица, получающие химиотерапию, должны избегать контактов с людьми, которые недавно получили живую вакцину.
Дом
- В доме нельзя носить обувь снаружи
- Избегать любого контакта со стулом или мочой животных
- Избегать застоя воды, например, вазы, чашки для протезов, увлажнители
- Поддерживать чистоту печи и каналов
- Заменять фильтры воздуха или нагревателя ежемесячно
- Верхнюю одежду необходимо часто стирать в химчистке
Стоматологическая гигиена и гигиена полости рта
- Используйте зубную щетку с мягкой щеткой, чтобы остановить порезы во рту
- Не используйте зубную нить
- Промыть протезы свежей водой
- Полоскать рот хорошо и часто
- Любые запланированные или необходимые стоматологические работы необходимо предварительно обсудить с врачом.
- Антибактериальная терапия необходима после любой чистки зубов или другой работы
Образ жизни
- Обычные упражнения
- Достаточно отдыха
- Научитесь справляться со стрессом
- Узнайте об этой болезни.Знание — сила.
Диета для нейтропении
Так называемая нейтропеническая диета направлена на уменьшение количества поступающей в организм пищи, которая может содержать высокий уровень бактерий. В нашей пище обычно есть хорошие бактерии, но есть и плохие. Те, кто здоровы, обычно могут есть вредные бактерии, но это не относится к другим, у которых ослаблены иммунные функции.
Сырые фрукты и овощи
Свежие фрукты и овощи обычно несут бактерии даже после тщательной мойки.Людям с нейтропенией следует избегать сырых овощей, зелени, свежей сальсы, салатных батончиков и большинства свежих фруктов. Бананы и апельсины безопасны. Следует избегать непастеризованных фруктовых или овощных соков.
Сырые зерна
Можно использовать большинство крахмалов и злаков, но следует избегать любых злаков и хлеба, содержащих сырые орехи или овес. Сырые орехи и овес не подвергаются нагреванию, поэтому бактерии процветают. Также избегайте сырых макаронных изделий и не используйте для выпечки хлеба с активными дрожжами.
Редкое мясо и непастеризованные молочные продукты
Избегайте готовой или сырой рыбы, мяса или птицы. Все мясо должно быть хорошо прожарено. Эта диета запрещает сашими и суши, а также любые свежие мясные деликатесы, а также лосось / копченый лосось. Недоваренные яйца могут представлять опасность. Избегайте непастеризованного сыра, йогурта или молока.
Напитки без обработки
Пастеризация убивает все вредные живые микробы, поэтому любые фруктовые или овощные соки должны пройти эту процедуру.Избегайте холодных чаев. Колодезную воду необходимо кипятить не менее 1 минуты.
.
