Антитела класса IgG к капсидному антигену вируса Эпштейна-Барр (anti- Epstein-Barr viral capsid antigens IgG, EBV VCA IgG)
Метод определения Хемилюминесцентный иммуноанализ.
Исследуемый материал Сыворотка крови
Доступен выезд на дом
Онлайн-регистрацияМаркёр текущей или перенесённой инфекции вирусом Эпштейна-Барр.
Специфическая серологическая диагностика инфекции вирусом Эпштейна-Барр и вызванного этим вирусом инфекционного мононуклеоза основана на использовании комбинации тестов, выявляющих наличие IgG и IgM антител к различным антигенам, что позволяет дифференцировать инфекцию и уточнить стадию патологического процесса.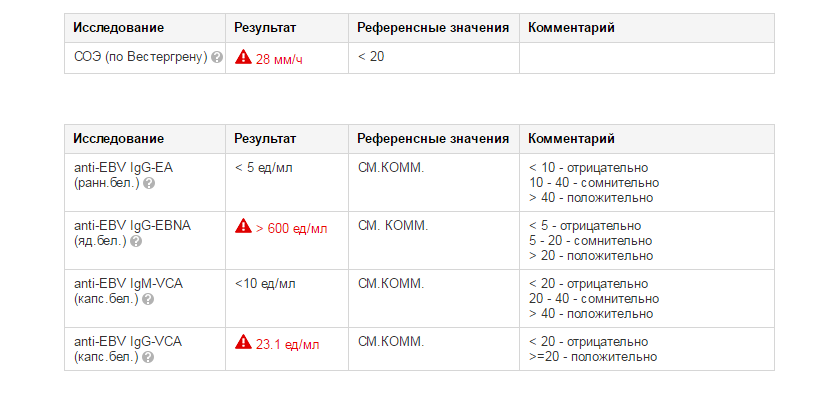
VCA IgG появляются вскоре после VCA IgM и в острой стадии инфекции обнаруживаются практически у всех больных. После выздоровления VCA IgG сохраняются пожизненно. При реактивации инфекции титры этих антител растут. Отрицательный результат данного теста обычно исключает прошлую инфекцию, хотя не всегда исключает острую инфекцию, если взятие крови было произведено в раннем периоде острой фазы, когда VCA IgG находятся ещё на неопределяемом уровне. При сохраняющихся клинических подозрениях в таких случаях следует повторить исследование через 10 — 14 дней для выявления сероконверсии. Положительный результат VCA IgG говорит об имевшей место экспозиции к вирусу. Дополнительное исследование VCA IgM (тест № 186) и EBNA IgG (тест № 187), а также EA-IgG (тест № 255) позволяет определить фазу инфекции (острая стадия, выздоровление, пастинфекция, реактивация).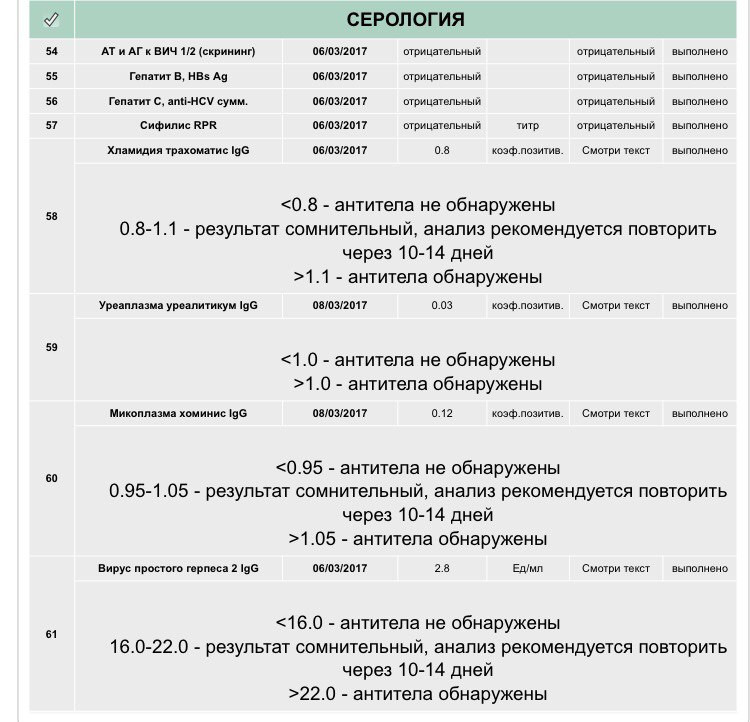
Тест используется в комбинации с тестами в Независимой лаборатории ИНВИТРО — анти-EA IgG № 255, анти-VCA IgM № 186, анти-EBNA IgG № 187 (см. таблицу).
Литература
- Инфекционные болезни у детей. Ред. Д. Марри. М. Практика, 2006. 928 с.
- Gorgievski-Hrisoho, W Hinderer, H Nebel-Schickel, et. al. Serodiagnosis of infectious mononucleosis by using recombinant Epstein-Barr virus antigens and enzyme-linked immunosorbent assay technology. J Clin Microbiol. 1990 October; 28(10): 2305 — 2311.
Анализы в KDL. Антитела к капсидному антигену вируса Эпштейна-Барр (Epstein-Barr virus), IgG
Вирус Эпштейна-Барр – вирус группы герпеса, связан с заболеванием инфекционным мононуклеозом. Считается, что ВЭБ- инфекция причастна к развитию лимфомы Беркитта, злокачественной носоглоточная карцинома. Вирус может размножаться в клетках верхних дыхательных путей, пищеварительного тракта и В-лимфоцитах. Заражение может произойти воздушно-капельным, контактно-бытовым или половым путем, так же в редких случаях возможно при медицинских манипуляциях.
Считается, что ВЭБ- инфекция причастна к развитию лимфомы Беркитта, злокачественной носоглоточная карцинома. Вирус может размножаться в клетках верхних дыхательных путей, пищеварительного тракта и В-лимфоцитах. Заражение может произойти воздушно-капельным, контактно-бытовым или половым путем, так же в редких случаях возможно при медицинских манипуляциях.
Заразиться можно как от больного человека, так и от здорового носителя. У людей со здоровой иммунной системой контакт с вирусом может пройти бессимптомно; вирус долго остается в организме в «спящей» форме, никак себя не проявляя. Заболевание чаще развивается у детей и подростков и при поступлении больших количеств вируса в организм. Вирус активно размножается и выделяется со слюной в течение примерно 6 месяцев. При заболевании могут наблюдаться: увеличение лимфатических узлов, повышение температуры тела, боли в мышцах и суставах, боли в горле, головная боль. По мере клинического выздоровления, симптомы исчезают, и вирус переходит в латентную форму.
В России инфицированность вирусом Эпштейна-Барр у детей составляет до 50%, а у взрослых около 90%. Из-за того, что в большинстве случаев болезнь протекает бессимптомно или с напоминающими обычную простуду, проявлениями, большинство носителей даже не знает, что они заражены. Одним из современных и эффективных методов диагностики встречи с вирусом является анализ крови на антитела к капсидному антигену вируса Эпштейна-Барр.
Известно, что вирус имеет четыре основных антигена: ранний, капсидный, мембранный и ядерный. Антигены вируса провоцируют иммунную систему на синтез соответствующих антител. Антитела к капсидному антигену могут появиться достаточно рано, уже со 2-ой недели с момента заражения, и достигают пиковых значений ко второму месяцу болезни. После выздоровления IgG к капсидному антигену сохраняются пожизненно, и их присутствие в крови свидетельствует о перенесенной инфекции и о наличии иммунитета к вирусу.
Антитела обладают определенной способностью связываться с антигенами вируса. Прочность такого связывания антигенов с антителами называется авидностью – это общее свойство всех антигенов и антител, в том числе и антител к вирусу Эпштейна – Барр. Прочность связывания антитела с вирусом выражена индексом авидности, который становится выше с прошествием времени от первой встречи с инфекцией.
В каких случаях обычно назначают исследование?
- Для подтверждения диагноза при клинических подозрениях на инфекционный мононуклеоз;
- Для оценки стадии течения заболевания;
- Для подтверждения заражения вирусом Эпштейна – Барр в прошлом при лимфопролиферативных и онкологических заболеваниях, связываемых с данным вирусом;
- При появлении симптомов гриппа и ОРВИ у беременных;
- При контакте человека с больным для оценки напряженности его иммунной системы и восприимчивости к инфекции.
Что именно определяется в процессе анализа?
Проводится определение концентрации антител класса IgG к капсидному антигену вируса Эпштейна-Барр в крови методом иммунохемилюминесцентного анализа.
Что означают результаты теста?
Положительный результат говорит о наличии у пациента иммунитета (после ранее перенесенной инфекции) либо о стадии выздоровления текущего заболевания. Отрицательный результат возможен при отсутствии инфекции либо ее ранней стадии, когда еще низкая концентрация антител к вирусу в крови; если есть подозрение на заражение вирусом Эпштейн-Барр, анализ рекомендуется повторить спустя 2-4 недели. Также отрицательный результат может быть получен при нарушениях синтеза антител у данного конкретного пациента
Сроки выполнения теста.
Результат исследования можно получить спустя 2-3 дня после сдачи анализа.
Как подготовиться к анализу?
Следует придерживаться общих правил подготовки к взятию крови из вены. Кровь можно сдавать не ранее, чем через 3 часа после приема пищи в течение дня, или утром натощак. Чистую воду можно пить в обычном режиме.
Анализы в KDL. Антитела к капсидному антигену вируса Эпштейна-Барр (Epstein-Barr virus), IgM
Вирус Эпштейна-Барр — основной возбудитель инфекционного мононуклеоза.
Наличие антител IgM к капсидному антигену (Epstein-Barr virus VCA) указывает на первичную инфекцию (эти антитела в большинстве случаев исчезают в пределах 3 месяцев после начала инфекции). Первичная инфекция характеризуется наличие иммуноглобулинов М при отсутствии антител класса IgG к ядерному антигену. Также IgM могут выявляться при хронически активном вирусе и при реактивации процесса.
В каких случаях обычно назначают исследование уровня антител к капсидному антигену вируса Эпштейна-Барр (Epstein-Barr virus VCA) IgМ?
- Клинические симптомы, подозрительные на инфекционный мононуклеоз
- Уточнение стадии ВЭБ-инфекции
- Для установления диагноза при ангинах в рамках дифференциальной диагностики
Как трактовать результаты теста?
Результат – обнаружено
- Острый и подострый период инфекции, вызванной ВЭБ (при отсутствии антитела к ядерному антигену IgG).

- Хроническая инфекция или реактивация (определяются также антитела к ядерному антигену IgG и антитела к капсидному антигену IgG).
Результат – не обнаружено
- Нет инфекции ВЭБ
- Инкубационный или ранний период заболевания (не успели выработаться антитела IgM)
- Поздняя инфекция (определяются только антитела класса IgG)
Сроки выполнения теста.
2-3 дня.
Как подготовиться к анализу?
Кровь берётся утром натощак или в течение дня или не ранее, чем через 3 часа после приёма пищи.
Вирус Эпштейна-Барр EBV (Epstein-Barr) в диагностическом центре «МедиСкан» в Домодедово
ЕBV (ВЭБ) — вирус, инфицирующий В-лимфоциты и вызывающий латентную инфекцию. EBV-синдром включает мононуклеоз и опухоли типа карциномы, В-клеточной лимфомы. EBV может вызвать энцефалит у взрослых больных СПИД и интерстициальный пневмонии у детей. 90-95% инфекционного мононуклеоза связано с EBV; остальные случаи связаны с цитомегаловирусом, Toxoplasma gondii, ВИЧ, аденовирусом или краснухой.
Различают следующие разновидности антигенов EBV:
- EBV-VCA — капсидный антиген вируса Эпштейна-Барр.
- EBV-EА — ранний антиген вируса Эпштейна-Барр.
- EBV-EBNA — ядерный антиген вируса Эпштейна-Барр.
Антитела к вирусному капсидному антигену IgM и IgG появляются в острой стадии; IgM снижается за 1-3 месяца; IgG может персистировать на низком уровне всю жизнь. Высокие титры IgG-вирусного капсидного антигена отмечены при лимфоме Беркитта и носоглоточной карциноме и у пациентов с иммуносупрессией.
Позитивные титры IgM- и IgG-EBV-VCA являются диагностическими признаками острого инфекционного процесса ( в том числе мононуклеоза). Диагностикумы выпускаются к антителам обоих классов — IgM и IgG.
Антитела к раннему антигену (к ранним белкам вируса) появляются также в острой стадии, но нарастание их происходит медленнее. Снижение уровня этих антител происходит спустя 2 месяца после инфицирования и могут исчезнуть вообще через год после инфицирования.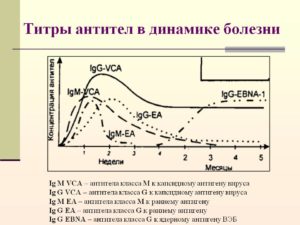 Диагностикумы выпускаются только для выявления антител IgG к раннему антигену (ранним белкам вируса).
Диагностикумы выпускаются только для выявления антител IgG к раннему антигену (ранним белкам вируса).
Для мониторирования инфицирования из этих двух видов антител нагляднее определять антитела к капсидному антигену.
Антитела к ядерному антигену появляются гораздо позже, спустя 4 недели после инфицирования, достигают высоких уровней и могут сохраняться всю жизнь, как показатель иммунитета (IgG-антитела). Определение антител класса IgM к ядерному антигену не имеет диагностического значения. Диагностикумы выпускаются к антителам класса IgG к ядерному антигену.
Для мониторирования инфицирования в нашей лаборатории предлагаются следующие виды тестов по определению антител к антигенам ВЭБ:
- АТ к ВЭБ-капсидный антиген (IgM) (VCA).
- АТ к ВЭБ-капсидный антиген (IgG) (VCA).
- АТ к ВЭБ-ранний антиген (ранние белки, IgG (EA).
- АТ к ВЭБ-ядерный антиген (IgG) (EBNA).
Дополнительное исследование — качественное и полуколичественное! Определение ЕВ-вируса в цельной крови пациента методом ПЦР.
Диагностическая значимость уровней ДНК и антител к капсидному антигену вируса Эпштейна–Барр в плазме крови больных раком носоглотки в неэндемическом регионе | Гурцевич
1. Young L.S., Rickinson A.B. Epstein-Barr virus: 40 years on. Nat Rev Cancer 2004;4:757–68.
2. Gu A.D., Zeng M.S., Qian C.N. The criteria to confirm the role of Epstein-Barr virus in nasopharyngeal carcinoma initiation. Int J Mol Sci 2012;13(10):13737–47.
3. Chang C.M., Yu K.J., Mbulaiteye S.M. et al. The extent of genetic diversity of Epstein-Barr virus and its geographic and disease patterns: a need for reappraisal. Virus Res 2009;143(2):209–21.
4. Yu M.C., Yuan J.M. Epidemiology of nasopharyngeal carcinoma. Semin Cancer Biol 2002;12(6):421–9.
Semin Cancer Biol 2002;12(6):421–9.
5. Licitra L., Bernier J., Cvitkovic E. et al. Cancer of the nasopharynx. Crit Rev Oncol Hematol 2003;45(2):199–213.
6. Давыдов М.И., Аксель Е.М. Статистика злокачественных новообразований в России и странах СНГ. Вестник РОНЦ им. Н.Н. Блохина РАМН 2008;19(2 прил. 1). [Davydov M.I., Axel E.M. Statistics of malignant neoplasms in Russia and CIS Countries. Vestnik RONC im. N.N. Blokhina RAMN = Herald of the N.N. Blokhin Russian Cancer Research Center with the RAMS 2008;19(2 Suppl 1). (In Russ.)].
7. Barnes L., Eveson J.W., Reichart P., Sidransky D. Pathology and genetics of head and neck tumors. Lyon: IARC Press, 2005.
8. Luo S., Zhao L., Wang J.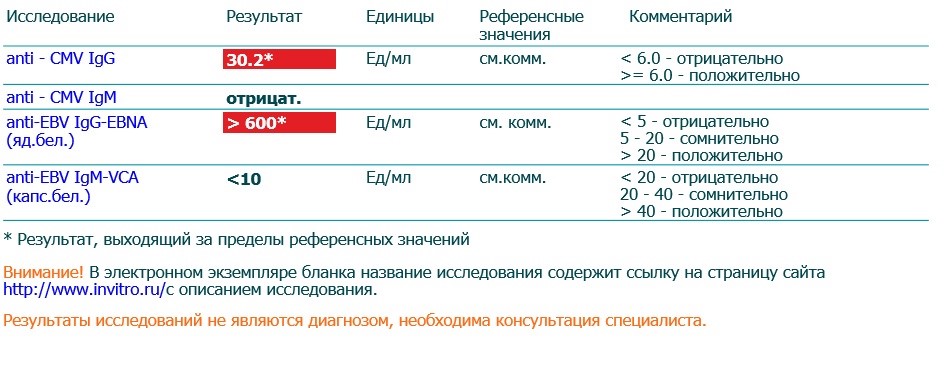 et al. Clinical outcomes for early-stage nasopharyngeal carcinoma with predominantly WHO II histology treated by intensity-modulated radiation therapy with or without chemotherapy in nonendemic region of China. Head Neck 2014;36(6):841–7.
et al. Clinical outcomes for early-stage nasopharyngeal carcinoma with predominantly WHO II histology treated by intensity-modulated radiation therapy with or without chemotherapy in nonendemic region of China. Head Neck 2014;36(6):841–7.
9. Brennan B. Nasopharyngeal carcinoma. Orphanet J Rare Dis 2006;1:23.
10. Cho W.C. Nasopharyngeal carcinoma: molecular biomarker discovery and progress. Mol Cancer 2007;6:1.
11. Hubert A., De-The G. Dietary behavior, way of life, and nasopharyngeal cancer. Bull Cancer 1982;69(5):476–82.
12. Li J., Qian C.N., Zeng Y.X. Regulatory T cells and EBV associated malignancies. Int Immunopharmacol 2009;9(5):590–2.
13. Li X., Fasano R., Wang E. et al. HLA associations with nasopharyngeal carcinoma. Curr Mol Med 2009;9(6):751–65.
Li X., Fasano R., Wang E. et al. HLA associations with nasopharyngeal carcinoma. Curr Mol Med 2009;9(6):751–65.
14. Yeung W.M., Zong Y.S., Chiu C.T. et al. Epstein-Barr virus carriage by nasopharyngeal carcinoma in situ. Int J Cancer 1993;53(5):746–50.
15. Gurtsevitch V., Ruiz R., Stepina V. et al. Epstein-Barr viral serology in nasopharyngeal carcinoma patients in the USSR and Cuba, and its value for differential diagnosis of the disease. Int J Cancer 1986;37(3): 375–81.
16. Pearson G.R. Epstein-Barr virus and nasopharyngeal carcinoma. J Cell Biochem Suppl 1993;17F:150–4.
17. Ho H.C., Ng M.H., Kwan H.C. Factors affecting serum IgA antibody to Epstein-Barr viral capsid antigens in nasopharyngeal carcinoma.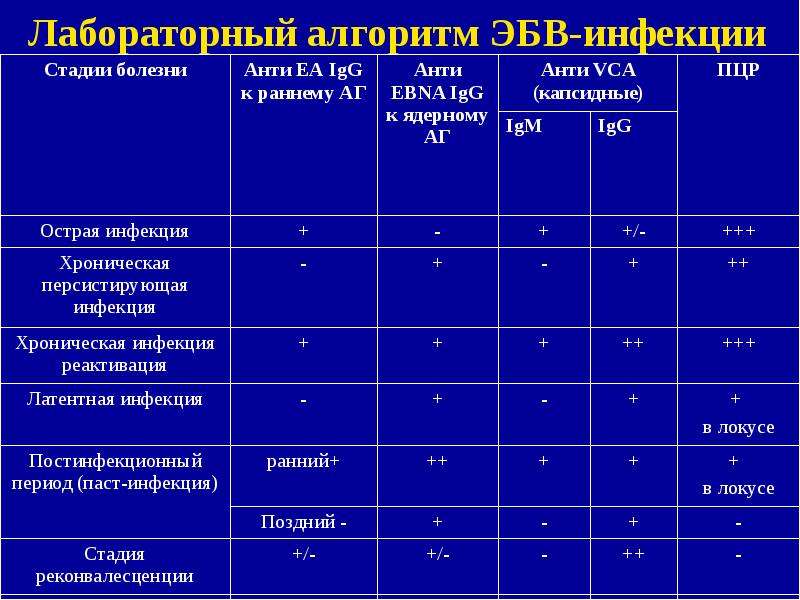 Br J Cancer 1978;37(3):356–62.
Br J Cancer 1978;37(3):356–62.
18. Song C., Yang S. A meta-analysis on the EBV DNA and VCA-IgA in diagnosis of nasopharyngeal carcinoma. Pak J Med Sci 2013;29(3):885–90.
19. Lichtenstein A.V., Melkonyan H.S., Tomei L.D., Umansky S.R. Circulating nucleic acids and apoptosis. Ann NY Acad Sci 2001;945:239–49.
20. Sidransky D. Emerging molecular markers of cancer. Nat Rev Cancer 2002;2(3):210–9.
21. Skvortsova T.E., Rykova E.Y., Tamkovich S.N. et al. Cell-free and cell-bound circulating DNA in breast tumours: DNA quantification and analysis of tumour-related gene methylation. Br J Cancer 2006;94(10):1492–5.
22. Lo Y.M., Chan L.Y., Chan A.T. et al. Quantitative and temporal correlation between circulating cell-free Epstein-Barr virus DNA and tumor recurrence in nasopharyngeal carcinoma. Cancer Res 1999;59(21): 5452–5.
Lo Y.M., Chan L.Y., Chan A.T. et al. Quantitative and temporal correlation between circulating cell-free Epstein-Barr virus DNA and tumor recurrence in nasopharyngeal carcinoma. Cancer Res 1999;59(21): 5452–5.
23. Hou X., Zhao C., Guo Y. et al. Different Clinical significance of pre- and posttreatment plasma Epstein-Barr virus DNA load in nasopharyngeal carcinoma treated with radiotherapy. Clin Oncol (R Coll Radiol) 2011; 23(2):128–33.
24. Wang W.Y., Twu C.W., Chen H.H. et al. Plasma EBV DNA clearance rate as a novel prognostic marker for metastatic/recurrent nasopharyngeal carcinoma. Clin Cancer Res 2010;16(3):1016–24.
25. Kondratova V.N., Botezatu I.V., Shelepov V.P., Lichtenstein A.V. Tube gel isotachophoresis: a method for quantitative isolation of nucleic acids from diluted solutions. Anal Biochem 2011;408(2):304–8.
Anal Biochem 2011;408(2):304–8.
26. Lawrence J.B., Villnave C.A., Singer R.H. Sensitive, high-resolution chromatin and chromosome mapping in situ: presence and orientation of two closely integrated copies of EBV in a lymphoma line. Cell 1988;52(1): 51–61.
27. Botezatu I.V., Kondratova V.N., Shelepov V.P., Lichtenstein A.V. DNA melting analysis: application of the «open tube» format for detection of mutant KRAS. Anal Biochem 2011;419(2):302–8.
28. Гурцевич В.Э., Степина В.Н., Сенюта Н.Б. и др. Гуморальный иммунный ответ к вирусу Эпштейна–Барр в диагностике рака носоглотки (обзор литературы и 30-летний опыт собственных исследований). Вестник РОНЦ им. Н.Н. Блохина РАМН 2011;22(2):20–30. [Gurtsevich V.E., Stepina V.N., Senyuta N.B. et al. Humoral immune response to Epstein–Barr virus in diagnostics of nasopharyngeal carcinoma (review of references and 30-year experience of own studies). Vestnik RONC im. N.N. Blokhina RAMN = Herald of the N.N. Blokhin Russian Cancer Research Center with the RAMS 2011;22(2): 20–30. (In Russ.)].
Vestnik RONC im. N.N. Blokhina RAMN = Herald of the N.N. Blokhin Russian Cancer Research Center with the RAMS 2011;22(2): 20–30. (In Russ.)].
29. Leung S.F., Chan K.C., Ma B.B. et al. Plasma Epstein-Barr viral DNA load at midpoint of radiotherapy course predicts outcome in advanced-stage nasopharyngeal carcinoma. Ann Oncol 2014; 25(6):1204–8.
Антитела класса IgG к капсидному антигену вируса Эпштейна-Барр
Синонимы: определение антител IgG к капсидному антигену вируса Эпштейна-Барр (ВЭБ, EBC), иммуноглобулин класса G к капсидному белку вируса Эпштейна-Барр, ВЭБ VCA-IgG, анти-VCA класса IgG, EBC VCA-IgG, Epstein-Barr viral capcid antogens IgG, EBV-VCA IgG, VCA IgG, Anti-EBV (VCA) IgG, EBV-IgG anti-VCA.
Связанные тесты: определение антител IgM к капсидному антигену вируса Эпштейна-Барр, выявление ДНК вируса Эпштейна-Барр, определение антител IgG к капсидному антигену вируса Эпштейна-Барр, авидность; определение ранних антигенов вируса Эпштейна-Барр,IgG; определение ядерных антигенов вируса Эпштейна-Барр, IgG; определение антител к ВИЧ 1,2 типа, общий анализ крови, биохимический анализ крови (Алт, Аст).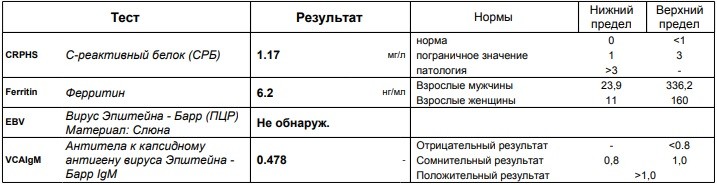
Исследование позволит вашему врачу:Антитела класса IgG к вирусу Эпштейна-Барр являются специфическими маркерами, свидетельствующими о текущем или перенесенном инфекционном мононуклеозе.
- Подтвердить текущий или перенесенный инфекционный мононуклеоз;
- Оценить стадию текущего инфекционного мононуклеоза;
- Оценить восприимчивость организма к инфекции, вызванной вирусом Эпштейна-Барр;
- Диагностировать лимфопролиферативные заболевания, связанные с вирусом Эпштейна-Барр;
- Диагностировать онкологические заболевания, связанные с вирусом Эпштейна-Барр.
Исследование рекомендуется проводить при:
- Боли в горле;
- Увеличении лимфатических узлов;
- Увеличении селезенки и/или печени;
- Лихорадке;
- Быстрой утомляемости;
- Людям, находившимся в тесном контакте с больными инфекционным мононуклеозом;
- Беременным с симптомами гриппа.

Метод:
Иммуноферментный анализ (ИФА).
Материал для исследования:
Сыворотка крови.
Подготовка к исследованиюИсследование проводится натощак. После последнего приема пищи должно пройти не менее 8 часов.
Особые условия:
Предварительная запись не требуется.
Формат выдачи результата:
«положительный», «отрицательный», «неопределенный».
Положительный результат может свидетельствовать о:
- Текущем или недавно перенесенном инфекционном мононуклеозе;
- Наличии активного иммунитета вследствие перенесенного ранее инфекционного мононуклеоза;
- Реактивации вируса Эпштейна-Барр.
Отрицательный результат может свидетельствовать о:
- Отсутствии вируса Эпштейна-Барр;
- Ранней стадии инфекционного мононуклеоза;
- Низком содержании вируса Эпштейна-Барр в крови;
- Отсутствии иммунного ответа или слабом иммунитете.

Комментарий:
Для выявления полной картины заболевания проводят серию серологических тестов.
Интерпретация результатов комплексного серологического тестирования при ВЭБ-инфекции
| Фаза инфекции | Капсидный антиген IgM | Капсидный антиген IgG | Наличие низкоавидных VCA-IgG | Ранний антиген IgG | Ядерный антиген IgG |
|---|---|---|---|---|---|
| Инкубационный период или отсутствие инфекции | – | – | Не определяют | – | – |
| Очень ранняя первичная инфекция | + | – | Не определяют | – | – |
| Ранняя первичная инфекция | + | + | + | + | – |
| Поздняя первичная инфекция | ± | + | ± | + | ± |
| Атипичная первичная инфекция | – | + | ± | + | ± |
| Реактивация | + | + | – | + | + |
| Ранняя паст-инфекция | – | + | ± | + | + |
| Поздняя паст-инфекция | – | + | – | – | + |
| Поздняя паст-инфекция, иммуносупрессия | – | + | – | – | – |
| Хроническая инфекция | ± | + | – | + | ± |
| Атипичная реактивация | – | + | – | + | + |
Авидность IgG к капсидному антигену Вирус Эпштейна-Барр (ВЭБ)
Описание
Вирус Эпштейна-Барр (ВЭБ) – это ДНК-содержащий вирус, является вирусом герпеса человека 4-го типа, относится к подсемейству гамма-герпесвирусов. ВЭБ имеет глобальное распространение и обнаруживается у населения всего земного шара.
ВЭБ имеет глобальное распространение и обнаруживается у населения всего земного шара.
Заразиться можно от больного человека и от здорового носителя вируса. ВЭБ передается от человека к человеку воздушно-капельным путем (при чихании, кашле, через слюну, при поцелуях), контактно-бытовым путем (через предметы), при половых контактах, при беременности вирус может проходить через плаценту и инфицировать плод, вирус может передаваться при переливании крови.
ВЭБ поражает эпителиальные клетки слизистых оболочек (дыхательных путей, пищеварительной системы, половых органов), а также клетки иммунной системы, в том числе В-лимфоциты, в которых происходит размножение вируса.
Чаще всего вирусом заражаются в детстве. У детей инфекция в основном протекает бессимптомно или в стертой форме (в виде респираторной инфекции). У взрослых людей в 90% случаев инфекция также протекает без признаков заболевания.
Инфицирование ВЭБ может проявляться в виде инфекционного мононуклеоза: повышается температура тела, возникает боль в горле, увеличиваются лимфатические узлы, печень и селезенка. При проведении клинического анализа крови выявляется увеличение лимфоцитов, могут быть обнаружены атипичные мононуклеары.
При проведении клинического анализа крови выявляется увеличение лимфоцитов, могут быть обнаружены атипичные мононуклеары.
После первичного инфицирования вирус Эпштейна—Барр остается в организме пожизненно, персистируя в В-лимфоцитах и отдельных клетках эпителия. В определенных условиях, при снижении иммунитета, гормональных перестройках, после перенесенных заболеваний, вирус может активироваться.
При хроническом течении инфекции может развиться синдром хронической усталости.
ВЭБ может принимать участие в развитии некоторых опухолей: лимфомы Беркетта, карциномы носоглотки, болезни Ходжкина, саркомы Капоши. Заболевания, вызванные вирусом Эпштейн-Барр, встречаются редко. Чаще они развиваются у лиц с генетической предрасположенностью или выраженным иммунодефицитным состоянием.
Для чего определяют иммуноглобулины?
Антитела (иммуноглобулины) характеризуют течение инфекции. Определение антител в крови является методом косвенной диагностики инфекции, они показывают реакцию иммунной системы человека на внедрение возбудителя.
Организм человека вырабатывает антитела к белкам (антигенам) вируса Эпштейна-Барр, наиболее важными для диагностики являются антитела к капсидному антигену вируса (VCA), к раннему антигену (EA), к ядерному антигену (NA).
По мере формирования иммунного ответа к инфекции антитела разных классов сменяют друг друга. Сначала на проникновение чужеродного микроорганизма начитают вырабатываться специфичные к данному возбудителю иммуноглобулины класса М (IgM), позже специфичные иммуноглобулины класса G (IgG).
Антитела к разным белкам вируса синтезируются в определенные сроки от инфицирования ВЭБ. Анализ комплекса антител позволяет установить стадию заболевания, контролировать эффективность лечения.
Что показывает анализ на авидность IgG к капсидному антигену ВЭБ?
Защитные антитела связываются с попавшими в организм человека вирусами и бактериями (антигенами), чтобы нейтрализовать их. Авидность — это прочность связи антигена с антителом.
На начальных этапах инфекции IgG непрочно связывают антиген, обладают низкой авидностью, в дальнейшем прочность связи укрепляется и начинают вырабатываться высокоавидные антитела.
По индексу авидности можно установить давность инфицирования, отличить первичную инфекцию от реактивации или перенесенной инфекции в прошлом.
Низкоавидные антитела характерны для первичного инфицирования, они выявляются в течение первого месяца от инфицирования ВЭБ, могут определяться до нескольких месяцев. Затем происходит созревание антител и увеличение индекса авидности.
Высокоавидные антитела свидетельствуют о давнем инфицировании, перенесенной инфекции в прошлом.
Тесты на авидность проводят в случае положительных результатов определения антител, чтобы исключить или подтвердить первичное инфицирование.
Кому показано обследование на авидность IgG к капсидному антигену ВЭБ?
- Людям с проявлениями инфекционного мононуклеоза.

- Людям с подозрением на инфекцию, вызванную ВЭБ.
Какие тесты может назначить врач для диагностики инфицирования вирусом Эпштейна-Барр?
Для диагностики инфекции, вызванной ВЭБ, проводятся исследования крови на антитела к различным белкам вируса, по анализам устанавливается стадия инфекции.
Методом ИФА определяются:
- вирус Эпштейна-Барр IgM к капсидному антигену IgM-VCA,
- вирус Эпштейна-Барр IgG к капсидному антигену IgG-VCA,
- авидность IgG к капсидному антигену ВЭБ,
- вирус Эпштейна-Барр IgG к раннему антигену IgG-EA,
- вирус Эпштейна-Барр IgG к ядерному антигену IgG-NA.
Методом ПЦР анализа проводят прямое обнаружение вируса в биологическом материале, определяется количество ДНК ВЭБ в пробах пациента.
Результата анализа
Полученный результат исследования обязательно должен интерпретировать лечащий врач с учетом всех данных о состоянии здоровья пациента и комплекса проведенных лабораторных анализов.
Правила подготовки
Тест на вирус Эпштейна-Барра (EBV): цель, процедура и риски
Мы включаем продукты, которые, по нашему мнению, полезны для наших читателей. Если вы покупаете по ссылкам на этой странице, мы можем получить небольшую комиссию. Вот наш процесс.
Что такое тест на вирус Эпштейна-Барра?
Вирус Эпштейна-Барра (ВЭБ) является членом семейства вирусов герпеса. Это один из самых распространенных вирусов, заражающих людей по всему миру.
По данным Центров по контролю и профилактике заболеваний, большинство людей в какой-то момент своей жизни заразятся ВЭБ.
Вирус обычно не вызывает симптомов у детей. У подростков и взрослых он вызывает заболевание, называемое инфекционным мононуклеозом, или мононуклеозом, примерно в 35-50 процентах случаев.
Также известный как «болезнь поцелуев», ВЭБ обычно передается через слюну. Очень редко заболевание передается через кровь или другие жидкости организма.
Тест на ВЭБ также известен как «антитела к ВЭБ». Это анализ крови, используемый для выявления ВЭБ-инфекции. Тест определяет наличие антител.
Это анализ крови, используемый для выявления ВЭБ-инфекции. Тест определяет наличие антител.
Антитела — это белки, которые иммунная система вашего организма выделяет в ответ на вредное вещество, называемое антигеном. В частности, тест на EBV используется для выявления антител к антигенам EBV. Тест может выявить как текущую, так и перенесенную инфекцию.
Ваш врач может назначить этот тест, если у вас появятся какие-либо признаки и симптомы моно. Симптомы обычно длятся от одной до четырех недель, но в некоторых случаях они могут длиться до трех-четырех месяцев. К ним относятся:
Ваш врач может также принять во внимание ваш возраст и другие факторы при принятии решения о назначении теста или нет.Моно чаще всего встречается у подростков и молодых людей в возрасте от 15 до 24 лет.
Тест на ВЭБ — это анализ крови. Во время теста кровь берется в кабинете врача или в амбулаторной клинической лаборатории (или больничной лаборатории). Кровь берется из вены, обычно на внутренней стороне локтя. Процедура состоит из следующих этапов:
Процедура состоит из следующих этапов:
- Место прокола очищается антисептиком.
- Эластичная лента оборачивается вокруг плеча, чтобы вена набухала от крови.
- В вену осторожно вводится игла для забора крови в прикрепленный флакон или пробирку.
- Резинка снята с руки.
- Проба крови отправлена в лабораторию для анализа.
Очень мало (или даже ноль) антител может быть обнаружено на ранней стадии болезни. Таким образом, возможно, потребуется повторить анализ крови через 10–14 дней.
Как и при любом анализе крови, существует небольшой риск кровотечения, синяков или инфекции в месте прокола. При введении иглы вы можете почувствовать умеренную боль или резкий укол.Некоторые люди чувствуют головокружение или слабость после анализа крови.
Нормальный результат означает, что в вашем образце крови не было антител против EBV. Это означает, что вы никогда не были инфицированы EBV и не болеете моно. Тем не менее, вы все равно можете получить его в любой момент в будущем.
Ненормальный результат означает, что тест обнаружил антитела к EBV. Это означает, что вы в настоящее время инфицированы EBV или были инфицированы этим вирусом в прошлом. Ваш врач может определить разницу между прошлой и текущей инфекцией на основании наличия или отсутствия антител, которые борются с тремя специфическими антигенами.
Три антитела, которые ищет тест, — это антитела к вирусному капсидному антигену (VCA) IgG, VCA IgM и ядерному антигену Эпштейна-Барра (EBNA). Уровень антител, обнаруженный в крови, называемый титром, никак не влияет на то, как долго вы страдаете этим заболеванием или насколько серьезным оно является.
- Присутствие антител VCA IgG указывает на то, что инфекция ВЭБ произошла недавно или в прошлом.
- Наличие антител VCA IgM и отсутствие антител к EBNA означает, что инфекция произошла недавно.
- Наличие антител к EBNA означает, что заражение произошло в прошлом. Антитела к EBNA развиваются через шесть-восемь недель после заражения и присутствуют на протяжении всей жизни.

Как и в любом другом тесте, бывают ложноположительные и ложноотрицательные результаты. Ложноположительный результат теста показывает, что у вас есть болезнь, хотя на самом деле это не так. Ложноотрицательный результат теста означает, что вы не болеете, хотя на самом деле болеете. Спросите своего врача о любых последующих процедурах или шагах, которые помогут убедиться, что результаты ваших анализов точны.
Нет известных методов лечения, противовирусных препаратов или вакцин для монотерапии. Однако есть вещи, которые вы можете сделать, чтобы облегчить симптомы:
- Поддерживайте водный баланс и пейте много жидкости.
- Больше отдыхайте и избегайте интенсивных занятий спортом.
- Примите безрецептурные болеутоляющие, например ибупрофен (Адвил) или ацетаминофен (Тайленол).
Вирус трудно поддается лечению, но симптомы обычно проходят сами по себе в течение одного-двух месяцев.
После того, как вы выздоровеете, EBV останется в ваших кровяных клетках в спящем состоянии до конца вашей жизни.
Это означает, что ваши симптомы исчезнут, но вирус останется в вашем теле и может время от времени активироваться, не вызывая симптомов. В это время можно передать вирус другим людям через рот в рот.
Эпштейн-Барр | Мононуклеоз | Лабораторные испытания | Моно
Вирус Эпштейна-Барра (EBV), также известный как вирус герпеса человека 4, представляет собой гамма-вирус герпеса, который встречается только у людей. Лабораторные исследования могут помочь определить, подвержен ли человек заражению ВЭБ, имеет ли он недавнюю или прошлую инфекцию.
Медицинские работники могут проводить тестирование на антитела к следующим антигенам, связанным с EBV:
На этой микрофотографии изображены лейкозные клетки, содержащие вирус Эпштейна-Барра, с использованием метода окрашивания FA.
- Антиген вирусного капсида (VCA)
- Анти-VCA IgM появляются на ранней стадии инфицирования EBV и обычно исчезают в течение четырех-шести недель.
- Anti-VCA IgG появляется в острой фазе EBV-инфекции, достигает пика через две-четыре недели после начала, незначительно снижается, а затем сохраняется на протяжении всей жизни человека.

- Ранний антиген (EA)
Anti-EA IgG появляется в острой фазе болезни и обычно падает до неопределяемого уровня через три-шесть месяцев. У многих людей обнаружение антител к EA является признаком активной инфекции. Однако 20% здоровых людей могут иметь антитела против EA в течение многих лет. - Ядерный антиген EBV (EBNA)
Антитело к EBNA, определенное с помощью стандартного иммунофлуоресцентного теста, не обнаруживается в острой фазе EBV-инфекции, но медленно проявляется через два-четыре месяца после появления симптомов и сохраняется на протяжении всего остального периода. жизнь.Другие иммуноферментные анализы EBNA могут давать ложноположительные результаты. - Тест на одно пятно
Тест на одно пятно не рекомендуется для общего использования. Антитела, обнаруживаемые Monospot, могут быть вызваны другими причинами, кроме инфекционного мононуклеоза. Более того, исследования показали, что Monospot дает как ложноположительные, так и ложноотрицательные результаты. Например, гетерофильные антитела, обнаруживаемые с помощью Monospot, часто отсутствуют у детей с инфекционным мононуклеозом. В лучшем случае тест Monospot может указывать на то, что у человека типичный случай инфекционного мононуклеоза, но не подтверждает наличие инфекции EBV.
Например, гетерофильные антитела, обнаруживаемые с помощью Monospot, часто отсутствуют у детей с инфекционным мононуклеозом. В лучшем случае тест Monospot может указывать на то, что у человека типичный случай инфекционного мононуклеоза, но не подтверждает наличие инфекции EBV.
Интерпретация тестов на антитела к EBV
Тесты на антителак ВЭБ обычно не нужны для диагностики инфекционного мононуклеоза. Однако могут потребоваться специальные тесты на антитела для определения причины заболевания у людей, у которых нет типичного случая инфекционного мононуклеоза или есть другие заболевания, которые могут быть вызваны инфекцией EBV. Симптомы инфекционного мононуклеоза обычно проходят в течение четырех недель. Если человек болеет более шести месяцев и не имеет лабораторно подтвержденного диагноза ВЭБ-инфекции, следует рассмотреть другие причины хронического заболевания или синдрома хронической усталости.
Интерпретация тестов на антитела к ВЭБ требует знакомства с этими тестами и доступа к клинической информации пациента.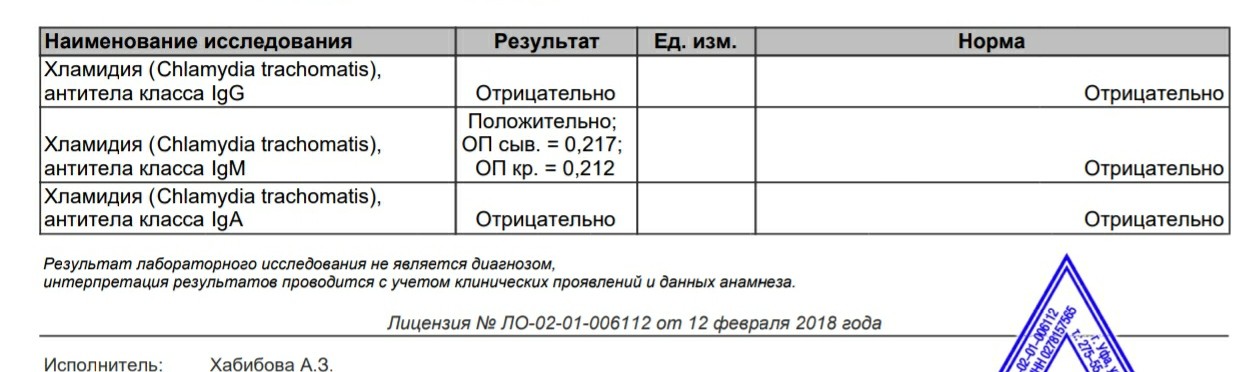
Интерпретация тестов на антитела к ВЭБ и диагностика инфекции ВЭБ резюмируется следующим образом:
- Восприимчивость к инфекции
Люди считаются восприимчивыми к ВЭБ-инфекции, если у них нет антител к VCA. - Первичная (новая или недавняя) инфекция
Считается, что люди имеют первичную инфекцию ВЭБ, если у них есть IgM к VCA, но нет антител к EBNA.Другие результаты, которые убедительно указывают на первичную инфекцию, — это высокий или повышающийся уровень анти-VCA IgG и отсутствие антител к EBNA по крайней мере после четырех недель болезни. Излечение болезни может произойти до того, как появятся диагностические уровни антител. В редких случаях у людей с активной инфекцией EBV может не быть обнаруживаемых антител, специфичных для EBV. - Инфекция в прошлом
Наличие антител как к VCA, так и к EBNA свидетельствует о перенесенной инфекции (от нескольких месяцев до лет назад).Поскольку более 90% взрослых инфицированы ВЭБ, у большинства взрослых обнаруживаются антитела к ВЭБ, полученные от инфекции годами ранее. Высокие или повышенные уровни антител могут присутствовать в течение многих лет и не являются признаком недавней инфекции.
Высокие или повышенные уровни антител могут присутствовать в течение многих лет и не являются признаком недавней инфекции.
Тестирование парных образцов сыворотки в острой фазе и в фазе выздоровления не помогает различать недавние и перенесенные ВЭБ-инфекции. В большинстве случаев ответ антител происходит быстро во время первичной инфекции EBV. Клинические проявления инфекционного мононуклеоза возникают одновременно с появлением антител IgG и IgM к VCA.Однако структура антител нестабильна до появления симптомов.
Тесты на антитела к вирусу Эпштейна-Барра (EBV)
Источники, использованные в текущем обзоре
(апрель 2011 г.) Су-Мэй Цао и др. Колебания серологических антител к вирусу Эпштейна-Барра и риск карциномы носоглотки: проспективное скрининговое исследование с последующим 20-летним наблюдением. PLOS One. Доступно в Интернете по адресу http://journals.plos.org/plosone/article?id=10.1371/journal.pone.0019100. По состоянию на 12 июня 2016 г.
(январь 2014 г.) Центры по контролю и профилактике заболеваний. Вирус Эпштейна-Барра и инфекционный мононуклеоз. Доступно в Интернете по адресу http://www.cdc.gov/epstein-barr/laboratory-testing.html. По состоянию на 11 июня 2016 г.
(октябрь 2015 г.) Cunha, B.A., et al. Обследование при инфекционном мононуклеозе. Medscape. Доступно в сети по адресу http://emedicine.medscape.com/article/222040-workup. Проверено 13 июня 2016 г.
(август 2004 г.) Хесс, Р. Рутинная диагностика вируса Эпштейна-Барра с лабораторной точки зрения: все еще сложно после 35 лет. Журнал клинической микробиологии. Доступно в Интернете по адресу http://www.ncbi.nlm.nih.gov/pmc/articles/PMC497621/. По состоянию на 11 июня 2016 г.
(2015) Решкова В.В. и др. Оценка противовирусных антител против вируса Эпштейна-Барра и нейротрансмиттеров у пациентов с фибромиалгией. Журнал неврологии и неврологии . Доступно в Интернете по адресу http://www.jneuro.com/neurology-neuroscience/evaluation-of-antiviral-antibodies-against-epsteinbarr-virus-and-neurotransmitters-in-patients-with-fibromyalgia. php? aid = 7360. По состоянию на 11 июня 2016 г.
php? aid = 7360. По состоянию на 11 июня 2016 г.
Источники, использованные в предыдущих обзорах
Томас, Клейтон Л., редактор (1997). Циклопедический медицинский словарь Табера. Компания F.A. Davis, Филадельфия, Пенсильвания [18-е издание].
Пагана, Кэтлин Д. и Пагана, Тимоти Дж. (2001). Справочник по диагностическим и лабораторным испытаниям Мосби, 5-е издание: Mosby, Inc., Сент-Луис, Миссури. С. 373-375.
Эбелл, М. (1 октября 2004 г.). Инфекционный мононуклеоз вируса Эпштейна-Барра.Американский семейный врач [Интернет-журнал]. Доступно в Интернете по адресу http://www.aafp.org/afp/20041001/1279.html.
Леви Д. (19 января 2004 г., обновлено). Тест на вирус Эпштейна-Барра. Медицинская энциклопедия MedlinePlus [Он-лайн информация]. Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/003513.htm.
(© 1995-2005). Инфекция вируса Эпштейна-Барра. Руководство Merck — Second Home Edition [Электронная информация]. Доступно в Интернете по адресу http://www.merck.com/mmhe/sec17/ch298/ch298f.html.
Доступно в Интернете по адресу http://www.merck.com/mmhe/sec17/ch298/ch298f.html.
(© 2005). Вирус Эпштейна-Барра. Руководство ARUP по клиническим лабораторным исследованиям [он-лайн информация]. Доступно в Интернете по адресу http://www.aruplab.com/guides/clt/tests/clt_a238.jsp#1147825.
Шмид С., руководитель группы по герпесвирусам (13 сентября 2005 г., обновлено). Вирус Эпштейна-Барра и инфекционный мононуклеоз. CDC, Национальный центр инфекционных заболеваний [онлайн-информация]. Доступно в Интернете по адресу http://www.cdc.gov/ncidod/diseases/ebv.htm.
Пагана, Кэтлин Д. и Пагана, Тимоти Дж.(© 2007). Справочник по диагностическим и лабораторным испытаниям Мосби, 8-е издание: Mosby, Inc., Сент-Луис, Миссури. С. 401-403.
Ву, А. (2006). Клиническое руководство по лабораторным исследованиям Титца, четвертое издание. Сондерс Эльзевир, Сент-Луис, Миссури. С. 1556-1557.
Томас, Клейтон Л., редактор (1997). Циклопедический медицинский словарь Табера. Компания F.A. Davis, Филадельфия, Пенсильвания [18-е издание]. Стр. 663.
Компания F.A. Davis, Филадельфия, Пенсильвания [18-е издание]. Стр. 663.
Смит, Д. С. (6 августа 2007 г.). Тест на вирус Эпштейна-Барра. Медицинская энциклопедия MedlinePlus [Он-лайн информация].Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/003513.htm. Доступ 23.11.08.
Беннет, Н. Дж. И Домачовске, Дж. (12 августа 2008 г.). Мононуклеоз и вирусная инфекция Эпштейна-Барра. eMedicine [Он-лайн информация]. Доступно в Интернете по адресу http://www.emedicine.com/ped/TOPIC705.HTM. Доступ 23.11.08.
(© 2006-2008). Вирус Эпштейна-Барра — EBV. ARUP Консультации [Он-лайн информация]. Доступно в Интернете по адресу http://www.arupconsult.com/Topics/InfectiousDz/Viruses/EBV.html. Доступ 23.11.08.
Персонал клиники Мэйо (28 июня 2008 г.). Мононуклеоз. MayoClinic [Он-лайн информация]. Доступно в Интернете по адресу http://www.mayoclinic.com/health/mononucleosis/DS00352. Доступ 23.11.08.
(ноябрь 2005 г.). Инфекционный мононуклеоз. Пособие Merck для специалистов здравоохранения [Он-лайн информация]. Доступно в Интернете по адресу http://www.merck.com/mmpe/sec14/ch289/ch289f.html?qt=EBV&alt=sh. Доступ 23.11.08.
Пособие Merck для специалистов здравоохранения [Он-лайн информация]. Доступно в Интернете по адресу http://www.merck.com/mmpe/sec14/ch289/ch289f.html?qt=EBV&alt=sh. Доступ 23.11.08.
Peridin F, et. al (опубликовано в сети 28 марта 2007 г.).Сравнение коммерческих и собственных ПЦР-анализов в реальном времени для количественного определения ДНК вируса Эпштейна-Барра (EBV) в плазме. BMC Microbiol . 2007; 7: 22. Доступно в Интернете по адресу http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=pmc1852802. По состоянию на январь 2009 г.
(обновлено 2 февраля 2009 г.) Центры по контролю и профилактике заболеваний. Вирус Эпштейна-Барра и инфекционный мононуклеоз. Доступно в Интернете по адресу http://www.cdc.gov/ncidod/diseases/ebv.htm. По состоянию на февраль 2009 г.
Беннет, Н.и Домачовске Дж. (обновлено 30 мая 2012 г.). Детский мононуклеоз и вирусная инфекция Эпштейна-Барра. Справочник по Medscape [Он-лайн информация]. Доступно в Интернете по адресу http://emedicine. medscape.com/article/963894-overview. По состоянию на ноябрь 2012 г.
medscape.com/article/963894-overview. По состоянию на ноябрь 2012 г.
Форвик, Л. (Обновлено 24 августа 2011 г.). Тест на вирус Эпштейна-Барра. Медицинская энциклопедия MedlinePlus [Он-лайн информация]. Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/003513.htm. По состоянию на ноябрь 2012 г.
Дельгадо, Дж.et. al. (Обновлено в августе 2012 г.). Вирус Эпштейна-Барра — EBV. ARUP Консультации [Он-лайн информация]. Доступно в Интернете по адресу http://www.arupconsult.com/Topics/EBV.html?client_ID=LTD. По состоянию на ноябрь 2012 г.
(© 1995-2012). Профиль антител к вирусу Эпштейна-Барра (EBV), сыворотка. Клиника Мэйо Медицинские лаборатории Мэйо [Он-лайн информация]. Доступно в Интернете по адресу http://www.mayomedicallaboratories.com/test-catalog/Overview/84421. По состоянию на ноябрь 2012 г.
Кунья Б. и Леви К. (Обновлено 21 сентября 2011 г.).Инфекционный мононуклеоз. Справочник по Medscape [Он-лайн информация]. Доступно в Интернете по адресу http://emedicine. medscape.com/article/222040-overview. По состоянию на ноябрь 2012 г.
medscape.com/article/222040-overview. По состоянию на ноябрь 2012 г.
Персонал клиники Мэйо (26 июня 2010 г.). Мононуклеоз. Клиника Мэйо [Он-лайн информация]. Доступно в Интернете по адресу http://www.mayoclinic.com/print/mononucleosis/DS00352/DSECTION=all&METHOD=print. По состоянию на ноябрь 2012 г.
Пагана, К. Д. и Пагана, Т. Дж. (© 2011). Справочник Мосби по диагностическим и лабораторным испытаниям, 10-е издание: Mosby, Inc., Сент-Луис, Миссури. С. 407-409.
Kasper DL, Braunwald E, Fauci AS, Hauser SL, Longo DL, Jameson JL eds, (2005) Harrison’s Principles of Internal Medicine, 16th Edition, McGraw Hill, pp 1046-1048.
Клиническая диагностика и лечение Генри с помощью лабораторных методов. 21-е изд. Макферсон Р., Пинкус М., ред. Филадельфия, Пенсильвания: Saunders Elsevier: 2007, стр. 555-556.
Мини-обзор Гесса Р.: Рутинная лабораторная диагностика вируса Эпштейна-Барра, перспектива: спустя 35 лет все еще сложно. Журнал клинической микробиологии , август 2004 г. , Vol. 42, No. 8., Pg. 3381–3387.
, Vol. 42, No. 8., Pg. 3381–3387.
Панель полного исследования вируса Эпштейна-Барра
Панель полного исследования вируса Эпштейна-Барра
Химия
6240 RCP
356-3527
Средний сбор:
| Пробирка сепаратора плазмы 4,5 мл |
Альтернативный Медиа коллекции:
Розовая верхняя пробирка 6 мл (K2-EDTA) или Красная верхняя пробирка 5 мл (активатор свертывания)
Минимум:
3.0 мл цельной крови или ДВА устройства Microtainer ® .
График испытаний:
24 часа в сутки, 7 дней в неделю, включая праздники.
Turn Around Время:
3 часа (при поступлении в лабораторию)
Базовый диапазон:
Референсные диапазоны изменены с 11.12.2012. Контрольный диапазон для всех аналитов (Heterophile IgM, VCA IgG, VCA IgM, EBNA): 0,8 AI или меньше: отрицательно 0.9-1.0 AI: неопределенный 1.1 AI или выше: положительный
Пояснительные данные:
Вирус Эпштейна-Барра (EBV) является этиологическим агентом инфекционного мононуклеоз. Инфекцию ВЭБ трудно диагностировать с помощью лабораторные испытания; однако большинство острых инфекций могут быть распознается путем тестирования сыворотки пациента на гетерофильные антитела (например, методом латексной агглютинации "Моноспот"), который обычно появляются в течение первых 3 недель болезни, но затем быстро исчезают в течение нескольких недель.Гетерофильные антитела обнаруживаются в очень высоких процент младенцев и детей старшего возраста с острым мононуклеозом. Тем не менее, примерно в 10% случаев гетерофильные антитела не развиваются. Взрослые. В случаях, когда есть подозрение на ВЭБ, но гетерофильные антитела не обнаружен, оценка панели из 4 антител к EBV может быть полезно: Гетерофил IgM Вирусный капсидный антиген (VCA) IgG VCA IgM Ядерные антитела против ВЭБ (EBNA) Заражение EBV обычно происходит в раннем возрасте, как правило, как инфекционный мононуклеоз.Другие расстройства, вызванные инфекцией ВЭБ, включают: были признаны, включая лимфому Беркитта и носоглотку карцинома. Инфекция ВЭБ также может вызывать лимфопролиферативные синдромы, особенно у пациентов, перенесших почечный или костный мозг трансплантации и у больных СПИДом. Наличие антител IgM к VCA указывает на недавнюю первичную инфекцию EBV. Наличие антител VCA IgG иногда указывает на инфекцию. в прошлом. Антитела к EBNA развиваются через 6-8 недель после первичного инфекции и обычно обнаруживаются на всю жизнь.Более 90% от нормы взрослое население имеет антитела класса IgG к VCA и EBNA. Несколько у пациентов, инфицированных EBV, не разовьется антитела к EBNA (примерно 5% -10%). Интерпретация серологических паттернов ВЭБ адаптирована на основе результатов J. Clin. Microbiol. 47 (10): 3204-3210, 2009. В таблице ниже вероятные интерпретации 16 паттернов, возможных из четырех анализы в панели EBV. В целях классификации неопределенные / сомнительные результаты считаются отрицательными в таблице ниже.
Результаты всегда следует интерпретировать вместе с история болезни пациента и физикальное обследование. Гетерофил VCA VCA EBNA IgM IgM IgG IgG Интерпретация Neg Neg Neg Neg EBV наивный Neg Pos Neg Neg Первичная острая ВЭБ-инфекция Pos Neg Neg Neg Первичная острая ВЭБ-инфекция Pos Pos Neg Neg Первичная острая ВЭБ-инфекция Neg Pos Pos Neg Первичная острая ВЭБ-инфекция Pos Neg Pos Neg Первичная острая ВЭБ-инфекция Pos Pos Pos Neg Первичная острая ВЭБ-инфекция Neg Pos Neg Pos Восстановление после / реактивация EBV-инфекции Neg Pos Pos Pos Восстановление после / реактивация инфекции EBV Pos Neg Pos Pos Восстановление после / реактивация EBV-инфекции Pos Pos Neg Pos Восстановление после / реактивация EBV-инфекции Pos Pos Pos Pos Выход из / реактивация EBV-инфекции Neg Neg Pos Neg Прошедшая инфекция ВЭБ Neg Neg Pos Pos Прошедшая инфекция ВЭБ Pos Neg Neg Pos Неизвестно * Neg Neg Neg Pos Неизвестно * * Эти два паттерна необычны и имеют неизвестное значение.

Комментарии:
Номер ссылки :
Klutts JS et al. Доказательный подход к интерпретации
Серологические паттерны вируса Эпштейна-Барра. J. Clin. Microbiol. 47 (10):
3204-3210.
Методология:
Мультиплексный иммуноферментный анализ
Код CPT:
86308 (гетерофил), 86664 (EBNA), 86665×2 (VCA IgG и IgM)
Доказательный подход к интерпретации серологических паттернов вируса Эпштейна-Барра
РЕЗЮМЕ
Диагностика инфекции, вызванной вирусом Эпштейна-Барра (EBV), основана на клинических симптомах и серологических маркерах, включая следующие: иммуноглобулин G (IgG) и антитела IgM к вирусному капсидному антигену (VCA), гетерофильным антителам и антителам IgG к раннему диффузному антигену EBV (EA-D) и ядерному антигену (EBNA-1).Использование всех пяти маркеров дает 32 возможных серологических образца. В результате интерпретация серологии ВЭБ остается сложной задачей. Целью этого исследования было использование большой популяции пациентов для разработки основанных на доказательствах инструментов для интерпретации результатов ВЭБ. В этом исследовании было использовано 1846 образцов сыворотки, которые были отправлены в лабораторию для проведения тестирования на ВЭБ по назначению врача. Обзор карт был проведен для более чем 800 пациентов, и диагнозы были выставлены на основании назначенного врачом тестирования, клинической картины и истории болезни.Тестирование всех пяти антител против EBV проводилось отдельно на всех образцах сыворотки с использованием системы Bio-Rad BioPlex 2200. Предполагаемый диагноз ВЭБ (основанный на предыдущих публикациях) сравнивался с диагнозом ВЭБ на основе обзора медицинских карт для каждого серологического образца. Интересно, что из 32 возможных серологических паттернов только 12 наблюдались у ≥10 пациентов. Остальные 20 паттернов невозможно было интерпретировать, потому что они встречались очень редко. Были созданы две простые в использовании таблицы для интерпретации серологических паттернов EBV в зависимости от того, используются ли три (EBV VCA IgG, IgM и гетерофильный) или пять маркеров.
В этом исследовании было использовано 1846 образцов сыворотки, которые были отправлены в лабораторию для проведения тестирования на ВЭБ по назначению врача. Обзор карт был проведен для более чем 800 пациентов, и диагнозы были выставлены на основании назначенного врачом тестирования, клинической картины и истории болезни.Тестирование всех пяти антител против EBV проводилось отдельно на всех образцах сыворотки с использованием системы Bio-Rad BioPlex 2200. Предполагаемый диагноз ВЭБ (основанный на предыдущих публикациях) сравнивался с диагнозом ВЭБ на основе обзора медицинских карт для каждого серологического образца. Интересно, что из 32 возможных серологических паттернов только 12 наблюдались у ≥10 пациентов. Остальные 20 паттернов невозможно было интерпретировать, потому что они встречались очень редко. Были созданы две простые в использовании таблицы для интерпретации серологических паттернов EBV в зависимости от того, используются ли три (EBV VCA IgG, IgM и гетерофильный) или пять маркеров. Использование этих двух таблиц позволяет интерпретировать> 95% серологических результатов BioPlex. Это первое в своем роде научно-обоснованное исследование серологии ВЭБ.
Использование этих двух таблиц позволяет интерпретировать> 95% серологических результатов BioPlex. Это первое в своем роде научно-обоснованное исследование серологии ВЭБ.
Вирус Эпштейна-Барра (ВЭБ) — это гамма-герпесвирус, который вызывает ряд клинических синдромов, включая острый мононуклеоз и посттрансплантационное лимфопролиферативное заболевание, и был связан с рядом злокачественных новообразований (6). Большинство людей инфицированы ВЭБ в раннем взрослом возрасте. После первоначальной инфекции вирус становится латентным в B-лимфоцитах и может реактивироваться в более позднем возрасте, вызывая посттрансплантационное лимфопролиферативное заболевание у пациентов с ослабленным иммунитетом после трансплантации, лимфому центральной нервной системы у пациентов со СПИДом или более классическое острое вирусное заболевание, связанное с EBV, у некоторых пациенты, инфицированные другими вирусами (6).
Острая инфекция, вызванная ВЭБ, может широко варьироваться в зависимости от тяжести и проявления заболевания, от бессимптомной инфекции до серьезной, опасной для жизни версии мононуклеоза с сопутствующим поражением печени и спленомегалией (6). Кроме того, другие острые вирусные синдромы, в том числе вызванные вирусами гепатита и цитомегаловирусом (CMV), могут приводить к аналогичным клиническим синдромам. Разнообразие симптомов и их совпадение с другими вирусными инфекциями подчеркивают важность лабораторных исследований в диагностике острого заболевания, связанного с ВЭБ.Серологические маркеры EBV-инфекции были и остаются наиболее часто используемыми диагностическими инструментами для этой цели.
Кроме того, другие острые вирусные синдромы, в том числе вызванные вирусами гепатита и цитомегаловирусом (CMV), могут приводить к аналогичным клиническим синдромам. Разнообразие симптомов и их совпадение с другими вирусными инфекциями подчеркивают важность лабораторных исследований в диагностике острого заболевания, связанного с ВЭБ.Серологические маркеры EBV-инфекции были и остаются наиболее часто используемыми диагностическими инструментами для этой цели.
Анализы с использованием антител иммуноглобулина G (IgG) и IgM к антигену вирусного капсида (VCA) и гетерофильных антител (IgM) являются наиболее часто выполняемыми серологическими тестами на ВЭБ. Также могут быть определены IgG-антитела к раннему диффузному антигену EBV (EA-D) и ядерному антигену (EBNA-1). Если измерить все пять антител, можно получить 32 возможных серологических образца (Таблица 1).Предполагаемые диагнозы, представленные в таблице 1, получены из различных источников (5, 6, 11). Однако есть разногласия по поводу назначения определенных шаблонов. Таким образом, несмотря на наш опыт использования этих диагностических тестов, интерпретация серологических паттернов ВЭБ остается сложной задачей (4).
Таким образом, несмотря на наш опыт использования этих диагностических тестов, интерпретация серологических паттернов ВЭБ остается сложной задачей (4).
Все возможные серологические образцы и предполагаемые диагнозы ВЭБ на основе опубликованных отчетов a
Bio-Rad Laboratories (Геркулес, Калифорния) недавно представила мультиплексную платформу (BioPlex 2200), которая может измерять все пять из этих антител. от одного образца в двух реакционных сосудах.Мы и другие специалисты недавно оценили эту платформу на предмет ее эффективности в сравнении с различными тестами предикатов и показали, что она работает достаточно хорошо (3, 7).
Целью этого исследования было использование большой популяции пациентов для разработки основанных на фактических данных, простых в использовании таблиц для интерпретации мультиплексированных результатов EBV. Насколько нам известно, это исследование является первым в своем роде.
МАТЕРИАЛЫ И МЕТОДЫ
Образцы пациентов и тестирование на ВЭБ. Две тысячи шестьдесят четыре последовательных образца сыворотки отправлены в больницу Барнс-Еврей и Св.С 13 октября 2004 г. по 28 декабря 2007 г. были задействованы лаборатории детской больницы Луи для проведения назначенных врачом анализов на ВЭБ. Популяция пациентов представлена как стационарными, так и амбулаторными пациентами, а также большим количеством пациентов до и после трансплантации, а также образцами из кабинетов врачей третичного уровня. Образцы замораживали на срок до 30 месяцев при -70 ° C, размораживали и немедленно анализировали. Тестирование всех пяти антител проводилось с помощью тестов IgG (EBV VCA, EBV EA-D и EBV NA) и IgM (EBV VCA и гетерофил) на автоматизированной платформе BioPlex 2200 в соответствии с инструкциями производителя.Эти анализы одобрены FDA, а пороговые значения для положительных, отрицательных и сомнительных результатов были установлены производителем ранее; эти ограничения использовались в этом исследовании. Двести восемнадцать экземпляров были исключены.
Две тысячи шестьдесят четыре последовательных образца сыворотки отправлены в больницу Барнс-Еврей и Св.С 13 октября 2004 г. по 28 декабря 2007 г. были задействованы лаборатории детской больницы Луи для проведения назначенных врачом анализов на ВЭБ. Популяция пациентов представлена как стационарными, так и амбулаторными пациентами, а также большим количеством пациентов до и после трансплантации, а также образцами из кабинетов врачей третичного уровня. Образцы замораживали на срок до 30 месяцев при -70 ° C, размораживали и немедленно анализировали. Тестирование всех пяти антител проводилось с помощью тестов IgG (EBV VCA, EBV EA-D и EBV NA) и IgM (EBV VCA и гетерофил) на автоматизированной платформе BioPlex 2200 в соответствии с инструкциями производителя.Эти анализы одобрены FDA, а пороговые значения для положительных, отрицательных и сомнительных результатов были установлены производителем ранее; эти ограничения использовались в этом исследовании. Двести восемнадцать экземпляров были исключены.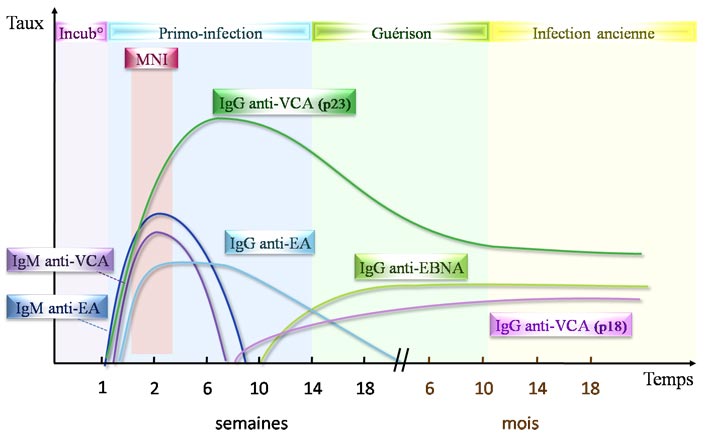 Сто сорок пять из 2064 образцов были исключены из-за ≥1 сомнительного результата BioPlex (примечание: 5 из 145 образцов имели 2 эквивалентных результата; таким образом, 150 сомнительных результатов / 10320 общих результатов = 1,5% наблюдаемых сомнительных результатов). 47 образцов были исключены из-за недостаточного количества образцов для тестирования.Двадцать шесть были исключены из-за недостаточной идентификации пациентов, связанных с образцом. Из оставшихся 1846 образцов в исследовании возраст варьировался от <1 года до> 90 лет, с примерно 45% пациентов в возрасте до 20 лет.
Сто сорок пять из 2064 образцов были исключены из-за ≥1 сомнительного результата BioPlex (примечание: 5 из 145 образцов имели 2 эквивалентных результата; таким образом, 150 сомнительных результатов / 10320 общих результатов = 1,5% наблюдаемых сомнительных результатов). 47 образцов были исключены из-за недостаточного количества образцов для тестирования.Двадцать шесть были исключены из-за недостаточной идентификации пациентов, связанных с образцом. Из оставшихся 1846 образцов в исследовании возраст варьировался от <1 года до> 90 лет, с примерно 45% пациентов в возрасте до 20 лет.
Тестирование на ВЭБ по назначению врача.EBV anti-VCA IgG Анализы EBV против VCA IgM и против EBNA-1 IgG проводили с использованием анализа Captia (Trinity Biotech USA, Джеймстаун, Нью-Йорк), как описано во вкладышах производителей на автоматизированной платформе Dynex DSX (Шантильи, Вирджиния).Анализ гетерофильных антител Status Mono (LifeSign LLC, Somerset, NJ) выполняли, как описано во вкладыше к упаковке производителя.
Обзор карты и классификация болезненного состояния. Один врач, который не знал результатов BioPlex, просмотрел все медицинские записи. Резюме случаев регистрировались в стандартизированных формах, а собранная информация включала назначенные врачом серологические исследования ВЭБ и ЦМВ, анамнез пациента, соответствующие результаты физикального обследования, включая лихорадку, лимфаденопатию, фарингит, сыпь, недомогание или гепатоспленомегалию, результаты ручного и автоматического общего анализа крови. и результаты любых сопутствующих микробиологических исследований.Используя все доступные клинические и лабораторные данные, рецензент назначил каждому пациенту один из пяти возможных диагнозов ВЭБ (наивный, первичный острый, перенесенная инфекция, выздоровление / реактивация или неизвестный).
Пациенты были признаны наивными по отношению к ВЭБ, если у них были отрицательные результаты по VCA IgG, EA-D и / или EBNA-1 и либо отсутствовали IgM или гетерофильные антитела, либо не было клинического подозрения на острую инфекцию.
Первичная острая инфекция преимущественно ассоциировалась с наличием утомляемости, недомогания, субфебрильной лихорадки, шейной лимфаденопатии, глоточных симптомов с миндалинным экссудатом или без него, пятнисто-папулезной или патологической сыпи, гепатоспленомегалии или повышением уровня печеночных ферментов и повышением мононуклеаров клетки и атипичные лимфоциты.Отсутствие другого подходящего диагноза и наличие соответствующих острых серологий (IgM и гетерофильные антитела) учитывались, но не были необходимы для диагностики острой инфекции EBV.
Пациенты с перенесенной инфекцией определялись как пациенты с положительной серологией IgG к VCA или EBNA-1 без подозрения на острую инфекцию.
Выздоровление определялось как положительная острая серология или остаточные симптомы спустя более 2 недель от начала заболевания. Реактивация рассматривалась как возникновение острой инфекции у пациента, о котором известно, что он является серопозитивным по VCA IgG и / или EBNA-1 IgG.
Категория «неизвестно» была зарезервирована для пациентов, которые не могли быть отнесены к одной из других категорий и имели противоречивые клинические и серологические картины.
Для двух наиболее распространенных серологических паттернов, соответствующих наивной и прошлой инфекции (паттерны 1 и 12), рецензенту было предоставлено на рассмотрение только 20% медицинских записей пациентов. До начала этого исследования было получено одобрение институционального наблюдательного совета Школы медицины Вашингтонского университета.
Статистика.Чувствительность, специфичность, прогностические значения, отношения шансов и значения P вместе со всеми 95% доверительными интервалами были рассчитаны с использованием программного обеспечения Prism (Prism Software Corporation, Ирвин, Калифорния).
РЕЗУЛЬТАТЫ
Тестирование BioPlex EBV было проведено на 1846 образцах. Распространенность всех 32 возможных серологических паттернов показана в таблицах 2 и 3. Из 32 возможных серологических паттернов, которые могли возникнуть, 10 паттернов не встречались ни в одном из 1846 образцов, а еще 10 паттернов встречались в <10 из 1846 образцов. .Можно сделать несколько выводов о серологических паттернах, которые встречаются так редко. По этой причине данные разбиты на шаблоны, которые наблюдались у ≥10 пациентов (Таблица 2), и шаблоны, которые наблюдались у <10 пациентов (Таблица 3). Для каждого серологического образца BioPlex EBV также показан диагноз EBV, основанный на обзоре медицинских карт. Обзор медицинских карт был проведен для всех пациентов, за исключением пациентов со схемами 1 и 12 в таблице 2, где были рассмотрены репрезентативные 20% пациентов.В таблице 2 соответствие между предполагаемым диагнозом ВЭБ и доказательным диагнозом ВЭБ показано жирным шрифтом. Также рассчитываются и отображаются прогнозные значения. Никаких расчетов на основе данных таблицы 3 не производилось, так как трудно сделать выводы относительно связи любого из этих паттернов с диагнозом ВЭБ у такого небольшого числа пациентов.
Из 32 возможных серологических паттернов, которые могли возникнуть, 10 паттернов не встречались ни в одном из 1846 образцов, а еще 10 паттернов встречались в <10 из 1846 образцов. .Можно сделать несколько выводов о серологических паттернах, которые встречаются так редко. По этой причине данные разбиты на шаблоны, которые наблюдались у ≥10 пациентов (Таблица 2), и шаблоны, которые наблюдались у <10 пациентов (Таблица 3). Для каждого серологического образца BioPlex EBV также показан диагноз EBV, основанный на обзоре медицинских карт. Обзор медицинских карт был проведен для всех пациентов, за исключением пациентов со схемами 1 и 12 в таблице 2, где были рассмотрены репрезентативные 20% пациентов.В таблице 2 соответствие между предполагаемым диагнозом ВЭБ и доказательным диагнозом ВЭБ показано жирным шрифтом. Также рассчитываются и отображаются прогнозные значения. Никаких расчетов на основе данных таблицы 3 не производилось, так как трудно сделать выводы относительно связи любого из этих паттернов с диагнозом ВЭБ у такого небольшого числа пациентов.
Серологические паттерны и диагностика ВЭБ для 12/32 серологических паттернов, которые имели место у ≥10 пациентов a
ТАБЛИЦА 3.Серологические паттерны и диагностика ВЭБ для 20/32 серологических паттернов, которые имели место у <10 пациентов a
Целью этого исследования было разработать основанные на доказательствах простые в использовании таблицы для интерпретации множественных результатов ВЭБ. Для этого все образцы EBV с прогнозируемыми значениями <50% были удалены из таблицы 2 (образцы 2, 29 и 30). В таблице 4 показаны оставшиеся девять серологических паттернов, которые имели достаточно высокие прогностические значения, чтобы считать их связанными с конкретным диагнозом ВЭБ, вместе с рассчитанными диагностическими параметрами для каждого верифицированного паттерна.Следует отметить, что три паттерна (15, 17 и 22), которые, как предполагалось, указывали на выздоровление / реактивацию, были фактически определены как указывающие на перенесенную инфекцию на основании диагноза, основанного на доказательствах. Кроме того, для правильного расчета чувствительности числа серологических паттернов были скорректированы в таблице 4, чтобы включить тех пациентов, случаи которых не рассматривались. Например, для шаблона 12 710 пациентов, данные которых не были проанализированы (см. Таблицу 2), были распределены по пяти диагностическим группам EBV на основе относительной частоты встречаемости среди репрезентативных 182 пациентов с этим шаблоном, которые были рассмотрены.Поскольку 171 из 182 (94%) пациентов были диагностированы как «перенесенная инфекция», 94% из 710 неопрошенных пациентов (667 пациентов) были добавлены в категорию «перенесенная инфекция» в Таблице 4. Остальные 43 непроверенных пациента были распределены по другие различные диагностические категории таким же образом.
Кроме того, для правильного расчета чувствительности числа серологических паттернов были скорректированы в таблице 4, чтобы включить тех пациентов, случаи которых не рассматривались. Например, для шаблона 12 710 пациентов, данные которых не были проанализированы (см. Таблицу 2), были распределены по пяти диагностическим группам EBV на основе относительной частоты встречаемости среди репрезентативных 182 пациентов с этим шаблоном, которые были рассмотрены.Поскольку 171 из 182 (94%) пациентов были диагностированы как «перенесенная инфекция», 94% из 710 неопрошенных пациентов (667 пациентов) были добавлены в категорию «перенесенная инфекция» в Таблице 4. Остальные 43 непроверенных пациента были распределены по другие различные диагностические категории таким же образом.
Доказательная проверка девяти серологических паттернов ВЭБ для интерпретации мультиплексированных серологических результатов ВЭБ
Потому что врачи обычно заказывают только VCA IgG и IgM и гетерофильные антитела для определения стадии EBV или серологического исследования. Статус пациентов. Таблица 5 иллюстрирует частоту этих восьми возможных серологических паттернов в нашей популяции пациентов.Прогностические значения для пациентов, правильно идентифицированных серологически, были рассчитаны так же, как и в таблице 2. Четыре из восьми возможных моделей с прогностическими значениями> 50% и достаточным количеством пациентов показаны в таблице 6 вместе с расчетами комбинированных прогностических значений и чувствительность. Подобно Таблице 4, пациенты, чьи записи не были просмотрены, были включены в Таблицу 6 на основе частот паттернов для пациентов, чьи записи были рассмотрены в Таблицах 2 и 3.
Статус пациентов. Таблица 5 иллюстрирует частоту этих восьми возможных серологических паттернов в нашей популяции пациентов.Прогностические значения для пациентов, правильно идентифицированных серологически, были рассчитаны так же, как и в таблице 2. Четыре из восьми возможных моделей с прогностическими значениями> 50% и достаточным количеством пациентов показаны в таблице 6 вместе с расчетами комбинированных прогностических значений и чувствительность. Подобно Таблице 4, пациенты, чьи записи не были просмотрены, были включены в Таблицу 6 на основе частот паттернов для пациентов, чьи записи были рассмотрены в Таблицах 2 и 3.
Серологические паттерны и диагнозы ВЭБ для 1846 пациентов из исследования, использующих только BioPlex Результаты анализа VCA IgG, VCA IgM и гетерофильных антител
ТАБЛИЦА 6.Доказательная проверка четырех серологических паттернов ВЭБ для интерпретации результатов анализа VCA IgG, VCA IgM и гетерофильных антител
ОБСУЖДЕНИЕ
Диагностика заболевания, связанного с EBV, основывается на клинических симптомах и лабораторных исследованиях. Нельзя недооценивать важность серологического тестирования на заболевания, связанные с ВЭБ. Однако связь между конкретным диагнозом ВЭБ и серологическими паттернами в основном основана на предположениях. Хотя недавно была проведена оценка использования мультиплексной технологии для обнаружения антител к EBV (1, 3, 7, 9, 12), это первое научно-обоснованное исследование такого рода, направленное на сопоставление большого количества клинических диагнозов с серологическими показателями EBV. узоры.Здесь мы проанализировали почти 1850 образцов, получив более 10 000 результатов индивидуальных серологических тестов, и изучили медицинские записи более 800 пациентов.
Нельзя недооценивать важность серологического тестирования на заболевания, связанные с ВЭБ. Однако связь между конкретным диагнозом ВЭБ и серологическими паттернами в основном основана на предположениях. Хотя недавно была проведена оценка использования мультиплексной технологии для обнаружения антител к EBV (1, 3, 7, 9, 12), это первое научно-обоснованное исследование такого рода, направленное на сопоставление большого количества клинических диагнозов с серологическими показателями EBV. узоры.Здесь мы проанализировали почти 1850 образцов, получив более 10 000 результатов индивидуальных серологических тестов, и изучили медицинские записи более 800 пациентов.
Из 1846 образцов, проанализированных в этом исследовании, 98% (1810/1846) имели один из 12 различных серологических образцов (Таблица 2). Остальные 20 паттернов (таблица 3) были настолько необычными, что невозможно сделать вывод об их связи с конкретным диагнозом ВЭБ. Среди паттернов, которые не были распространены (таблица 3), были паттерны, которые были положительными по VCA IgG вместе с другими положительными маркерами первичной острой инфекции (VCA IgM, EA-D IgG и / или гетерофил; номера паттернов 3, 6, 7, 8, 10 и 11). Традиционно предполагалось, что VCA IgG будет положительным у большого процента пациентов, положительных на VCA IgM и / или гетерофильные антитела (5, 6), но этого не наблюдалось в этой популяции. Вероятная причина этого различия заключается в том, что анализ BioPlex был разработан с расчетом на то, что наборы IgG и IgM будут использоваться вместе. Анализ VCA IgG выявляет антитела к антигену р18 EBV, который, как ранее было показано, является поздним маркером инфекции (2). Таким образом, анализ BioPlex VCA IgG с меньшей вероятностью будет положительным у пациентов с ранними острыми инфекциями.
Традиционно предполагалось, что VCA IgG будет положительным у большого процента пациентов, положительных на VCA IgM и / или гетерофильные антитела (5, 6), но этого не наблюдалось в этой популяции. Вероятная причина этого различия заключается в том, что анализ BioPlex был разработан с расчетом на то, что наборы IgG и IgM будут использоваться вместе. Анализ VCA IgG выявляет антитела к антигену р18 EBV, который, как ранее было показано, является поздним маркером инфекции (2). Таким образом, анализ BioPlex VCA IgG с меньшей вероятностью будет положительным у пациентов с ранними острыми инфекциями.
Еще одно наблюдение, основанное на данных в таблице 2, заключается в том, что случаи с паттернами, предположительно относящимися к восстановлению / реактивации (паттерны 15, 17 и 22), были фактически определены как прошедшие заражение при просмотре графиков. Записи многих из этих пациентов были подвергнуты неслепому пересмотру, и даже при знании всей их серологической картины ВЭБ почти все все еще считались находящимися в стадии прошлой инфекции. Это позволяет предположить, что подавляющее большинство пациентов с этими тремя паттернами клинически можно считать имеющими прошлую инфекцию без указания на текущий процесс заболевания, связанного с ВЭБ.Возможно, что у многих из этих пациентов была доброкачественная реактивация ВЭБ. У пациентов с латентным EBV вирус может реактивироваться. Однако у иммунокомпетентных пациентов эта реактивация обычно не прогрессирует до литической стадии репликации вируса и практически не имеет клинических последствий (10). Таким образом, во время обзора симптомов пациента и других клинических данных не будет свидетельств активного процесса, но у пациента будут свидетельства перенесенной инфекции. Расчеты прогнозных значений, показанные в таблицах 2 и 5, не выполнялись для этих шаблонов, поскольку эти вычисления предполагали, что предполагаемый этап является правильным назначением для этих шаблонов.Для Таблицы 4 образцы 15, 17 и 22 были включены в расчеты комбинированной чувствительности и прогностической ценности для прогнозирования прошлой инфекции, а не восстановления / реактивации.
Это позволяет предположить, что подавляющее большинство пациентов с этими тремя паттернами клинически можно считать имеющими прошлую инфекцию без указания на текущий процесс заболевания, связанного с ВЭБ.Возможно, что у многих из этих пациентов была доброкачественная реактивация ВЭБ. У пациентов с латентным EBV вирус может реактивироваться. Однако у иммунокомпетентных пациентов эта реактивация обычно не прогрессирует до литической стадии репликации вируса и практически не имеет клинических последствий (10). Таким образом, во время обзора симптомов пациента и других клинических данных не будет свидетельств активного процесса, но у пациента будут свидетельства перенесенной инфекции. Расчеты прогнозных значений, показанные в таблицах 2 и 5, не выполнялись для этих шаблонов, поскольку эти вычисления предполагали, что предполагаемый этап является правильным назначением для этих шаблонов.Для Таблицы 4 образцы 15, 17 и 22 были включены в расчеты комбинированной чувствительности и прогностической ценности для прогнозирования прошлой инфекции, а не восстановления / реактивации.
Как мы ранее описывали, гетерофильный анализ на платформе BioPlex отличается от стандартных гетерофильных тестов латексной агглютинации тем, что он выявляет только антитела IgM, имеет числовое, а не визуальное отсечение и использует очищенный антиген эритроцитов лошади, а не бычий антиген. (8). В этом отчете мы использовали набор данных, отличный от представленного здесь, и показали, что гетерофильный анализ BioPlex повышает диагностическую ценность как для взрослых, так и для детей (8).Из таблиц 2 и 5 в текущем исследовании очевидно, что гетерофильный анализ действительно улучшает прогностическую ценность для диагностики острой инфекции. Сравнивая образцы 2 и 5 в таблице 2, образцы 4 и 9 в таблице 2 и образцы B и C в таблице 5, прогностическая ценность для диагностики острой инфекции значительно выше, если у пациента есть положительные гетерофильные антитела. Еще одна причина этого открытия заключается в том, что мы ранее показали, что существуют другие причины ложноположительного результата на VCA IgM, особенно острая инфекция, вызванная CMV или Toxoplasma (8). Таким образом, большинство пациентов, у которых был образец 2 в таблице 2, вероятно, имели одно из этих состояний и не имели первичной острой инфекции EBV. Однако ложноположительный результат VCA IgM гораздо менее вероятен при одновременном положительном гетерофильном анализе.
Таким образом, большинство пациентов, у которых был образец 2 в таблице 2, вероятно, имели одно из этих состояний и не имели первичной острой инфекции EBV. Однако ложноположительный результат VCA IgM гораздо менее вероятен при одновременном положительном гетерофильном анализе.
Девять паттернов, представленных в Таблице 4, являются наиболее распространенными и имеют достаточно высокие ассоциации со стадией ВЭБ, чтобы их можно было считать показательными для этих соответствующих стадий. Интересно, что эти шаблоны могут быть использованы для диагностики более 95% пациентов в этом исследовании (1757/1846 пациентов) с хорошей диагностической точностью.В нашей популяции пациентов у нас были пациенты, которых оценивали на предмет острого заболевания и серологического статуса до трансплантации. В результате диагностическая полезность, показанная в таблицах 4 и 6, может отличаться, если демографические данные пациентов значительно различаются (например, в основном это острые педиатрические пациенты и несколько пациентов перед трансплантацией). Это следует учитывать при экстраполяции наших данных в другие центры.
Это следует учитывать при экстраполяции наших данных в другие центры.
Антитела IgG и IgM к VCA и гетерофильные антитела обычно являются единственными тремя антителами, протестированными в клинической практике для определения статуса ВЭБ или для диагностики острого заболевания, связанного с ВЭБ.В таблице 5 представлены восемь возможных серологических образцов с использованием только этих трех антител. В таблице 6 представлены расчеты с использованием наиболее общих шаблонов (подобных тем, которые показаны в таблице 4) и только для этих трех антител. Сравнение чувствительности и прогностических значений в таблицах 4 и 6 показывает, что использование всех пяти антител обеспечивает лучшую чувствительность для диагностики первичной острой инфекции EBV, поскольку только 53% пациентов, у которых определена первичная острая инфекция, были идентифицированы с использованием трех аналитов, по сравнению с 64%, когда используются все пять антител.Одной из основных причин этого является более высокая прогностическая ценность, наблюдаемая, когда пациенты имеют как положительные антитела VCA IgM, так и EA-D IgG, по сравнению с только положительными антителами VCA IgM (см. Таблицу 2, образцы 2 и 4). В таблице 5 образец C содержит как EA-D IgG-позитивных, так и -отрицательных пациентов, и прогностическая ценность для этого шаблона (41,7%) недостаточна, чтобы рассматривать его как связанное с первичным острым заболеванием. Напротив, образец 4 в таблице 2 действительно имел достаточную прогностическую ценность и мог быть включен в расчеты чувствительности в таблице 4.
Прогностические значения при использовании трех антител для прогнозирования диагноза ВЭБ были аналогичны прогнозам, сделанным с использованием всех пяти аналитов. Одна из вероятных причин этого связана с проведением анализа BioPlex VCA IgG, как обсуждалось выше. Поскольку BioPlex VCA IgG имеет сильную связь с прошлой инфекцией и, таким образом, вряд ли будет положительным у пациентов с ранним острым заболеванием, поэтому не так важно проводить анализ EBNA-1 IgG, чтобы убедиться, что пациент действительно в прошлом. -инфекционная стадия.Кроме того, за исключением относительно небольшого числа пациентов с первичной острой EBV-инфекцией, EA-D IgG мало пригодился. Что касается прогностических значений, следует отметить, что эти значения зависят от распространенности ВЭБ-болезни в данной популяции. В нашем учреждении мы тестируем пациентов до и после трансплантации, тем самым снижая общую распространенность острого ВЭБ-заболевания. Центры должны учитывать это при применении этих таблиц к своим пациентам и вносить поправки на их распространенность.
Следует отметить, что, как описано выше, существуют различия в анализах VCA-IgG и гетерофильных антител на платформе BioPlex 2200 по сравнению с другими анализами. Это говорит о том, что показанные здесь модели интерпретации специфичны для использования с результатами BioPlex. Однако в этом исследовании и двух предыдущих исследованиях (3, 7) было очень сильное (от 92 до 97%) соответствие между BioPlex 2200 и результатами предикатного анализа. Таким образом, таблицы 4 и 6 также могут быть полезны для интерпретации серологических результатов EBV, полученных с помощью других анализов, но, очевидно, необходимы дальнейшие исследования для подтверждения этой гипотезы.
На основании этих данных мы рекомендуем научно обоснованный подход к интерпретации серологических паттернов BioPlex EBV. Мы предлагаем использовать Таблицу 4 для интерпретации серологических паттернов, когда заказаны пять серологических тестов, и из-за большей наблюдаемой чувствительности мы также рекомендуем тестировать все пять антител при попытке диагностировать первичное острое заболевание EBV. Мы также предоставляем Таблицу 6 для использования, когда заказываются только EBV VCA IgG, IgM и гетерофильные антитела, и предполагаем, что тестирования только этих трех антител достаточно при попытке просто установить серологический статус EBV пациента.Мы считаем, что только образцы, которые появляются в этих таблицах, могут быть интерпретированы с уверенностью, поскольку данных недостаточно для поддержки интерпретации других серологических образцов. Мы не предлагаем и не рекомендуем изолированное использование этих таблиц для диагностики заболеваний, связанных с ВЭБ, но мы предлагаем, чтобы они представляли собой основанный на фактических данных инструмент, который можно использовать в сочетании с другими лабораторными и клиническими параметрами для классификации болезни ВЭБ. сцена.
СНОСКИ
- Поступило 26 января 2009 г.
- Возвращено для модификации 22 мая 2009 г.
- Принято 29 июля 2009 г.
- Авторское право © 2009 Американское общество микробиологии
ССЫЛКИ
- 1.25
Баетенс, Д. 2001. Рассеяние света парными частицами: новый метод серодиагностики инфекции вируса Эпштейна-Барра. J. Med. Virol. 64 : 519-525.
- 2.↵
Бауэр, Г. 2001. Простота через сложность: иммуноблоттинг с рекомбинантными антигенами как новый золотой стандарт серологии вируса Эпштейна-Барра. Clin. Лаборатория 47 : 223-230.
- 3.↵
Бинникер, М. Дж., Д. Дж. Есперсен, Дж. А. Харринг, Л. О. Роллинз и Э. М. Бейто. 2008. Оценка иммуноанализа с множественным потоком для обнаружения антител, специфичных к вирусу Эпштейна-Барра. Clin. Вакцина Immunol.15 : 1410-1413.
- 4.↵
Hess, R.Д. 2004. Рутинная диагностика вируса Эпштейна-Барра с лабораторной точки зрения: все еще сложно после 35 лет. J. Clin. Microbiol.42 : 3381-3387.
- 5.↵
Jensen, H. B. 2006. Вирус Эпштейна-Барра, стр. 637-647. В Б. Детрик, Р. Г. Гамильтон и Дж. Д. Фолдс (ред.), Руководство по молекулярной и клинической лабораторной иммунологии, 7-е изд. ASM Press, Вашингтон, округ Колумбия.
- 6.↵
Johannsen, E.К., Р. Т. Скули и К. М. Кэй. 2005. Вирус Эпштейна-Барра (инфекционный мононуклеоз), с. 1801-1820 гг. В Г. Л. Манделл, Дж. Э. Беннет и Р. Долин (ред.), Принципы и практика инфекционных болезней, 6-е изд., Вып. 2. Эльзевир, Филадельфия, Пенсильвания.
- 7.↵
Klutts, J. S., R. S. Liao, W. M. Dunne, Jr., и A. M. Gronowski. 2004. Оценка иммунологического статуса вируса Эпштейна-Барра. J. Clin.Microbiol.42 : 4996-5000.
- 8.↵
Клутц, Дж. С., А. Х. Ву, А. Смит, Б. Йен-Либерман и А. М. Гроновски. 2008. Диагностические характеристики нового автоматизированного теста на гетерофильные антитела у взрослых и детей. Диаг. Microbiol. Заразить. Дис.61 : 351-353.
- 9.↵
Мартинс, Т. Б., К. М. Литвин и Х. Р. Хилл. 2008. Оценка иммуноанализа множественных флуоресцентных микросфер для определения серологического статуса вируса Эпштейна-Барра.Am. J. Clin. Патол. 129 : 34-41.
- 10.↵
Рикинсон, А. Б. и Э. Кифф. 2007. Вирус Эпштейна-Барра, стр. 2655-2700. В Д. М. Книп и П. М. Хоули (ред.), Филдс-вирусология, 5-е изд. Липпинкотт-Рэйвен, Филадельфия, Пенсильвания.
- 11.↵
Сторч, Г.А. 2000. Диагностическая вирусология. Clin. Заразить. Дис.31 : 739-751.
- 12.↵
Зейтиноглу, А., И. Алтуглу, Э. Каратас и Р. Язан Сертоз. 2008. Сравнение иммунофлуоресцентного анализа и мультиплексного иммуноанализа на основе микрочастиц для обнаружения антител к вирусному капсидному антигену вируса Эпштейна-Барра. J. Virol. Методы 148 : 300-302.
| Описание теста | Профиль антител к вирусу Эпштейна-Барра (EBV), сыворотка | Скопируйте эту информацию в буфер обмена |
|---|---|---|
| Синоним (ы) | Профиль EBV Ab | Скопируйте эту информацию в буфер обмена |
| Идентификатор теста | SEBV | Скопируйте эту информацию в буфер обмена |
| Общая информация | Полезно для: | Скопируйте эту информацию в буфер обмена |
| Тип образца | Сыворотка | Скопируйте эту информацию в буфер обмена |
| Требования к образцам | SST | Скопируйте эту информацию в буфер обмена |
| Устойчивость | Охлаждение (предпочтительно) 14 дней | Скопируйте эту информацию в буфер обмена |
| Неприемлемые условия образца | Отказ от общего гемолиза | Скопируйте эту информацию в буфер обмена |
| Методология | Мультиплексный проточный иммуноанализ (MFI) | Скопируйте эту информацию в буфер обмена |
| Расчетный ТАТ | 1-2 дня | Скопируйте эту информацию в буфер обмена |
| График испытаний | Понедельник-воскресенье | Скопируйте эту информацию в буфер обмена |
| Тест включает | EBVM EBV VCA IgM Ab | Скопируйте эту информацию в буфер обмена |
| Код (а) CPT | 86664 | Скопируйте эту информацию в буфер обмена |
| Минимальный объем пробы | 0.6 мл | Скопируйте эту информацию в буфер обмена |
| Контрольный диапазон | Вирус Эпштейна-Барра (EBV) ВИРУСНЫЙ АНТИГЕН КАПСИДА (VCA) АНТИТЕЛЫ IgM | Скопируйте эту информацию в буфер обмена |
| Лаборатория исполнительского мастерства | Майо | Скопируйте эту информацию в буфер обмена |
| Код (а) LOINC | 30339-6, 30340-4, 22296-8, 69048-7 | Скопируйте эту информацию в буфер обмена |
Как тестирование на антитела, специфичные к вирусу Эпштейна-Барра (EBV), используется в диагностике инфекционного мононуклеоза (моно)?
Sprunt TPV, Evans FA.Мононуклеарный лейкоцитоз в ответ на острую инфекцию (инфекционный мононуклеоз). Бюллетень больницы Джона Хопкинса . Балтимор, 1920. 31: 410-417.
Аалто С.М., Линнавуори К., Пелтола Х. и др. Иммунореактивация вируса Эпштейна-Барра вследствие первичной инфекции цитомегаловирусом. J Med Virol . 1998, ноябрь 56 (3): 186-91. [Медлайн].
Akashi K, Eizuru Y, Sumiyoshi Y, et al. Краткий отчет: тяжелый инфекционный мононуклеозоподобный синдром и первичная инфекция вируса герпеса 6 человека у взрослого. N Engl J Med . 15 июля 1993 г. 329 (3): 168-71. [Медлайн].
Аль-Джитави С.А., Хакуз Б.А., Казими С.М. Ложноположительный тест на моноспот при системной красной волчанке. Br J Ревматол . 1987 26 февраля (1): 71. [Медлайн].
Али Дж. Спонтанный разрыв селезенки у пациентов с инфекционным мононуклеозом. Банка J Surg . 1993 Февраль, 36 (1): 49-52. [Медлайн].
Allday MJ, Кроуфорд DH.Роль эпителия в персистенции ВЭБ и патогенезе В-клеточных опухолей. Ланцет . 16 апреля 1988 г. 1 (8590): 855-7. [Медлайн].
Андерсон, Мэриленд, Кеннеди, Калифорния, Льюис А.В. и др. Ретробульбарный неврит, осложняющий острую инфекцию, вызванную вирусом Эпштейна-Барра. Clin Infect Dis . 1994 Май. 18 (5): 799-801. [Медлайн].
Андерссон Дж. Клинические и иммунологические соображения при заболеваниях, связанных с вирусом Эпштейна-Барра. Scand J Infect Dis Suppl .1996. 100: 72-82. [Медлайн].
Андерссон Дж., Эрнберг И. Управление вирусными инфекциями Эпштейна-Барра. Am J Med . 1988 29 августа. 85 (2A): 107-15. [Медлайн].
Андерссон JP. Клинические аспекты вирусной инфекции Эпштейна-Барра. Scand J Infect Dis Suppl . 1991. 80: 94-104. [Медлайн].
Андиман В.А., Миллер Г. Антительные ответы на вирус Эпштейна-Барра. Роуз Н.Р., Фридман Х., ред. Руководство по клинической иммунологии .2-е изд. Вашингтон, округ Колумбия: Американское общество микробиологии; 1980. 628-633.
Асгари ММ, Бегос ДГ. Спонтанный разрыв селезенки при инфекционном мононуклеозе: обзор. Йельский университет биологии медицины . 1997 март-апрель. 70 (2): 175-82. [Медлайн].
Auwaerter PG. Инфекционный мононуклеоз в среднем возрасте. ЯМА . 1999 г. 3 февраля. 281 (5): 454-9. [Медлайн].
Baciewicz AM, Chandra R. Сыпь, вызванная цефпрозилом при инфекционном мононуклеозе. Энн Фармакотер . 2005 Май. 39 (5): 974-5. [Медлайн].
Balfour HH, Holman CJ, Hokanson KM, et al. Проспективное клиническое исследование взаимодействия вируса Эпштейна-Барра и хозяина во время острого инфекционного мононуклеоза. J Заразить Dis . 2005 г. 1. 192 (9): 1505-12. [Медлайн].
Бендер CE. Значение кортикостероидов в лечении инфекционного мононуклеоза. ЯМА . 1967, 20 февраля. 199 (8): 529-31. [Медлайн].
Бергер Р.Г., Рааб-Трауб Н. Острый моноартрит, вызванный инфекционным мононуклеозом. Am J Med . 1999 августа 107 (2): 177-8. [Медлайн].
Bigazzi C, Galieni P, Scarinci R et al. 11q- и конституциональная трисомия X у пациента с острым нелимфоцитарным лейкозом M5b. Haematologica . 1993 май-июнь. 78 (3): 185-6. [Медлайн].
Берд А.Г., Бриттон С. Взаимосвязь между вирусом Эпштейна-Барра и лимфомой. Семин Гематол . 19 октября 1982 г. (4): 285-300. [Медлайн].
Bonoan JT, Cunha BA. Лимфома в сравнении с инфекционным мононуклеозом, отрицательным по ВЭБ. Инфекция Дис Практика . 1998. 22: 63-64.
Brooks LA, Crook T, Crawford DH. Вирус Эпштейна-Барра и лимфомы. Инфекции и рак человека . Харбор, Нью-Йорк: издательство Cold Spring Harbor Press; 1999. 98-123.
Buchwald DS, Rea TD, Katon WJ и др.Острый инфекционный мононуклеоз: характеристики пациентов, сообщающих о неудаче выздоровления. Am J Med . 2000 ноябрь 109 (7): 531-7. [Медлайн].
Берджио Г. Р., Монафо В. Инфекционный мононуклеоз через пятьдесят лет после открытия теста Пола-Баннелла. Инфекция . 1983 янв-фев. 11 (1): 1-5. [Медлайн].
Кэмерон Б., Бхарадвадж М., Берроуз Дж. И др. Затяжное заболевание после инфекционного мононуклеоза связано с нарушением иммунитета, но не с повышенной вирусной нагрузкой. J Заразить Dis . 2006 г., 1. 193 (5): 664-71. [Медлайн].
Картер Р.Л. Гранулоциты при инфекционном мононуклеозе. Картер Р.Л., Пенман Г.Г., ред. Инфекционный мононуклеоз . Бостон, Массачусетс: Научные публикации Блэквелла; 1969. 111-120.
Картер Р.Л., Пенман Х.Г. Инфекционный мононуклеоз . Бостон, Массачусетс: Научные публикации Блэквелла; 1969.
Chaganti S, Heath EM, Bergler W., Kuo M, Buettner M, Niedobitek G и др.Колонизация вирусом Эпштейна-Барра субпопуляций В-клеток миндалин и периферической крови при первичной инфекции и персистенции. Кровь . 18 июня 2009 г. 113 (25): 6372-81. [Медлайн].
Чанг RS. Холл ГК, изд. Инфекционный мононуклеоз . Бостон, Массачусетс: издательство Thieme Medical Publishers; 1980.
Сыродель Ш. Инфекционный мононуклеоз. Семин Гематол . 1988 июл.25 (3): 261-8. [Медлайн].
Cohen JI.Вирус Эпштейна-Барра и иммунная система. Прятки. ЯМА . 1997 13 августа. 278 (6): 510-3. [Медлайн].
Cohen JI. Инфекция вируса Эпштейна-Барра. N Engl J Med . 2000 17 августа. 343 (7): 481-92. [Медлайн].
Cohen JI. Лимфопролиферативное заболевание, вызванное вирусом Эпштейна-Барра, связанное с приобретенным иммунодефицитом. Медицина (Балтимор) . 1991 г., 70 (2): 137-60. [Медлайн].
Коннелли КП, ДеВитт ЛД.Неврологические осложнения инфекционного мононуклеоза. Педиатр Нейрол . 1994 Май. 10 (3): 181-4. [Медлайн].
Cunha BA. ЦМВ инфекционный мононуклеоз, проявляющийся как FUO. Emerg Med . 2001. 33: 73-75.
Cunha BA. Мононуклеоз ВЭБ у пожилых пациентов. Emerg Med . 1996. 27: 82-84.
Cunha BA. Мононуклеоз ВЭБ. Инфекция Дис Практика . 1994. 18: 8.
Cunha BA.Ложноположительные гетерофильные тесты на инфекционный мононуклеоз ВЭБ. Инфекция Дис Практика . 2001. 25: 7-9.
Cunha BA. Гетерофилонегативный инфекционный мононуклеоз. Инфекция Дис Практика . 2001. 25: 17-19.
Cunha BA, Mickail N, Laguerre M. Бабезиоз, имитирующий инфекционный мононуклеоз вируса Эпштейна-Барра (EBV): еще одна причина ложноположительных тестов на моноспот. J Заражение . 2012 май. 64 (5): 531-2. [Медлайн].
Кунья Б.А., Микейл Н., Петелин А.П. Синдром, подобный инфекционному мононуклеозу, вероятно, связан с инфекцией вируса Коксаки А. Сердце легкое . 2012 сен-окт. 41 (5): 522-4. [Медлайн].
Дэвидсон И. Серологическая диагностика инфекционного мононуклеоза. ЯМА . 1937. 108: 289-295.
Decker GR, Berberian BJ, Sulica VI. Периорбитальный отек и отек век: начальное проявление острого инфекционного мононуклеоза. Кутис . 1991 Май. 47 (5): 323-4. [Медлайн].
Дауни Х, Мак-Кинли, Калифорния. Острый лимфаденоз по сравнению с острым лимфолейкозом. Арка Интер Мед . 1923. 32: 82-112.
Dror Y, Blachar Y, Cohen P, et al. Системная красная волчанка, связанная с острой инфекцией вируса Эпштейна-Барра. Am J Kidney Dis . 1998, ноябрь 32 (5): 825-8. [Медлайн].
Эпштейн MA, Achong BC. Вирус Эпштейна-Барра .Нью-Йорк, штат Нью-Йорк: Спрингер-Верлаг; 1979.
Fafi-Kremer S, Morand P, Brion JP, et al. Длительное выделение инфекционного вируса Эпштейна-Барра после инфекционного мононуклеоза. J Заразить Dis . 2005 15 марта. 191 (6): 985-9. [Медлайн].
Фарли Д.Р., Зитлоу С.П., Бэннон М.П. и др. Самопроизвольный разрыв селезенки из-за инфекционного мононуклеоза. Mayo Clin Proc . 1992 сентябрь 67 (9): 846-53. [Медлайн].
Фаррелл П.Дж.Роль HLA в восприимчивости к инфекционному мононуклеозу. Дж. Клин Инвест . 2007 октябрь 117 (10): 2756-8. [Медлайн].
Феранчак А.П., Тайсон Р.В., Наркевич М.Р. и др. Фульминантный вирусный гепатит Эпштейна-Барра: ортотопическая трансплантация печени и обзор литературы. Транспл. Хирургии печени . 1998 г., 4 (6): 469-76. [Медлайн].
Финч SC. Лабораторные данные при инфекционном мононуклеозе. Картер Р.Л., Пенман Г.Г., ред. Инфекционный мононуклеоз .Бостон, Массачусетс: Научные публикации Блэквелла; 1969. 47-52.
Finkel M, Parker GW, Fangelau HA. Гепатит инфекционного мононуклеоза: опыт 235 случаев. Мил Мед . 1964 июн. 129: 533-8. [Медлайн].
Fleisher GR, Pasquariello PS, Warren WS, et al. Внутрисемейная передача инфекций вируса Эпштейна-Барра. J Педиатр . 1981, январь 98 (1): 16-9. [Медлайн].
Fogeda M, de Ory F, Avellón A, Echevarría JM.Дифференциальная диагностика инфекции вируса гепатита E, цитомегаловируса и вируса Эпштейна-Барра у пациентов с подозрением на гепатит E. J Clin Virol . 2009 Июль 45 (3): 259-61. [Медлайн].
Gaffey MJ, Weiss LM. Связь вируса Эпштейна-Барра с неоплазией человека. Патол Анну . 1992. 27 Pt 1: 55-74. [Медлайн].
Джилл М.В., Кунья Б.А. Колонизация стрептококками против инфекции. Инфекция Дис Практика .1994. 18:16.
Glaser SL, Lin RJ, Stewart SL, Ambinder RF, Jarrett RF, Brousset P и др. Болезнь Ходжкина, ассоциированная с вирусом Эпштейна-Барра: эпидемиологические характеристики в международных данных. Инт Дж. Рак . 1997, 7 февраля. 70 (4): 375-82. [Медлайн].
Godshall SE, Kirchner JT. Инфекционный мононуклеоз. Сложности общего синдрома. Постградская медицина . 2000 июн. 107 (7): 175-9, 183-4, 186. [Medline].
Gold WL, Kapral MK, Witmer MR, et al.Постангинальная септицемия как опасное для жизни осложнение инфекционного мононуклеоза. Clin Infect Dis . 1995 Май. 20 (5): 1439-40. [Медлайн].
Голдакр М.Дж., Уоттон С.Дж., Йейтс Д.Г. Связь между инфекционным мононуклеозом и раком: исследования связи записей. Эпидемиологическая инфекция . 2009 Май. 137 (5): 672-80. [Медлайн].
Gray J, Wreghitt TG, Pavel P, et al. Инфекция вируса Эпштейна-Барра у реципиентов сердца и сердца-легкого: частота и клиническое влияние. J Пересадка легкого сердца . 1995 июл-авг. 14 (4): 640-6. [Медлайн].
Halevy J, Ash S. Инфекционный мононуклеоз у госпитализированных пациентов старше сорока лет. Am J Med Sci . 1988 Февраль 295 (2): 122-4. [Медлайн].
Han XY, Hellerstedt BA, Koller CA. Постспленэктомический цитомегаловирусный мононуклеоз — отдельный клинико-патологический синдром. Am J Med Sci . 2010 апр. 339 (4): 395-9. [Медлайн].
Хаверкос Х.В., Амзель З., Дротман Д.П.Неблагоприятные вирусно-лекарственные взаимодействия. Ред. Заразить Dis . 1991 июль-август. 13 (4): 697-704. [Медлайн].
Henle W, Henle GE, Horwitz CA. Специфические диагностические тесты вируса Эпштейна-Барра при инфекционном мононуклеозе. Хум Патол . 1974 Сентябрь 5 (5): 551-65. [Медлайн].
Эрнандес А.М., Шибата Д. Неходжкинская лимфома, связанная с вирусом Эпштейна-Барра, у ВИЧ-инфицированных пациентов. Лимфома лейк . 1995 16 (3-4) января: 217-21. [Медлайн].
Херрод HG, Доу LW, Салливан JL. Стойкая инфекция вируса Эпштейна-Барра, имитирующая ювенильный хронический миелогенный лейкоз: иммунологические и гематологические исследования. Кровь . 1983 июн. 61 (6): 1098-104. [Медлайн].
Hjalgrim H, Smedby KE, Rostgaard K и др. Инфекционный мононуклеоз, социальная среда в детстве и риск лимфомы Ходжкина. Cancer Res . 2007 г. 1. 67 (5): 2382-8. [Медлайн].
Hoagland RJ. Инфекционный мононуклеоз . Нью-Йорк, штат Нью-Йорк: Grune & Stratton; 1967.
Hoagland RJ. Инфекционный мононуклеоз. Am J Med . 1952, 13 августа (2): 158-71. [Медлайн].
Hoagland RJ. Клинические проявления инфекционного мононуклеоза: сообщение о двухстах случаях. Am J Med Sci . 1960. 240: 21-29.
Horwitz CA, Henle W., Henle G, et al. Инфекционный мононуклеоз у пациентов в возрасте от 40 до 72 лет: сообщение о 27 случаях, в том числе 3 без ответа гетерофилы-антитела. Медицина (Балтимор) . 1983 июл.62 (4): 256-62. [Медлайн].
Horwitz CA, Henle W., Henle G, et al. Долгосрочное серологическое наблюдение пациентов на вирус Эпштейна-Барра после выздоровления от инфекционного мононуклеоза. J Заразить Dis . 1985 июн. 151 (6): 1150-3. [Медлайн].
Hurt C, Tammaro D. Диагностическая оценка заболеваний, подобных мононуклеозу. Am J Med . 2007 Октябрь 120 (10): 911.e1-8. [Медлайн].
Hurt C, Таммаро Д.Диагностическая оценка заболеваний, подобных мононуклеозу. Am J Med . 2007 Октябрь 120 (10): 911.e1-8. [Медлайн].
Шлоссберг Д. Инфекционный мононуклеоз . 2-е изд. Нью-Йорк: Спрингер-Верлаг; 1988.
Jacobs BC, Rothbarth PH, van der Meche FG, et al. Спектр предшествующих инфекций при синдроме Гийена-Барре: исследование случай-контроль. Неврология . 1998 Октябрь 51 (4): 1110-5. [Медлайн].
Jappe U.Амоксициллин-индуцированная экзантема у пациентов с инфекционным мононуклеозом: аллергия или временная иммуностимуляция ?. Аллергия . 2007 декабрь 62 (12): 1474-5. [Медлайн].
Дженсон HB. Острые осложнения инфекционного мононуклеоза вируса Эпштейна-Барра. Curr Opin Pediatr . 2000 июн. 12 (3): 263-8. [Медлайн].
Джонсон DH, Cunha BA. Серология вируса Эпштейна-Барра. Инфекция Дис Практика . 1995. 19: 26-27.
Кано К., Милгром Ф.Гетерофильные антигены и антитела в медицине. Curr Top Microbiol Immunol . 1977. 77: 43-69. [Медлайн].
Каплан Дж. М., Келлер М. С., Трой С. Обструкция носоглотки при инфекционном мононуклеозе. Ам Фам Врач . 1987, январь, 35 (1): 205-9. [Медлайн].
Кайе К.М., Кифф Э. Инфекция вируса Эпштейна-Барра и инфекционный мононуклеоз. Горбач С.Л., Бартлетт Дж. Г., Блэклоу Н. Р., ред. Инфекционные болезни . Филадельфия, Пенсильвания: WB Saunders Co; 1992 г.1646–1654.
Ханна Р., Мосс DJ, Берроуз С.Р. Стратегии вакцинации против заболеваний, связанных с вирусом Эпштейна-Барра: уроки исследований иммунной регуляции, опосредованной цитотоксическими Т-клетками. Иммунол Ред. . 1999, август 170: 49-64. [Медлайн].
Вирус Киффа Э. Эпштейна-Барра и его репликация. Филдс Б.Н., Книп Д.М., Хоули П.М., ред. Отделение вирусологии . 3-е изд. Филадельфия, Пенсильвания: Lippincott Williams & Wilkins; 1996. 2343-2396.
Кифф Э., Дамбо Т., Хеллер М. и др. Биология и химия вируса Эпштейна-Барра. J Заразить Dis . 1982 Октябрь, 146 (4): 506-17. [Медлайн].
Китадзава Ю., Сайто Ф., Номура С. и др. Случай гемофагоцитарного лимфогистиоцитоза после первичной инфекции вирусом Эпштейна-Барра. Clin Appl Thromb Hemost . 2007 июл.13 (3): 323-8. [Медлайн].
Кляйн Э, Масуччи МГ. Клеточно-опосредованный иммунитет против В-лимфоцитов, инфицированных вирусом Эпштейна-Барра. Спрингер Семин Иммунопатол . 1982. 5 (1): 63-73. [Медлайн].
Klein NC, Petelin A, Cunha BA. Mycoplasma pneumoniae, предшествующая синдрому Лемьера, вызванному Fusobacterium nucleatum, осложненному острым инфекционным мононуклеозом вируса Эпштейна-Барра (EBV) у иммунокомпетентного хозяина. Сердце легкое . 2013 Январь 42 (1): 74-6. [Медлайн].
Klemola E, Von Essen R, Henle G, et al. Заболевание, подобное инфекционному мононуклеозу, с отрицательным результатом теста на агглютинацию гетерофилов.Клинические особенности в отношении антител к вирусу Эпштейна-Барра и цитомегаловирусу. J Заразить Dis . 1970 Июнь 121 (6): 608-14. [Медлайн].
Koj IG, Cunha BA. Инфекционный мононуклеоз ВЭБ с мучительной болезненностью кожи головы. Инфекция Дис Практика . 1998. 22:83.
Конволинка CW, Wyatt DB. Разрыв селезенки и инфекционный мононуклеоз. J Emerg Med . 1989 сентябрь-октябрь. 7 (5): 471-5. [Медлайн].
Lagona E, Sharifi F, Voutsioti A, et al.Инфекционный мононуклеоз вируса Эпштейна-Барра, ассоциированный с острым бескаменным холециститом. Инфекция . 2007 апр. 35 (2): 118-9. [Медлайн].
Лай П.К., Альперс М.П. Клеточно-опосредованный иммунный ответ человека на вирусную инфекцию Эпштейна-Барра (EB). Comp Immunol Microbiol Infect Dis . 1979. 2 (4): 565-85. [Медлайн].
Лам КМ, Кроуфорд DH. Онкогенный потенциал вируса Эпштейна-Барра. Crit Rev Oncog . 1991 г.2 (3): 229-45. [Медлайн].
LeClaire AC, Martin CA, Hoven AD. Сыпь, связанная с применением пиперациллина / тазобактама при инфекционном мононуклеозе. Энн Фармакотер . 2004 июн. 38 (6): 996-8. [Медлайн].
Левин Д., Тилтон Р.К., Парри М.Ф. и др. Ложноположительные тесты EBNA IgM и IgG на инфекционный мононуклеоз у детей. Педиатрия . 1994 декабрь 94 (6, часть 1): 892-4. [Медлайн].
Либовиц Д.Вирус Эпштейна-Барра и клеточный сигнальный путь в лимфомах от пациентов с ослабленным иммунитетом. N Engl J Med . 1998, 14 мая. 338 (20): 1413-21. [Медлайн].
Линде А. Диагностика заболеваний, связанных с вирусом Эпштейна-Барра. Scand J Infect Dis Suppl . 1996. 100: 83-8. [Медлайн].
Luzuriaga K, Sullivan JL. Инфекционный мононуклеоз. N Engl J Med . 2010 27 мая. 362 (21): 1993-2000. [Медлайн].
MacGowan JR, Mahendra P, Ager S, et al.Тромбоцитопения и спонтанный разрыв селезенки, связанные с инфекционным мононуклеозом. Clin Lab Haematol . 1995 марта 17 (1): 93-4. [Медлайн].
MacMahon EM, Glass JD, Hayward SD и др. Вирус Эпштейна-Барра при первичной лимфоме центральной нервной системы, связанной со СПИДом. Ланцет . 1991, 19 октября. 338 (8773): 969-73. [Медлайн].
Maddern BR, Werkhaven J, Wessel HB, et al. Инфекционный мононуклеоз с обструкцией дыхательных путей и парезом множественных черепных нервов. Отоларингол Хирургия головы и шеи . 1991 апр. 104 (4): 529-32. [Медлайн].
Maki DG, Reich RM. Инфекционный мононуклеоз у спортсмена. Диагностика, осложнения и лечение. Am J Sports Med . 1982 Май-июнь. 10 (3): 162-73. [Медлайн].
Маркин Р.С. Проявления заболеваний печени, связанных с вирусом Эпштейна-Барра. Печень . 1994 14 февраля (1): 1-13. [Медлайн].
Markin RS, Linder J, Zuerlein K, et al.Гепатит при инфекционном мононуклеозе со смертельным исходом. Гастроэнтерология . 1987 декабрь 93 (6): 1210-7. [Медлайн].
Маруяма К., Ушику Х., Конду Ю. Утолщение стенки желчного пузыря у детей с инфекционным мононуклеозом. J Clin Ультразвук . 1994 ноябрь-декабрь. 22 (9): 576-8. [Медлайн].
Мейсон WR младший, Адамс EK. Инфекционный мононуклеоз; анализ 100 случаев с особым вниманием к диагностике, тестам функции печени и лечению отдельных случаев преднизоном. Am J Med Sci . 1958 Oct.236 (4): 447-59 passim. [Медлайн].
Mendoza N, Diamantis M, Arora A, Bartlett B, Gewirtzman A, Tremaine AM и др. Кожно-слизистые проявления инфекции вирусом Эпштейна-Барра. Ам Дж. Клин Дерматол . 2008. 9 (5): 295-305. [Медлайн].
Mendoza N, Diamantis M, Arora A, Bartlett B, Gewirtzman A, Tremaine AM и др. Кожно-слизистые проявления инфекции вирусом Эпштейна-Барра. Ам Дж. Клин Дерматол .2008. 9 (5): 295-305. [Медлайн].
Milpied N, Coste-Burel M, Accard F, et al. Связанное с вирусом Эпштейна-Барра В-клеточное лимфопролиферативное заболевание после немиелоаблативной трансплантации аллогенных стволовых клеток. Пересадка костного мозга . 1999 23 марта (6): 629-30. [Медлайн].
Mroczek EC, Weisenburger DD, Grierson HL, et al. Смертельный инфекционный мононуклеоз и вирус-ассоциированный гемофагоцитарный синдром. Arch Pathol Lab Med .1987 июн. 111 (6): 530-5. [Медлайн].
Мюррей Б.Дж. Медицинские осложнения инфекционного мононуклеоза. Ам Фам Врач . 1984 30 ноября (5): 195-9. [Медлайн].
Налесник М.А., Старзл Т.Э. Вирус Эпштейна-Барра, инфекционный мононуклеоз и посттрансплантационные лимфопролиферативные нарушения. Научные исследования по трансплантологии . 1994 Сентябрь 4 (1): 61-79. [Медлайн].
Nystad TW, Myrmel H. Распространенность первичной инфекции по сравнению с реактивированной вирусом Эпштейна-Барра у пациентов с антителами VCA IgG, VCA IgM и EBNA-1 и с подозрением на инфекционный мононуклеоз. Дж. Клин Вирол . 2007 апр. 38 (4): 292-7. [Медлайн].
Оно Т., Уэда Ю., Кисимото В., Аримото-Миямото К., Такеока Т., Цуджи М. Инфекционный мононуклеоз, вызванный вирусом Эпштейна-Барра, после двух отдельных эпизодов вирус-ассоциированного гемофагоцитарного синдрома. Медицинский работник . 2009. 48 (13): 1169-73. [Медлайн].
Окано М, Брутто ТГ. Острые или хронические опасные для жизни заболевания, связанные с инфекцией вируса Эпштейна-Барра. Am J Med Sci .2012 июн. 343 (6): 483-9. [Медлайн].
Окано М, Брутто ТГ. Гемофагоцитарный синдром, связанный с вирусом Эпштейна-Барра, и фатальный инфекционный мононуклеоз. Ам Дж. Гематол . 1996 Октябрь 53 (2): 111-5. [Медлайн].
Окано М., Тиле Г.М., Дэвис Дж. Р. и др. Вирус Эпштейна-Барра и болезни человека: последние достижения в диагностике. Clin Microbiol Ред. . 1988 июл.1 (3): 300-12. [Медлайн].
Ooka T, de Turenne-Tessier M, Stolzenberg MC.Связь между выработкой антител к ранним антигенам вируса Эпштейна-Барра (EBV) и различными заболеваниями, связанными с EBV. Спрингер Семин Иммунопатол . 1991. 13 (2): 233-47. [Медлайн].
Oren I, Sobel JD. Вирус герпеса человека 6 типа: обзор. Clin Infect Dis . 1992 14 марта (3): 741-6. [Медлайн].
Osamah H, Finkelstein R, Brook JG. Рабдомиолиз, осложняющий острую инфекцию, вызванную вирусом Эпштейна-Барра. Инфекция .1995 март-апрель. 23 (2): 119-20. [Медлайн].
Пол Младший, Бруннелл WW. Наличие гетерофильных антител при инфекционном мононуклеозе. Am J Med Sci . 1932. 183: 90-104.
Penman HG. Смертельный инфекционный мононуклеоз: критический обзор. Дж. Клин Патол . 1970 декабря 23 (9): 765-71. [Медлайн].
Pflugfelder SC, Crouse CA, Atherton SS, et al. Офтальмологические проявления инфекции вирусом Эпштейна-Барра. Int Ophthalmol Clin . 1993 Зима. 33 (1): 95-101. [Медлайн].
Pullen H, Wright N, Murdoch JM. Реакции гиперчувствительности к антибактериальным препаратам при инфекционном мононуклеозе. Ланцет . 1967, 2 декабря (7527): 1176-8. [Медлайн].
Purtilo DT. Вирус Эпштейна-Барра: спектр его проявлений у человека. South Med J . 1987 августа 80 (8): 943-7. [Медлайн].
Purtilo DT, Сакамото К.Вирус Эпштейна-Барра и болезнь человека: иммунные ответы определяют клинические и патологические проявления. Хум Патол . 1981, 12 августа (8): 677-9. [Медлайн].
Рикинсон AB, Фокс CP. Вирус Эпштейна-Барра и инфекционный мононуклеоз: чему нас могут научить студенты. J Заразить Dis . 2013 Январь 207 (1): 6-8. [Медлайн].
Рикинсон AB, Мосс DJ. Ответ цитотоксических Т-лимфоцитов человека на инфекцию вируса Эпштейна-Барра. Анну Рев Иммунол .1997. 15: 405-31. [Медлайн].
Робинсон JE. Биология циркулирующих В-лимфоцитов, инфицированных вирусом Эпштейна-Барра, во время инфекционного мононуклеоза. Йельский университет биологии медицины . 1982 май-август. 55 (3-4): 311-6. [Медлайн].
Росалки С.Б., Джонс Т.Г., Верней А.Ф. Трансаминазы и исследования функции печени при инфекционном мононуклеозе. Br Med J . 1960 26 марта, 1 (5177): 929-32. [Медлайн].
Safran D, Bloom GP.Спонтанный разрыв селезенки вследствие инфекционного мононуклеоза. Am Surg . 1990 Октябрь 56 (10): 601-5. [Медлайн].
Sanefuji M, Ohga S, Kira R, Nomura A, Torisu H, Takada H и др. Менингоэнцефаломиелит, связанный с вирусом Эпштейна-Барра: интратекальная реактивация вируса у иммунокомпетентного ребенка. J Детский нейрол . 2008 23 сентября (9): 1072-7. [Медлайн].
Schaller RJ, советник FL. Инфекционный мононуклеоз у детей раннего возраста. Am J Emerg Med . 1995 июл.13 (4): 438-40. [Медлайн].
Шлоссберг Д. Инфекционный мононуклеоз . 2-е изд. Нью-Йорк, штат Нью-Йорк: Спрингер-Верлаг; 1989.
Schmader KE, van der Horst CM, Klotman ME. Вирус Эпштейна-Барра и пожилой хозяин. Ред. Заразить Dis . 1989 янв-фев. 11 (1): 64-73. [Медлайн].
Schmitz H, Volz D, Krainick-Riechert C, et al. Острые инфекции вируса Эпштейна-Барра у детей. Мед Микробиол Иммунол . 1972. 158 (1): 58-63. [Медлайн].
Schnipper LE. Вирус Эпштейна-Барра и лимфопролиферативные заболевания человека. Прог Гематол . 1981. 12: 275-97. [Медлайн].
Шумахер HR, Якобсон Ва, Бемиллер CR. Лечение инфекционного мононуклеоза. Энн Интерн Мед. . 1963. 58: 217-228.
Шумахер HR, Якобсон Вашингтон, Бемиллер CR. Лечение инфекционного мононуклеоза. Энн Интерн Мед. . 1952. 36: 1498-1512.
Seemayer TA, Oligny LL, Gartner JG. Вирус Эпштейна-Барра: исторические, биологические, патологические и онкологические соображения. Перспектива Педиатр Патол . 1981. 6: 1-33. [Медлайн].
Seitanidis B. Сравнение теста Monospot с тестом Пола-Баннелла при инфекционном мононуклеозе и других заболеваниях. Дж. Клин Патол . 1969 Май. 22 (3): 321-3. [Медлайн].
Шашаты Г.Г., Атамер МА.Гемолитико-уремический синдром, связанный с инфекционным мононуклеозом. Ам Дж. Дис Детский . 1974 Май. 127 (5): 720-2. [Медлайн].
Шурин СБ. Инфекционный мононуклеоз. Педиатрическая клиника North Am . 1979 Май. 26 (2): 315-26. [Медлайн].
Ситки-Грин Д.Л., Эдвардс Р.Х., Ковингтон М.М. и др. Биология вируса Эпштейна-Барра при инфекционном мононуклеозе. J Заразить Dis . 2004 г., 1. 189 (3): 483-92. [Медлайн].
Статтер МБ, Лю округ Колумбия.Безоперационное лечение тупой травмы селезенки при инфекционном мононуклеозе. Am Surg . 2005 Май. 71 (5): 376-8. [Медлайн].
Стир AC. Болезнь Лайма. N Engl J Med . 31 августа 1989 г. 321 (9): 586-96. [Медлайн].
Straus SE. Острые прогрессирующие инфекции вируса Эпштейна-Барра. Анну Рев Мед . 1992. 43: 437-49. [Медлайн].
Straus SE, Cohen JI, Tosato G и др. Конференция NIH.Инфекции вируса Эпштейна-Барра: биология, патогенез и лечение. Энн Интерн Мед. . 1993 г., 1. 118 (1): 45-58. [Медлайн].
Sugden B. Вирус Эпштейна-Барра: человеческий патоген, вызывающий лимфопролиферацию in vivo и in vitro. Ред. Заразить Dis . 1982 сентябрь-октябрь. 4 (5): 1048-61. [Медлайн].
Салливан JL. Гематологические последствия заражения вирусом Эпштейна-Барра. Гематол Онкол Клин Норт Ам . 1987 Сентябрь 1 (3): 397-417.[Медлайн].
Сумая CV. Инфекция вирусом Эпштейна-Барра: расширенный спектр. Adv Pediatr Infect Dis . 1986. 1: 75-97. [Медлайн].
Сумая CV. Инфекции вируса Эпштейна-Барра у детей. Curr Probl Pediatr . 1987 г., 17 (12): 677-745. [Медлайн].
Сумая CV. Серологические тесты на вирус Эпштейна-Барра: диагностические показания и интерпретации. Pediatr Infect Dis . 1986 май-июнь.5 (3): 337-42. [Медлайн].
Сумая CV. Инфекционный мононуклеоз и другие ВЭБ-инфекции: факторы диагностики. Управление лабораторией . 1986. 24: 37-43.
Сумая CV. Серологическое тестирование на вирус Эпштейна-Барра — достижения в интерпретации. J Заразить Dis . 1985 июн. 151 (6): 984-7. [Медлайн].
Сумая К.В., Энч Ю. Инфекционный мононуклеоз вируса Эпштейна-Барра у детей. I. Клинические и общие лабораторные данные. Педиатрия . 1985 июн. 75 (6): 1003-10. [Медлайн].
Теглия О., Кунья Б.А. Цитомегаловирусный мононуклеоз. Emerg Med . 1991. 23: 135-138.
Tosato G, Taga K, Angiolillo AL, et al. Вирус Эпштейна-Барра как возбудитель гематологических заболеваний. Baillieres Clin Haematol . 1995 марта 8 (1): 165-99. [Медлайн].
Триантос Д., Портер С.Р., Скалли С. и др. Волосатая лейкоплакия полости рта: клинико-патологические особенности, патогенез, диагностика и клиническое значение. Clin Infect Dis . 1997 25 декабря (6): 1392-6. [Медлайн].
Тайнелл Э., Аврелий Э., Бранделл А. и др. Лечение острого инфекционного мононуклеоза ацикловиром и преднизолоном: многоцентровое двойное слепое плацебо-контролируемое исследование. J Заразить Dis . 1996 Август 174 (2): 324-31. [Медлайн].
van der Horst C, Joncas J, Ahronheim G, et al. Отсутствие эффекта перорального ацикловира для лечения острого инфекционного мононуклеоза. J Заразить Dis . 1991 Октябрь 164 (4): 788-92. [Медлайн].
Vaughan JH. Вирус Эпштейна-Барра при аутоиммунитете. Спрингер Семин Иммунопатол . 1995. 17 (2-3): 203-30. [Медлайн].
Видрих Дж. А., Валенский Р. П., Сакс П. Е. и др. Положительные тесты на гетерофильные антитела к вирусу Эпштейна-Барра у пациентов с первичной инфекцией вируса иммунодефицита человека. Am J Med . 2001 15 августа. 111 (3): 192-4. [Медлайн].
Vouloumanou EK, Rafailidis PI, Falagas ME.Современная диагностика и лечение инфекционного мононуклеоза. Curr Opin Hematol . 2012 19 января (1): 14-20. [Медлайн].
Уоллис С. Все началось с поцелуя (возможно). Ланцет . 2007 15 декабря. 370 (9604): 2068. [Медлайн].
Белая ЛР, Карофский ПС. Обзор клинических проявлений, лабораторных данных и осложнений инфекционного мононуклеоза. Вис Мед Дж. . 1985 декабрь 84 (12): 19-25. [Медлайн].
Белый Нью-Джерси, Juel-Jensen BE.Инфекционный мононуклеозный гепатит. Semin Liver Dis . 1984 ноября, 4 (4): 301-6. [Медлайн].
Вольф П., Дорфман Р., МакКленахан Дж. И др. Ложноположительный точечный тест на инфекционный мононуклеоз при лимфоме. Рак . 1970 марта 25 (3): 626-8. [Медлайн].
Вонг С.Ю., Беннет Б. Естественная история тяжелой тромбоцитопении при инфекционном мононуклеозе. Постградская медицина J . 1982, апрель, 58 (678): 249-51. [Медлайн].
Ямасита С., Мураками С., Изуми Ю. и др.Тяжелая хроническая активная инфекция вируса Эпштейна-Барра, сопровождающаяся вирус-ассоциированным гемофагоцитарным синдромом, мозжечковой атаксией и энцефалитом. Психиатрическая клиника Neurosci . 1998 Август 52 (4): 449-52. [Медлайн].
Зиглер Дж. Л., Дрю В. Л., Майнер Р. К. и др. Вспышка лимфомы Беркитта у гомосексуальных мужчин. Ланцет . 1982, 18 сентября. 2 (8299): 631-3. [Медлайн].
Engelmann I, Nasser H, Belmiloudi S, et al. Клинически тяжелый энцефалит, вызванный вирусом Эпштейна-Барра, с легкими нарушениями спинномозговой жидкости у иммунокомпетентного подростка: описание случая. Диагностика Microbiol Infect Dis . 2013 июн. 76 (2): 232-4. [Медлайн].
Муньос-Гомес С., Кунья Б.А. Парвовирус B19 имитирует инфекционный мононуклеоз вируса Эпштейна-Барра у взрослого. Am J Med . 2013 май. 126 (5): e7-8. [Медлайн].
Cunha BA, Petelin A, George S. Лихорадка неизвестного происхождения (FUO) у пожилого взрослого, вызванная вирусом Эпштейна-Барра (EBV), проявляющаяся как «тифоидный мононуклеоз», имитирующий лимфому. Сердце легкое .2013 янв-фев. 42 (1): 79-81. [Медлайн].
Hsu DT, Ruf M, O’Shea S, Costelloe S, Peck J, Tong CY. Диагностика ВИЧ-инфекции у пациентов с заболеванием, напоминающим железистую лихорадку, в системе первичной медико-санитарной помощи: упускаем ли мы первичную ВИЧ-инфекцию? ВИЧ Мед . 2013 14 января (1): 60-3. [Медлайн].
Кессенич Р.Р., Фланаган М. Диагностика инфекционного мононуклеоза. Практика медсестры . 2015 15 августа. 40 (8): 13-4, 16. [Medline].


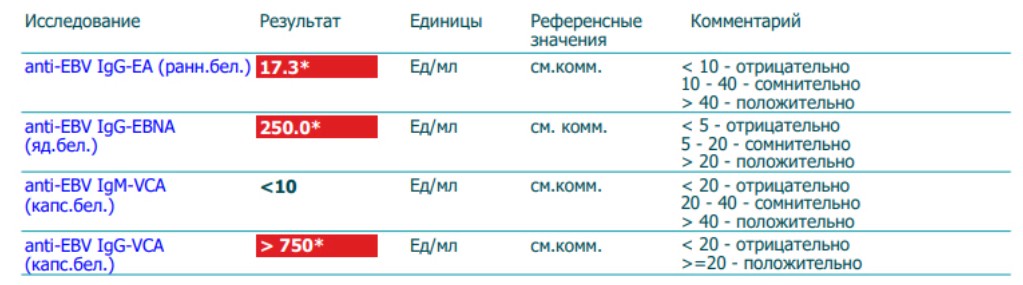




 Например, гетерофильные антитела, обнаруживаемые с помощью Monospot, часто отсутствуют у детей с инфекционным мононуклеозом. В лучшем случае тест Monospot может указывать на то, что у человека типичный случай инфекционного мононуклеоза, но не подтверждает наличие инфекции EBV.
Например, гетерофильные антитела, обнаруживаемые с помощью Monospot, часто отсутствуют у детей с инфекционным мононуклеозом. В лучшем случае тест Monospot может указывать на то, что у человека типичный случай инфекционного мононуклеоза, но не подтверждает наличие инфекции EBV. Высокие или повышенные уровни антител могут присутствовать в течение многих лет и не являются признаком недавней инфекции.
Высокие или повышенные уровни антител могут присутствовать в течение многих лет и не являются признаком недавней инфекции. 9-1.0 AI: неопределенный
1.1 AI или выше: положительный
9-1.0 AI: неопределенный
1.1 AI или выше: положительный 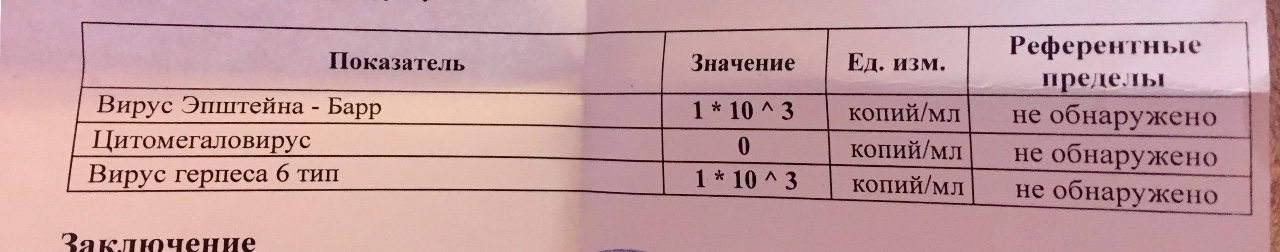 Другие расстройства, вызванные инфекцией ВЭБ, включают:
были признаны, включая лимфому Беркитта и носоглотку
карцинома. Инфекция ВЭБ также может вызывать лимфопролиферативные синдромы,
особенно у пациентов, перенесших почечный или костный мозг
трансплантации и у больных СПИДом.
Наличие антител IgM к VCA указывает на недавнюю первичную инфекцию
EBV. Наличие антител VCA IgG иногда указывает на инфекцию.
в прошлом. Антитела к EBNA развиваются через 6-8 недель после первичного
инфекции и обычно обнаруживаются на всю жизнь.Более 90% от нормы
взрослое население имеет антитела класса IgG к VCA и EBNA. Несколько
у пациентов, инфицированных EBV, не разовьется
антитела к EBNA (примерно 5% -10%).
Интерпретация серологических паттернов ВЭБ адаптирована на основе результатов J.
Clin. Microbiol. 47 (10): 3204-3210, 2009. В таблице ниже
вероятные интерпретации 16 паттернов, возможных из четырех
анализы в панели EBV. В целях классификации
неопределенные / сомнительные результаты считаются отрицательными в таблице
ниже.
Другие расстройства, вызванные инфекцией ВЭБ, включают:
были признаны, включая лимфому Беркитта и носоглотку
карцинома. Инфекция ВЭБ также может вызывать лимфопролиферативные синдромы,
особенно у пациентов, перенесших почечный или костный мозг
трансплантации и у больных СПИДом.
Наличие антител IgM к VCA указывает на недавнюю первичную инфекцию
EBV. Наличие антител VCA IgG иногда указывает на инфекцию.
в прошлом. Антитела к EBNA развиваются через 6-8 недель после первичного
инфекции и обычно обнаруживаются на всю жизнь.Более 90% от нормы
взрослое население имеет антитела класса IgG к VCA и EBNA. Несколько
у пациентов, инфицированных EBV, не разовьется
антитела к EBNA (примерно 5% -10%).
Интерпретация серологических паттернов ВЭБ адаптирована на основе результатов J.
Clin. Microbiol. 47 (10): 3204-3210, 2009. В таблице ниже
вероятные интерпретации 16 паттернов, возможных из четырех
анализы в панели EBV. В целях классификации
неопределенные / сомнительные результаты считаются отрицательными в таблице
ниже. Результаты всегда следует интерпретировать вместе с
история болезни пациента и физикальное обследование.
Гетерофил VCA VCA EBNA
IgM IgM IgG IgG Интерпретация
Neg Neg Neg Neg EBV наивный
Neg Pos Neg Neg Первичная острая ВЭБ-инфекция
Pos Neg Neg Neg Первичная острая ВЭБ-инфекция
Pos Pos Neg Neg Первичная острая ВЭБ-инфекция
Neg Pos Pos Neg Первичная острая ВЭБ-инфекция
Pos Neg Pos Neg Первичная острая ВЭБ-инфекция
Pos Pos Pos Neg Первичная острая ВЭБ-инфекция
Neg Pos Neg Pos Восстановление после / реактивация EBV-инфекции
Neg Pos Pos Pos Восстановление после / реактивация инфекции EBV
Pos Neg Pos Pos Восстановление после / реактивация EBV-инфекции
Pos Pos Neg Pos Восстановление после / реактивация EBV-инфекции
Pos Pos Pos Pos Выход из / реактивация EBV-инфекции
Neg Neg Pos Neg Прошедшая инфекция ВЭБ
Neg Neg Pos Pos Прошедшая инфекция ВЭБ
Pos Neg Neg Pos Неизвестно *
Neg Neg Neg Pos Неизвестно *
* Эти два паттерна необычны и имеют неизвестное значение.
Результаты всегда следует интерпретировать вместе с
история болезни пациента и физикальное обследование.
Гетерофил VCA VCA EBNA
IgM IgM IgG IgG Интерпретация
Neg Neg Neg Neg EBV наивный
Neg Pos Neg Neg Первичная острая ВЭБ-инфекция
Pos Neg Neg Neg Первичная острая ВЭБ-инфекция
Pos Pos Neg Neg Первичная острая ВЭБ-инфекция
Neg Pos Pos Neg Первичная острая ВЭБ-инфекция
Pos Neg Pos Neg Первичная острая ВЭБ-инфекция
Pos Pos Pos Neg Первичная острая ВЭБ-инфекция
Neg Pos Neg Pos Восстановление после / реактивация EBV-инфекции
Neg Pos Pos Pos Восстановление после / реактивация инфекции EBV
Pos Neg Pos Pos Восстановление после / реактивация EBV-инфекции
Pos Pos Neg Pos Восстановление после / реактивация EBV-инфекции
Pos Pos Pos Pos Выход из / реактивация EBV-инфекции
Neg Neg Pos Neg Прошедшая инфекция ВЭБ
Neg Neg Pos Pos Прошедшая инфекция ВЭБ
Pos Neg Neg Pos Неизвестно *
Neg Neg Neg Pos Неизвестно *
* Эти два паттерна необычны и имеют неизвестное значение.
